文档内容
D.室温下Na与空气中O 反应制取NaO
下学期期末测试卷 02 2 2 2
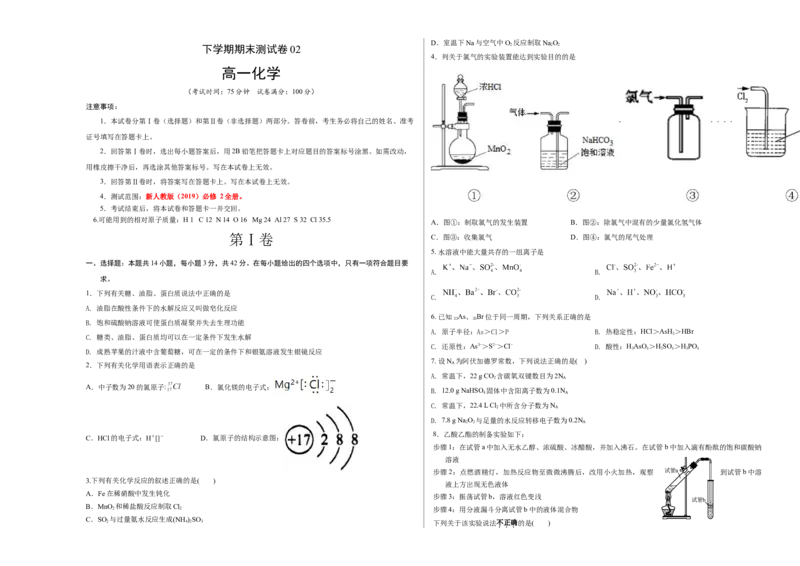
4.列关于氯气的实验装置能达到实验目的的是
高一化学
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考
证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:新人教版(2019)必修 2全册。
5.考试结束后,将本试卷和答题卡一并交回。
6.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Mg 24 Al 27 S 32 Cl 35.5
A.图①:制取氯气的发生装置 B.图②:除氯气中混有的少量氯化氢气体
第Ⅰ卷 C.图③:收集氯气 D.图④:氯气的尾气处理
5. 水溶液中能大量共存的一组离子是
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题目要
A. B.
求。
1.下列有关糖、油脂、蛋白质说法中正确的是
C. D.
A. 油脂在酸性条件下的水解反应又叫做皂化反应
6. 已知 As、 Br位于同一周期,下列关系正确的是
33 35
B. 饱和硫酸钠溶液可使蛋白质凝聚并失去生理功能
A. 原子半径:As>Cl>P B. 热稳定性:HCl>AsH >HBr
3
C. 糖类、油脂、蛋白质均可以在一定条件下发生水解
C. 还原性:As3->S2->Cl- D. 酸性:HAsO >HSO >HPO
3 4 2 4 3 4
D. 成熟苹果的汁液中含葡萄糖,可在一定的条件下和银氨溶液发生银镜反应
7. 设N 为阿伏加德罗常数,下列说法正确的是( )
2.下列有关化学用语表示正确的是 A
A. 常温下,22 g CO 含碳氧双键数目为2N
2 A
A.中子数为20的氯原子: B.氯化镁的电子式:
B. 12.0 g NaHSO 固体中含阳离子数为0.1N
4 A
C. 常温下,22.4 L Cl 中所含分子数为N
2 A
D. 7.8 g Na O 与足量的水反应转移电子数为0.2N
2 2 A
8.乙酸乙酯的制备实验如下:
C.HCl的电子式:H+[]- D.氯原子的结构示意图:
步骤1:在试管a中加入无水乙醇、浓硫酸、冰醋酸,并加入沸石。在试管 b中加入滴有酚酞的饱和碳酸钠
溶液
步骤2:点燃酒精灯,加热反应物至微微沸腾后,改用小火加热,观察 试管a 到试管b中溶
3.下列有关化学反应的叙述正确的是( )
液上方出现无色液体
A.Fe在稀硝酸中发生钝化
步骤3:振荡试管b,溶液红色变浅
试管b
B.MnO 和稀盐酸反应制取Cl
2 2 步骤4:用分液漏斗分离试管b中的液体混合物
C.SO 与过量氨水反应生成(NH )SO
2 4 2 3 下列关于该实验说法不正确的是( )A.试管a中放入沸石的目的是防止加热时液体暴沸
B.导管不伸入试管b中液面以下,其目的是防止倒吸
C 用洁净铂丝蘸取某溶液在火焰上灼烧,火焰呈黄色 溶液中有Na+,无K+
C.步骤3中溶液红色变浅,是因为碳酸钠与乙醇发生反应
D.步骤4中应先放出水相后再从分液漏斗上口倒出乙酸乙酯
D 向某溶液中先加KSCN无明显现象,再滴氯水,溶液变红 溶液中一定含有Fe2+
9.对乙烯的结构,下列说法正确的是( )
A.A B.B C.C D.D
A.乙烯分子在空间上呈平面结构
13.在一密闭容器中充入1mol 和1molI ,压强为P(Pa),并在一定温度下使其发生反应:
2
B.乙烯的球棍模型为
。下列操作中,能使其反应速率减慢的有
C.乙烯的电子式为
D.乙烯的结构简式为CHCH
2 2
①保特容器容积不变,向其中充入1mol ②保持容器容积不变,向其中充入1mol ( 不参加反应)③
10.下列离子方程式书写正确的是( )
A.氧化钠与水反应:O2-+HO===2OH-
2
B.硫酸铜溶液与氢氧化钡溶液混合:SO+Ba2+===BaSO ↓ 保持容器内压强不变,向其中充入1mol ( 不参加反应)④保持容器内压强不变,向其中充入1mol
4
C.氯化亚铁溶液中通入氯气:Fe2++Cl===Fe3++2Cl-
2
D.氯气通入溴化钠溶液中:Cl+2Br-===2Cl-+Br
2 2 和1mol ⑤提高起始反应温度
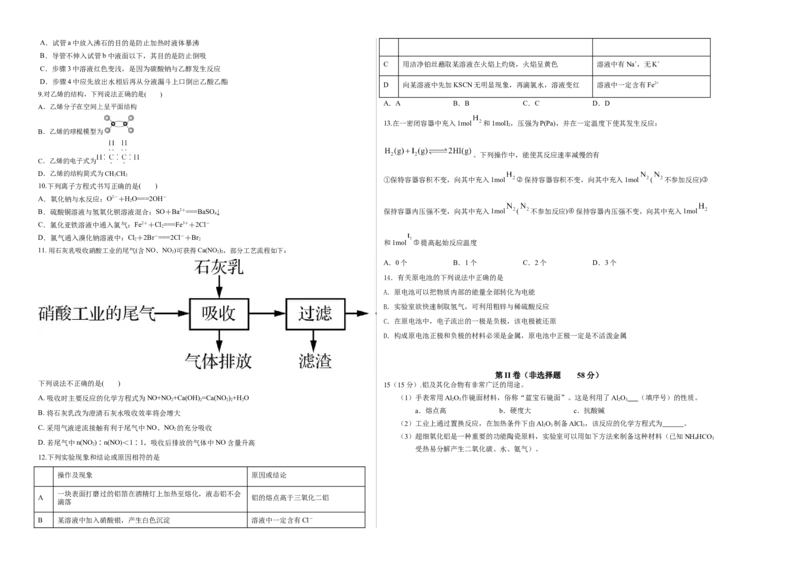
11. 用石灰乳吸收硝酸工业的尾气(含NO、NO)可获得Ca(NO),部分工艺流程如下:
2 2 2
A.0个 B.1个 C.2个 D.3个
14.有关原电池的下列说法中正确的是
A.原电池可以把物质内部的能量全部转化为电能
B.实验室欲快速制取氢气,可利用粗锌与稀硫酸反应
C.在原电池中,电子流出的一极是负极,该电极被还原
D.构成原电池正极和负极的材料必须是金属,原电池中正极一定是不活泼金属
第II卷(非选择题 58分)
下列说法不正确的是( ) 15(15分).铝及其化合物有非常广泛的用途。
A. 吸收时主要反应的化学方程式为NO+NO +Ca(OH) =Ca(NO)+H O (1)手表常用Al O 作镜面材料,俗称“蓝宝石镜面”。这是利用了Al O (填序号)的性质。
2 2 2 2 2 2 3 2 3
a.熔点高 b.硬度大 c.抗酸碱
B. 将石灰乳改为澄清石灰水吸收效率将会增大
(2)工业上通过置换反应,在加热条件下由Al O 制备AlCl ,该反应的化学方程式为 。
C. 采用气液逆流接触有利于尾气中NO、NO 的充分吸收 2 3 3
2
(3)超细氧化铝是一种重要的功能陶瓷原料,实验室可以用如下方法来制备这种材料(已知NH HCO
4 3
D. 若尾气中n(NO )∶n(NO)<1∶1,吸收后排放的气体中NO含量升高
2
受热易分解产生二氧化碳、水、氨气)。
12.下列实验现象和结论或原因相符的是
操作及现象 原因或结论
一块表面打磨过的铝箔在酒精灯上加热至熔化,液态铝不会
A 铝的熔点高于三氧化二铝
滴落
B 某溶液中加入硝酸银,产生白色沉淀 溶液中一定含有Cl-【解释及结论】
试回答下列问题。 (1)NO 与水反应的离子方程式为____________。
2
① 已知反应1过滤后所得滤渣1的成分为NH 4 Al(SO 4 ) 2 ;反应2除生成NH 4 Al(OH) 2 CO 3 外,还有多种 (2)步骤I中,通入N 2 的目的是____________。
生成物,其中有一种是气体,该气体为 。
(3)将步骤II中圆底烧瓶内的实验现象补充完整:____________。
② 判断NH Al(OH) CO 沉淀已洗涤干净的方法是 。
4 2 3
(4)步骤III所发生反应的化学方程式为 。
③ 已知反应3灼烧生成Al O 和气态混合物,则反应3的化学方程式为 ▲ 。
2 3
(5)该实验验证NO 与水反应产物的实验证据包括____________(填序号)。
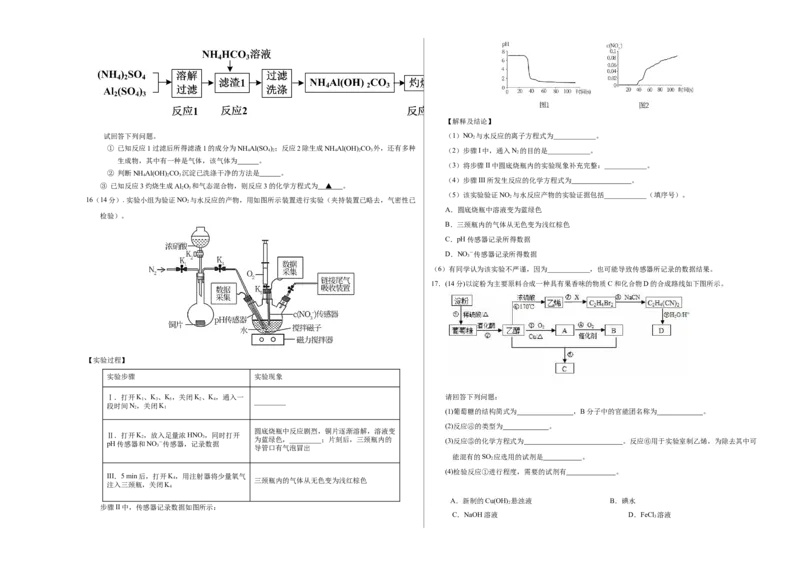
16(14分). 实验小组为验证NO 与水反应的产物,用如图所示装置进行实验(夹持装置已略去,气密性已 2
2
A.圆底烧瓶中溶液变为蓝绿色
检验)。
B.三颈瓶内的气体从无色变为浅红棕色
C.pH传感器记录所得数据
D.NO -传感器记录所得数据
3
(6)有同学认为该实验不严谨,因为____________,也可能导致传感器所记录的数据结果。
17.(14分)以淀粉为主要原料合成一种具有果香味的物质C和化合物D的合成路线如下图所示。
【实验过程】
实验步骤 实验现象
Ⅰ.打开K、K、K,关闭K、K,通入一 请回答下列问题:
1 3 5 2 4 _________
段时间N,关闭K
2 1
(1)葡萄糖的结构简式为 ,B分子中的官能团名称为 。
(2)反应⑧的类型为 。
圆底烧瓶中反应剧烈,铜片逐渐溶解,溶液变
Ⅱ.打开K,放入足量浓HNO,同时打开
2 3 为蓝绿色,_________;片刻后,三颈瓶内的 (3)反应⑤的化学方程式为 。反应⑥用于实验室制乙烯,为除去其中可
pH传感器和NO -传感器,记录数据
3 导管口有气泡冒出
能混有的SO 应选用的试剂是 。
2
(4)检验反应①进行程度,需要的试剂有 。
III.5 min后,打开K,用注射器将少量氧气
4 三颈瓶内的气体从无色变为浅红棕色
注入三颈瓶,关闭K
4
A.新制的Cu(OH) 悬浊液 B.碘水
2
步骤II中,传感器记录数据如图所示:
C.NaOH溶液 D.FeCl 溶液
3(5)乙烯的同系物丙烯(CH=CH-CH)可以通过加聚反应生成高分子化合物,其结构简式
2 3
是 。
18.(15分)水合肼(N H·H O)是一种精细化工原料,常用于医药、农药、染料、航天等领域。实验室模拟尿
2 4 2
素法制备NH·H O并进一步制取副产品NaSO 的流程图如图所示。
2 4 2 2 3
已知:①NH·H O具有强还原性,易被氧化成N。
2 4 2 2
① 一定条件下,碱性NaClO溶液与尿素溶液反应生成NH·H O。
2 4 2
⑴吸收塔内发生反应的离子方程式为 。
⑵为提高吸收塔内NaOH的有效利用率,将二氧化锰和浓盐酸制取的Cl 通入吸收塔前
2
应进行的操作是 (填操作名称),选用的试剂是 。
⑶反应器内生成水合肼的化学方程式为
。
⑷制备过程中要控制反应器内NaClO溶液的供给量,其主要目的是
(用离子方程式表示)。
⑸副产品NaSO 常用作还原性漂白剂。在测定某液体葡萄糖中NaSO 残留量时,取50.0 mL样品,先
2 3 2 3
通入足量Cl,用盐酸酸化后再加入足量的氯化钡溶液,充分反应,过滤,洗涤,干燥,称量固体质
2
量为0.11g。通入足量Cl 发生反应的离子方程式为 ,该样品中NaSO 残留量为
2 2 3
g·L-1(以SO 计,结果保留1位小数)。
2