文档内容
2025-2026 学年度高二第一学期期中学业水平质量监测
化学试题
注意事项
1.本试卷共10页,满分为100分,考试时间为75分钟。考试结束后,请将答题卡交回。
2.答题前,请务必将自己的姓名、考试号等用0.5毫米黑色墨水的签字笔填写在答题卡的规定位置。
3.作答选择题,必须用2B铅笔将答题卡上对应选项的方框涂满、涂黑;如需改动,请用橡皮擦干净后,再选
涂其他答案。作答非选择题,必须用0.5毫米黑色墨水的签字笔在答题卡上的指定位置作答,在其他位置作
答一律无效。
一、单选题(共13小题 满分39分)
1.我国科学家在一颗距离地球100光年的行星上发现了不可思议的“水世界”,引起了全球科学界的轰动。
下列有关说法正确的是
A.温度升高,水的电离平衡正向移动, 增大,溶液呈酸性
B.常温下, 的盐酸溶液中,
C.由水电离出的 时,溶液一定呈中性
D.向水中加入 固体后(溶液温度不变), 增大,水的电离程度增大
2.下列说法中,可以证明醋酸是弱电解质的是
A. 醋酸溶液中,
B. 时,醋酸溶液的
C. 的醋酸溶液恰好与 的 溶液完全反应
D. 时,醋酸溶液的导电性比盐酸弱
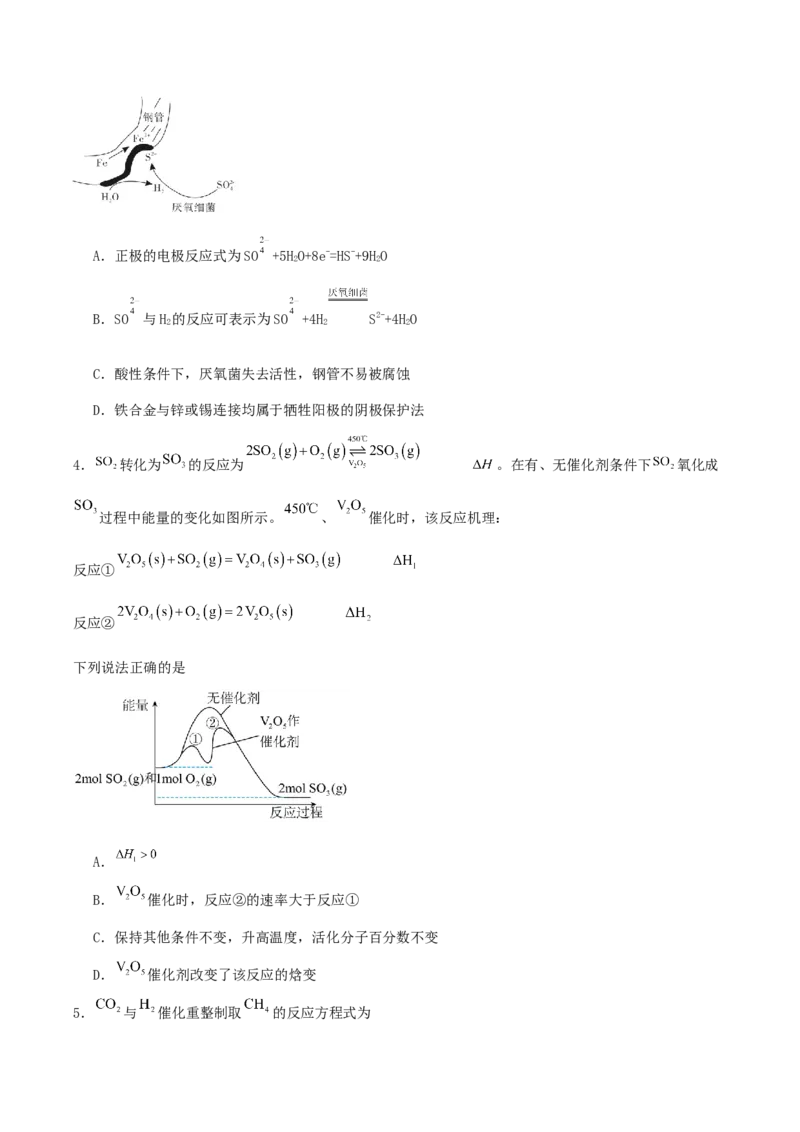
3.在潮湿的深层土壤中,钢管主要发生厌氧腐蚀,有关厌氧腐蚀的机理有多种,其中一种理论为厌氧细
菌(该厌氧细菌最佳生存环境在pH为7~8之间)可促使SO 与H 反应生成S2-,加速钢管的腐蚀,其反应原
2
理如图所示。下列说法正确的是A.正极的电极反应式为SO +5HO+8e-=HS-+9HO
2 2
B.SO 与H 的反应可表示为SO +4H S2-+4HO
2 2 2
C.酸性条件下,厌氧菌失去活性,钢管不易被腐蚀
D.铁合金与锌或锡连接均属于牺牲阳极的阴极保护法
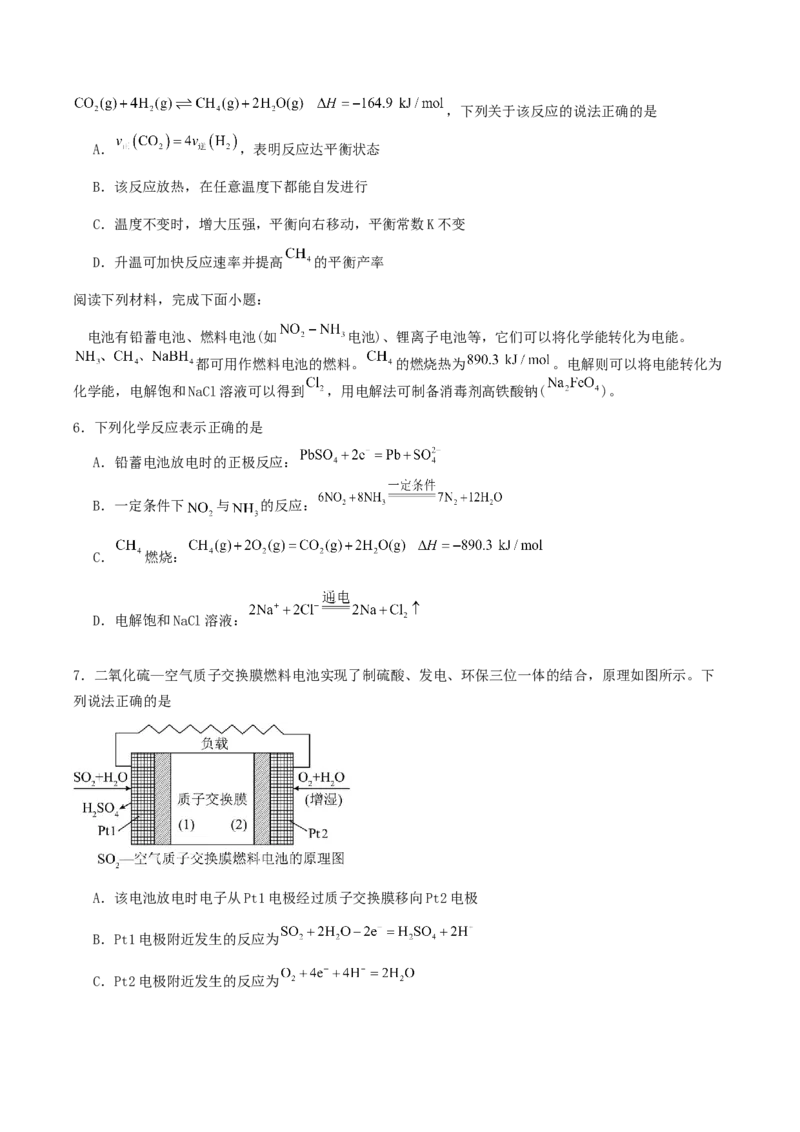
4. 转化为 的反应为 。在有、无催化剂条件下 氧化成
过程中能量的变化如图所示。 、 催化时,该反应机理:
反应①
反应②
下列说法正确的是
A.
B. 催化时,反应②的速率大于反应①
C.保持其他条件不变,升高温度,活化分子百分数不变
D. 催化剂改变了该反应的焓变
5. 与 催化重整制取 的反应方程式为,下列关于该反应的说法正确的是
A. ,表明反应达平衡状态
B.该反应放热,在任意温度下都能自发进行
C.温度不变时,增大压强,平衡向右移动,平衡常数K不变
D.升温可加快反应速率并提高 的平衡产率
阅读下列材料,完成下面小题:
电池有铅蓄电池、燃料电池(如 电池)、锂离子电池等,它们可以将化学能转化为电能。
都可用作燃料电池的燃料。 的燃烧热为 。电解则可以将电能转化为
化学能,电解饱和NaCl溶液可以得到 ,用电解法可制备消毒剂高铁酸钠( )。
6.下列化学反应表示正确的是
A.铅蓄电池放电时的正极反应:
B.一定条件下 与 的反应:
C. 燃烧:
D.电解饱和NaCl溶液:
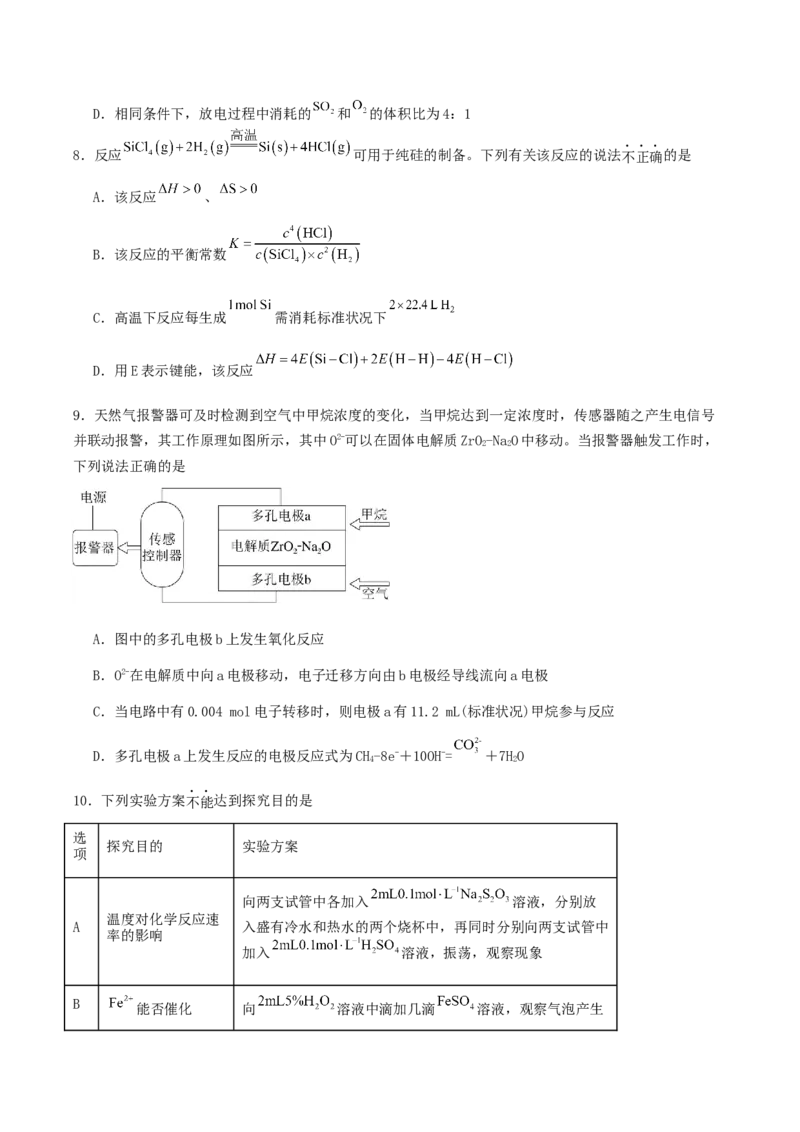
7.二氧化硫—空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的结合,原理如图所示。下
列说法正确的是
A.该电池放电时电子从Pt1电极经过质子交换膜移向Pt2电极
B.Pt1电极附近发生的反应为
C.Pt2电极附近发生的反应为D.相同条件下,放电过程中消耗的 和 的体积比为4:1
8.反应 可用于纯硅的制备。下列有关该反应的说法不正确的是
A.该反应 、
B.该反应的平衡常数
C.高温下反应每生成 需消耗标准状况下
D.用E表示键能,该反应
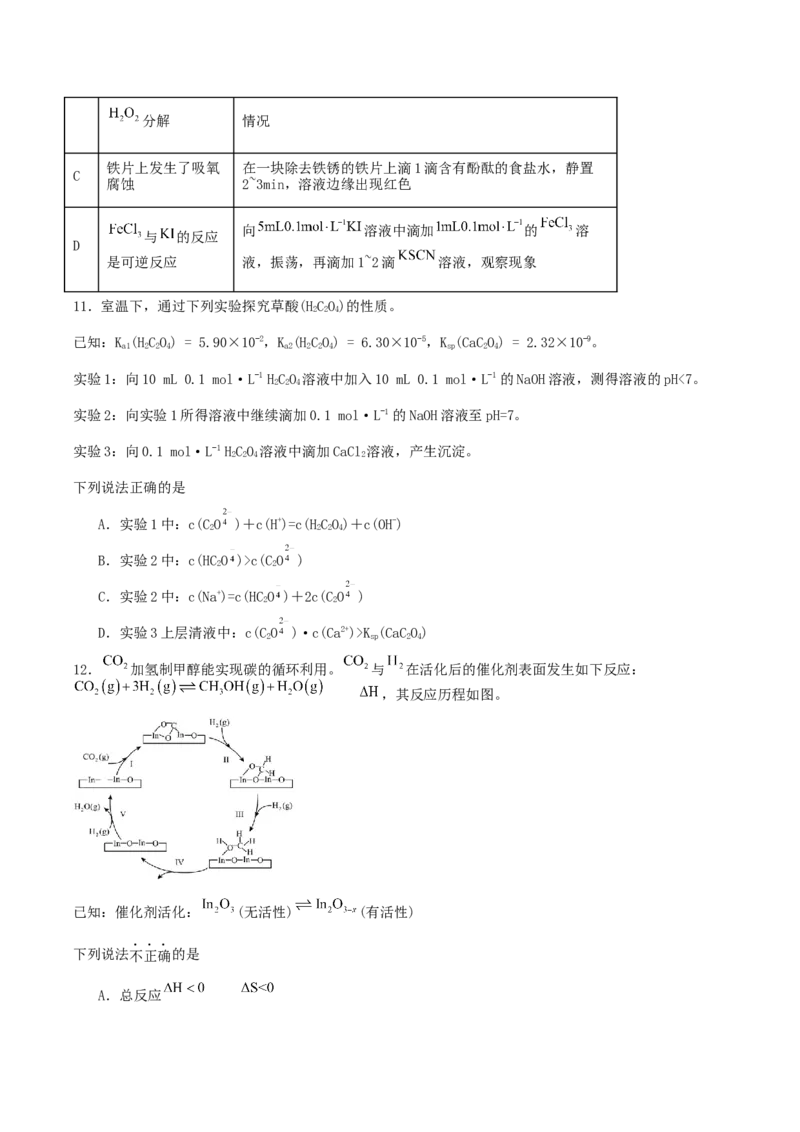
9.天然气报警器可及时检测到空气中甲烷浓度的变化,当甲烷达到一定浓度时,传感器随之产生电信号
并联动报警,其工作原理如图所示,其中O2-可以在固体电解质ZrO-NaO中移动。当报警器触发工作时,
2 2
下列说法正确的是
A.图中的多孔电极b上发生氧化反应
B.O2-在电解质中向a电极移动,电子迁移方向由b电极经导线流向a电极
C.当电路中有0.004 mol电子转移时,则电极a有11.2 mL(标准状况)甲烷参与反应
D.多孔电极a上发生反应的电极反应式为CH-8e-+10OH-= +7HO
4 2
10.下列实验方案不能达到探究目的是
选
探究目的 实验方案
项
向两支试管中各加入 溶液,分别放
温度对化学反应速
A 入盛有冷水和热水的两个烧杯中,再同时分别向两支试管中
率的影响
加入 溶液,振荡,观察现象
B
能否催化 向 溶液中滴加几滴 溶液,观察气泡产生分解 情况
铁片上发生了吸氧 在一块除去铁锈的铁片上滴1滴含有酚酞的食盐水,静置
C
腐蚀 2~3min,溶液边缘出现红色
向 溶液中滴加 的 溶
与 的反应
D
是可逆反应 液,振荡,再滴加1~2滴 溶液,观察现象
11.室温下,通过下列实验探究草酸(HCO)的性质。
2 2 4
已知:K (HCO) = 5.90×10−2,K (HCO) = 6.30×10−5,K (CaCO) = 2.32×10−9。
a1 2 2 4 a2 2 2 4 sp 2 4
实验1:向10 mL 0.1 mol·L−1 HCO 溶液中加入10 mL 0.1 mol·L−1 的NaOH溶液,测得溶液的pH<7。
2 2 4
实验2:向实验1所得溶液中继续滴加0.1 mol·L−1 的NaOH溶液至pH=7。
实验3:向0.1 mol·L−1 HCO 溶液中滴加CaCl 溶液,产生沉淀。
2 2 4 2
下列说法正确的是
A.实验1中:c(CO )+c(H+)=c(HCO)+c(OH-)
2 2 2 4
B.实验2中:c(HCO )>c(CO )
2 2
C.实验2中:c(Na+)=c(HCO )+2c(CO )
2 2
D.实验3上层清液中:c(CO )·c(Ca2+)>K (CaCO)
2 sp 2 4
12. 加氢制甲醇能实现碳的循环利用。 与 在活化后的催化剂表面发生如下反应:
,其反应历程如图。
已知:催化剂活化: (无活性) (有活性)
下列说法不正确的是
A.总反应B.过程Ⅱ中 发生氧化反应
C.历程中有 、 键的形成和断裂
D. 无活性的可能原因是 结构中缺少氧空位
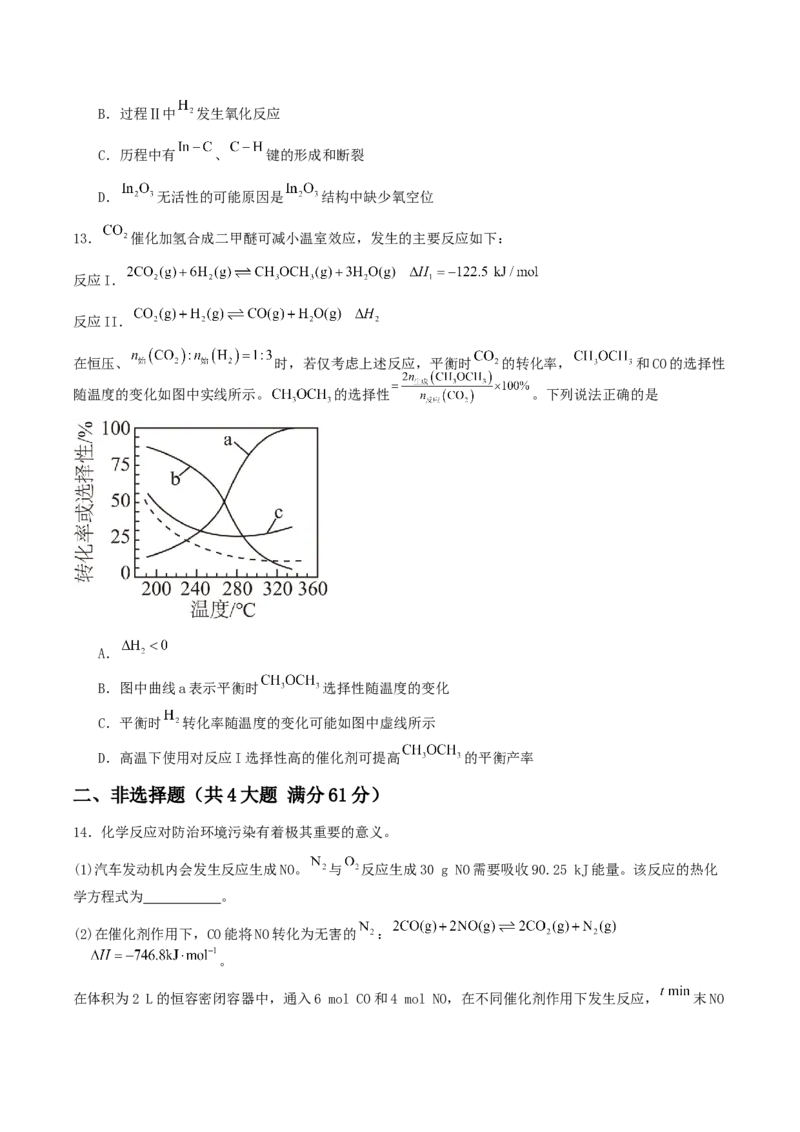
13. 催化加氢合成二甲醚可减小温室效应,发生的主要反应如下:
反应I.
反应II.
在恒压、 时,若仅考虑上述反应,平衡时 的转化率, 和CO的选择性
随温度的变化如图中实线所示。 的选择性 。下列说法正确的是
A.
B.图中曲线a表示平衡时 选择性随温度的变化
C.平衡时 转化率随温度的变化可能如图中虚线所示
D.高温下使用对反应I选择性高的催化剂可提高 的平衡产率
二、非选择题(共4大题 满分61分)
14.化学反应对防治环境污染有着极其重要的意义。
(1)汽车发动机内会发生反应生成NO。 与 反应生成30 g NO需要吸收90.25 kJ能量。该反应的热化
学方程式为 。
(2)在催化剂作用下,CO能将NO转化为无害的 :
。
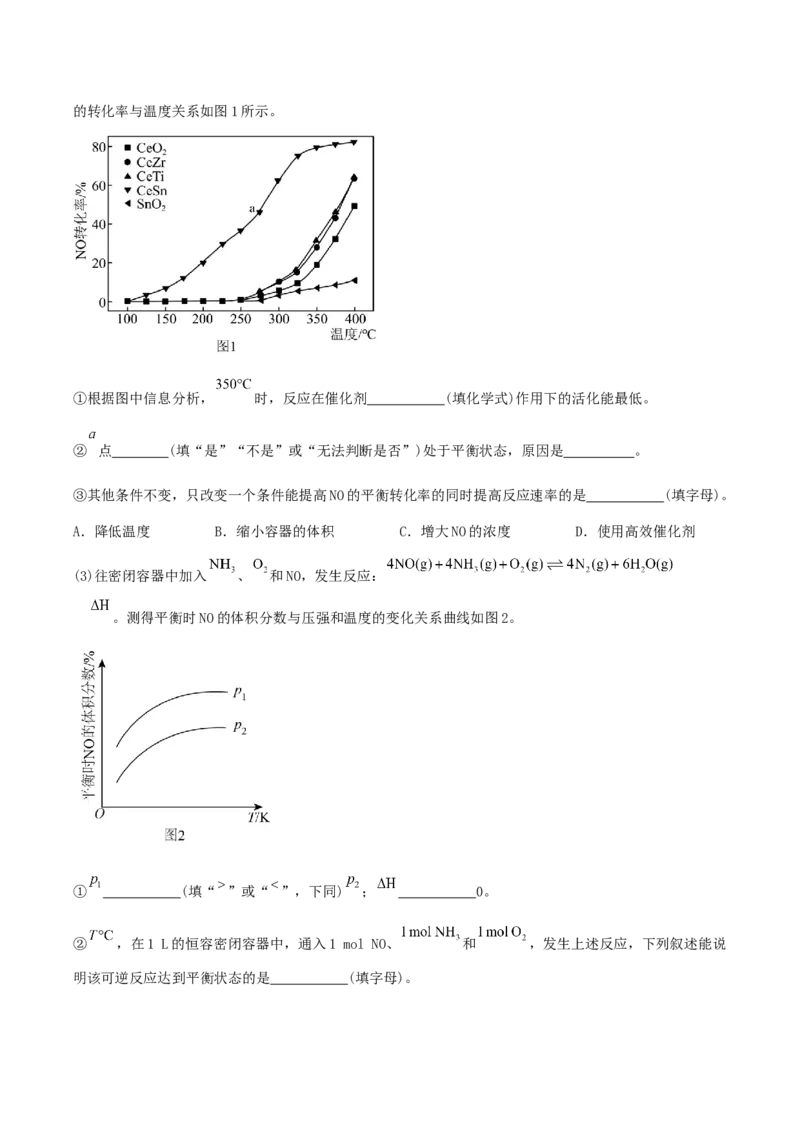
在体积为2 L的恒容密闭容器中,通入6 mol CO和4 mol NO,在不同催化剂作用下发生反应, 末NO的转化率与温度关系如图1所示。
①根据图中信息分析, 时,反应在催化剂 (填化学式)作用下的活化能最低。
② 点 (填“是”“不是”或“无法判断是否”)处于平衡状态,原因是 。
③其他条件不变,只改变一个条件能提高NO的平衡转化率的同时提高反应速率的是 (填字母)。
A.降低温度 B.缩小容器的体积 C.增大NO的浓度 D.使用高效催化剂
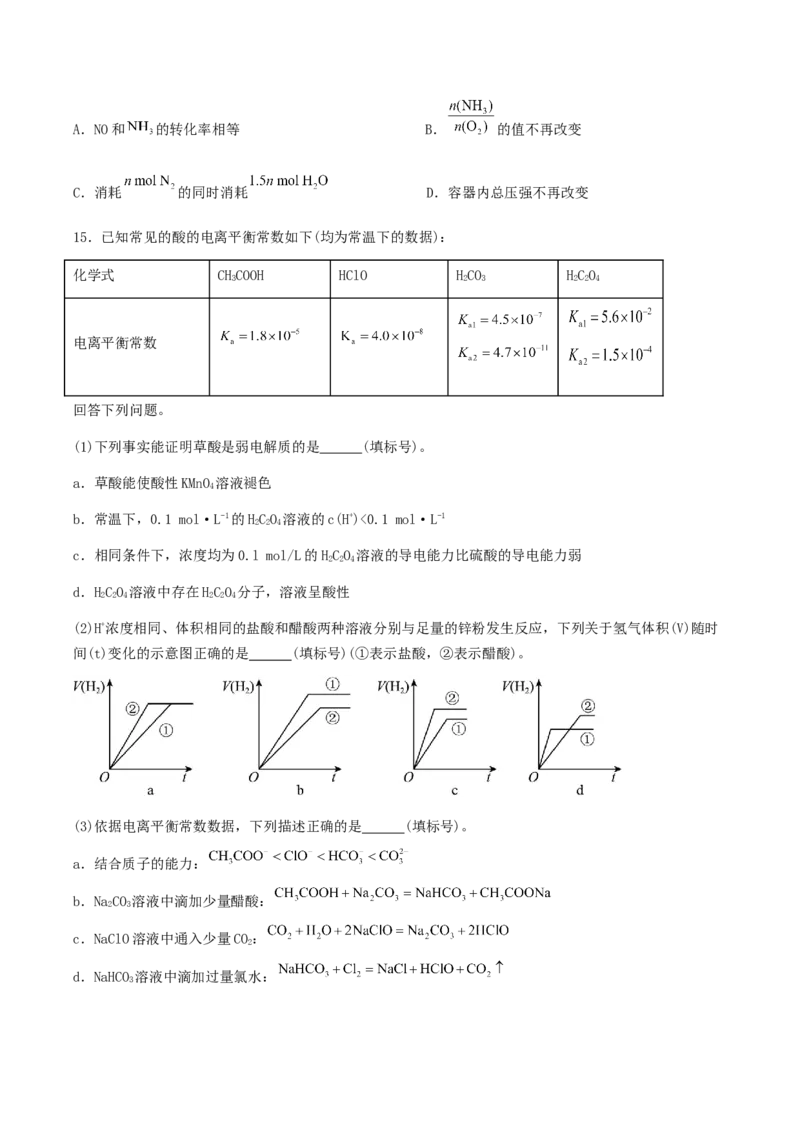
(3)往密闭容器中加入 、 和NO,发生反应:
。测得平衡时NO的体积分数与压强和温度的变化关系曲线如图2。
① (填“ ”或“ ”,下同) ; 0。
② ,在1 L的恒容密闭容器中,通入1 mol NO、 和 ,发生上述反应,下列叙述能说
明该可逆反应达到平衡状态的是 (填字母)。A.NO和 的转化率相等 B. 的值不再改变
C.消耗 的同时消耗 D.容器内总压强不再改变
15.已知常见的酸的电离平衡常数如下(均为常温下的数据):
化学式 CHCOOH HClO HCO HCO
3 2 3 2 2 4
电离平衡常数
回答下列问题。
(1)下列事实能证明草酸是弱电解质的是 (填标号)。
a.草酸能使酸性KMnO 溶液褪色
4
b.常温下,0.1 mol·L-1的HCO 溶液的c(H+)<0.1 mol·L-1
2 2 4
c.相同条件下,浓度均为0.l mol/L的HCO 溶液的导电能力比硫酸的导电能力弱
2 2 4
d.HCO 溶液中存在HCO 分子,溶液呈酸性
2 2 4 2 2 4
(2)H+浓度相同、体积相同的盐酸和醋酸两种溶液分别与足量的锌粉发生反应,下列关于氢气体积(V)随时
间(t)变化的示意图正确的是 (填标号)(①表示盐酸,②表示醋酸)。
(3)依据电离平衡常数数据,下列描述正确的是 (填标号)。
a.结合质子的能力:
b.NaCO 溶液中滴加少量醋酸:
2 3
c.NaClO溶液中通入少量CO:
2
d.NaHCO 溶液中滴加过量氯水:
3(4)常温下 溶液加水稀释后,下列各项中数值变大的是 (填标号)。
a. b. c. d.
(5)下列方法中,可以使 溶液中 电离程度增大的是 (填标号)。
a.加入少量 的稀盐酸 b.加热
c.加水稀释至 d.加入少量冰醋酸
(6)常温下,向 溶液中滴加 溶液至 溶液中 。
16.用磷铁渣(含 、 及少量杂质)制备 的方案如下:
(1)分离磷与铁。向磷铁渣粉中加入碳酸钠焙烧,生成 和 ,充分溶解后过滤,再经处理可得到
粗品 和 固体。写出焙烧过程中 发生的化学方程式 。
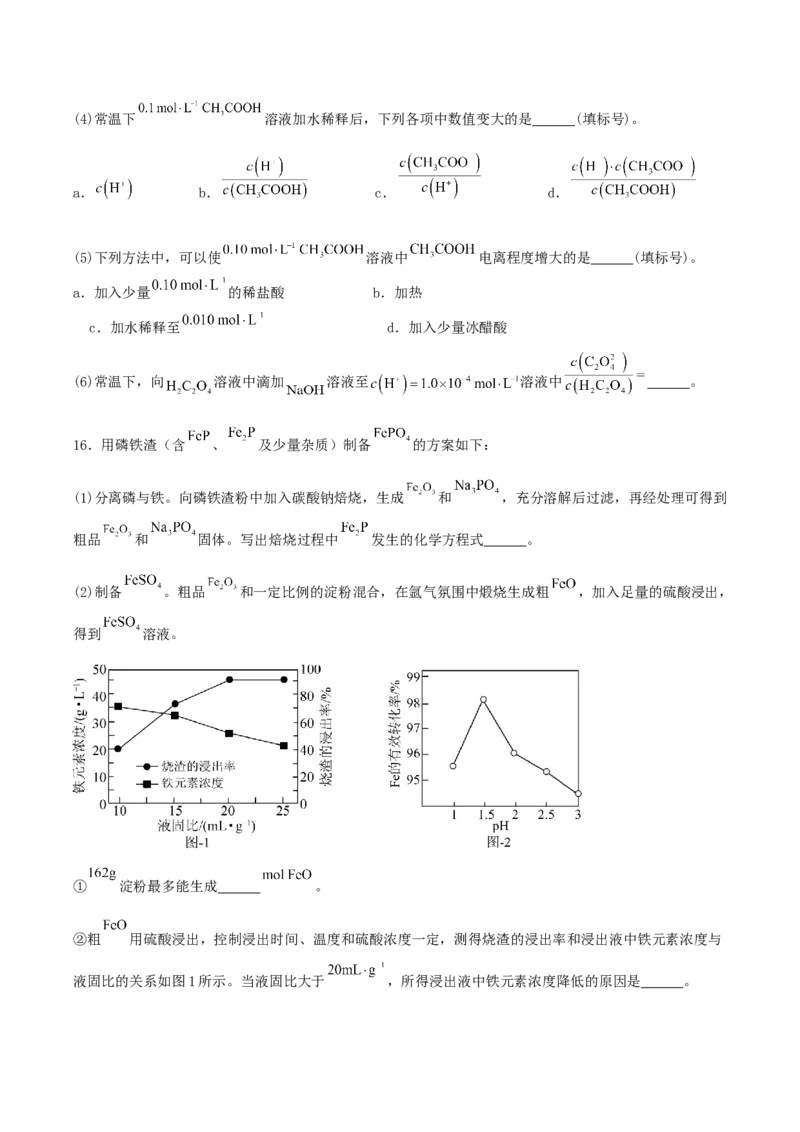
(2)制备 。粗品 和一定比例的淀粉混合,在氩气氛围中煅烧生成粗 ,加入足量的硫酸浸出,
得到 溶液。
① 淀粉最多能生成 。
②粗 用硫酸浸出,控制浸出时间、温度和硫酸浓度一定,测得烧渣的浸出率和浸出液中铁元素浓度与
液固比的关系如图1所示。当液固比大于 ,所得浸出液中铁元素浓度降低的原因是 。[已知烧渣的浸出率 ,液固比 ]
(3)制备 。其他条件一定,制备 时测得 的有效转化率 与溶液 的关系如
图2所示。请补充完整制备 的实验方案:取一定量已除杂后的 溶液,加入足量的 溶液,
,直至取所得溶液滴加 溶液不产生蓝色沉淀为止。 ,干燥,得到 (须使
用的试剂有: , , , )。
(4)测定粗品中 含量。准确称取 产品,加入足量硫酸溶解后配成 溶液。取 于锥
形瓶中,用 溶液滴定(反应原理为 ,未配平。
杂质不参与反应),恰好完全反应时,消耗 溶液 。计算产品中 的质量分数
(写出计算过程)。
17.尿素 为农业生产常用氮肥。回答下列问题:
I.工业合成
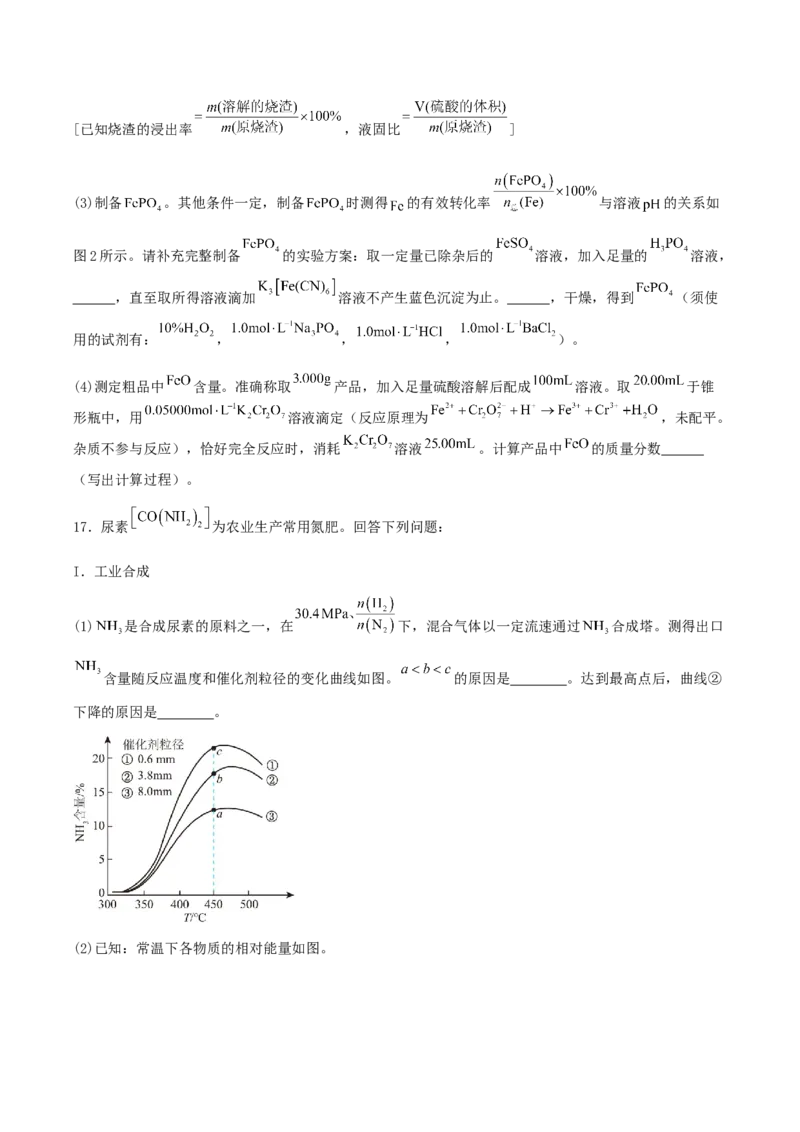
(1) 是合成尿素的原料之一,在 下,混合气体以一定流速通过 合成塔。测得出口
含量随反应温度和催化剂粒径的变化曲线如图。 的原因是 。达到最高点后,曲线②
下降的原因是 。
(2)已知:常温下各物质的相对能量如图。则反应 的 。
(3)模拟工业合成尿素。高温高压下,存在如下液相平衡体系。
主反应:
副反应:
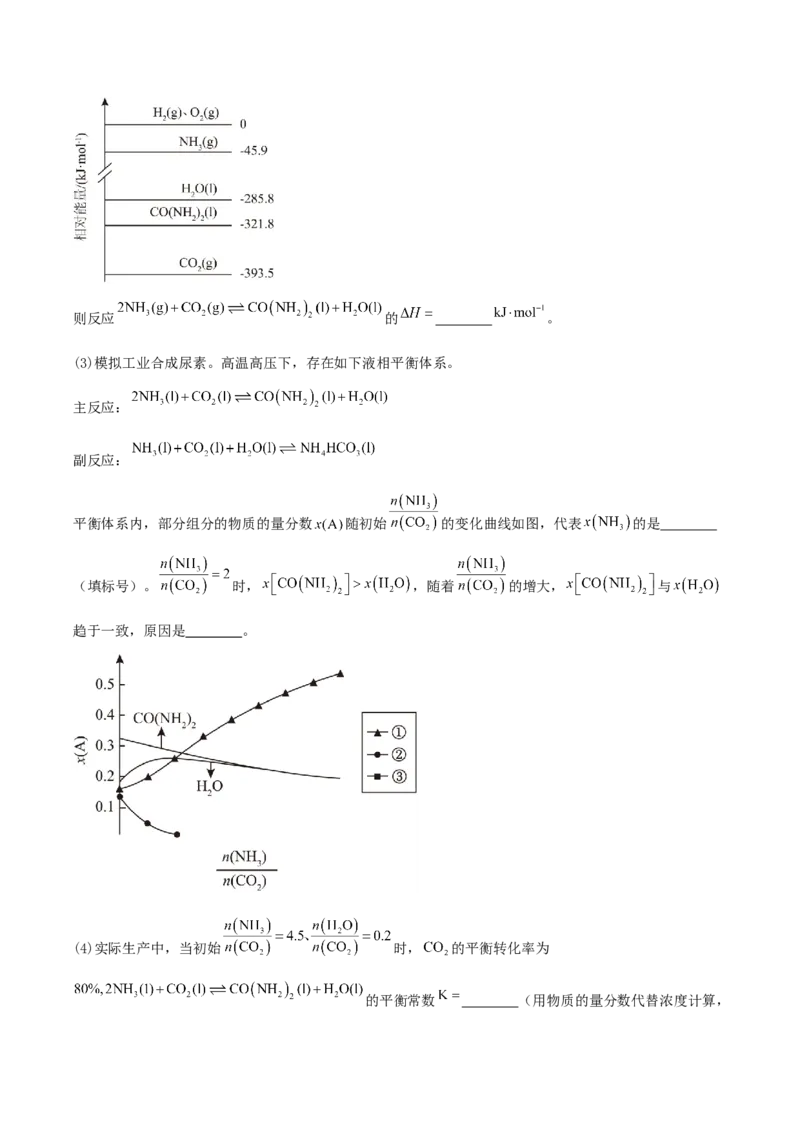
平衡体系内,部分组分的物质的量分数 随初始 的变化曲线如图,代表 的是
(填标号)。 时, ,随着 的增大, 与
趋于一致,原因是 。
(4)实际生产中,当初始 时, 的平衡转化率为
的平衡常数 (用物质的量分数代替浓度计算,忽略副反应,保留1位小数)。
Ⅱ.电催化合成
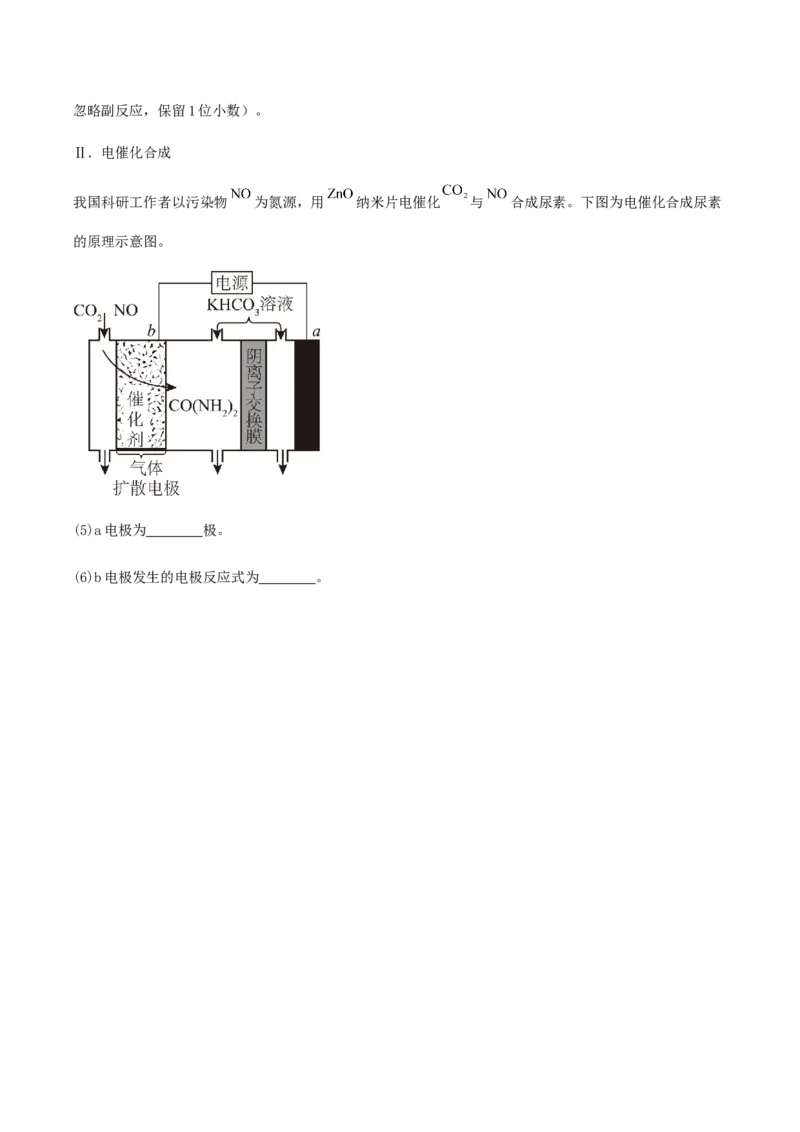
我国科研工作者以污染物 为氮源,用 纳米片电催化 与 合成尿素。下图为电催化合成尿素
的原理示意图。
(5)a电极为 极。
(6)b电极发生的电极反应式为 。