文档内容
济宁市实验中学 2022 级高三 10 月月考化学试题
注意事项:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间90分钟。
2.答题前,考生务必将姓名、班级等个人信息填写在答题卡指定位置。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对
应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题
区域内作答。超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
可能用到的相对原子质量:H:1 C:12 O:16 Na:23 Cl:35.5 Fe:56
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1. 汉·陈琳《武军赋》:“铠则东胡阙巩,百炼精钢”。下列说法正确的是
A. 钢是合金,合金是指含有两种或两种以上金属的混合物
B. 百炼成钢的过程就是改变生铁中碳含量的过程
C. 铁比铜活泼,铁的发现、大量冶炼和使用均早于铜
D. 铁是比较活泼的金属,自然界中不存在游离态的铁
【答案】B
【解析】
【详解】A.钢是铁和碳的合金,合金是两种或两种以上金属、或金属与非金属熔合而成的具有金属特性
的物质,A错误;
B.百炼成钢的过程就是使生铁中碳含量降低的过程,B正确;
C.铁比铜活泼,铜的冶炼、使用均早于铁,C错误;
D.铁是比较活泼的金属,容易与氧气等发生反应,陨铁中存在游离态的铁,D错误;
故选B。
2. 在生活中,化学知识起了重要作用。下列说法正确的是
A. 食品中放入盛有硅胶颗粒的小袋,可以防止食品被氧化
B. “84”消毒液是以NaClO为有效成分的消毒液,与盐酸混合可以提升消毒效果
C. 葡萄酒酿制过程中添加少量 ,起到杀菌抗氧化作用
D. 可以用醋酸和淀粉溶液检验加碘盐中的
【答案】C
【解析】【详解】A.食品中放入盛有硅胶颗粒小袋的目的是防止食品受潮变质,A错误;
B.“84”消毒液的主要成分次氯酸钠能与盐酸反应生成有毒的氯气,所以“84”消毒液不能与盐酸混合,可
能会发生意外事故,B错误;
C. 可以在葡萄酒酿制过程中起到杀菌抗氧化作用,C正确;
D.淀粉遇到单质碘显蓝色,醋酸与 不能生成碘单质,淀粉溶液遇到 无现象,D错误;
故选C。
3. 镁和铝都是较活泼的金属,下列叙述正确的是
A. 第一电离能:
B. 工业上常通过电解 溶液的方法制取金属
C. 将 溶液蒸干可制得无水
D. 历史上曾用反应: 制铝;现代工业用反应:
制铷,所以活动性:
【答案】A
【解析】
【详解】A.Mg的价电子为3s2,s轨道全满,比较稳定,较难失去电子,因此第一电离能大于Al,A正确;
B.电解MgCl 溶液得到Mg(OH) 、H、Cl,电解熔融的MgCl 可以制得Mg,B错误;
2 2 2 2 2
C.由于Al3+水解,且HCl易挥发,蒸干AlCl 溶液得到的是Al(OH) ,C错误;
3 3
D.Mg置换Rb的反应有一定的可逆性,将生成的Rb蒸气抽出使平衡正向移动,与Mg、Rb的金属活动性
无关,D错误;
故选A。
4. 物质的性质决定其用途,下列有关物质性质和应用的关系正确的是
A. SiO 是酸性氧化物,能用氢氟酸(HF)雕刻玻璃
2
B. 碳酸氢铵受热易分解,可用作植物生长的肥料
C. 钠能与水剧烈反应,可用作95%乙醇的强除水剂D. BeO熔点高,可用作耐火材料
【答案】D
【解析】
【详解】A.HF能与SiO 反应,可以用氢氟酸雕刻玻璃,但是与SiO 是酸性氧化物无关,A错误;
2 2
B.碳酸氢铵中含氮元素,可用作植物生长的肥料,与其受热易分解无关,B错误;
C.钠与乙醇会反应,故不能用作95%乙醇的强除水剂,C错误;
D.BeO为离子晶体,半径小,熔点高,可用作耐火材料,D正确;
故选D。
5. 下列反应原理中,不符合工业冶炼金属实际情况的是
A. B.
C. D.
【答案】A
【解析】
【详解】A.Mg为活泼金属,通常用电解熔融的氯化镁的方法冶炼,A错误;
B.Fe处于金属活动性顺序表中处于中间位置的金属,通常是用还原剂(C、CO、H、活泼金属等)将金属
2
从其化合物中还原出来,B正确;
C.Hg为不活泼金属,可以直接用加热分解的方法将金属从其化合物中还原出来,C正确;
D.Al为活泼金属,通常用电解熔融的氧化铝的方法冶炼,D正确;
故选A。
6. 金属及其化合物转化关系是化学学习的重要内容之一。下列各组物质的转化关系中不全部是通过一步反
应完成的是
A. Na→NaOH→Na CO→NaCl B. Al→Al O→Al(OH) →A1Cl
2 3 2 3 3 3
C. Mg→MgCl →Mg(OH) →MgSO D. Fe→Fe(NO )→Fe (OH) →Fe O
2 2 4 3 3 3 2 3
【答案】B
【解析】
【详解】A.钠和水反应生成氢氧化钠,氢氧化钠与二氧化碳反应生成碳酸钠,碳酸钠与盐酸反应生成氯化
钠,能一步完成,A项不符合;
B.氧化铝和水不反应,所以氧化铝不能通过一步反应生成氢氧化铝,B项符合题意;C.镁与盐酸生成氯化镁,氯化镁与氢氧化钠反应生成氢氧化镁,氢氧化镁与硫酸反应生成硫酸镁,能一步
完成,C项不符合;
D.铁与过量的稀硝酸生成硝酸铁,硝酸铁与氢氧化钠生成氢氧化铁,氢氧化铁受热分解生成氧化铁,能一
步完成,D项不符合;
答案选B。
7. “褪色”是高中化学实验中一种常见且重要的现象。以下实验中的“褪色”现象与所得结论相匹配的是
选
实验操作 结论
项
A 向滴有酚酞的 溶液中通入Cl Cl 具有漂白性
2 2
B 向酸性 液中滴入乙醇 乙醇具有还原性
C 向滴有碘水的淀粉溶液中通入SO SO 具有漂白性
2 2
D 向 与 的混合溶液中加入铁粉 比 更易与 配位
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A.向滴有酚酞的 溶液中通入Cl 生成氯化钠、次氯酸钠和水,碱性减弱,溶液褪色,不
2
能证明Cl 具有漂白性,A错误;
2
B.向酸性 液中滴入乙醇,乙醇具有还原性使酸性高锰酸钾溶液褪色,B正确;
C.向滴有碘水的淀粉溶液中通入SO ,发生 ,体现了SO 具有还原性,C
2 2
错误;
D.向 与 的混合溶液中加入铁粉,发生反应 ,不是Fe比 更易与
配位,D错误;
故选B。
8. 根据海水综合利用的工业流程图,判断下列说法正确的是已知: 受热生成 和HCl气体等。
A. 过程①的除杂试剂先后顺序及操作是 、 、稀盐酸,过滤、蒸发结晶
B. 在过程③中将 灼烧即可制得无水
C. 过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题
D. 在过程④、⑥反应中每氧化0.4mol 需消耗4.48L
【答案】C
【解析】
【分析】海水蒸发得到粗盐和母液,粗盐通过精制得到精盐,电解饱和食盐水得到氯气、氢气和NaOH,
母液加氢氧化钙反应生成氢氧化镁沉淀,氢氧化镁与盐酸反应后经过蒸发浓缩、冷却结晶等操作生成
MgCl ·6H O,MgCl ·6H O在HCl气流中加热生成无水MgCl ,NaBr中通入氯气生成Br ,Br 与SO 水溶
2 2 2 2 2 2 2 2
液反应生成溴离子,溴离子被氯气氧化生成高浓度的Br 。
2
【详解】A.过程①中氯化钡须在碳酸钠之前加入,否则无法除去多余的钡离子,同时还需要加入氢氧化
钠除去镁离子,A错误;
B.MgCl ·6H O受热生成Mg(OH)Cl和HCl,过程③需要在HCl气流中加热使MgCl ·6H O失去结晶水生成
2 2 2 2
无水MgCl ,B错误;
2
C.Br 与SO 的水溶液反应生成HBr和HSO ,两种产物都是强酸,因此反应后溶液呈强酸性,生产中需
2 2 2 4
解决其对设备的腐蚀问题,C正确;
D.过程④、⑥中反应的离子方程式为2Br-+Cl=Br +2Cl-,每氧化0.4mol溴离子需消耗氯气0.2mol,但是
2 2
选项中并未说明是标准状况下,无法计算0.2mol氯气的体积,D错误;
故答案选C。
9. 下列关于实验室制取SO 的实验,其中叙述正确的是
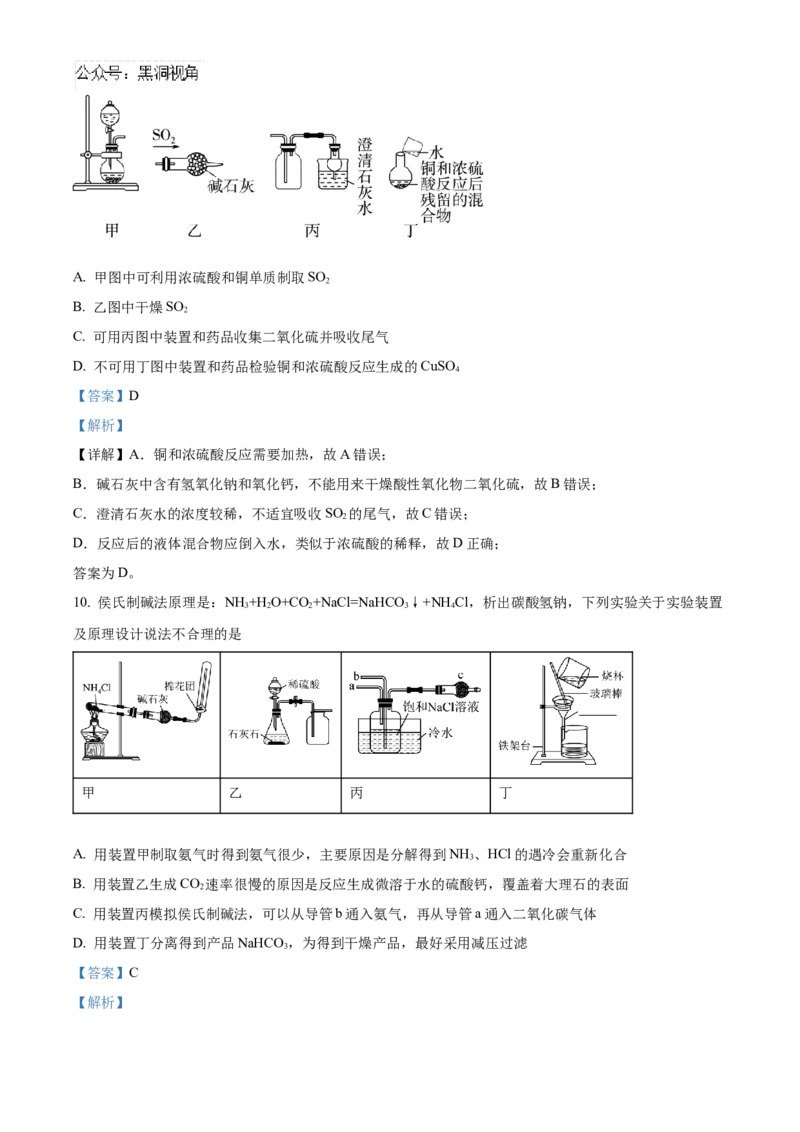
2A. 甲图中可利用浓硫酸和铜单质制取SO
2
B. 乙图中干燥SO
2
C. 可用丙图中装置和药品收集二氧化硫并吸收尾气
D. 不可用丁图中装置和药品检验铜和浓硫酸反应生成的CuSO
4
【答案】D
【解析】
【详解】A.铜和浓硫酸反应需要加热,故A错误;
B.碱石灰中含有氢氧化钠和氧化钙,不能用来干燥酸性氧化物二氧化硫,故B错误;
C.澄清石灰水的浓度较稀,不适宜吸收SO 的尾气,故C错误;
2
D.反应后的液体混合物应倒入水,类似于浓硫酸的稀释,故D正确;
答案为D。
10. 侯氏制碱法原理是:NH +H O+CO+NaCl=NaHCO ↓+NHCl,析出碳酸氢钠,下列实验关于实验装置
3 2 2 3 4
及原理设计说法不合理的是
甲 乙 丙 丁
A. 用装置甲制取氨气时得到氨气很少,主要原因是分解得到NH 、HCl的遇冷会重新化合
3
B. 用装置乙生成CO 速率很慢的原因是反应生成微溶于水的硫酸钙,覆盖着大理石的表面
2
C. 用装置丙模拟侯氏制碱法,可以从导管b通入氨气,再从导管a通入二氧化碳气体
D. 用装置丁分离得到产品NaHCO ,为得到干燥产品,最好采用减压过滤
3
【答案】C
【解析】【分析】
【详解】A.氯化铵分解后生成氨气和氯化氢,两种气体在试管口重新化合生成氯化铵,则用装置甲制取
氨气时得到氨气的量很少,故A正确;
B.生成硫酸钙微溶,包裹在碳酸钙表面,则装置乙制取二氧化碳时,往往反应不充分,大理石利用率太
低,故B正确;
C.氨气极易溶于水,故应该a管通入氨气,b管通入二氧化碳,故C错误;
D.用装置丁过滤分离得到产品 NaHCO ,减压过滤,可防止碳酸氢钠分解,故D正确;
3
故答案选C。
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题意,全
都选对得4分,选对但不全的得2分,有选错的得0分。
11. 用如图装置制备次氯酸并验证其氧化性,Cl 可以与含水碳酸钠反应得到ClO气体和NaHCO ,下列说
2 2 3
法错误的是( )
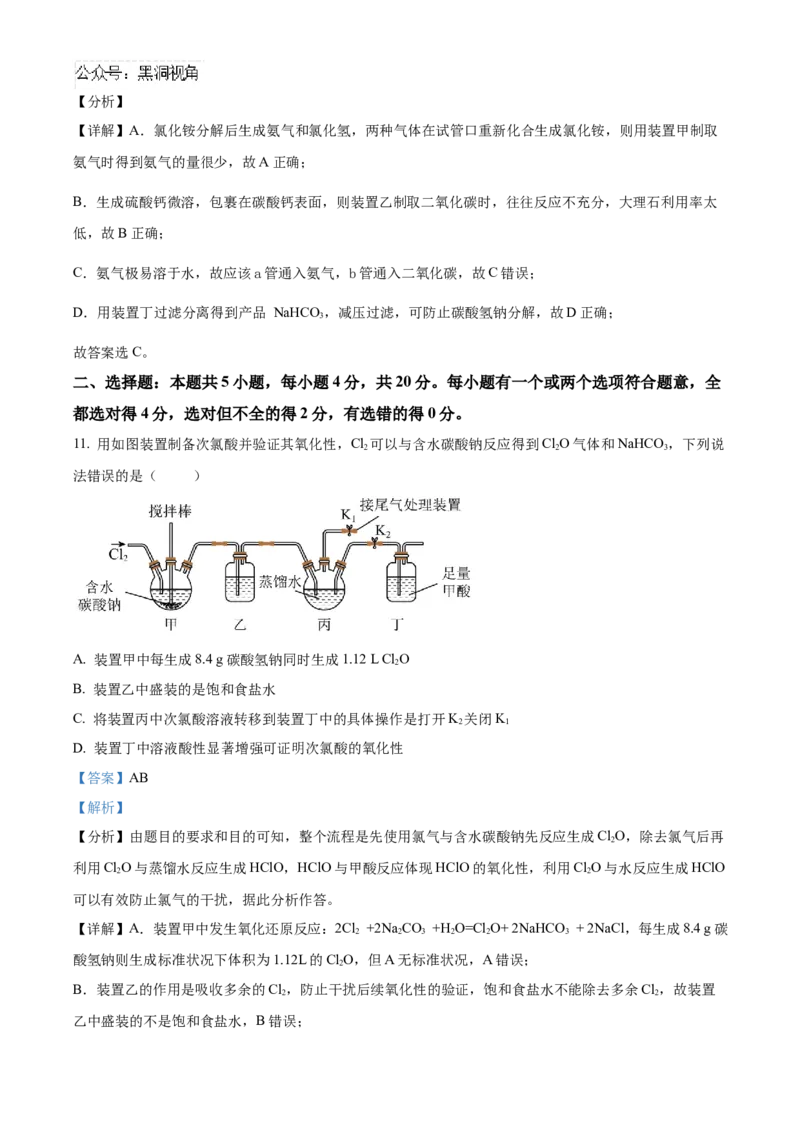
A. 装置甲中每生成8.4 g碳酸氢钠同时生成1.12 L Cl O
2
B. 装置乙中盛装的是饱和食盐水
C. 将装置丙中次氯酸溶液转移到装置丁中的具体操作是打开K 关闭K
2 1
D. 装置丁中溶液酸性显著增强可证明次氯酸的氧化性
【答案】AB
【解析】
【分析】由题目的要求和目的可知,整个流程是先使用氯气与含水碳酸钠先反应生成ClO,除去氯气后再
2
利用ClO与蒸馏水反应生成HClO,HClO与甲酸反应体现HClO的氧化性,利用ClO与水反应生成HClO
2 2
可以有效防止氯气的干扰,据此分析作答。
【详解】A.装置甲中发生氧化还原反应:2Cl +2Na CO +H O=Cl O+ 2NaHCO + 2NaCl,每生成8.4 g碳
2 2 3 2 2 3
酸氢钠则生成标准状况下体积为1.12L的ClO,但A无标准状况,A错误;
2
B.装置乙的作用是吸收多余的Cl,防止干扰后续氧化性的验证,饱和食盐水不能除去多余Cl,故装置
2 2
乙中盛装的不是饱和食盐水,B错误;C.装置丙中打开K,关闭K,可以利用压强能将装置中的液体压入装置丁中,使生成的HClO与甲酸反
2 1
应,C正确;
D.装置丁中溶液酸性显著,说明发生反应HClO+ HCOOH=HCl+CO ↑+H O,可证明次氯酸的氧化性,D
2 2
正确;
故答案为:AB。
12. 硫酸是重要化工原料,工业生产制取硫酸的原理示意图如下。
下列说法不正确的是
A. I的化学方程式:
B. Ⅱ中的反应条件都是为了提高 平衡转化率
C. 将黄铁矿换成硫黄可以减少废渣的产生
D. 生产过程中产生的尾气可用碱液吸收
【答案】B
【解析】
【分析】黄铁矿和空气中的O 在加热条件下发生反应,生成SO 和Fe O,SO 和空气中的O 在
2 2 3 4 2 2
400~500℃、常压、催化剂的作用下发生反应得到SO ,用98.3%的浓硫酸吸收SO ,得到HSO 。
3 3 2 4
【详解】A.反应I是黄铁矿和空气中的O 在加热条件下发生反应,生成SO 和Fe O,化学方程式:
2 2 3 4
,故A正确;
B.反应Ⅱ条件要兼顾平衡转化率和反应速率,还要考虑生产成本,如Ⅱ中“常压、催化剂”不是为了提高
平衡转化率,故B错误;
C.将黄铁矿换成硫黄,则不再产生 ,即可以减少废渣产生,故C正确;
D.硫酸工业产生的尾气为 、 ,可以用碱液吸收,故D正确;
故选B。
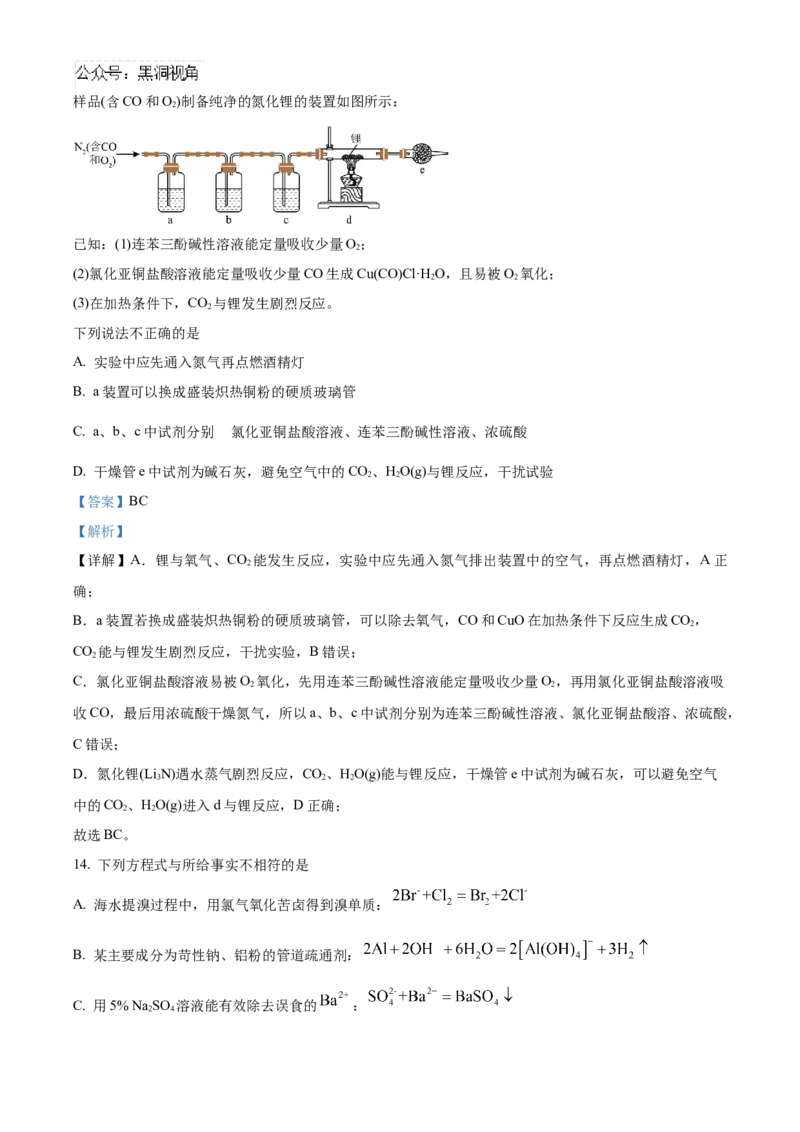
13. 氮化锂(Li N) 常作固体电解质和催化剂,遇水蒸气剧烈反应生成氢氧化锂和氨气。某实验小组用氮气
3样品(含CO和O)制备纯净的氮化锂的装置如图所示:
2
已知:(1)连苯三酚碱性溶液能定量吸收少量O;
2
(2)氯化亚铜盐酸溶液能定量吸收少量CO生成Cu(CO)Cl·H O,且易被O 氧化;
2 2
(3)在加热条件下,CO 与锂发生剧烈反应。
2
下列说法不正确的是
A. 实验中应先通入氮气再点燃酒精灯
B. a装置可以换成盛装炽热铜粉的硬质玻璃管
为
C. a、b、c中试剂分别 氯化亚铜盐酸溶液、连苯三酚碱性溶液、浓硫酸
D. 干燥管e中试剂为碱石灰,避免空气中的CO、HO(g)与锂反应,干扰试验
2 2
【答案】BC
【解析】
【详解】A.锂与氧气、CO 能发生反应,实验中应先通入氮气排出装置中的空气,再点燃酒精灯,A正
2
确;
B.a装置若换成盛装炽热铜粉的硬质玻璃管,可以除去氧气,CO和CuO在加热条件下反应生成CO,
2
CO 能与锂发生剧烈反应,干扰实验,B错误;
2
C.氯化亚铜盐酸溶液易被O 氧化,先用连苯三酚碱性溶液能定量吸收少量O,再用氯化亚铜盐酸溶液吸
2 2
收CO,最后用浓硫酸干燥氮气,所以a、b、c中试剂分别为连苯三酚碱性溶液、氯化亚铜盐酸溶、浓硫酸,
C错误;
D.氮化锂(Li N)遇水蒸气剧烈反应,CO、HO(g)能与锂反应,干燥管e中试剂为碱石灰,可以避免空气
3 2 2
中的CO、HO(g)进入d与锂反应,D正确;
2 2
故选BC。
14. 下列方程式与所给事实不相符的是
A. 海水提溴过程中,用氯气氧化苦卤得到溴单质:
B. 某主要成分为苛性钠、铝粉的管道疏通剂:
C. 用5% Na SO 溶液能有效除去误食的 :
2 4D. 泡沫灭火器灭火原理:
【答案】D
【解析】
【详解】A.海水提溴过程中,用氯气氧化苦卤得到溴单质离子方程式: ,故A正
确;
B.主要成分为苛性钠、铝粉的管道疏通剂反应的离子方程式:
,故B正确;
C.用5% Na SO 溶液除去误食的 离子方程式: ,故C正确;
2 4
D.泡沫灭火器灭火原理离子方程式: ,故D错误;
故选D。
15. 氮化钙 是一种重要的化学试剂。某化学兴趣小组用如图所示装置(部分夹持装置已略去)制备
(易与水反应),下列说法错误的是
A. 与水反应主要生成氢氧化钙和肼
B. 实验开始前,首先应检查装置的气密性
C. 实验中每消耗 ,同时消耗
D. 前后两处浓硫酸的作用分别是干燥 及防止空气中的水进入装置乙
【答案】AC【解析】
【分析】本实验利用氮气和钙反应制备氮化钙。装置甲为制备氮气的装置,发生的反应是:
,浓硫酸干燥氮气,乙中为制备装置,由于氮化钙与水易反应,最后一处的浓
硫酸可以防止空气中的水蒸气进入装置乙。
【详解】A. 与水发生非氧化还原反应生成氢氧化钙和氨气,A错误;
B.该装置要制备气体,实验开始前要检查装置的气密性,B正确;
C.实验进行过程中,每消耗6gCa,转移电子的物质的量为 ,亚硝酸根中N元素为+3
价,1mol亚硝酸根参与反应转移电子物质的量为3mol,故消耗亚硝酸根的物质的量为0.1mol,C错误;
D.据以上分析可知,前后两处浓硫酸的作用分别是干燥N 及防止空气中的水进入装置乙,D正确;
2
故选AC。
三、非选择题:本题共5小题,共60分
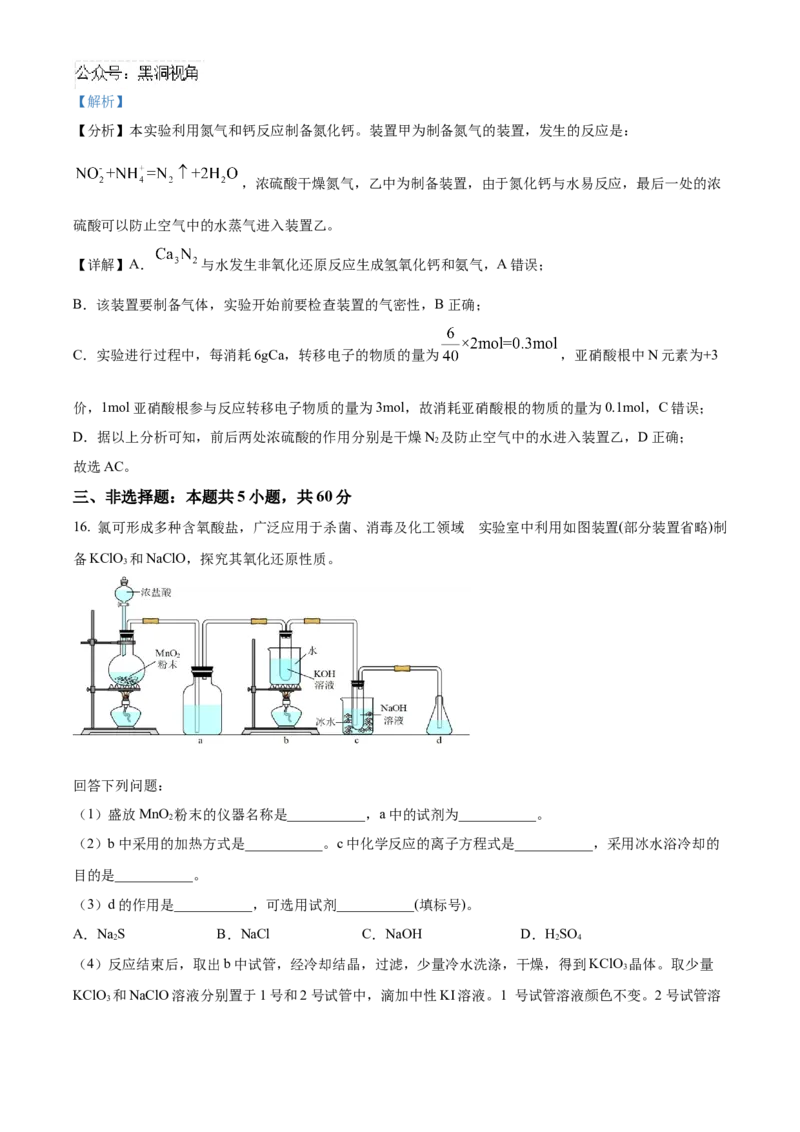
16. 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域 。实验室中利用如图装置(部分装置省略)制
备KClO 和NaClO,探究其氧化还原性质。
3
回答下列问题:
(1)盛放MnO 粉末的仪器名称是___________,a中的试剂为___________。
2
(2)b中采用的加热方式是___________。c中化学反应的离子方程式是___________,采用冰水浴冷却的
目的是___________。
(3)d的作用是___________,可选用试剂___________(填标号)。
A.NaS B.NaCl C.NaOH D.HSO
2 2 4
(4)反应结束后,取出b中试管,经冷却结晶,过滤,少量冷水洗涤,干燥,得到KClO 晶体。取少量
3
KClO 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1 号试管溶液颜色不变。2号试管溶
3液变为棕色,加入CCl 振荡,静置后CCl 层显___________色。可知该条件下KClO 的氧化能力
4 4 3
___________(填“大于”或“小于”)NaClO。
(5)84消毒液的有效成分为NaClO,不可与酸性清洁剂混用的原因是___________(用离子方程式表示)。
【答案】(1) ①. 圆底烧瓶 ②. 饱和食盐水
(2) ①. 水浴加热 ②. Cl+2OH-=Cl-+ClO-+H O ③. 避免生成NaClO
2 2 3
(3) ①. 吸收尾气(Cl ),防止污染环境 ②. AC
2
(4) ①. 紫 ②. 小于
(5)ClO-+Cl-+2H+=Cl↑+H O
2 2
【解析】
【分析】由装置图可知,浓盐酸和二氧化锰在加热条件下反应制取氯气,a装置可除去氯气中混有的氯化
氢,应盛有饱和食盐水,b装置中在水浴加热条件下氯气与KOH溶液反应制备KClO,c装置中在冰水浴
3
条件下氯气与NaOH溶液反应制备NaClO,d装置用来吸收尾气,防止空气污染。
【小问1详解】
由装置图可知,盛放MnO 粉末的仪器是圆底烧瓶;浓盐酸和二氧化锰在加热条件下反应制取氯气,产生
2
的氯气中混有氯化氢杂质,除去氯化氢需要将气体通过饱和食盐水,故a中的试剂为饱和食盐水。
【小问2详解】
b装置的加热方式为水浴加热。c装置中氯气与氢氧化钠发生反应的离子方程式为Cl+2OH-=ClO-+Cl-
2
+H O。温度较高时会生成氯酸钠,故采用冰水浴冷却的目的是避免生成NaClO。
2 3
【小问3详解】
的
氯气有毒,能污染空气,反应后剩余 氯气要进行尾气吸收,d是尾气处理装置,吸收尾气(Cl ),防止污
2
染环境;氯气能与NaS反应生成氯化钠和硫单质,也能与NaOH溶液反应生成氯化钠、次氯酸钠和水,与
2
NaCl、HSO 均不反应,所以吸收氯气可以用NaS溶液、氢氧化钠溶液,故选AC。
2 4 2
【小问4详解】
2号试管溶液变为棕色,说明生成了碘,加入CCl 振荡,发生萃取,静置后CCl 层显紫色。取少量KClO
4 4 3
和NaClO溶液分别滴加到1号和2号试管中,滴加KI溶液,1号试管颜色不变,2号变为棕色,说明2号
生成了碘,可知该条件下KClO 的氧化能力小于NaClO。
3
【小问5详解】
84消毒液的有效成分为NaClO,还含由氯化钠,在酸性条件下,溶液中的氯离子和次氯酸根离子发生归中
反应生成氯气,故不可与酸性清洁剂混用的原因是ClO-+Cl-+2H+=Cl↑+H O。
2 2
17. KCr O 是一种重要的化工原料。以铬铁矿(主要成分为FeO·Cr O,还含有Al O 等杂质)为原料制备
2 2 7 2 3 2 3KCr O 的一种工艺流程如下:
2 2 7
已知:(a)Cr O +HO 2CrO +2H+
2 2
(b)不同温度下各物质的溶解度:
物质 KCl NaCl KCr O NaCr O
2 2 7 2 2 7
溶解度(g/100g H O) 0 ℃ 28 35.7 4.7 163
2
40 ℃ 40.1 36.4 26.3 215
80 ℃ 51.3 38 70 376
(c)步骤①的主要反应为:2FeO·Cr O+4NaCO+7NaNO 4NaCrO+Fe O+4CO↑+7NaNO
2 3 2 3 3 2 4 2 3 2 2。
(1)“滤渣1”和“滤渣2”的主要成分分别是___________、___________(填化学式)。写出步骤③的离子反应
方程式___________;步骤④中调pH,以下试剂可选用___________(填标号)。
a.NH B.KOH C.CHCOOH D.HCl
3 3
(2)在步骤⑤中加入适量KCl,___________,过滤得到KCr O 固体。
2 2 7
(3)某工厂用a kg铬铁矿粉(含Cr O 40%)制KCr O,最终得到产品b kg,产率为___________×100%(列
2 3 2 2 7
计算式)。
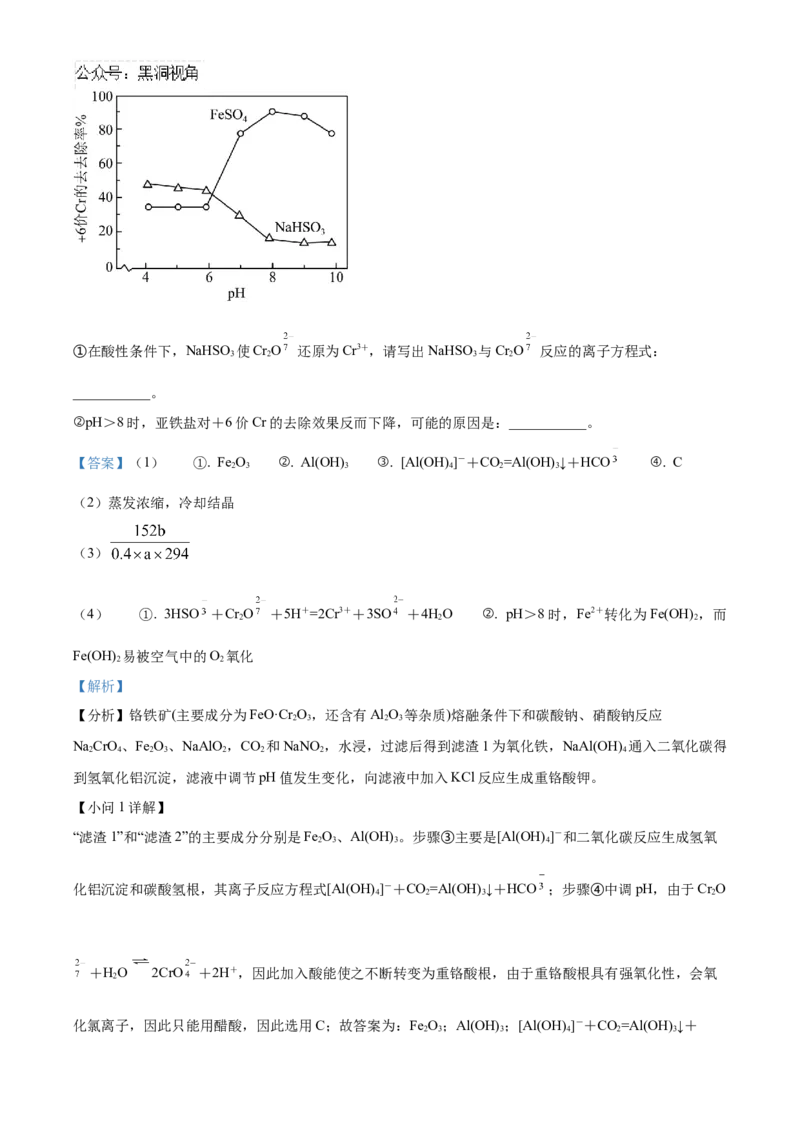
(4)化学还原法可除去废水中的Cr O ,取含Cr O 的模拟水样在不同pH条件下,分别向每个水样中
2 2
加一定量的FeSO 、NaHSO,搅拌,充分反应,然后滴加Ca(OH) 悬浊液,静置沉淀,测定+6价Cr的去
4 3 2
除率,实验结果如图所示。①在酸性条件下,NaHSO 使Cr O 还原为Cr3+,请写出NaHSO 与Cr O 反应的离子方程式:
3 2 3 2
___________。
②pH>8时,亚铁盐对+6价Cr的去除效果反而下降,可能的原因是:___________。
【答案】(1) ①. Fe O ②. Al(OH) ③. [Al(OH) ]-+CO=Al(OH) ↓+HCO ④. C
2 3 3 4 2 3
(2)蒸发浓缩,冷却结晶
(3)
(4) ①. 3HSO +Cr O +5H+=2Cr3++3SO +4HO ②. pH>8时,Fe2+转化为Fe(OH) ,而
2 2 2
Fe(OH) 易被空气中的O 氧化
2 2
【解析】
【分析】铬铁矿(主要成分为FeO·Cr O,还含有Al O 等杂质)熔融条件下和碳酸钠、硝酸钠反应
2 3 2 3
NaCrO、Fe O、NaAlO ,CO 和NaNO ,水浸,过滤后得到滤渣1为氧化铁,NaAl(OH) 通入二氧化碳得
2 4 2 3 2 2 2 4
到氢氧化铝沉淀,滤液中调节pH值发生变化,向滤液中加入KCl反应生成重铬酸钾。
【小问1详解】
“滤渣1”和“滤渣2”的主要成分分别是Fe O、Al(OH) 。步骤③主要是[Al(OH) ]-和二氧化碳反应生成氢氧
2 3 3 4
化铝沉淀和碳酸氢根,其离子反应方程式[Al(OH) ]-+CO=Al(OH) ↓+HCO ;步骤④中调pH,由于Cr O
4 2 3 2
+HO 2CrO +2H+,因此加入酸能使之不断转变为重铬酸根,由于重铬酸根具有强氧化性,会氧
2
化氯离子,因此只能用醋酸,因此选用C;故答案为:Fe O;Al(OH) ;[Al(OH) ]-+CO=Al(OH) ↓+
2 3 3 4 2 3HCO ;C。
【小问2详解】
在步骤⑤中加入适量KCl,得到KCr O 溶液,根据不同温度不同物质的溶解度,通过蒸发浓缩,冷却结
2 2 7
晶,过滤得到KCr O 固体;故答案为:蒸发浓缩,冷却结晶。
2 2 7
【小问3详解】
某工厂用a kg铬铁矿粉(含Cr O 40%)制KCr O,根据Cr O~KCr O,理论得到KCr O 的质量为最终
2 3 2 2 7 2 3 2 2 7 2 2 7
得到产品b kg,产率为 ;故答案为: 。
【小问4详解】
①在酸性条件下,NaHSO 使Cr O 还原为Cr3+,HSO 被氧化为SO ,根据得失电子守恒、质量守恒和
3 2
电荷守恒得到NaHSO 与Cr O 反应的离子方程式:3HSO +Cr O +5H+=2Cr3++3SO +4HO;故答
3 2 2 2
案为:3HSO +Cr O +5H+=2Cr3++3SO +4HO。
2 2
②pH>8时,亚铁盐对+6价Cr的去除效果反而下降,可能的原因是pH>8时,Fe2+转化为Fe(OH) ,而
2
Fe(OH) 易被空气中的O 氧化,导致亚铁离子浓度降低,与重铬酸根反应减少;故答案为:是pH>8时,
2 2
Fe2+转化为Fe(OH) ,而Fe(OH) 易被空气中的O 氧化。
2 2 2
18. (三草酸合铁酸钾)是制备负载型活性铁催化剂的主要原料。回答下列问题:
Ⅰ.现利用如下装置检验三草酸合铁酸钾受热分解所得产物中是否含有 , 。
(1)正确的连接顺序为___________(填小写标号,仪器可重复使用)。
(2)实验过程中需持续通入 的目的是___________、___________。(3)证明产物中有 的现象是___________。
Ⅱ.测定三草酸合铁酸钾中铁元素的含量。
(4)称取 三草酸合铁酸钾样品,配成 待测溶液,所需玻璃仪器除烧杯、玻璃棒、量筒外还有
___________(填仪器名称)。
(5)取 上述溶液于锥形瓶中,加入稀硫酸酸化,再滴加 溶液至与 恰好反应,反应
的离子方程式为___________。
(6)向(5)反应后溶液中加入适量还原剂将 恰好完全还原为 ,加入稀硫酸酸化后,继续加
溶液时恰好与 反应。晶体中铁元素的质量分数表达式为___________。
【答案】(1)
(2) ①. 排尽装置中空气 ②. 使反应产生的气体全部进入后续装置
(3)E中澄清石灰水不变浑浊,B中黑色固体变红,B后面的C中澄清石灰水变浑浊
(4) 容量瓶、胶头滴管
(5)
(6) ×100%
【解析】
【分析】A用于样品的分解,C中的澄清石灰水用来检验二氧化碳,D用来吸收二氧化碳、E检验二氧化
碳是否吸收完全,F可吸收水蒸气,检验三草酸合铁酸钾受热分解所得产物是否含有CO、CO,应先检验
2
二氧化碳再吸收二氧化碳防止干扰检验一氧化碳,用B检验一氧化碳再通入C中检验一氧化碳与氧化铜反
应的产物二氧化碳,故先将分解产物通入C、D、E、F检验并吸收CO、再干燥后依次通入氧化铜、澄清
2
石灰水检验是否又生成CO;若气体产物中含有CO,则装置中的现象是B中黑色固体变红,E中澄清石灰
2
水不变浑浊,且B后面的C中澄清石灰水变浑浊。
【小问1详解】
据分析,检验三草酸合铁酸钾受热分解所得产物是否含有CO、CO,先将分解产物通入C检验CO,再通
2 2
入D、E、F吸收CO、检验二氧化碳是否吸收完全、吸收水蒸气,再依次通入氧化铜、澄清石灰水检验
2CO,所以连接装置的顺序为:a→d→e→f→g→b→c→d(e);
【小问2详解】
实验过程中需持续通入N 的目的是将排尽装置中空气并将生成的CO、CO 转移到后续的检验装置中;
2 2
【小问3详解】
若气体产物中含有CO,则装置中的现象是E中澄清石灰水不变浑浊,B中黑色固体变红,B后面的C中澄
清石灰水变浑浊;
【小问4详解】
称取 三草酸合铁酸钾样品,配成 待测溶液,所需玻璃仪器除烧杯、玻璃棒、量筒外还有
250mL容量瓶、胶头滴管;
【小问5详解】
酸性 溶液与 发生氧化还原反应,根据得失电子守恒可得反应的离子方程式为
;
【小问6详解】
用cmol•L-1KMnO 溶液滴定上述25mL待测液至终点,消耗KMnO 溶液VL,消耗MnO 的物质的量为:n
4 4
(MnO )=cmol/L×VL=cVmol,根据化合价升降相等可得反应关系式:5Fe2+~MnO ,则n(Fe2+)=5n
(MnO )=5cVmol,m(Fe2+)=56g/mol×5cVmol,所以mg样品中铁的质量分数= =
。
19. 三星堆出土的金面具等金制品揭示了人类古文明对黄金的使用。Ⅰ.金的结构与性质
(1)金的价电子排布为 ,它在周期表中的位置为_______。
(2)金面具的制作过程包含了淘金、冶金、铸金、锤鍱等工艺,以下金的性质中,与其金属键有关的是
_______(填字母)
A. 有金属光泽 B. 有较高的熔点 C. 有很好的延展性 D. 有良好的导电性
Ⅱ.金的冶炼
(3)金的化学性质很稳定,单独用浓盐酸或浓硝酸均不能将金溶解,但将浓硝酸与浓盐酸按体积比 配
制成王水,则可以溶解金,发生的反应如下: 。
①王水溶金过程中,硝酸的作用是_______。
②盐酸的作用是:提供 与生成的 配位,降低了 浓度,提高 的还原性。
③ 可被浓硝酸轻易溶解,但王水溶解 的效果却不好,原因可能是_______。
④ 可用 粉还原,完成“沉金”。 被 完全还原时,消耗 的物质的量是
_______ 。
(4)在碱性条件下用 溶液也可溶金。(已知: 是一种易挥发的弱酸。)
①补全 溶液溶金反应的离子方程式:_______。
② 中配位原子是C,结合电子式说明C可以作为配位原子的原因:_______。
③已知 的氧化性随溶液酸性的增强而增强。工业上常选 的 溶液进行溶金,不选更低
的原因可能是_______(写出一种即可)。
【答案】(1)第六周期第IB族 (2)ABCD
(3) ①. 氧化性、酸性 ②. 银和氯离子不能生成配合物而是形成氯化银沉淀 ③. 1.5(4) ①. ②. 碳原子的电负性小于氮原子电负
性,碳原子对孤对电子的束缚力较弱,更易提供孤对电子对 ③. 增加剧毒HCN的挥发
【解析】
【小问1详解】
由金的价电子排布式 ,可知金在周期表中的位置为第六周期第IB族。
【小问2详解】
金属键是金属阳离子和自由电子之间的强烈相互作用;有金属光泽的原因是金属键中对应的自由电子对可
见光吸收后再放出,表现为反射率高;金属键越强金属的熔点越高;有很好的延展性是由于金属受到外力
作用时,晶体中的各原子层发生相对滑动,但不会改变原来的排列方式,金属阳离子与自由电子之间的金
属键没有被破坏;有良好的导电性是由于在外加电场作用下,金属晶体中的电子气定向移动而形成电流,
故选ABCD。
【小问3详解】
硝酸中氮元素化合价为+5价,反应后生成一氧化氮中的氮元素化合价为+2价,氮元素化合价降低,发生
还原反应,故硝酸作氧化剂且提供酸性环境,浓硝酸具有强氧化性,将银氧化为银离子使得银溶解度高,
王水能溶解金,是因为硝酸的强氧化性和盐酸中氯离子的配位性,让金溶解生成氯金酸 H[AuCl ],王水溶
4
解 的 效 果 不 好 , 可 能 是 银 和 氯 离 子 不 能 生 成 配 合 物 而 是 形 成 氯 化 银 沉 淀 ,
结合方程式可得 , 被 完
全还原时, 被 完全还原时,消耗 的物质的量1.5mol。
【小问4详解】
碱性环境且金元素化合价升高则氧元素化合价降低,结合得失电子守恒、电荷守恒、元素守恒得离子方程
式为 ;
由氰根电子式可知[:C N:]-,C、N均可提供孤对电子对,但碳原子的电负性小于氮原子电负性,碳原子对
孤对电子的束缚力较弱,碳原子更容易给中心原子提供孤对电子对形成配位键。
由已知可知HCN易挥发,低pH最大问题是增加剧毒HCN的挥发。
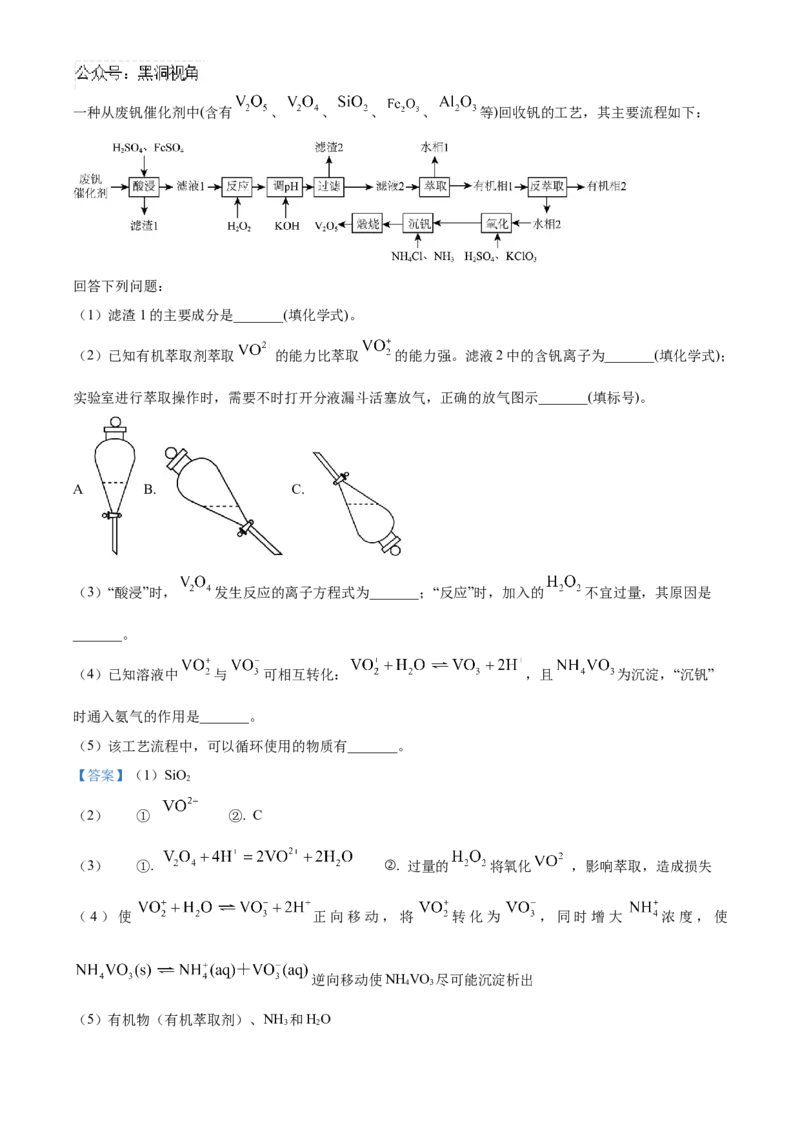
20. 五氧化二钒广泛用于冶金、化工等行业,用作合金添加剂、石油精炼用的催化剂等。科研人员研制了一种从废钒催化剂中(含有 、 、 、 、 等)回收钒的工艺,其主要流程如下:
回答下列问题:
(1)滤渣1的主要成分是_______(填化学式)。
(2)已知有机萃取剂萃取 的能力比萃取 的能力强。滤液2中的含钒离子为_______(填化学式);
实验室进行萃取操作时,需要不时打开分液漏斗活塞放气,正确的放气图示_______(填标号)。
A B. C.
.
(3)“酸浸”时, 发生反应的离子方程式为_______;“反应”时,加入的 不宜过量,其原因是
_______。
(4)已知溶液中 与 可相互转化: ,且 为沉淀,“沉钒”
时通入氨气的作用是_______。
(5)该工艺流程中,可以循环使用的物质有_______。
【答案】(1)SiO
2
.
(2) ① ②. C
(3) ①. ②. 过量的 将氧化 ,影响萃取,造成损失
(4)使 正向移动,将 转化为 ,同时增大 浓度,使
逆向移动使NH VO 尽可能沉淀析出
4 3
(5)有机物(有机萃取剂)、NH 和HO
3 2【解析】
【分析】从废钒催化剂中回收 ,由流程可知,“酸浸”时 转化为 , 转成VO2+,FeSO
4
可使 转化为VO2+,氧化铁、氧化铝均转化为金属阳离子,只有 SiO 不溶,则过滤得到的滤渣1为
2
SiO ,滤液中加过氧化氢将Fe2+氧化,再加KOH时,铁离子、铝离子转化为Fe(OH) 、Al(OH) 沉淀,同
2 3 3
时中和硫酸,过滤得到的滤渣2为Fe(OH) 、Al(OH) ,滤液2萃取、分液,水相中蒸发结晶分离出硫酸钾,
3 3
有机相1反萃取分离出有机萃取剂,水相含VO2+,氧化时发生3HO+ClO +6VO2+=6 +Cl−+6H
2
+,溶液中 与 可相互转化: +HO +2H+,“沉钒”得到偏钒酸铵(NH VO )沉淀,
2 4 3
“煅烧”时分解生成VO,以此来解答。
2 5
【小问1详解】
据分析可知,渣1的主要成分是SiO,故答案为SiO。
2 2
【小问2详解】
已知有机萃取剂萃取 的能力比萃取 的能力强,且根据流程分析可知,滤液2中的含钒离子为
;分液漏斗活塞放气时从下口放弃,所以正确的放气图示为C,故答案为 ;C。
【小问3详解】
“酸浸”时 转成VO2+, 发生反应的离子反应为 ;“反应”时,加入
的 不宜过量,过量的 将氧化 ,影响萃取,造成损失;故答案为
;过量的 将氧化 ,影响萃取,造成损失。
【小问4详解】
溶液中存在平衡 ,通入氨气,使溶液中OH−浓度增大,消耗了H+,该平衡正
移,从而使 尽可能都转化为 ,另外溶液中存在平衡 ,通入氨气,使溶液中 浓度增大,该平衡逆移,从而使NH VO 尽可能沉淀析出,则目的为使
4 3
正向移动,将 转化为 ,故答案为使 正
向移动,将 转化为 ,同时增大 浓度,使 逆向移动
使NH VO 尽可能沉淀析出。
4 3
【小问5详解】
NH 和HO可循环使用,“萃取”和“反萃取”时,有机萃取剂也可循环使用,可以循环使用的物质有有机物
3 2
(有机萃取剂)、NH 和HO,故答案为有机物(有机萃取剂)、NH 和HO。
3 2 3 2