文档内容
2010年高考理综化学试题(浙江卷)
1、下列说法中正确的是
A. 光导纤维、棉花、油脂、ABS树脂都是由高分子化合物组成的物质
B. 开发核能、太阳能等新能源,推广基础甲醇汽油,使用无磷洗涤剂都可直接降低碳
排放
C. 红外光谱仪、核磁共振仪、质谱仪都可用于有机化合物结构的分析
D. 阴极射线、-粒子散射现象及布朗运动的发现都对原子结构模型的建立作出了贡
献
2、有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+
与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一
种重要的半导体材料。下列说法中,正确的是
A. X、M两种元素只能形成X M型化合物
2
B. 由于W、Z、M元素的氢气化物相对分子质量依次减小,所以其沸点依次降低
C. 元素Y、Z、W的单质晶体属于同种类型的晶体
D. 元素W和M的某些单质可作为水处理中的消毒剂
3、Li-Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:
2Li+FeS+2e-=Li S+Fe有关该电池的下列中,正确的是
2
A. Li-Al在电池中作为负极材料,该材料中Li的化合价为+1价
B. 该电池的电池反应式为:2Li+FeS=Li S+Fe
2
C. 负极的电极反应式为Al-3 e-=Al3+
D. 充电时,阴极发生的电极反应式为:Li S+Fe-2e-=2Li++FeS
2
4、核黄素又称为维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳。
核黄素分子的结构为:
已知:+H O +
2
有关核黄素的下列说法中,不正确的是:
A.该化合物的分子式为C H N O
17 22 4 6
B.酸性条件下加热水解,有CO 生成
2
C.酸性条件下加热水解,所得溶液加碱后有NH 生成
3
D.能发生酯化反应
5、下列关于实验原理或操作的叙述中,不正确的是:
A、 从碘水中提取单质碘时,不能用无水乙醇代替CCl
4
B、 可用新制的Cu(OH) 悬浊液检验牙膏中存在的甘油
2
C、 纸层析实验中,须将滤纸上的试样点浸入展开剂中
D、 实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法
6、下列热化学方程式或离子方程式中,正确的是:
A、甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:
CH (g)+2O (g)=CO (g)+2H O(g) △H=-890.3kJ·mol-1
4 2 2 2
B.500℃、30MPa下,将0.5molN 和1.5mol H 置于密闭容器中充分反应生成NH (g),
2 2 3
放热19.3kJ,其热化学方程式为:
N (g)+3H (g) 2NH (g) △H=-38.6kJ·mol-1
2 2 3
C.氯化镁溶液与氨水反应:Mg2++2OH-=Mg(OH) ↓
2
D.氧化铝溶于NaOH溶液:Al O +2OH-+3H O=2Al(OH) -
2 3 2 4
7、某钠盐溶液中可能含有NO -、SO 2-、SO 2-、CO 2-、Cl-、I-等阴离子。某同学取
2 4 3 3
5份此溶液样品,分别进行了如下实验:
①用pH计测得溶液pH大于7
②加入盐酸,产生有色刺激性气体
③加入硝酸酸化的AgNO 溶液产生白色沉淀,且放出有色刺激性气体
3④加足量BaCl 溶液,产生白色沉淀,该沉淀溶于稀硝酸且放出气体,将气体通入品红溶
2
液,溶液不褪色
⑤加足量BaCl 溶液,产生白色沉淀,在滤液中加入酸化的(NH ) Fe(SO ) 溶液,
2 4 2 4 2
再滴加KSCN溶液,显红色
该同学最终确定在上述六种离子中仅含NO -、CO 2-、Cl-三种阴离子。
2 3
请分析,该同学只需要完成上述哪几个实验,即可得出此结论。
A. ①②④⑤ B. ③④ C. ③④⑤ D. ②③⑤
8、洗车安全气囊是行车安全的重要保障。当车辆发生碰撞的瞬间,安全装置通电点火使其
中的粉末分解释放出大量的氮气形成气囊,从而保护司机及乘客免受伤害。为研究安全气
囊工作的化学原理,取安全装置中的固体粉末进行实验。经组成分析,确定该粉末仅Na、
Fe、N、O四种元素。水溶性试验表明,固体粉末部分溶解。经检测,可溶物为化合物
甲;不溶物为红棕色固体,可溶于盐酸。
取13.0g化合物甲,加热使其完全分解,生成氮气和单质乙,生成的氮气折合成标准状
况下的体积为6.72L。单质乙就在高温隔绝空气的条件下与不溶物红棕色粉末反应生成化
合物丙和另和一种单质。化合物丙与空气接触可转化为可溶性盐。
请回答下列问题:
(1)甲的化学方程式为 ,丙的电子式为 。
(2)若丙在空气中转化为碳酸氢盐,则反应的化学方程式为 。
(3)单质乙与红棕色粉末发生反应的化学方程式为 ,安全气囊中红棕色粉末的作用
是 。
(4)以下物质中,有可能作为安全气囊中红棕色粉末替代品的是 。
A. KCl B. KNO C. Na S D. CuO
3 2
(5)设计一个实验方案,探究化合物丙与空气接触后生成可溶性盐的成分(不考虑结晶水
合物) 。
9、已知:
①25℃时弱电解质高电离平衡常数:K (CH COOH)=1.8×10-5,K (HSCN)=0.13;
a 3 a
难溶电解质的溶度积学数:K (CaF )=1.5×10-10
sp 2
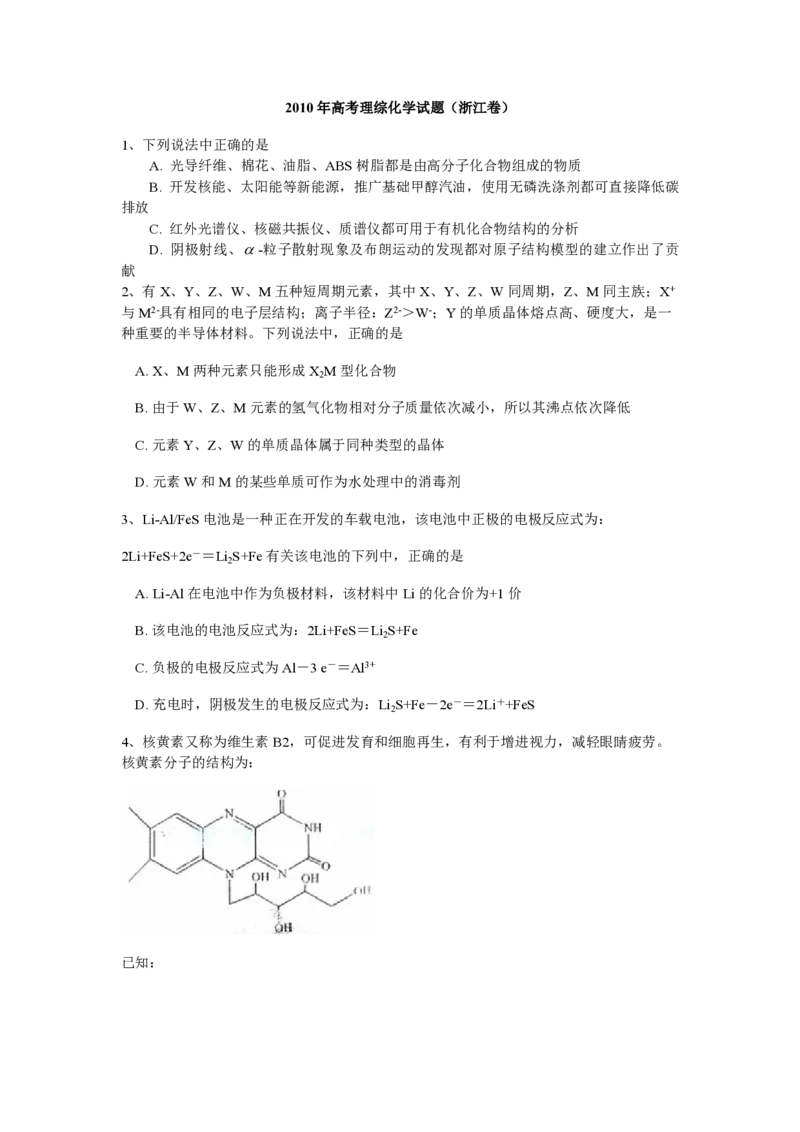
②25℃时,2.0×10-3mol·L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c
(HF)、c(F-)与溶液pH的变化关系,如下图所示:请根据以下信息回答下旬问题:
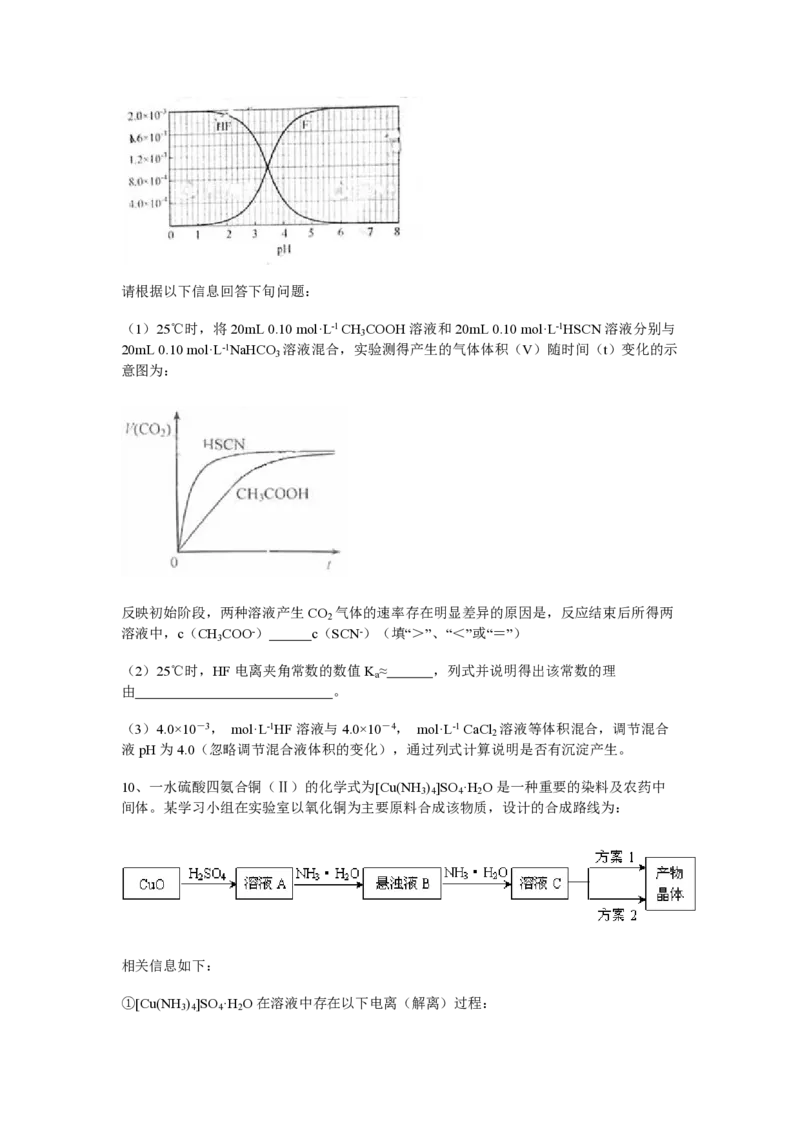
(1)25℃时,将20mL 0.10 mol·L-1 CH COOH溶液和20mL 0.10 mol·L-1HSCN溶液分别与
3
20mL 0.10 mol·L-1NaHCO 溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示
3
意图为:
反映初始阶段,两种溶液产生CO 气体的速率存在明显差异的原因是,反应结束后所得两
2
溶液中,c(CH COO-) c(SCN-)(填“>”、“<”或“=”)
3
(2)25℃时,HF电离夹角常数的数值K ≈ ,列式并说明得出该常数的理
a
由 。
(3)4.0×10-3, mol·L-1HF溶液与4.0×10-4, mol·L-1 CaCl 溶液等体积混合,调节混合
2
液pH为4.0(忽略调节混合液体积的变化),通过列式计算说明是否有沉淀产生。
10、一水硫酸四氨合铜(Ⅱ)的化学式为[Cu(NH ) ]SO ·H O是一种重要的染料及农药中
3 4 4 2
间体。某学习小组在实验室以氧化铜为主要原料合成该物质,设计的合成路线为:
相关信息如下:
①[Cu(NH ) ]SO ·H O在溶液中存在以下电离(解离)过程:
3 4 4 2[Cu(NH ) ]SO ·H O=[Cu(NH ) ]2++SO 2-+H O
3 4 4 2 3 4 4 2
[Cu(NH ) ]2+ Cu2++4NH
3 4 3
②(NH ) SO 在水中可溶,在乙醇中难溶。
4 2 4
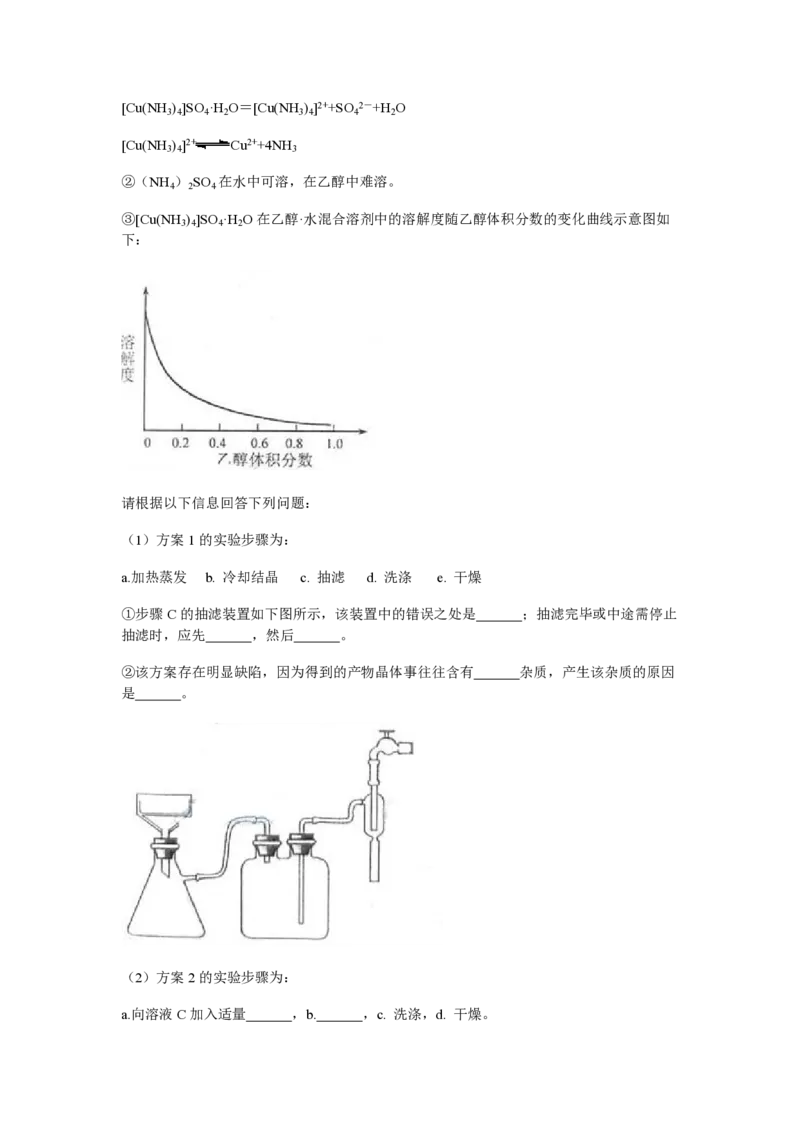
③[Cu(NH ) ]SO ·H O在乙醇·水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如
3 4 4 2
下:
请根据以下信息回答下列问题:
(1)方案1的实验步骤为:
a.加热蒸发 b. 冷却结晶 c. 抽滤 d. 洗涤 e. 干燥
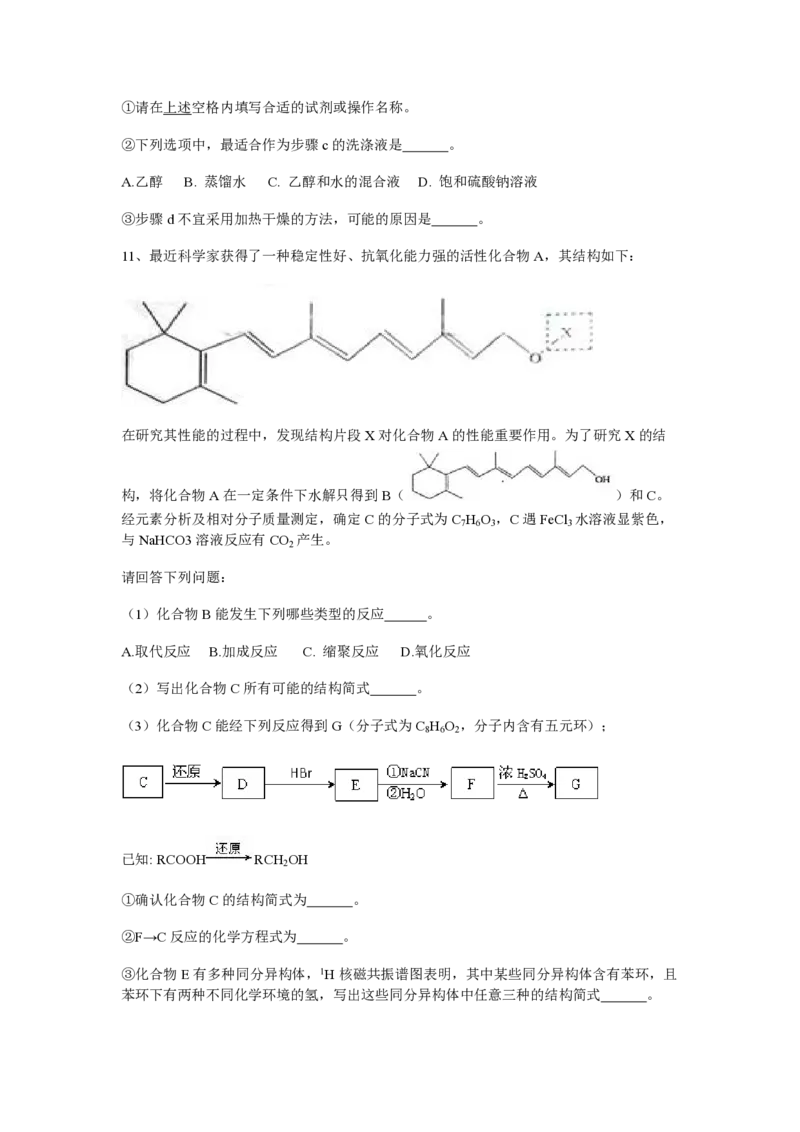
①步骤C的抽滤装置如下图所示,该装置中的错误之处是 ;抽滤完毕或中途需停止
抽滤时,应先 ,然后 。
②该方案存在明显缺陷,因为得到的产物晶体事往往含有 杂质,产生该杂质的原因
是 。
(2)方案2的实验步骤为:
a.向溶液C加入适量 ,b. ,c. 洗涤,d. 干燥。①请在上述空格内填写合适的试剂或操作名称。
②下列选项中,最适合作为步骤c的洗涤液是 。
A.乙醇 B. 蒸馏水 C. 乙醇和水的混合液 D. 饱和硫酸钠溶液
③步骤d不宜采用加热干燥的方法,可能的原因是 。
11、最近科学家获得了一种稳定性好、抗氧化能力强的活性化合物A,其结构如下:
在研究其性能的过程中,发现结构片段X对化合物A的性能重要作用。为了研究X的结
构,将化合物A在一定条件下水解只得到B( )和C。
经元素分析及相对分子质量测定,确定C的分子式为C H O ,C遇FeCl 水溶液显紫色,
7 6 3 3
与NaHCO3溶液反应有CO 产生。
2
请回答下列问题:
(1)化合物B能发生下列哪些类型的反应 。
A.取代反应 B.加成反应 C. 缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式 。
(3)化合物C能经下列反应得到G(分子式为C H O ,分子内含有五元环);
8 6 2
已知: RCOOH RCH OH
2
①确认化合物C的结构简式为 。
②F→C反应的化学方程式为 。
③化合物E有多种同分异构体,1H核磁共振谱图表明,其中某些同分异构体含有苯环,且
苯环下有两种不同化学环境的氢,写出这些同分异构体中任意三种的结构简式 。2010年浙江高考理综化学解析
2010年浙江省高考化学试题充分体现了新课程理念,严格按照《省学科指导意见》和
《考试说明》的要求命题,各种题型与样卷有较高的吻合度。题型继承了09年试题的风
格,突出化学主干知识的考查。客观题常规中见新意,注重学科基础知识的考查;主观题
除了有机题比较经典以外,其它三题创新力度较大,十分重视化学能力和科学素养的考
查。具体解读从以下几个方面:
一、选择题部分解读分析:选择题侧重考查元素周期律、热化学方程式、离子方程
式、有机化合物结构和官能团性质、原电池、化学实验基本方法和技能等知识。
7、【解析】答案:C。考查形式同 2010浙江高考参考卷第 7题,主要考查化学与生
活、生产、STS的等。A项错误,光导纤维不是高分子;B项错误,无磷洗涤剂与直接降
低碳排放无关; D项错误,阴极射线、布朗运动与原子结构模型的建立无关。
8、【解析】答案:D。考查形式同2010浙江高考参考卷第11题,主要在元素周期律
的推理判断能力的考查中渗透了结构、性质和用途等基础知识的考查;具体素推断为基础
看,考查了氢键、晶体类型与熔沸点的大小比较等规律。依据题意推断X-Na Y –Si Z
–S W –O M—Cl。A项错误,Na和O两种元素能形成Na O、Na O 两种化合物;B项
2 2 2
错误,因水分子间存在氢键、所以水的沸点最高;C项错误硅是原子晶体、硫是分子晶
体、氯气是分子晶体,所以三者晶体类型不同。
9、【解析】答案:B 。考查形式同 2010浙江高考参考卷第 13题,本题以新型 Li-
Al/FeS电池为载体,主要考查放电、充电的工作原理。A项错误,在负极材料中Li的化合
价为0价;C项错误,负极的电极反应式应该为Li-e=Li+;D项错误,充电时,阳极发生
氧化反应,阴极发生还原反应。
10、【解析】答案:A 。考查形式同2010浙江高考参考卷第9题,;本题在分析维生
素B2键线式的组成和性质的基础上,还包含了H CO 、NH +等无机化合物性质的测试,
2 3 4
具体根据有机物的结构特点考查酰胺键、醇羟基等官能团的性质。A项错误,因化合物的
分子式为C H N O ;B项正确酰胺键在酸性条件下加热水解可生产碳酸放出CO ;C项
17 20 4 6 2
正确,氨基酸性条件下加热水解后加碱可有NH 生成;D项正确因分子结构中有羟基所以
3
能发生酯化反应。
11、【解析】答案:C。考查形式同2010浙江高考参考卷第10题,主要考查实验基本
操作:萃取、纸层析、蒸馏、提纯及物质的检验,均出自选修6《实验化学》教材。A项
正确,从水溶液中萃取碘不能用酒精;B项正确新制的Cu(OH) 悬浊液和甘油出现绛蓝
2
色溶液,可以检验;C项错误在纸层析实验中,试样点不能浸入展开剂中;D项正确将乙
酸转化为沸点高乙酸盐,可以用蒸馏的方法将乙醇分离出。
12、【解析】答案:C。考查形式同2010浙江高考参考卷第8题其中AB两项改为热
化学方程式判断。 A项错误,标准燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物所
放出的能量,生成中的 H O须为液态;B项错误,因合成氨反应为可逆反应,即 0.5mol
2
N 和1.5molH 充分反应不会生成1mol NH (g);C项错误,因氨水是弱碱在写离子方程式
2 2 3
时不能拆成离子形式;D项正确将AlO —写成Al(OH) —。
2 4
13、【解析】答案:B。新增题型:考查形式类似于2010浙江高考参考卷中的25题的
压缩题但设问新颖,一改传统的物质(离子)推断,涉及到《实验化学》中的亚硝酸钠、
摩尔盐等;同时删去离子浓度比较的题型。根据③加入硝酸酸化的AgNO 溶液产生白色沉
3
淀,且放出有色刺激性气体可推断出一定有NO —、Cl—,根据④加足量BaCl2溶液,产生
2白色沉淀,在滤液中加入酸化的(NH ) Fe(SO ) 溶液,再滴加KSCN溶液,显红色可
4 2 4 2
推断出一定有NO —、CO 2—,所以答案选B。
2 3
二、主观题部分解读分析:主观题分别涉及元素化合物、化学反应基本原理,物质的
制备与提纯,有机化学等知识。在试题的设计上更加突出化学学科的思维特点和方法,如
元素与化合物、化学实验、有机化学等试题的问题设计中更加符合化学逻辑思维。所考查
的知识内容更凸现新课程的特色,加强了对化学数据信息吸收、整合、应用及实验探究能
力的考查。四道大题是对《考试说明》中要求的各项化学能力作了全面的测试。
第25题着重测试了化学发现思维能力,联系到汽车的安全气囊。要求考生经过定性判
断、定量分析推断出几种无机化合物,同时考查学生的化学用语表达能力。与往年多次考
查到的框图题相比较,我们认为这种试题更能体现化学学科特色。
【答案】:(1)NaN 、 (2)Na O+2CO +H O=2NaHCO
3 2 2 2 3
(3) 避免分解产生的金属钠可能产生的危害。(4)BD
(5)可溶性盐的成分可能是Na CO ,或NaHCO ,或Na CO 与 NaHCO 的混合物。
2 3 3 2 3 3
准确称取一定量的生成物,加热至恒重后,如试样无失重,则为Na CO ;如加热后
2 3
失重,根据失重的量在试样总质量中的比例,即可推断出试样为NaHCO ,或Na CO 与
3 2 3
NaHCO 的混合物。
3
【解析】
第26题侧重化学理论知识的考查,涉及到电离常数、离子积常数等。
【答案】:(1)HSCN的酸性比CH COOH强,其溶液中的c(H+)较大,故其溶液与
3
NaHCO 溶液的反应速率较快 <
3
(2)3.5×10-4
( 3
)
【 解 析】
第27题侧重化学实验能力的考查,直接选取《实验化学》模块的相关内容进行考查。
【答案】:(1)①布氏漏斗的劲口斜面未朝向抽滤瓶的直管口
断开连接安全瓶与抽气装置间的橡皮管 关闭抽气装置中的水龙头
②Cu(OH) 或Cu (OH) SO 加热蒸发过程中NH 挥发,使反应
2 2 2 4 3
[Cu(NH ) ]2+ Cu2+ + 4NH 平 衡 向 右 移 动 , 且 Cu2+ 发 生 水 解 。
3 4 3
(2)①乙醇 抽滤(或吸滤、减压过滤)② C ③ 加热易使[Cu(NH ) ] SO ·H O 分
3 4 4 2
解(失H O、失NH )
2 3
【解析】
第28题侧重有机分析推理能力的考查,取材于最新的活性化合物研究。
【答案】:(1)A、B、D
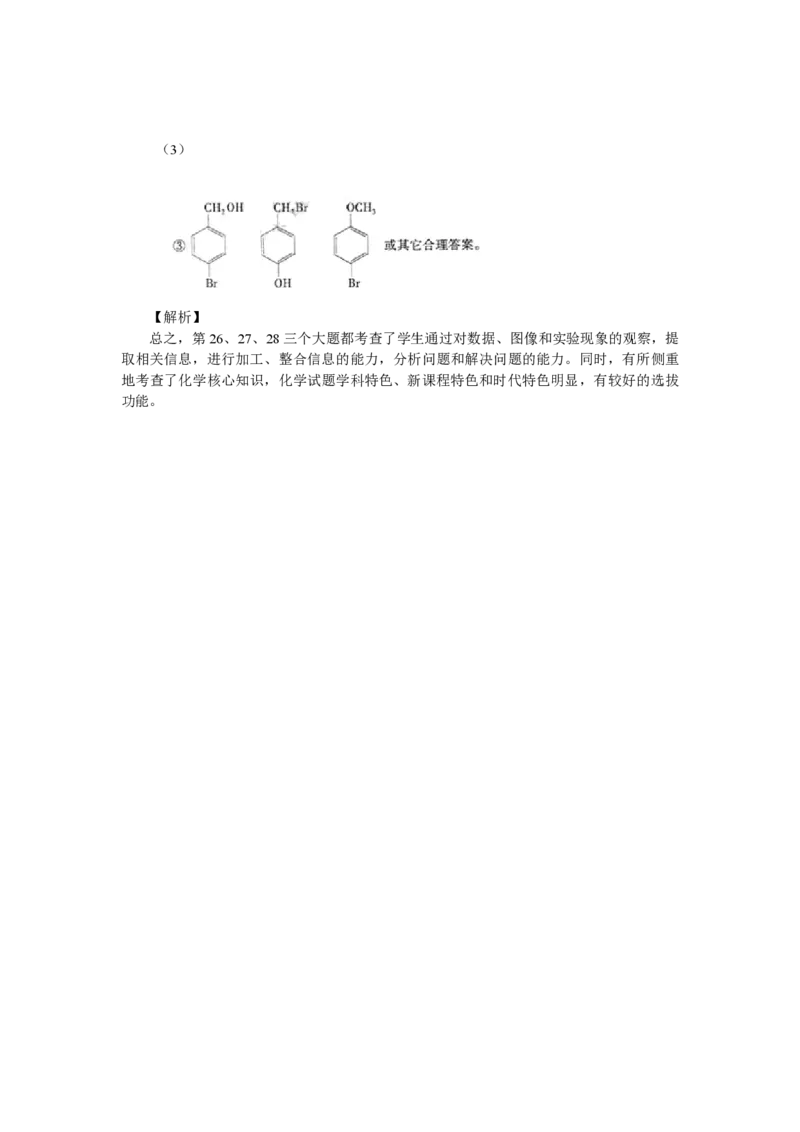
(2)(3)
【解析】
总之,第26、27、28三个大题都考查了学生通过对数据、图像和实验现象的观察,提
取相关信息,进行加工、整合信息的能力,分析问题和解决问题的能力。同时,有所侧重
地考查了化学核心知识,化学试题学科特色、新课程特色和时代特色明显,有较好的选拔
功能。