文档内容
2012年普通高等学校招生全国统一考试(广东卷)A
理科综合------化学卷解析
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Al 27 S 32 Cl 35.5 K 39 Ca 40
一、单项选择题:本大题共16小题,每小题4分,共64分。在每小题给出的四个选项中,只有
一个选项符合题目要求,选对的得4分,选错或不答的得0分。
7.化学与生活息息相关,下列说法不正确的是( )
A.用食醋可除去热水壶内壁的水垢
B.淀粉、油脂和蛋白质都是高分子化合物
C.自行车钢架生锈主要是电化学腐蚀所致
D.新型复合材料使用手机,电脑等电子产品更轻巧,使用和新潮
8.在水溶液中能大量共存的一组是( )
A.Fe2+、Al3+、ClO-、Cl- B.K+、Cu2+、OH-、NO -
3
C.NH +、Na+、Br-、SO 2- D.Mg2+、H+、SiO2-、SO 2-
4 4 3 4
9.下列实验能达到目的的是( )
A.用溴水鉴别苯和正己烷
B.用BaCl 溶液鉴别SO 2-和SO 2-
2 4 3
C.用浓HNO 与Cu反应制备NO
3 2
D.将混有HCl的Cl 通入饱和NaHCO 溶液中除去HCl
2 3
10.下列应用不涉及氧化还原反应的是( )
A.NaO 用作呼吸面具的供氧剂 B.工业上电解熔融状态Al O 制备Al
2 2 2 3
C.工业上利用合成氨实现人工固氮 D.实验室用NH Cl和Ca(OH) 制备NH
4 2 3
11.设n 为阿伏伽德罗常数的数值,下列说法正确的是( )
A
A.常温下,4gCH 含有n 个C-H共价键
4 A
B.1mol Fe与过量的稀HNO 反应,转移2n 个电子
3 A
C.1L 0.1mol·L-1 NaHCO 液含有0.1n 个HCO -
3 A 3
D.常温常压下,22.4L的NO 和CO 合气体含有2n 个O原子
2 2 A
12.下列陈述Ⅰ、Ⅱ正确并且有因果关系的是( )
选项 陈述Ⅰ 陈述Ⅱ
A SO 有漂白性 SO 可使溴水褪色
2 2
B SiO 有导电性 SiO 可用于制备光导纤维
2 2
C 浓硫酸有强氧化性 浓硫酸可用于干燥H 和CO
2
D Fe3+有氧化性 Fe3+溶液可用于回收旧电路板中的铜
二、双项选择题:本大提供9小题,每小题6分,共54分。在每小题给出四个选项中,有两个
选项符合题目要求,全部选对的得6分,只选对2个且正确的的3分,有选错或不答的得0分。
22.下图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )A.原子半径:Z>Y>X
B.气态氢化物的稳定性:R>W
C.WX 和水反应形成的化合物是离子化合物
3
D.Y和Z两者最高价氧化物对应的水化物能相互反应
23.对于常温下pH为2的盐酸,叙述正确的是 ( )
A.c(H+)=c(Cl-)+c(OH-)
B.与等体积pH=12的氨水混合后所得溶液显酸性
C.由HO电离出的c(H+)=1.0×10-12mol·L-1
2
D.与等体积0.01mol·L-1乙酸钠溶液混合后所得溶液中:c(Cl-)=c(CHCOO-)
3
非选择题
30.过渡金属催化的新型碳-碳偶联反应是近年来有机合成的研究热点之一,如反应①
Ⅰ Ⅱ
化合物Ⅱ可由化合物Ⅲ合成:
O
HO O
C 4 H 7 Br NaOH、H 2 O CH 3 CHCH CH 2 CH 3 C Cl CH 3 C OCHCH 3 CH 2
Δ 有机碱
CH
3
Ⅲ Ⅳ Ⅱ
(1)化合物I的分子式为______________。
(2)化合物Ⅱ与Br 加成的产物的结构简式为______________。
2
(3)化合物Ⅲ的结构简式为______________。
(4)在浓硫酸存在和加热条件下,化合物Ⅳ易发生消去反应生成不含甲基的产物,该反应方
O
程式为______________ ( 注明反应条件)。因此,在碱性条件下,由Ⅳ与 反应合成Ⅱ,
CH C Cl
3
其反应类型为___________。
(5)Ⅳ的一种同分异构体V能发生银镜反应。V与Ⅱ也可发生类似反应①的反应,生成化合
物Ⅵ,Ⅵ的结构简式为___________(写出其中一种)。
31.碘在科研与生活中有重要应用。某兴趣小组用0.50mol·L-1 KI、0.2%淀粉溶液、0.20mol·L
-1 K SO、0.10mol·L-1 Na SO 等试剂,探究反应条件对化学反应速率的影响。
2 2 8 2 2 3
已知:SO2-+2I-=2SO 2-+I(慢) I +2SO2-=2I-+SO2-(快)
2 8 4 2 2 2 3 4 6
(1)向KI、NaSO 与淀粉的混合溶液中加入一定量的KSO 溶液,当溶液中的_________耗
2 2 3 2 2 8尽后,溶液颜色将由无色变成为蓝色。为确保能观察到蓝色,SO2-与SO2-初始的物质的量
2 3 2 8
需满足的关系为:n(SO2-):n(SO2-) _______。
2 3 2 8
(2)为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验 体积V/mL
序号
KSO 溶液 水 KI溶液 NaSO 溶液 淀粉溶液
2 2 8 2 2 3
① 10.0 0.0 4.0 4.0 2.0
② 9.0 1.0 4.0 4.0 2.0
③ 8.0 Vx 4.0 4.0 2.0
表中Vx=____mL,理由是___________________。
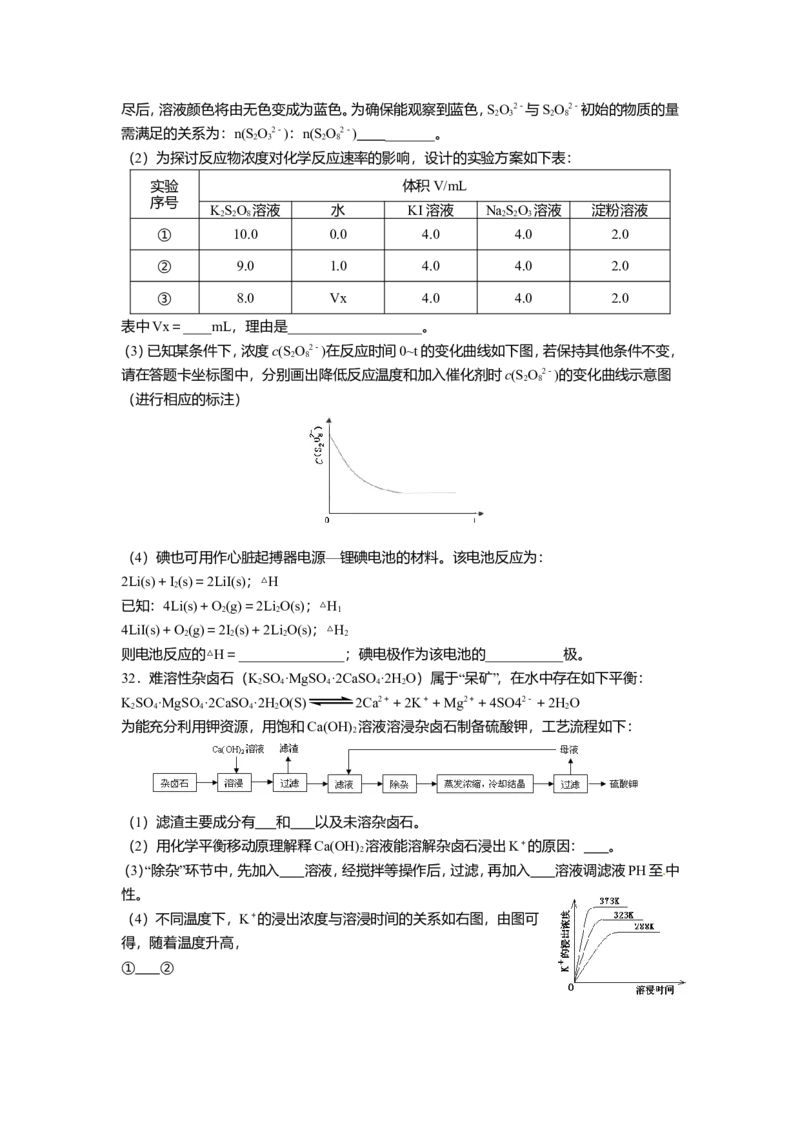
(3)已知某条件下,浓度c(SO2-)在反应时间0~t的变化曲线如下图,若保持其他条件不变,
2 8
请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时c(S O2-)的变化曲线示意图
2 8
(进行相应的标注)
(4)碘也可用作心脏起搏器电源—锂碘电池的材料。该电池反应为:]
2Li(s)+I(s)=2LiI(s);△H
2
已知:4Li(s)+O(g)=2LiO(s);△H
2 2 1
4LiI(s)+O(g)=2I(s)+2LiO(s);△H
2 2 2 2
则电池反应的△H=_______________;碘电极作为该电池的___________极。
32.难溶性杂卤石(KSO ·MgSO ·2CaSO·2H O)属于“呆矿”,在水中存在如下平衡:
2 4 4 4 2
KSO ·MgSO ·2CaSO·2H O(S) 2Ca2++2K++Mg2++4SO42-+2HO
2 4 4 4 2 2
为能充分利用钾资源,用饱和Ca(OH) 溶液溶浸杂卤石制备硫酸钾,工艺流程如下:
2
(1)滤渣主要成分有 和 以及未溶杂卤石。
(2)用化学平衡移动原理解释Ca(OH) 溶液能溶解杂卤石浸出K+的原因: 。
2
(3)“除杂”环节中,先加入 溶液,经搅拌等操作后,过滤,再加入 溶液调滤液PH至中
性。
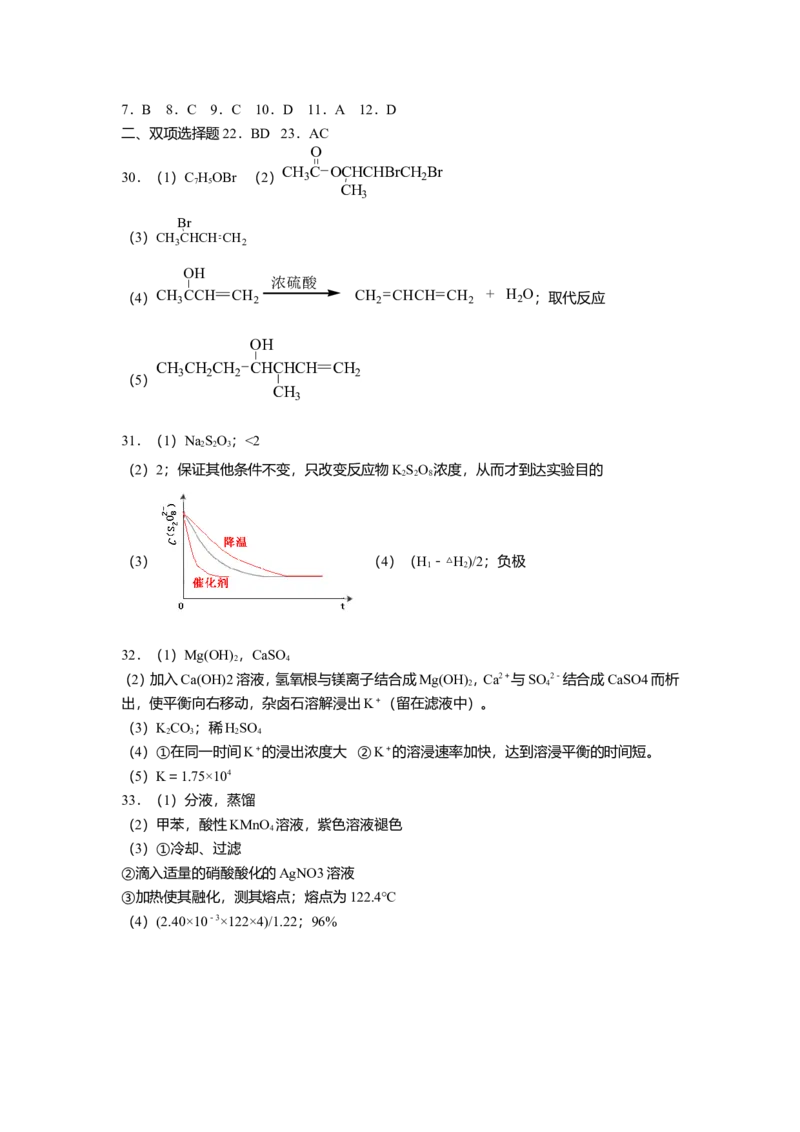
(4)不同温度下,K+的浸出浓度与溶浸时间的关系如右图,由图可
得,随着温度升高,
① ②(5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:
CaSO4(S)+CO2- CaCO (S)+SO 2-
3 3 4
已知298K时,Ksp(CaCO )=2.80×10-9,Ksp(CaSO )=4.90×10-5,求此温度下该反应的平衡
3 4
常数K(计算结果保留三位有效数字)。
33.苯甲酸广泛应用于制药和化工行业。某同学尝试用甲苯的氧化反应制备苯甲酸。
反应原理:
Δ
CH 3 + 2KMnO 4 COOK + KOH + 2 MnO 2 + 2 H 2 O
COOK + HCl COOH + KCl
实验方法:一定量的甲苯和KMnO 溶液在100℃反应一段时间后停止反应,按如下流程分离
4
出苯甲酸和回收未反应的甲苯。
已知:苯甲酸分子量是122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净
固体有机物一般都有固定熔点。
(1)操作Ⅰ为 ,操作Ⅱ为 。
(2)无色液体A是 ,定性检验A的试剂是 ,现象是 。
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不溶。该同学
推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明
推测正确。请在答题卡上完成表中内容。
序号 实验方案 实验现象 结论
① 将白色固体B加入水中,加热,溶 得到白色晶体和无色溶液
解,
② 取少量滤液于试管中, 生成白色沉淀 滤液含有Cl-
③ 干燥白色晶体, 白色晶体是苯
甲酸
(4)纯度测定:称取1.220g产品,配成100ml甲醇溶液,移取25.00ml溶液,滴定,消耗KOH
的物质的量为2.40×10-3mol。产品中苯甲酸质量分数的计算表达式为 ,计算结果为
(保留两位有效数字)。
答案一、单项选择题7.B 8.C 9.C 10.D 11.A 12.D
二、双项选择题22.BD 23.AC
O
CH C OCHCHBrCH Br
30.(1)C HOBr (2) 3 2
7 5
CH
3
Br
(3)CH CHCH CH
3 2
OH
浓硫酸
(4) CH 3 CCH CH 2 CH 2 CHCH CH 2 + H 2 O ;取代反应
OH
CH CH CH CHCHCH CH
3 2 2 2
(5)
CH
3
31.(1)NaSO;<2
2 2 3
(2)2;保证其他条件不变,只改变反应物KSO 浓度,从而才到达实验目的
2 2 8
(3) (4)(H-△H)/2;负极
1 2
32.(1)Mg(OH) ,CaSO
2 4
(2)加入Ca(OH)2溶液,氢氧根与镁离子结合成Mg(OH) ,Ca2+与SO 2-结合成CaSO4而析
2 4
出,使平衡向右移动,杂卤石溶解浸出K+(留在滤液中)。
(3)KCO;稀HSO
2 3 2 4
(4)①在同一时间K+的浸出浓度大 ②K+的溶浸速率加快,达到溶浸平衡的时间短。
(5)K=1.75×104
33.(1)分液,蒸馏
(2)甲苯,酸性KMnO 溶液,紫色溶液褪色
4
(3)①冷却、过滤
②滴入适量的硝酸酸化的AgNO3溶液
③加热使其融化,测其熔点;熔点为122.4℃
(4)(2.40×10-3×122×4)/1.22;96%