文档内容
2025 年云南省普通高等学校招生统一考试
化学
注意事项:
1.答卷前,考生务必用黑色碳素笔将自己的姓名、准考证号、考场号、座位号填写在答题卡
上,并认真核准条形码上的姓名、准考证号、考场号、座位号及科目,在规定的位置贴好条
形码。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,用黑色碳素笔将答案写在
答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 F 19 Na 23 S 32 Cl 35.5
Mn 55 Fe 56 Cu 64 Sb 122
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 画中有“化”,多彩中华。下列叙述正确的是
A. 岩彩壁画颜料所用贝壳粉,主要成分属于硅酸盐
B. 油画颜料调和剂所用核桃油,属于有机高分子
C. 竹胎漆画颜料赭石的主要成分氧化铁,耐酸、碱
D. 水墨画墨汁的主要成分碳,常温不易被氧化
2. 下列化学用语或图示表示正确的是
A. 的VSEPR模型:
B. 的电子式:
C. Cl的原子结构示意图:
D. 溶于水 的电离方程式:
3. 下列化学方程式错误的是A. 煤制水煤气:
B. 供氧:
C. 覆铜板制作印刷电路板:
D. 铅酸蓄电池放电:
4. 为阿伏加德罗常数的值。下列说法正确的是
A. 中原子的数目为
B. 所含中子的数目为
C. 粉和足量S完全反应,转移电子的数目为
D. 盐酸与足量 反应,生成 的数目为
5. 下列装置(省略部分夹持装置)或操作正确的是
B.配制 溶
A.制备
液
C.探究Na与 反应 D.探究温度对化学平衡的影响A. A B. B C. C D. D
6. 化合物Z是某真菌的成分之一,结构如图。下列有关该物质说法错误的是
A. 可形成分子间氢键
B. 与乙酸、乙醇均能发生酯化反应
C. 能与 溶液反应生成
D. 与 的 溶液反应消耗
7. 稻壳制备纳米Si的流程图如下。下列说法错误的是
A. 可与NaOH溶液反应
B. 盐酸在该工艺中体现了还原性
C. 高纯Si可用于制造硅太阳能电池
D. 制备纳米Si:
8. 某化学兴趣小组设计如下实验装置,通过测定反应前后质量的变化,验证 固体在酒精灯加热条
件下,受热分解的气态产物。
的
实验步骤:先缓慢通入Ar气,排尽装置内空气;关闭Ⅰ左侧阀门,点燃酒精灯;一段时间后,Ⅱ中灼热
铜网变黑,熄灭酒精灯甲;再次缓慢通入Ar气……
下列说法错误的是
A. 实验步骤中,点燃酒精灯的顺序为甲、乙、丙B. 整个过程中,若Ⅲ中灼热的铜网未变黑,则说明生成的 在Ⅱ中反应完全
C. 实验结束后,若Ⅰ中减少的质量等于Ⅱ中增加的质量,则分解的气态产物只有
D. 应远离热源、可燃物,并与还原性物质分开存放
9. 钙霞石是一种生产玻璃陶瓷的原料,所含M、Q、R、T、X、Y、Z为原子序数依次增大的前20号主族
元素,M是原子半径最小的元素,Q是形成物质种类最多的元素,R是地壳中含量最高的元素,T、X、Y
同周期,Q、X均与Y相邻,Z的原子序数等于M、R和T的原子序数之和。下列说法正确的是
A. M与Z可形成离子化合物 B. 原子半径:
C. 是极性分子 D. 电负性:
10. 铜催化下,由 电合成正丙醇的关键步骤如图。下列说法正确的是
A. Ⅰ到Ⅱ的过程中发生氧化反应 B. Ⅱ到Ⅲ的过程中有非极性键生成
C. Ⅳ的示意图为 D. 催化剂Cu可降低反应热
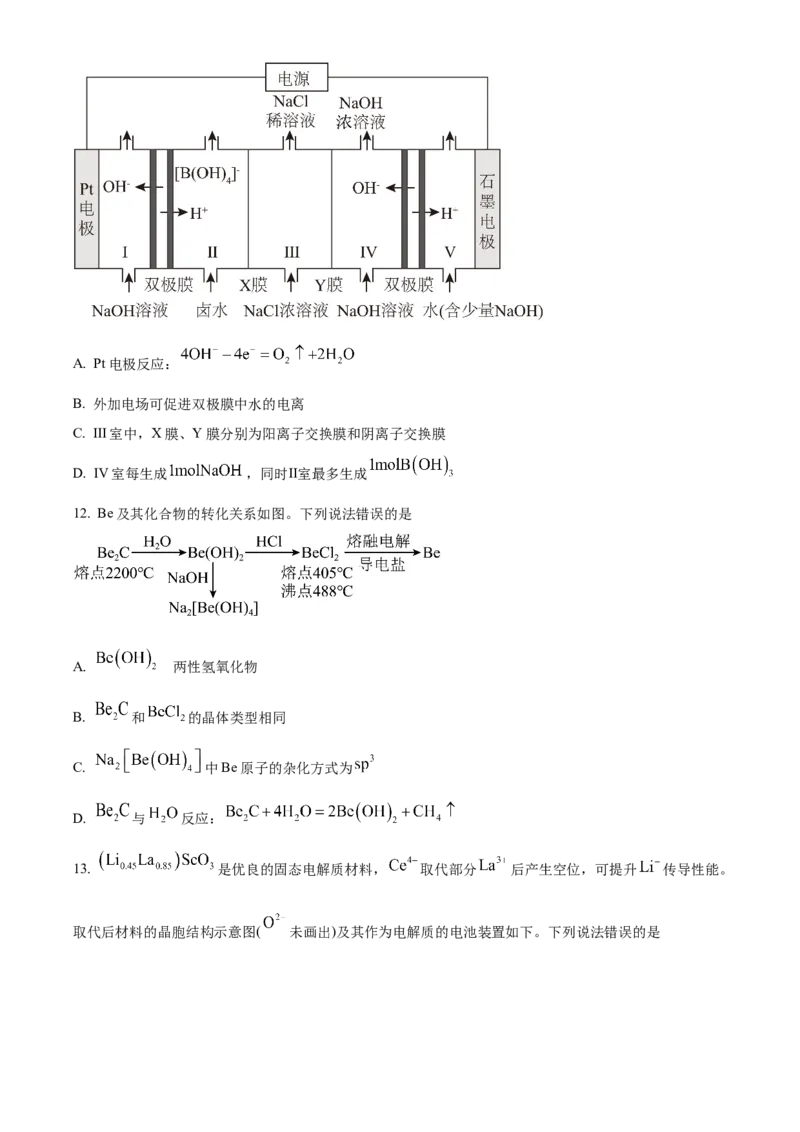
11. 一种用双极膜电渗析法卤水除硼的装置如图所示,双极膜中 解离的 和 在电场作用下向两
极迁移。除硼原理: 。下列说法错误的是A. Pt电极反应:
B. 外加电场可促进双极膜中水的电离
C. Ⅲ室中,X膜、Y膜分别为阳离子交换膜和阴离子交换膜
D. Ⅳ室每生成 ,同时Ⅱ室最多生成
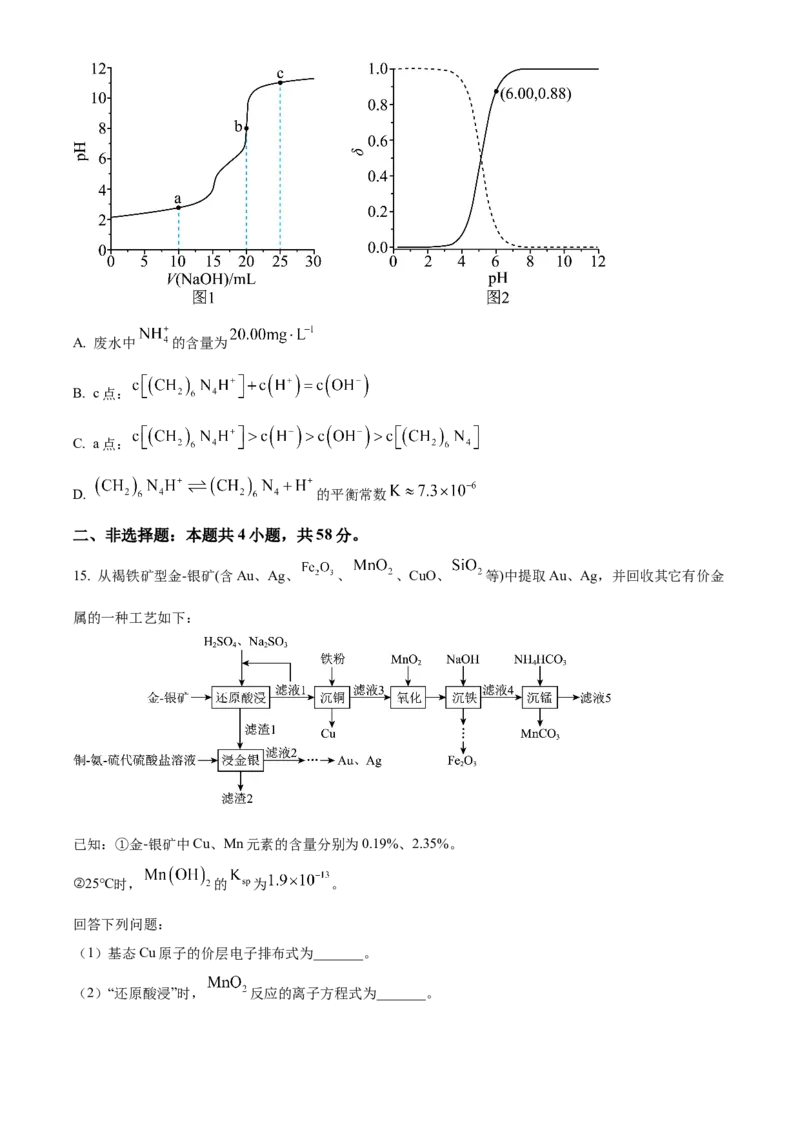
12. Be及其化合物的转化关系如图。下列说法错误的是
A. 是两性氢氧化物
B. 和 的晶体类型相同
C. 中Be原子的杂化方式为
D. 与 反应:
13. 是优良的固态电解质材料, 取代部分 后产生空位,可提升 传导性能。
取代后材料的晶胞结构示意图( 未画出)及其作为电解质的电池装置如下。下列说法错误的是A. 每个晶胞中 个数为12
B. 该晶胞在yz平面的投影为
C. 取代后,该电解质的化学式为
D. 若只有 发生迁移,外电路转移的电子数与通过截面MNPQ的 数目相等
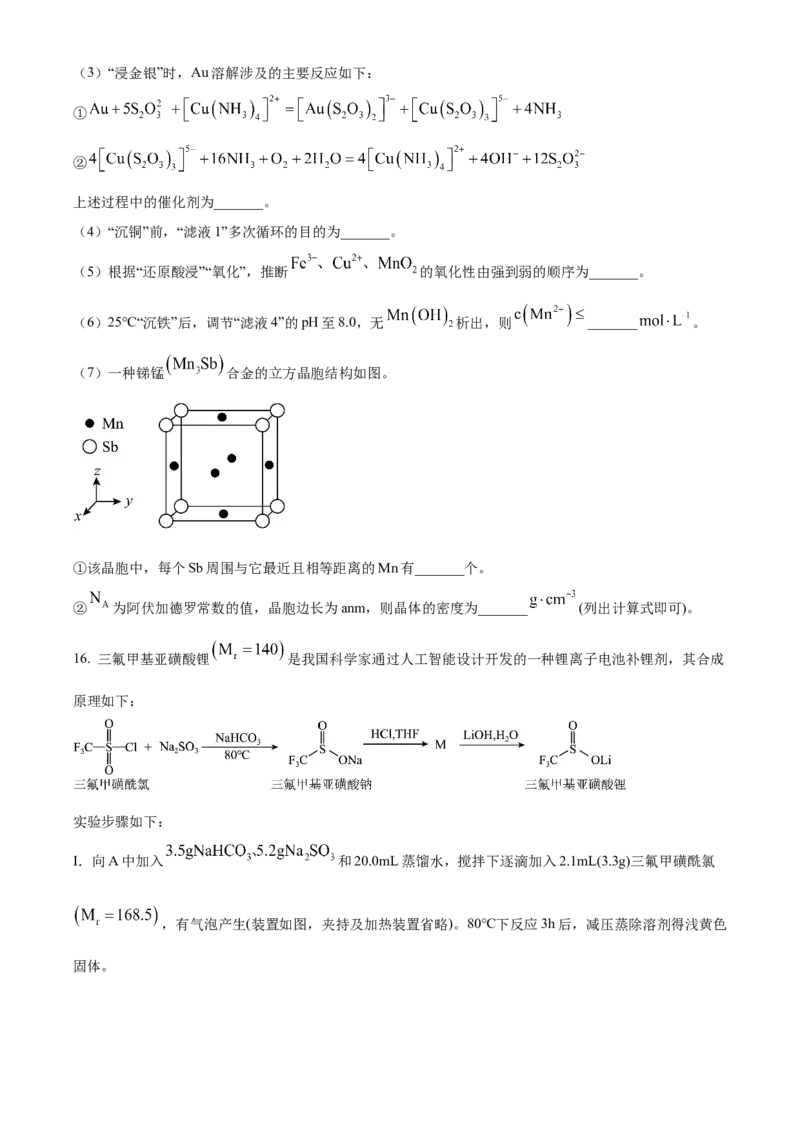
14. 甲醛法测定 的反应原理为 。取含 的废
水浓缩至原体积的 后,移取20.00mL,加入足量甲醛反应后,用 的NaOH标准溶液滴
定。滴定曲线如图1,含氮微粒的分布分数 与pH关系如图2[比如:
]。下列说法正确的是A. 废水中 的含量为
B. c点:
C. a点:
D. 的平衡常数
二、非选择题:本题共4小题,共58分。
15. 从褐铁矿型金-银矿(含Au、Ag、 、 、CuO、 等)中提取Au、Ag,并回收其它有价金
属的一种工艺如下:
已知:①金-银矿中Cu、Mn元素的含量分别为0.19%、2.35%。
②25℃时, 的 为 。
回答下列问题:
(1)基态Cu原子的价层电子排布式为_______。
(2)“还原酸浸”时, 反应的离子方程式为_______。(3)“浸金银”时,Au溶解涉及的主要反应如下:
①
②
上述过程中的催化剂为_______。
(4)“沉铜”前,“滤液1”多次循环的目的为_______。
(5)根据“还原酸浸”“氧化”,推断 的氧化性由强到弱的顺序为_______。
(6)25℃“沉铁”后,调节“滤液4”的pH至8.0,无 析出,则 _______ 。
(7)一种锑锰 合金的立方晶胞结构如图。
①该晶胞中,每个Sb周围与它最近且相等距离的Mn有_______个。
② 为阿伏加德罗常数的值,晶胞边长为anm,则晶体的密度为_______ (列出计算式即可)。
16. 三氟甲基亚磺酸锂 是我国科学家通过人工智能设计开发的一种锂离子电池补锂剂,其合成
原理如下:
实验步骤如下:
Ⅰ.向A中加入 和20.0mL蒸馏水,搅拌下逐滴加入2.1mL(3.3g)三氟甲磺酰氯
,有气泡产生(装置如图,夹持及加热装置省略)。80℃下反应3h后,减压蒸除溶剂得浅黄色
固体。Ⅱ.向上述所得固体中加入10.0mL四氢呋喃(THF),充分搅拌后,加入无水 ,振荡,抽滤、洗涤。
将所得滤液减压蒸除THF,得黏稠状固体。加入适量乙醇进行重结晶。
Ⅲ.将所得三氟甲基亚磺酸钠和3.0mLTHF加入圆底烧瓶中,搅拌溶解后逐滴加入足量浓盐酸,析出白色
固体。抽滤、洗涤。
Ⅳ.将滤液转入圆底烧瓶中,加入2.0mL蒸馏水和过量LiOH。室温搅拌反应1h后,减压蒸除溶剂,得粗
产品。加入适量乙醇进行重结晶,得产品1.1g。
已知:THF是一种有机溶剂,与水任意比互溶。
回答下列问题:
(1)仪器A的名称为_______,冷凝管中冷却水应从_______(填“b”或“c”)口通入。
(2)步骤Ⅰ反应中有气泡产生,其主要成分为_______。
(3)步骤Ⅱ中第一次洗涤的目的是_______。
的
(4)步骤Ⅲ中发生反应 化学方程式为_______,判断加入浓盐酸已足量的方法为_______。
(5)步骤Ⅳ中加入蒸馏水的作用是_______。
(6)三氟甲基亚磺酸锂的产率为_______(列出计算式即可)。
17. 我国科学家研发出一种乙醇(沸点78.5℃)绿色制氢新途径,并实现高附加值乙酸(沸点118℃)的生产,
主要反应为:
Ⅰ.
Ⅱ.
回答下列问题:
(1)乙醇可由秸秆生产,主要过程为
秸秆 纤维素 _______ 乙醇
(2)对于反应Ⅰ:①已知 则 _______
。
②一定温度下,下列叙述能说明恒容密闭容器中反应达到平衡状态的是_______(填标号)。
A.容器内的压强不再变化
B.混合气体的密度不再变化
C. 的体积分数不再变化
D.单位时间内生成 ,同时消耗
③反应后从混合气体分离得到 ,最适宜的方法为_______。
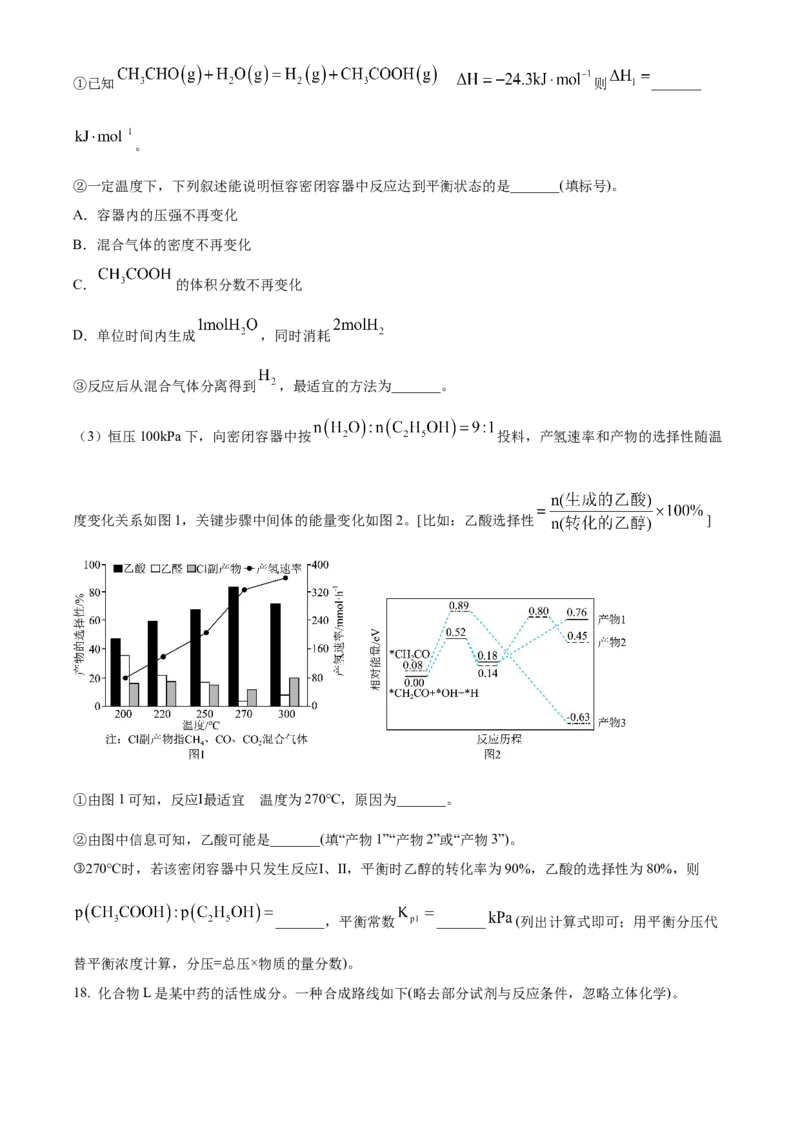
(3)恒压100kPa下,向密闭容器中按 投料,产氢速率和产物的选择性随温
度变化关系如图1,关键步骤中间体的能量变化如图2。[比如:乙酸选择性 ]
的
①由图1可知,反应Ⅰ最适宜 温度为270℃,原因为_______。
②由图中信息可知,乙酸可能是_______(填“产物1”“产物2”或“产物3”)。
③270℃时,若该密闭容器中只发生反应Ⅰ、Ⅱ,平衡时乙醇的转化率为90%,乙酸的选择性为80%,则
_______,平衡常数 _______ (列出计算式即可;用平衡分压代
替平衡浓度计算,分压=总压×物质的量分数)。
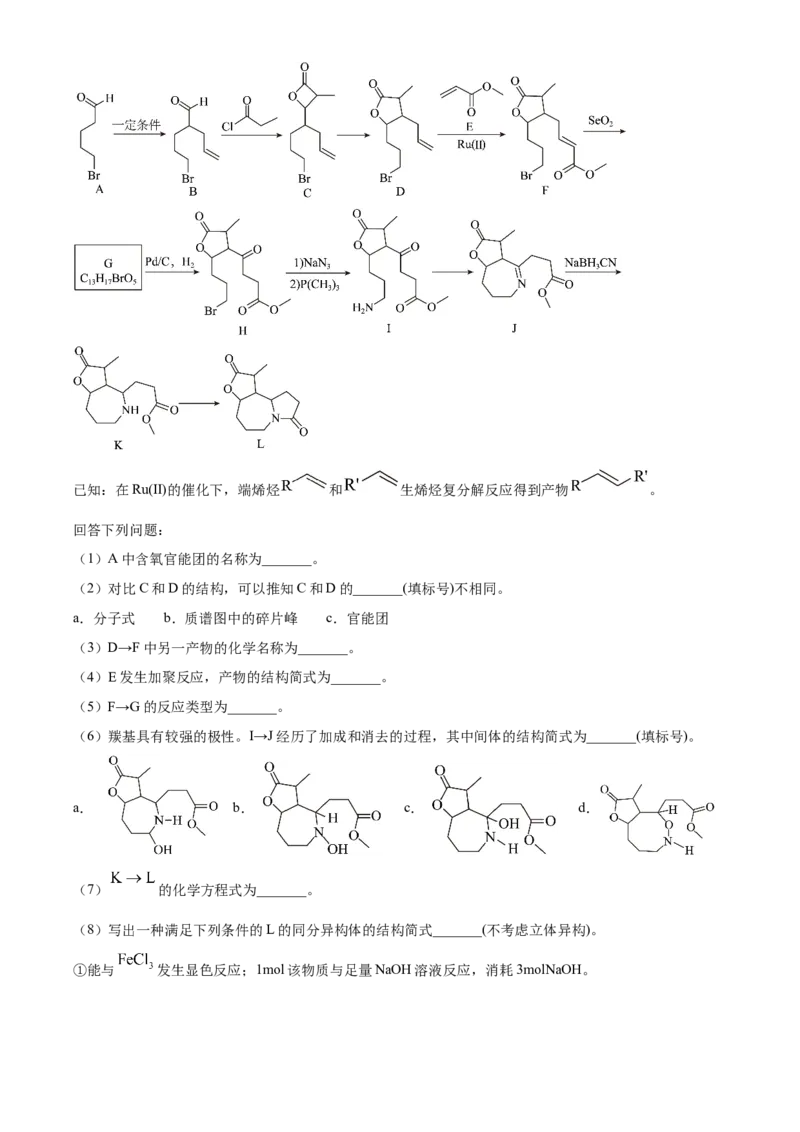
18. 化合物L是某中药的活性成分。一种合成路线如下(略去部分试剂与反应条件,忽略立体化学)。已知:在Ru(Ⅱ)的催化下,端烯烃 和 生烯烃复分解反应得到产物 。
回答下列问题:
(1)A中含氧官能团的名称为_______。
(2)对比C和D的结构,可以推知C和D的_______(填标号)不相同。
a.分子式 b.质谱图中的碎片峰 c.官能团
(3)D→F中另一产物的化学名称为_______。
(4)E发生加聚反应,产物的结构简式为_______。
(5)F→G的反应类型为_______。
(6)羰基具有较强的极性。I→J经历了加成和消去的过程,其中间体的结构简式为_______(填标号)。
a. b. c. d.
(7) 的化学方程式为_______。
(8)写出一种满足下列条件的L的同分异构体的结构简式_______(不考虑立体异构)。
①能与 发生显色反应;1mol该物质与足量NaOH溶液反应,消耗3molNaOH。②核磁共振氢谱显示6组峰,且峰面积比为 。
③含有酯基和氨基(或取代的氨基, , 和 可以是H或烃基)。