文档内容
专题 17 物质结构与性质(选修)
2020年高考真题
1.(2020年山东新高考)下列关于C、Si及其化合物结构与性质的论述错误的是
A.键能 、 ,因此C H 稳定性大于Si H
2 6 2 6
B.立方型SiC是与金刚石成键、结构均相似的共价晶体,因此具有很高的硬度
C.SiH 中Si的化合价为+4,CH 中C的化合价为-4,因此SiH 还原性小于CH
4 4 4 4
D.Si原子间难形成双键而C原子间可以,是因为Si的原子半径大于C,难形成 键
2.(2020年山东新高考)B NH(无机苯)的结构与苯类似,也有大π键。下列关于B NH 的说法错误的是
3 3 6 3 3 6
A.其熔点主要取决于所含化学键的键能
B.形成大π键的电子全部由N提供
C.分子中B和N的杂化方式相同
D.分子中所有原子共平面
3.(2020年新课标Ⅰ)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡
献而获得2019年诺贝尔化学奖。回答下列问题:
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为_________。
(2)Li及其周期表中相邻元素的第一电离能(I)如表所示。I(Li)> I (Na),原因是_________。I(Be)> I (B)>
1 1 1 1 1
I(Li),原因是________。
1
(3)磷酸根离子的空间构型为_______,其中P的价层电子对数为_______、杂化轨道类型为_______。
(4)LiFePO 的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶
4
点、共棱形成空间链结构。每个晶胞中含有LiFePO 的单元数有____个。
4
电池充电时,LiFeO 脱出部分Li+,形成Li FePO ,结构示意图如(b)所示,则x=_______,
4 1−x 4
n(Fe2+ )∶n(Fe3+)=_______。
4.(2020年新课标Ⅱ)钙钛矿(CaTiO )型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功
3能材料,回答下列问题:
(1)基态Ti原子的核外电子排布式为____________。
(2)Ti的四卤化物熔点如下表所示,TiF 熔点高于其他三种卤化物,自TiCl 至TiI 熔点依次升高,原因是
4 4 4
____________。
化合物 TiF TiCl TiBr TiI
4 4 4 4
熔点/℃ 377 ﹣24.12 38.3 155
(3)CaTiO 的晶胞如图(a)所示,其组成元素的电负性大小顺序是__________;金属离子与氧离子间的作用力
3
为__________,Ca2+的配位数是__________。
(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I﹣和有机碱离子 ,其晶胞如图(b)
所示。其中Pb2+与图(a)中__________的空间位置相同,有机碱 中,N原子的杂化轨道类型是
__________;若晶胞参数为a nm,则晶体密度为_________g·cm-3(列出计算式)。
(5)用上述金属卤化物光电材料制作的太阳能电池在使用过程中会产生单质铅和碘,降低了器件效率和使用
寿命。我国科学家巧妙地在此材料中引入稀土铕(Eu)盐,提升了太阳能电池的效率和使用寿命,其作用原
理如图(c)所示,用离子方程式表示该原理_______、_______。
5.(2020年新课标Ⅲ)氨硼烷(NH BH)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列
3 3
问题:(1)H、B、N中,原子半径最大的是______。根据对角线规则,B的一些化学性质与元素______的相似。
(2)NH BH 分子中,N—B化学键称为____键,其电子对由____提供。氨硼烷在催化剂作用下水解释放氢气:
3 3
3NH BH+6H O=3NH + +9H , 的结构如图所示: ;在该反应中,B原子的
3 3 2 3 2
杂化轨道类型由______变为______。
(3)NH BH 分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序
3 3
是__________。与NH BH 原子总数相等的等电子体是_________(写分子式),其熔点比
3 3
NH BH____________(填“高”或“低”),原因是在NH BH 分子之间,存在____________________,也
3 3 3 3
称“双氢键”。
(4)研究发现,氦硼烷在低温高压条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm,
α=β=γ=90°。氨硼烷的2×2×2超晶胞结构如图所示。
氨硼烷晶体的密度ρ=___________g·cm−3(列出计算式,设N 为阿伏加德罗常数的值)。
A
6.(2020年7月浙江选考)(1)气态氢化物热稳定性 大于 的主要原因是__________。
(2) 是离子化合物,各原子均满足8电子稳定结构, 的电子式是_______。
(3)常温下,在水中的溶解度乙醇大于氯乙烷,原因是__________。
7.(2020年江苏卷)以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵((NH )Fe(C HO))。
4 3 6 5 7 2
(1)Fe基态核外电子排布式为___________; 中与Fe2+配位的原子是________(填元素符号)。
(2)NH 分子中氮原子的轨道杂化类型是____________;C、N、O元素的第一电离能由大到小的顺序为
3
_______________。(3)与NH 互为等电子体的一种分子为_______________(填化学式)。
(4)柠檬酸的结构简式见图。1 mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为_________mol。
8.(2020年天津卷)Fe、Co、Ni是三种重要的金属元素。回答下列问题:
(1)Fe、Co、Ni在周期表中的位置为_________,基态Fe原子的电子排布式为__________。
(2)CoO的面心立方晶胞如图所示。设阿伏加德罗常数的值为N ,则CoO晶体的密度为______g﹒cm-3:三
A
种元素二价氧化物的晶胞类型相同,其熔点由高到低的顺序为_______。
(3)Fe、Co、Ni能与C1 反应,其中Co和为Ni均生产二氯化物,由此推断FeCl 、CoCl 和Cl 的氧化性由
2 3 3 2
强到弱的顺序为____,Co(OH) 与盐酸反应有黄绿色气体生成,写出反应的离子方程式:______。
3
(4)95℃时,将Ni片浸在不同质量分数的硫酸中,经4小时腐蚀后的质量损失情况如图所示,当
大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为_____。由于Ni与HSO 反应很慢,而与
2 4
稀硝酸反应很快,工业上选用HSO 和HNO 的混酸与Ni反应制备NiSO 。为了提高产物的纯度,在硫酸
2 4 3 4
中添加HNO 的方式为______(填“一次过量”或“少量多次”),此法制备NiSO 的化学方程式为_______。
3 4
9.(2020年山东新高考)CdSnAs 是一种高迁移率的新型热电材料,回答下列问题:
2
(1)Sn为ⅣA族元素,单质Sn与干燥Cl 反应生成SnCl 。常温常压下SnCl 为无色液体,SnCl 空间构型为
2 4 4 4_____________,其固体的晶体类型为_____________。
(2)NH 、PH 、AsH 的沸点由高到低的顺序为_____________(填化学式,下同),还原性由强到弱的顺序为
3 3 3
____________,键角由大到小的顺序为_____________。
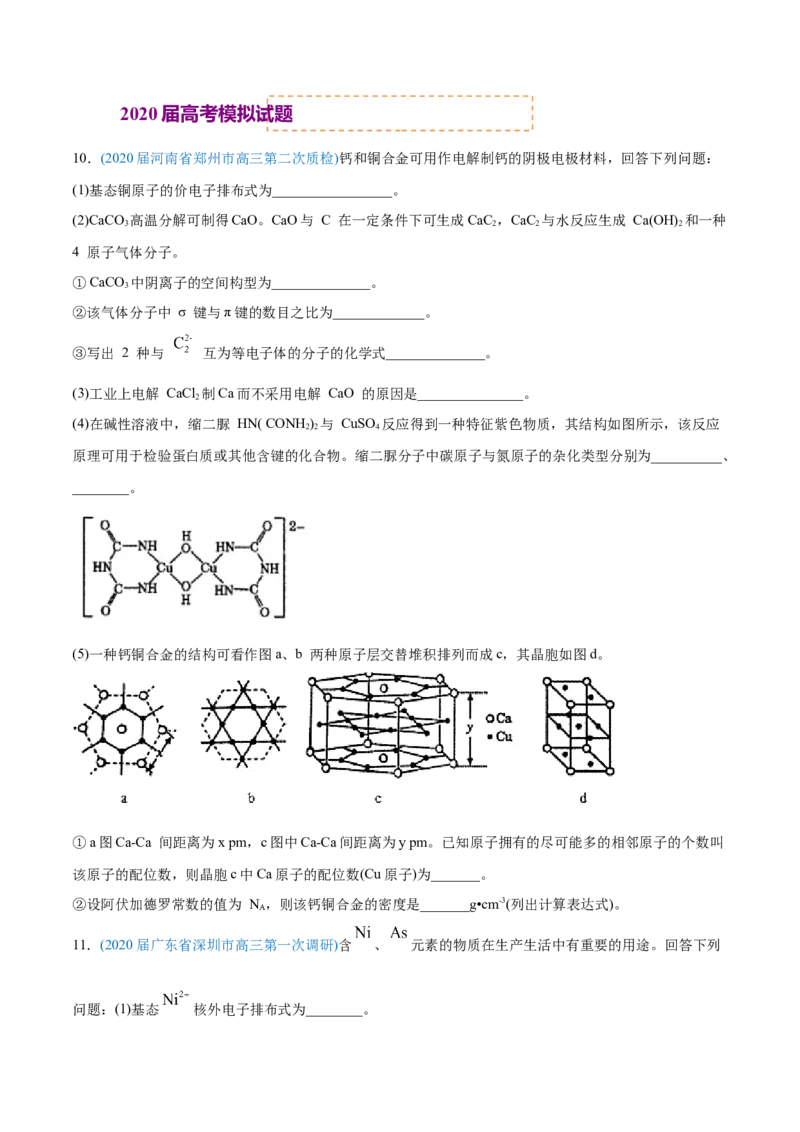
(3)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种
Cd2+配合物的结构如图所示,1mol该配合物中通过螯合作用形成的配位键有_________mol,该螯合物中N
的杂化方式有__________种。
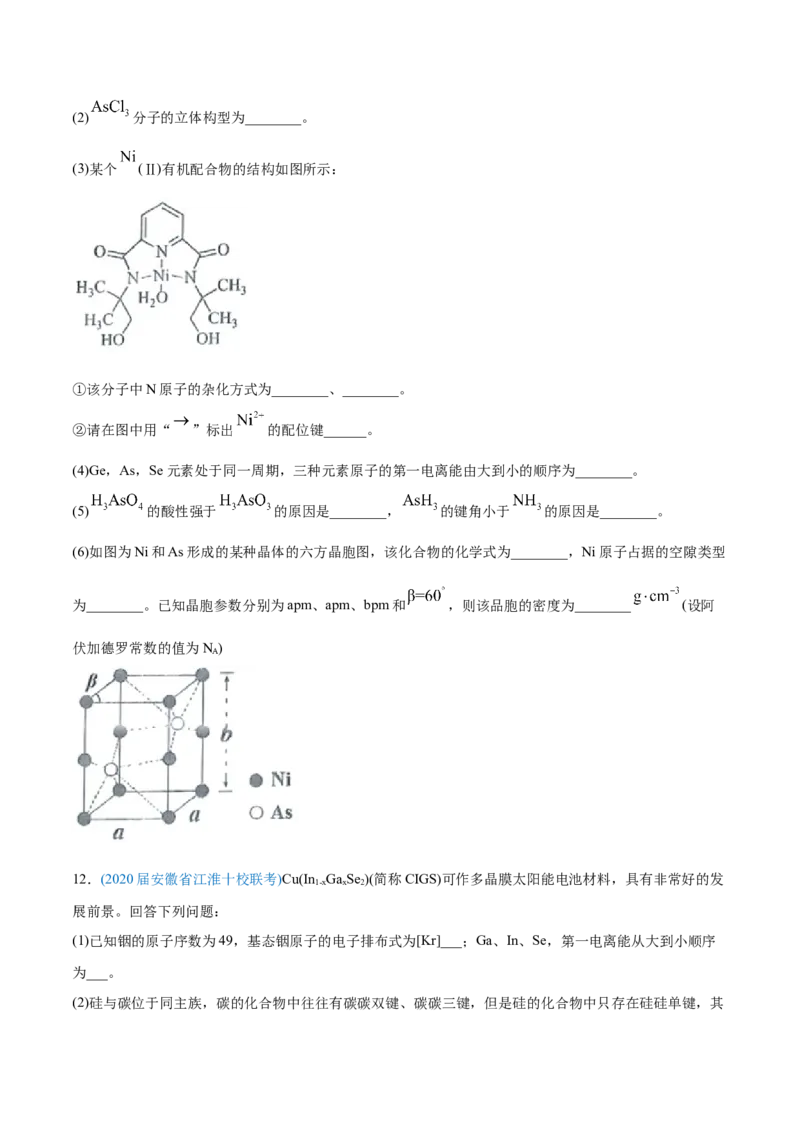
(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系
CdSnAs 的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示。
2
坐标原子 x y z
Cd 0 0 0
Sn 0 0 0.5
As 0.25 0.25 0.125
一个晶胞中有_________个Sn,找出距离Cd(0,0,0)最近的Sn_________(用分数坐标表示)。CdSnAs
2
晶体中与单个Sn键合的As有___________个。2020届高考模拟试题
10.(2020届河南省郑州市高三第二次质检)钙和铜合金可用作电解制钙的阴极电极材料,回答下列问题:
(1)基态铜原子的价电子排布式为_________________。
(2)CaCO 高温分解可制得CaO。CaO与 C 在一定条件下可生成CaC ,CaC 与水反应生成 Ca(OH) 和一种
3 2 2 2
4 原子气体分子。
①CaCO 中阴离子的空间构型为______________。
3
②该气体分子中 σ 键与π键的数目之比为_____________。
③写出 2 种与 互为等电子体的分子的化学式______________。
(3)工业上电解 CaCl 制Ca而不采用电解 CaO 的原因是_______________。
2
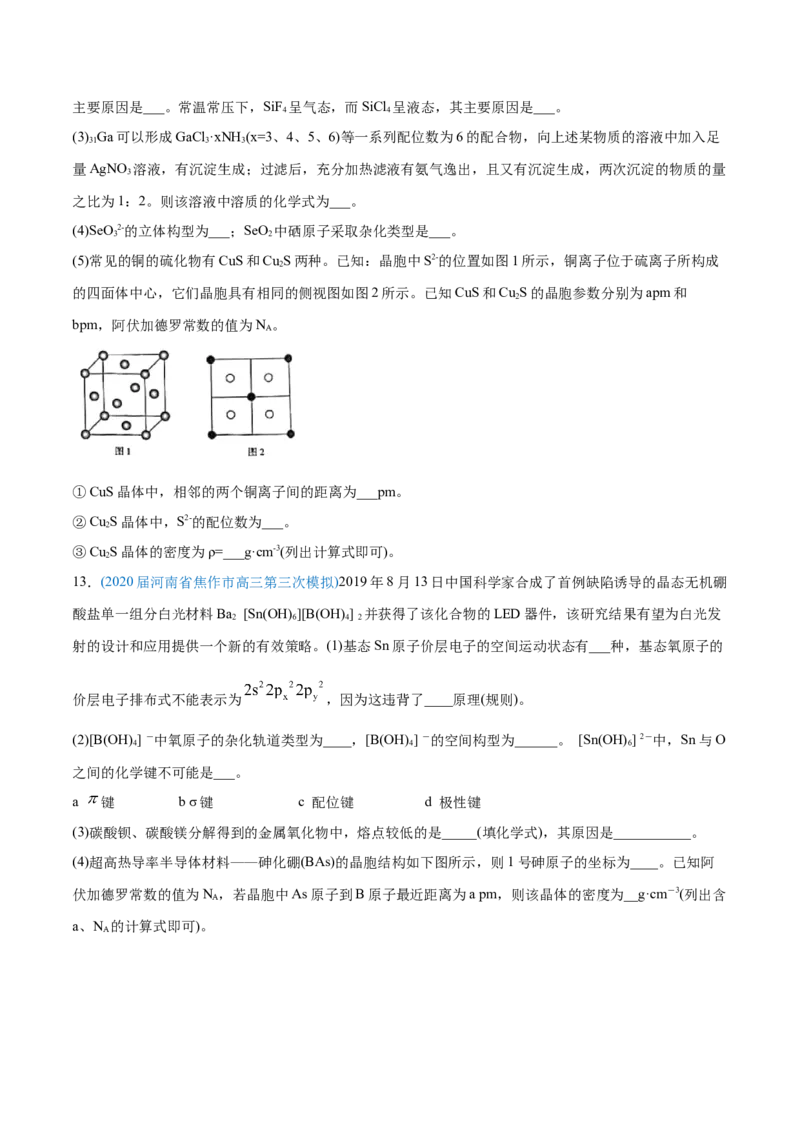
(4)在碱性溶液中,缩二脲 HN( CONH ) 与 CuSO 反应得到一种特征紫色物质,其结构如图所示,该反应
2 2 4
原理可用于检验蛋白质或其他含键的化合物。缩二脲分子中碳原子与氮原子的杂化类型分别为__________、
________。
(5)一种钙铜合金的结构可看作图a、b 两种原子层交替堆积排列而成c,其晶胞如图d。
①a图Ca-Ca 间距离为x pm,c图中Ca-Ca间距离为y pm。已知原子拥有的尽可能多的相邻原子的个数叫
该原子的配位数,则晶胞c中Ca原子的配位数(Cu原子)为_______。
②设阿伏加德罗常数的值为 N ,则该钙铜合金的密度是_______g•cm-3(列出计算表达式)。
A
11.(2020届广东省深圳市高三第一次调研)含 、 元素的物质在生产生活中有重要的用途。回答下列
问题:(1)基态 核外电子排布式为________。(2) 分子的立体构型为________。
(3)某个 (Ⅱ)有机配合物的结构如图所示:
①该分子中N原子的杂化方式为________、________。
②请在图中用“ ”标出 的配位键______。
(4)Ge,As,Se元素处于同一周期,三种元素原子的第一电离能由大到小的顺序为________。
(5) 的酸性强于 的原因是________, 的键角小于 的原因是________。
(6)如图为Ni和As形成的某种晶体的六方晶胞图,该化合物的化学式为________,Ni原子占据的空隙类型
为________。已知晶胞参数分别为apm、apm、bpm和 ,则该品胞的密度为________ (设阿
伏加德罗常数的值为N )
A
12.(2020届安徽省江淮十校联考)Cu(In GaSe )(简称CIGS)可作多晶膜太阳能电池材料,具有非常好的发
1-x x 2
展前景。回答下列问题:
(1)已知铟的原子序数为49,基态铟原子的电子排布式为[Kr]___;Ga、In、Se,第一电离能从大到小顺序
为___。
(2)硅与碳位于同主族,碳的化合物中往往有碳碳双键、碳碳三键,但是硅的化合物中只存在硅硅单键,其主要原因是___。常温常压下,SiF 呈气态,而SiCl 呈液态,其主要原因是___。
4 4
(3) Ga可以形成GaCl ·xNH (x=3、4、5、6)等一系列配位数为6的配合物,向上述某物质的溶液中加入足
31 3 3
量AgNO 溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,两次沉淀的物质的量
3
之比为1:2。则该溶液中溶质的化学式为___。
(4)SeO 2-的立体构型为___;SeO 中硒原子采取杂化类型是___。
3 2
(5)常见的铜的硫化物有CuS和Cu S两种。已知:晶胞中S2-的位置如图1所示,铜离子位于硫离子所构成
2
的四面体中心,它们晶胞具有相同的侧视图如图2所示。已知CuS和Cu S的晶胞参数分别为apm和
2
bpm,阿伏加德罗常数的值为N 。
A
①CuS晶体中,相邻的两个铜离子间的距离为___pm。
②Cu S晶体中,S2-的配位数为___。
2
③Cu S晶体的密度为ρ=___g·cm-3(列出计算式即可)。
2
13.(2020届河南省焦作市高三第三次模拟)2019年8月13日中国科学家合成了首例缺陷诱导的晶态无机硼
酸盐单一组分白光材料Ba [Sn(OH) ][B(OH) ] 并获得了该化合物的LED器件,该研究结果有望为白光发
2 6 4 2
射的设计和应用提供一个新的有效策略。(1)基态Sn原子价层电子的空间运动状态有___种,基态氧原子的
价层电子排布式不能表示为 ,因为这违背了____原理(规则)。
(2)[B(OH) ] -中氧原子的杂化轨道类型为____,[B(OH) ] -的空间构型为______。 [Sn(OH) ] 2-中,Sn与O
4 4 6
之间的化学键不可能是___。
a 键 b σ键 c 配位键 d 极性键
(3)碳酸钡、碳酸镁分解得到的金属氧化物中,熔点较低的是_____(填化学式),其原因是___________。
(4)超高热导率半导体材料——砷化硼(BAs)的晶胞结构如下图所示,则1号砷原子的坐标为____。已知阿
伏加德罗常数的值为N ,若晶胞中As原子到B原子最近距离为a pm,则该晶体的密度为__g·cm-3(列出含
A
a、N 的计算式即可)。
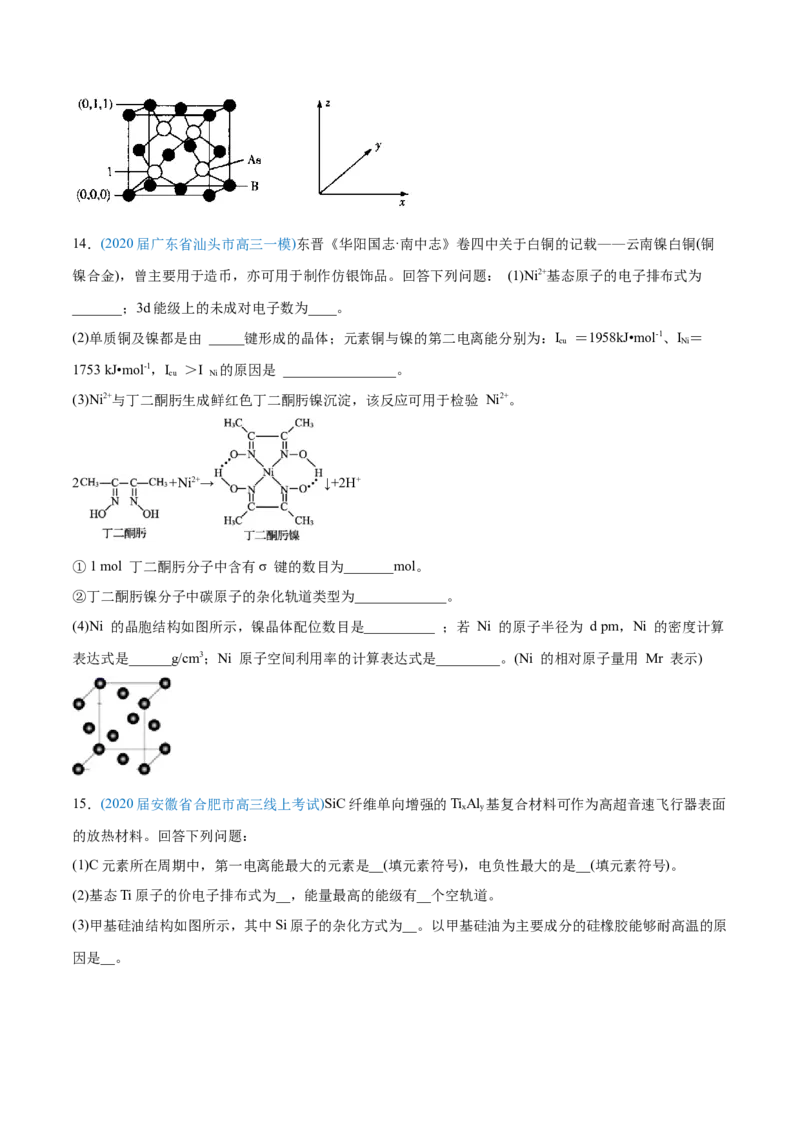
A14.(2020届广东省汕头市高三一模)东晋《华阳国志·南中志》卷四中关于白铜的记载——云南镍白铜(铜
镍合金),曾主要用于造币,亦可用于制作仿银饰品。回答下列问题: (1)Ni2+基态原子的电子排布式为
_______;3d能级上的未成对电子数为____。
(2)单质铜及镍都是由 _____键形成的晶体;元素铜与镍的第二电离能分别为:I =1958kJ•mol-1、I =
cu Ni
1753 kJ•mol-1,I >I 的原因是 ________________。
cu Ni
(3)Ni2+与丁二酮肟生成鲜红色丁二酮肟镍沉淀,该反应可用于检验 Ni2+。
2 +Ni2+→ ↓+2H+
①1 mol 丁二酮肟分子中含有σ 键的数目为_______mol。
②丁二酮肟镍分子中碳原子的杂化轨道类型为_____________。
(4)Ni 的晶胞结构如图所示,镍晶体配位数目是__________ ;若 Ni 的原子半径为 d pm,Ni 的密度计算
表达式是______g/cm3;Ni 原子空间利用率的计算表达式是_________。(Ni 的相对原子量用 Mr 表示)
15.(2020届安徽省合肥市高三线上考试)SiC纤维单向增强的Ti Al 基复合材料可作为高超音速飞行器表面
x y
的放热材料。回答下列问题:
(1)C元素所在周期中,第一电离能最大的元素是__(填元素符号),电负性最大的是__(填元素符号)。
(2)基态Ti原子的价电子排布式为__,能量最高的能级有__个空轨道。
(3)甲基硅油结构如图所示,其中Si原子的杂化方式为__。以甲基硅油为主要成分的硅橡胶能够耐高温的原
因是__。(4)Li CO、LiTiO 是锂离子电池中的常用材料,其中CO2-的空间构型为__,其含有的共价键类型有__。
2 3 2 3 3
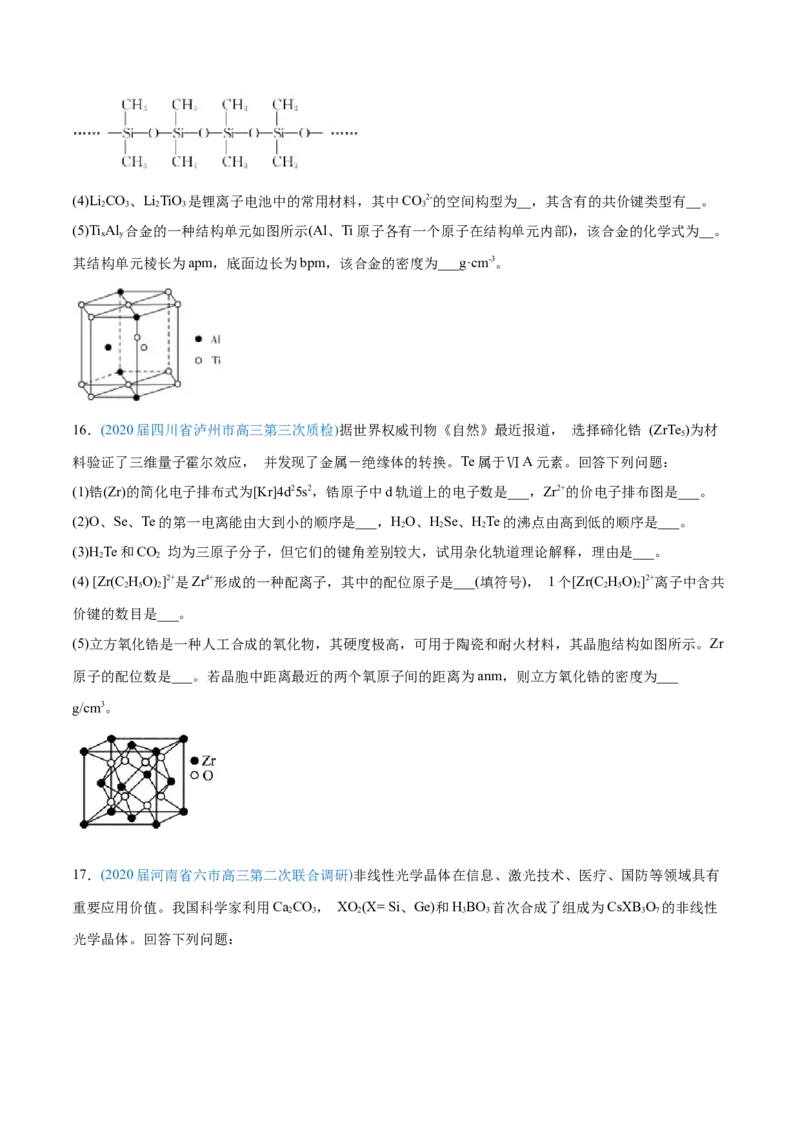
(5)Ti Al 合金的一种结构单元如图所示(Al、Ti原子各有一个原子在结构单元内部),该合金的化学式为__。
x y
其结构单元棱长为apm,底面边长为bpm,该合金的密度为___g·cm-3。
16.(2020届四川省泸州市高三第三次质检)据世界权威刊物《自然》最近报道, 选择碲化锆 (ZrTe )为材
5
料验证了三维量子霍尔效应, 并发现了金属-绝缘体的转换。Te属于ⅥA元素。回答下列问题:
(1)锆(Zr)的简化电子排布式为[Kr]4d25s2,锆原子中d轨道上的电子数是___,Zr2+的价电子排布图是___。
(2)O、Se、Te的第一电离能由大到小的顺序是___,HO、HSe、HTe的沸点由高到低的顺序是___。
2 2 2
(3)H Te和CO 均为三原子分子,但它们的键角差别较大,试用杂化轨道理论解释,理由是___。
2 2
(4) [Zr(C HO) ]2+是Zr4+形成的一种配离子,其中的配位原子是___(填符号), 1个[Zr(C HO) ]2+离子中含共
2 5 2 2 5 2
价键的数目是___。
(5)立方氧化锆是一种人工合成的氧化物,其硬度极高,可用于陶瓷和耐火材料,其晶胞结构如图所示。Zr
原子的配位数是___。若晶胞中距离最近的两个氧原子间的距离为anm,则立方氧化锆的密度为___
g/cm3。
17.(2020届河南省六市高三第二次联合调研)非线性光学晶体在信息、激光技术、医疗、国防等领域具有
重要应用价值。我国科学家利用Ca CO, XO (X= Si、Ge)和HBO 首次合成了组成为CsXB O 的非线性
2 3 2 3 3 3 7
光学晶体。回答下列问题:(1)基态硼原子的价电子排布图是____________,与硼处于同周期的非金属主族元素的第一电离能由大到小
的顺序为________________。
(2)B的简单氢化物BH,不能游离存在,常倾向于形成较稳定的B H 或与其他分子结合。
3 2 6
①B H 分子结构如图,则B原子的杂化方式为____________________。
2 6
②氨硼烷(NH BH)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子
3 3
是______________,写出一种与氨硼烷互为等电子体的分子_________(填分子式)。
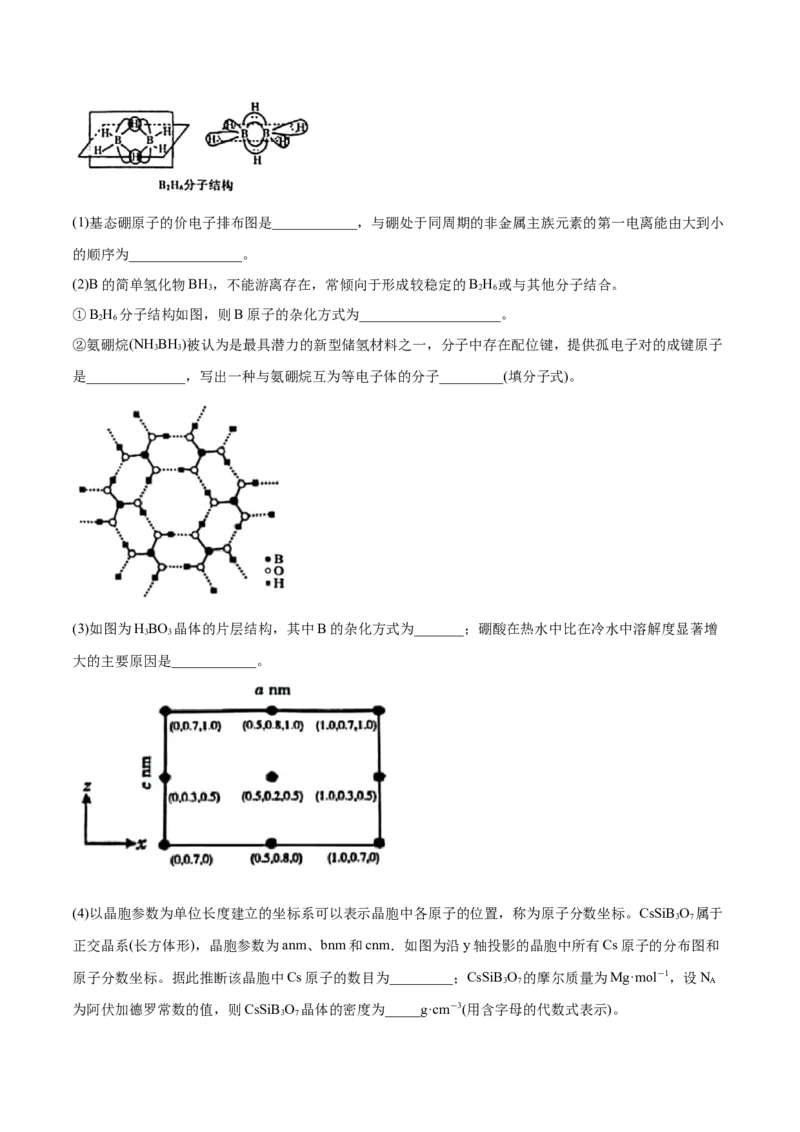
(3)如图为HBO 晶体的片层结构,其中B的杂化方式为_______;硼酸在热水中比在冷水中溶解度显著增
3 3
大的主要原因是____________。
(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子分数坐标。CsSiB O 属于
3 7
正交晶系(长方体形),晶胞参数为anm、bnm和cnm.如图为沿y轴投影的晶胞中所有Cs原子的分布图和
原子分数坐标。据此推断该晶胞中Cs原子的数目为_________;CsSiB O 的摩尔质量为Mg·mol-1,设N
3 7 A
为阿伏加德罗常数的值,则CsSiB O 晶体的密度为_____g·cm-3(用含字母的代数式表示)。
3 718.(2020届陕西省咸阳市高三模拟)某些过渡元素的相关化合物在化工、医药、材料等领域有着极为广泛
的应用。回答下列问题:(1)现有铜锌元素的4种微粒,①锌:[Ar]3d104s2;②锌:[Ar]3d104s1;③铜:
[Ar]3d104s1;④铜:[Ar]3d10。失去一个电子需要的最低能量由大到小的顺序是___(填字母)。
A ④②①③ B ④②③① C ①②④③ D ①④③②
(2)砷化镉(Cd As )是一种验证三维量子霍尔效应的材料。
3 2
①砷与卤素可形成多种卤化物,AsBr 、AsCl 、AsF 的熔点由低到高的顺序为__。砷酸的酸性弱于硒酸,
3 3 3
从分子结构的角度解释原因____。
②Cd2+与NH 形成配离子[Cd(NH )]2+中,配体的空间构型为__,画出配离子的结构式__(不考虑立体构型)。
3 3 4
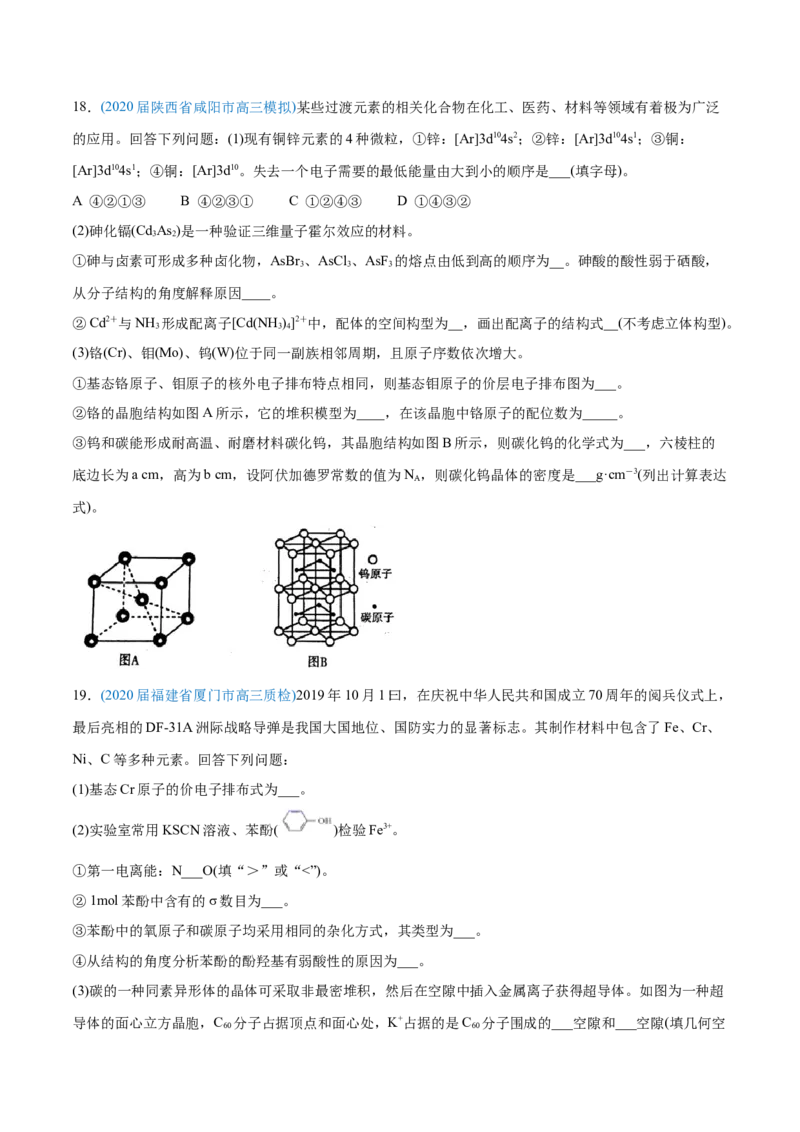
(3)铬(Cr)、钼(Mo)、钨(W)位于同一副族相邻周期,且原子序数依次增大。
①基态铬原子、钼原子的核外电子排布特点相同,则基态钼原子的价层电子排布图为___。
②铬的晶胞结构如图A所示,它的堆积模型为____,在该晶胞中铬原子的配位数为_____。
③钨和碳能形成耐高温、耐磨材料碳化钨,其晶胞结构如图B所示,则碳化钨的化学式为___,六棱柱的
底边长为a cm,高为b cm,设阿伏加德罗常数的值为N ,则碳化钨晶体的密度是___g·cm-3(列出计算表达
A
式)。
19.(2020届福建省厦门市高三质检)2019年10月1曰,在庆祝中华人民共和国成立70周年的阅兵仪式上,
最后亮相的DF-31A洲际战略导弹是我国大国地位、国防实力的显著标志。其制作材料中包含了Fe、Cr、
Ni、C等多种元素。回答下列问题:
(1)基态Cr原子的价电子排布式为___。
(2)实验室常用KSCN溶液、苯酚( )检验Fe3+。
①第一电离能:N___O(填“>”或“<”)。
②1mol苯酚中含有的σ数目为___。
③苯酚中的氧原子和碳原子均采用相同的杂化方式,其类型为___。
④从结构的角度分析苯酚的酚羟基有弱酸性的原因为___。
(3)碳的一种同素异形体的晶体可采取非最密堆积,然后在空隙中插入金属离子获得超导体。如图为一种超
导体的面心立方晶胞,C 分子占据顶点和面心处,K+占据的是C 分子围成的___空隙和___空隙(填几何空
60 60间构型);若C 分子的坐标参数分别为A(0,0,0),B( ,0, ),C(1,1,1)等,则距离A位置最近的
60
阳离子的原子坐标参数为___。
(4)Ni可以形成多种氧化物,其中一种NiO晶体晶胞结构为NaCl型,由于晶体缺陷,a的值为0.88,且晶
a
体中的Ni分别为Ni2+、Ni3+,则晶体Ni2与Ni3+产的最简整数比为___,晶胞参数为428pm,则晶体密度为
___g•cm-3(N 表示阿伏加德罗常数的值,列出表达式)。
A
20.(2020届河南省洛阳市高三第三次统考)层状复合金属氢氧化物(简称“层状氢氧化物”),主体层板由
二元(或多元)金属氢氧化物层构成,层间阴离子可以被其他阴离子取代,因此可以作为离子交换剂,在材
料、化工、医药和环境保护等方面有着广泛的用途。镁铝碳酸根型水滑石是人们最早发现的层状氢氧化物。
回答下列问题:
(1)下列状态的镁中,电离最外层一个电子所需能量最小的是___________(填标号)。
A. B. C. D.
(2)一种水滑石的化学式为MgAl (OH) CO•H O.其层板结构如图1。CO2-中碳的杂化类型是____。在图中
4 2 12 3 2 3
最小的一个二维菱形晶胞(以图中Al为顶点)中含有___________个Al3+。每个镁氧八面体周围有
_______________个相邻铝氧八面体和_______________个相邻镁氧八面体。
(3)水滑石中氢氧化物层的OH-和层间阴离子间的主要作用力为_______________,水滑石作为离子交换剂,
去除水体中阴离子去除效果依次为:PO 3->CrO 2->NO-,其原因是___________
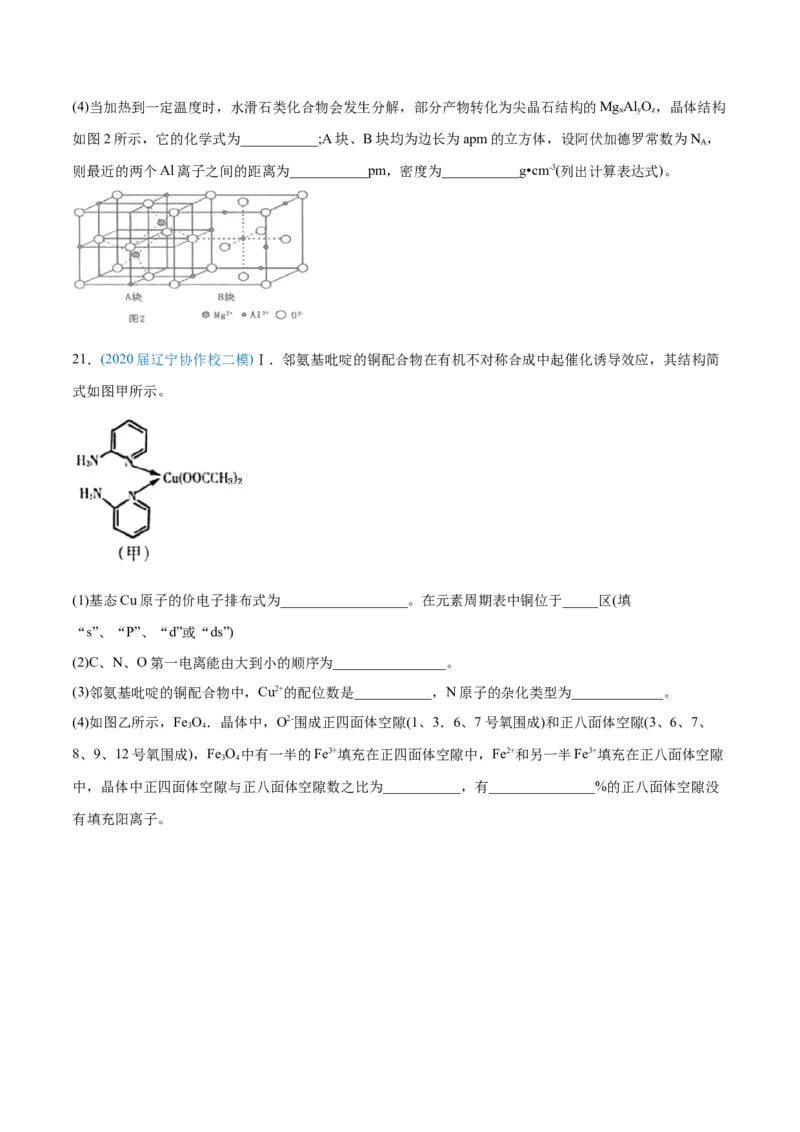
4 4 3(4)当加热到一定温度时,水滑石类化合物会发生分解,部分产物转化为尖晶石结构的MgAl O,晶体结构
x y z
如图2所示,它的化学式为___________;A块、B块均为边长为apm的立方体,设阿伏加德罗常数为N ,
A
则最近的两个Al离子之间的距离为___________pm,密度为___________g•cm-3(列出计算表达式)。
21.(2020届辽宁协作校二模)Ⅰ.邻氨基吡啶的铜配合物在有机不对称合成中起催化诱导效应,其结构简
式如图甲所示。
(1)基态Cu原子的价电子排布式为__________________。在元素周期表中铜位于_____区(填
“s”、“P”、“d”或“ds”)
(2)C、N、O第一电离能由大到小的顺序为________________。
(3)邻氨基吡啶的铜配合物中,Cu2+的配位数是___________,N原子的杂化类型为_____________。
(4)如图乙所示,Fe O.晶体中,O2-围成正四面体空隙(1、3.6、7号氧围成)和正八面体空隙(3、6、7、
3 4
8、9、12号氧围成),Fe O 中有一半的Fe3+填充在正四面体空隙中,Fe2+和另一半Fe3+填充在正八面体空隙
3 4
中,晶体中正四面体空隙与正八面体空隙数之比为___________,有_______________%的正八面体空隙没
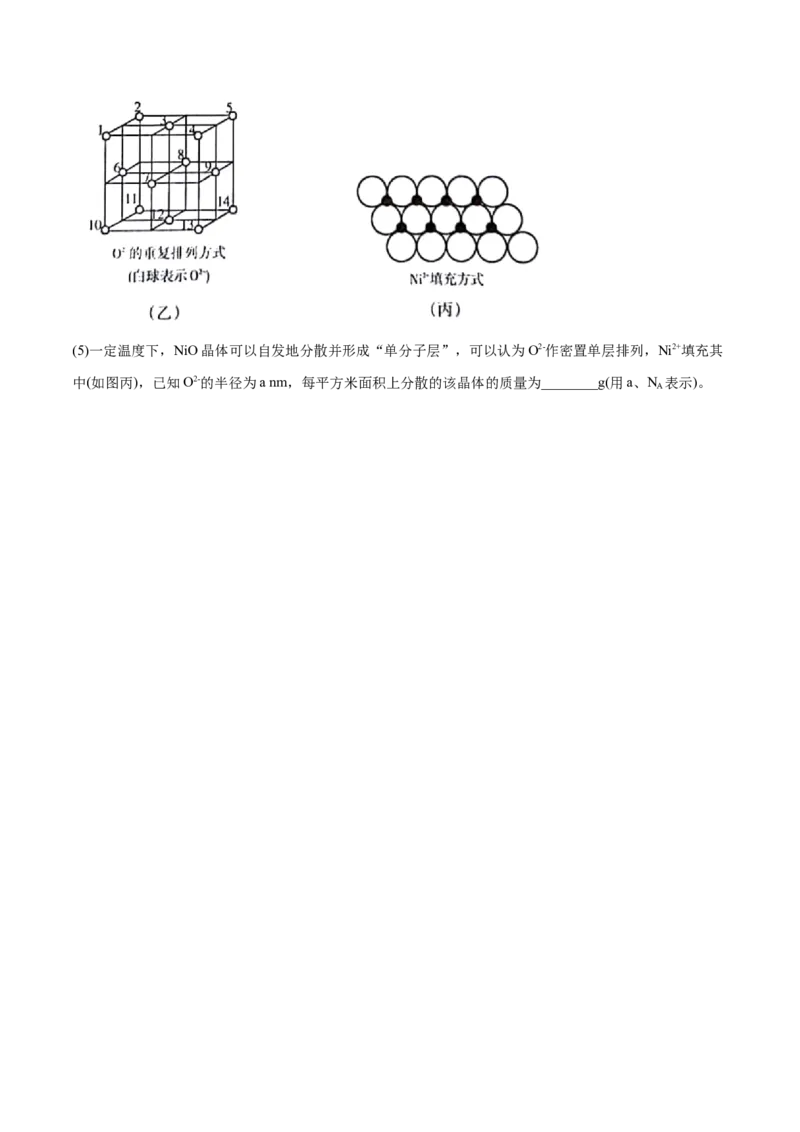
有填充阳离子。(5)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其
中(如图丙),已知O2-的半径为a nm,每平方米面积上分散的该晶体的质量为________g(用a、N 表示)。
A