文档内容
专题 31 盐类水解
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 盐类水解原理、影响因素及应用
考点二 水溶液中粒子浓度的数量关系
考点一 盐类水解原理、影响因素及应用
1.(2023·浙江·校联考三模)下列物质属于盐类且水溶液呈碱性的是
A.KCl B. C.BaO D.
2.(2023·浙江温州·乐清市知临中学校考一模)关于石灰氮( )的性质和推测不合理的是
A.具有碱性
B.属于离子化合物,含
C.与盐酸可发生氧化还原反应产生
D.水解可生成 和
3.(2023·广东惠州·统考模拟预测)化学让生活更美好。下列事实与盐类的水解无关的是
A.用明矾净水 B.用热的纯碱溶液清洗油污
C.用稀盐酸清除铁锈 D.配制 溶液时加入少量盐酸
4.(2023·广东清远·清新一中校考模拟预测)醛类可与 饱和溶液发生反应
(水溶性)。下列叙述错误的是
A.除去氯苯( )中微量杂质苯甲醛( ),加入饱和 溶液,且浓
度要尽可能大
1
原创精品资源学科网独家享有版权,侵权必究!B.将 转化为 ,加入的试剂可为HCl或NaOH
C.将醛类从水相中分离出来,只宜采用蒸馏法
D.室温下, 的电离常数 , , 的水溶液呈酸性
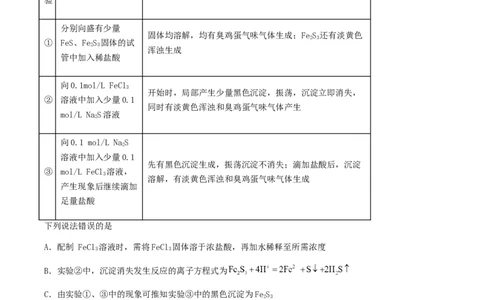
5.(2023·山东日照·统考一模)为探究FeCl 溶液与NaS溶液反应的产物,进行了如下实验(已知:FeS
3 2
和FeS 均为难溶于水的黑色固体)。
2 3
实
实验操作 实验现象
验
分别向盛有少量
固体均溶解,均有臭鸡蛋气味气体生成;FeS 还有淡黄色
2 3
① FeS、FeS 固体的试
2 3
浑浊生成
管中加入稀盐酸
向0.1mol/L FeCl
3
开始时,局部产生少量黑色沉淀,振荡,沉淀立即消失,
② 溶液中加入少量0.1
同时有淡黄色浑浊和臭鸡蛋气味气体产生
mol/L NaS溶液
2
向0.1 mol/L NaS
2
溶液中加入少量0.1
先有黑色沉淀生成,振荡沉淀不消失;滴加盐酸后,沉淀
③ mol/L FeCl 溶液,
3
溶解,有淡黄色浑浊和臭鸡蛋气味气体生成
产生现象后继续滴加
足量盐酸
下列说法错误的是
A.配制 FeCl 溶液时,需将FeCl 固体溶于浓盐酸,再加水稀释至所需浓度
3 3
B.实验②中,沉淀消失发生反应的离子方程式为
C.由实验①、③中的现象可推知实验③中的黑色沉淀为FeS
2 3
D. FeCl 溶液与NaS溶液反应的产物与反应体系的酸碱性有关
3 2
6.(2023·上海静安·统考二模)下列物质的水溶液显中性的是
A.FeSO B.KCl C.NaCO D.NaHCO
4 2 3 3
7.(2023·浙江杭州·浙江省临安中学校联考一模)氯化亚砜 又称亚硫酰氯,常温下为黄色的液
体,熔点 ,沸点 ,常用作有机合成工业中的氯化剂,遇水立即水解。下列说法不正确的是
A. 与 混合共热,可得无水B. 的空间结构为平面三角形
C. 与足量 溶液反应生成 和
D. 熔沸点比 高
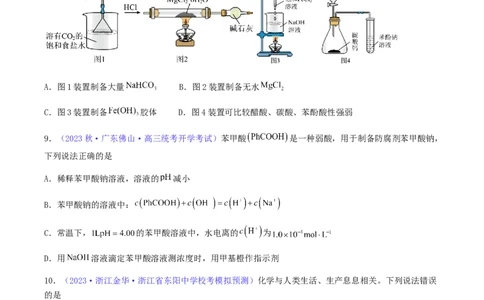
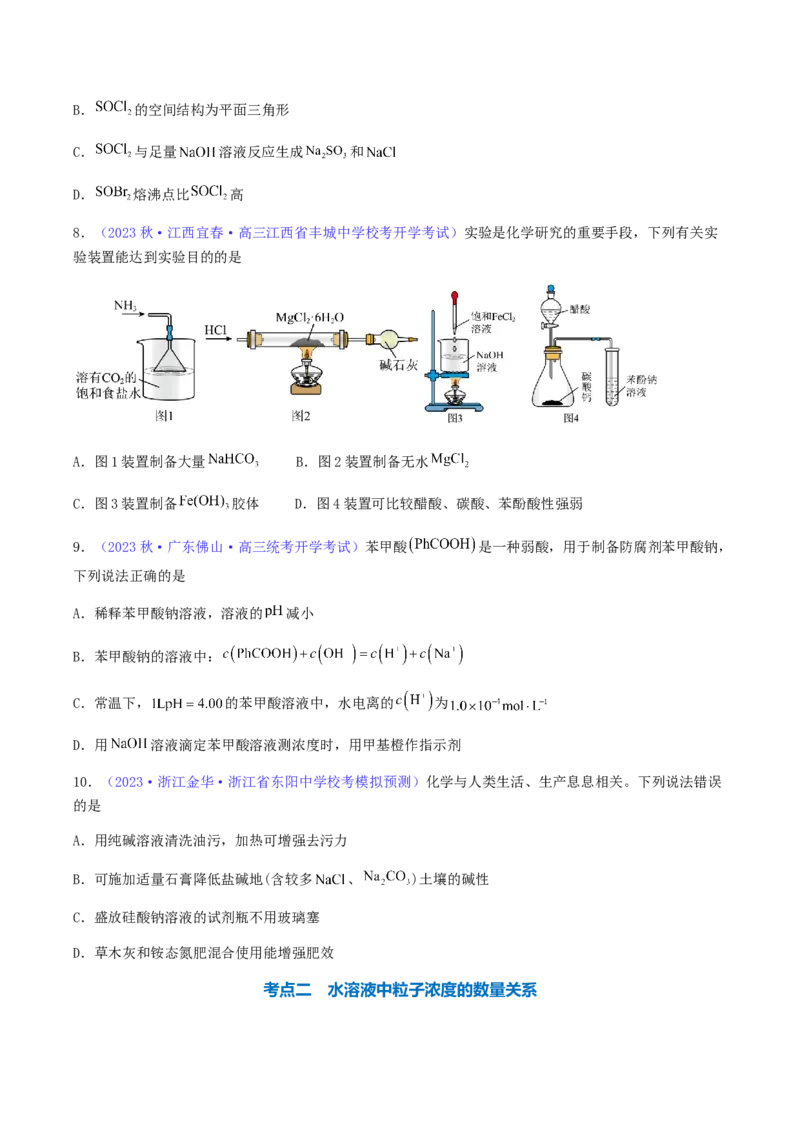
8.(2023秋·江西宜春·高三江西省丰城中学校考开学考试)实验是化学研究的重要手段,下列有关实
验装置能达到实验目的的是
A.图1装置制备大量 B.图2装置制备无水
C.图3装置制备 胶体 D.图4装置可比较醋酸、碳酸、苯酚酸性强弱
9.(2023秋·广东佛山·高三统考开学考试)苯甲酸 是一种弱酸,用于制备防腐剂苯甲酸钠,
下列说法正确的是
A.稀释苯甲酸钠溶液,溶液的 减小
B.苯甲酸钠的溶液中:
C.常温下, 的苯甲酸溶液中,水电离的 为
D.用 溶液滴定苯甲酸溶液测浓度时,用甲基橙作指示剂
10.(2023·浙江金华·浙江省东阳中学校考模拟预测)化学与人类生活、生产息息相关。下列说法错误
的是
A.用纯碱溶液清洗油污,加热可增强去污力
B.可施加适量石膏降低盐碱地(含较多 、 )土壤的碱性
C.盛放硅酸钠溶液的试剂瓶不用玻璃塞
D.草木灰和铵态氮肥混合使用能增强肥效
考点二 水溶液中粒子浓度的数量关系1.(2023·江苏南通·海门中学校考模拟预测)缓冲溶液可以抗御少量酸碱对溶液pH的影响。人体血液
里存在 缓冲体系,可使血液的pH稳定在7.4左右。当血液pH低于7.2或高于7.6时,会发
生酸中毒或碱中毒。 缓冲体系的缓冲作用可用下列平衡表示:
。实验室配制37℃时不同比例的 、
缓冲溶液。(已知该温度下 , ; )。下列说法正确的是
A.人体发生碱中毒时注射 溶液可以缓解症状
B. 的缓冲体系中:
C. 的缓冲体系中:
D. 的缓冲体系中:
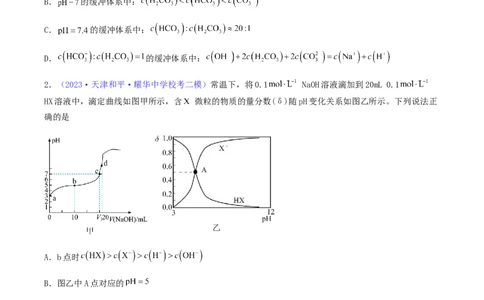
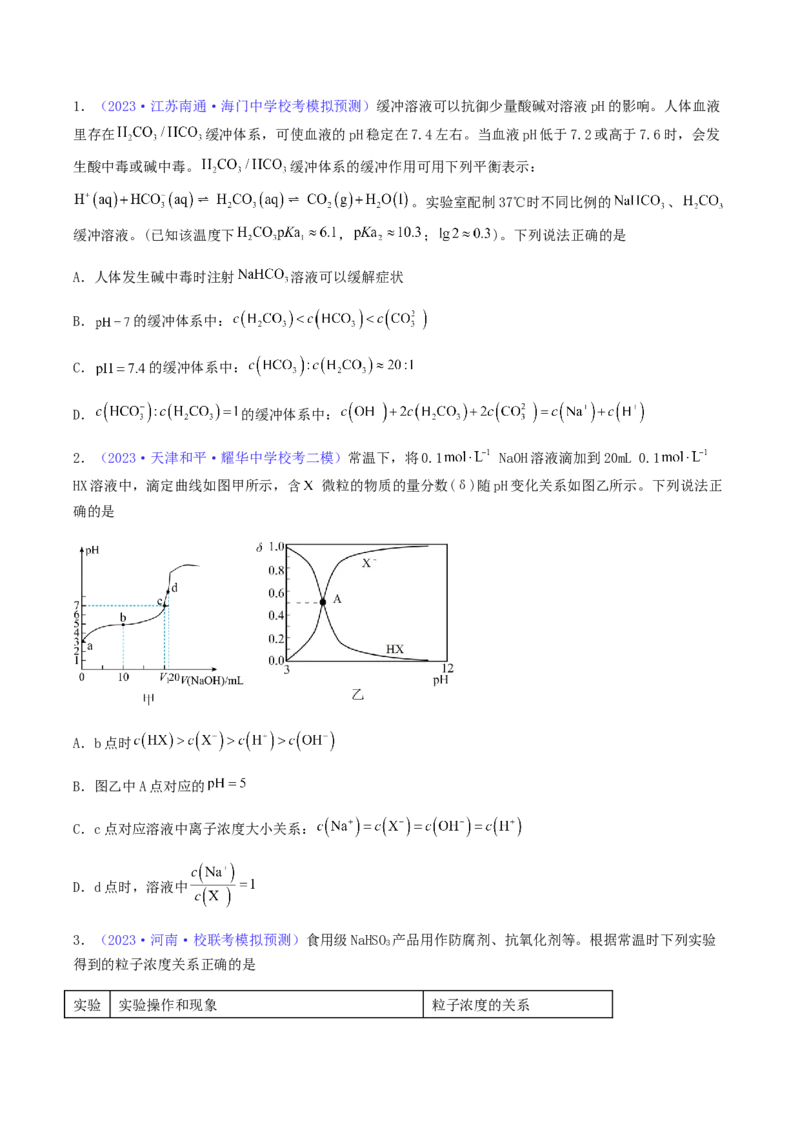
2.(2023·天津和平·耀华中学校考二模)常温下,将0.1 NaOH溶液滴加到20mL 0.1
HX溶液中,滴定曲线如图甲所示,含 微粒的物质的量分数(δ)随pH变化关系如图乙所示。下列说法正
确的是
A.b点时
B.图乙中A点对应的
C.c点对应溶液中离子浓度大小关系:
D.d点时,溶液中
3.(2023·河南·校联考模拟预测)食用级NaHSO 产品用作防腐剂、抗氧化剂等。根据常温时下列实验
3
得到的粒子浓度关系正确的是
实验 实验操作和现象 粒子浓度的关系向蓝色石蕊试纸上滴入2滴0.1 mol ·L-1NaHSO c(Na+) >c( ) >c(
3
①
溶液,试纸变红 ) >c(HSO)
2 3
c(Na+)-c( ) -c(
向10 mL0.1 mol ·L-1NaHSO 溶液中加入等体积
3
②
) -c(HSO) =0.05 mol
等浓度的NaOH溶液 2 3
·L-1
向0.1 mol ·L-1NaHSO 溶液中加入等浓度的
3
③ c( ) +c( )=c(Na+)
NaOH溶液至pH=7
A.①③ B.②③ C.①② D.①②③
4.(2023·江苏南通·校考模拟预测)室温下,通过下列实验探究 的性质。已知:25℃时,
的 、 的 。
实验1:配制 溶液,测得溶液 约为12;实验2:取 溶液,
向其中加入少量 固体充分搅拌,一段时间后过滤。向滤渣中加入足量稀盐酸,固体完全溶解;实验
3:取 溶液,向其中缓慢滴入等体积 稀盐酸。
下列说法正确的是
A.实验1所得溶液中,
B.根据实验2,可推测
C.实验3反应后溶液中存在:
D.25℃时,反应 的平衡常数
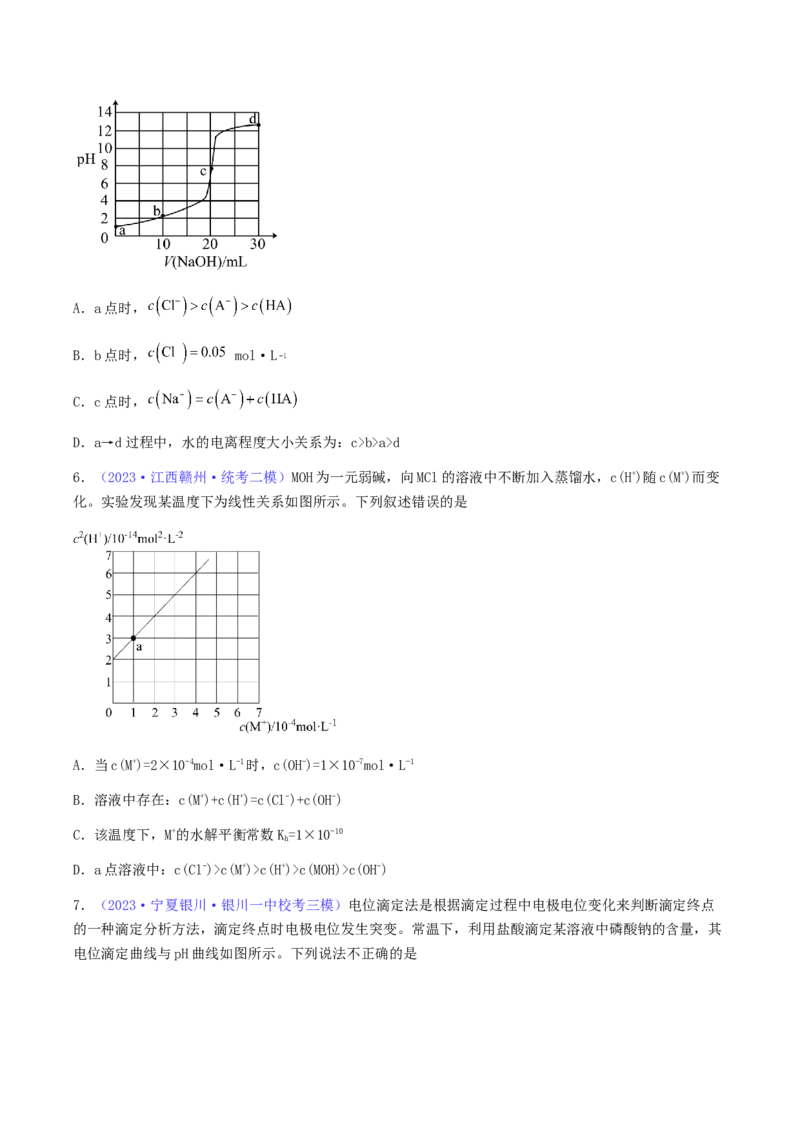
5.(2023·福建福州·统考模拟预测)室温下,将0.1 mol·L NaOH溶液滴入10 mL 0.1 mol·L HCl
和0.1 mol·L HA( )的混合溶液,测得混合溶液的pH随滴加的 的变化关系如图所示。
下列说法正确的是A.a点时,
B.b点时, mol·L
C.c点时,
D.a→d过程中,水的电离程度大小关系为:c>b>a>d
6.(2023·江西赣州·统考二模)MOH为一元弱碱,向MCl的溶液中不断加入蒸馏水,c(H+)随c(M+)而变
化。实验发现某温度下为线性关系如图所示。下列叙述错误的是
A.当c(M+)=2×10-4mol·L-1时,c(OH-)=1×10-7mol·L-1
B.溶液中存在:c(M+)+c(H+)=c(Cl-)+c(OH-)
C.该温度下,M+的水解平衡常数K=1×10-10
h
D.a点溶液中:c(Cl-)>c(M+)>c(H+)>c(MOH)>c(OH-)
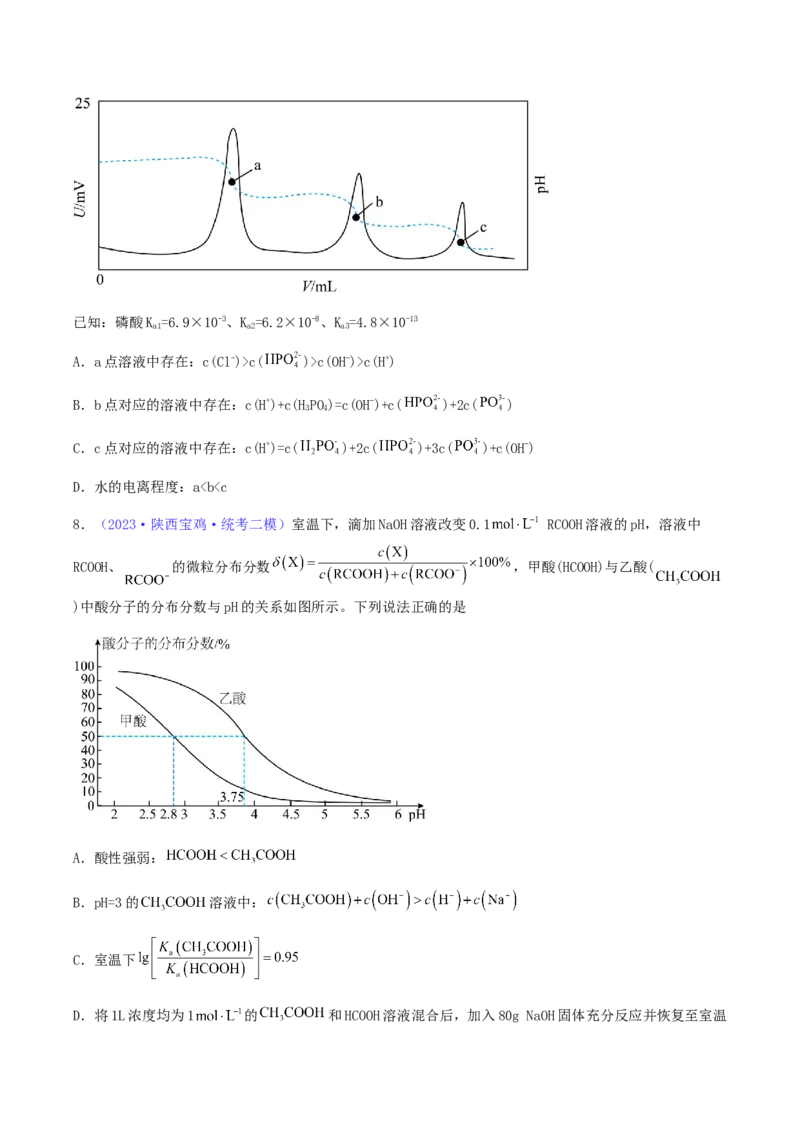
7.(2023·宁夏银川·银川一中校考三模)电位滴定法是根据滴定过程中电极电位变化来判断滴定终点
的一种滴定分析方法,滴定终点时电极电位发生突变。常温下,利用盐酸滴定某溶液中磷酸钠的含量,其
电位滴定曲线与pH曲线如图所示。下列说法不正确的是已知:磷酸K =6.9×10-3、K =6.2×10-8、K =4.8×10-13
a1 a2 a3
A.a点溶液中存在:c(Cl-)>c( )>c(OH-)>c(H+)
B.b点对应的溶液中存在:c(H+)+c(HPO)=c(OH-)+c( )+2c( )
3 4
C.c点对应的溶液中存在:c(H+)=c( )+2c( )+3c( )+c(OH-)
D.水的电离程度:a