文档内容
专题讲座(五) “位-构-性”综合推断题的解题方法
【考情分析】
元素推断题在历年高考中占有一定的比例(主要在选择题中体现),主要考查元素周期表中“位、构、
性”的关系及利用物质结构和性质进行综合推断的能力,要求熟练掌握短周期所有元素的结构特点、在周
期表中的位置以及它们的重要化合物的性质,在此基础上进行综合分析。如2019年全国卷Ⅰ第13题,卷
Ⅱ第9题,2018年全国卷Ⅰ第12题,卷Ⅱ第10题;2017年全国卷Ⅰ第12题,卷Ⅱ第9题等,都是结合原
子结构、元素周期表、元素及其化合物知识的综合考查。
【核心素养分析】
1.宏观辨识与微观探析:能从物质的宏观特征入手,对物质及其反应进行分类和表征。
2.证据推理与模型认知:能够通过对证据的分析,推出合理的结论;能解释证据与结论之间的关系。
3.科学态度与社会责任:具有理论联系实际的观念,能依据实际条件,结合所学的化学知识和方法,解决生产、
生活中简单的化学问题。
【知识梳理】
智能点一 推断元素的常用思路及常用步骤
1、推断元素的常用思路
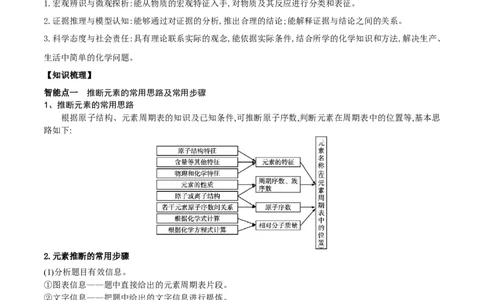
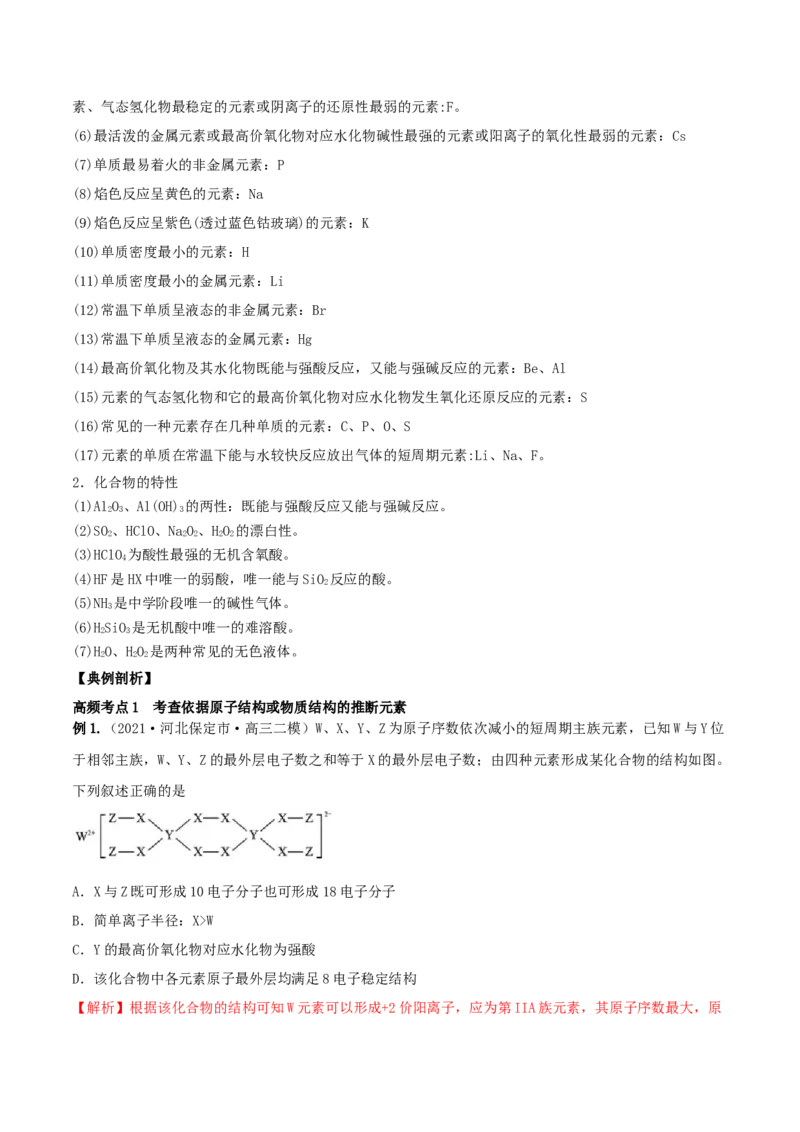
根据原子结构、元素周期表的知识及已知条件,可推断原子序数,判断元素在周期表中的位置等,基本思
路如下:
2.元素推断的常用步骤
(1)分析题目有效信息。
①图表信息——题中直接给出的元素周期表片段。
②文字信息——把题中给出的文字信息进行提炼。
③结构信息——题中给出的原子结构信息如微粒的质子数或电子数等。
(2)画出元素周期表片段,明确各元素的相对位置,推出元素。
(3)对照问题,结合元素周期律回答相应问题。
3.元素推断的方法
(1)对于简单的推断题只要应用有关知识点进行直接判断、比较或计算,即可找到答案。
(2)很多情况下只涉及短周期元素或前20号元素,可在草稿纸上画出一个只包含短周期或前20号元素的周
期表,对照此表进行推断。
(3)可利用题目暗示的突破口,联系其他条件,顺藤摸瓜,各个击破,推出结论。
4.“两步”快速突破元素推断题智能点二 元素推断的依据
(一)依据原子结构或物质结构推断元素
利用原子结构、核外电子排布特征为元素推断的突破口,是元素推断题的重要类型之一,题目通常以
文字叙述的形式给出元素原子的核外电子排布、位置关系等关键信息。解题时可结合短周期元素的原子结
构及元素的特殊性质,对元素进行合理的推断。
1.根据核外电子的排布三大规律推断元素
(1)最外层电子规律
最外层电子数(N) 3≤N<8 N=1或2 N>次外层电子数
第ⅠA族、第ⅡA
元素在周期 ⅢA族~ⅦA 第二周期(Li、Be)
族、第Ⅷ族、副
表中的位置 族 除外
族、0族元素氦
(2)“阴三、阳四”规律
某元素阴离子最外层电子数与次外层电子数相等,该元素位于第三周期;若为阳离子,则位
于第四周期。如S2-、K+最外层电子数与次外层电子数相等,则S位于第三周期,K位于第
四周期。
(3)“阴上、阳下”规律
电子层结构相同的离子,若电性相同,则位于同周期,若电性不同,则阳离子位于阴离子的
下一周期。如O2-、F-、Na+、Mg2+、Al3+电子层结构相同,则Na、Mg、Al位于O、F的下
一周期。
2.依据“等电子”微粒推断元素
(1)寻找“10电子”微粒和“18电子”微粒的方法
①“10电子”微粒②“18电子”微粒
CH—CH、HN—NH、HO—OH、F—F、F—CH、CH—OH……
3 3 2 2 3 3
(2)记忆其他等电子微粒
①“14电子”微粒:Si、N、CO、CH、C2-。
2 2 2 2
②“16电子”微粒:S、O、CH、HCHO。
2 2 4
(3)质子数和核外电子数分别相等的两种微粒关系
①可以是两种原子,如同位素原子。
②可以是两种分子,如CH、NH 等。
4 3
③可以是两种带电荷数相同的阳离子,如 NH+、HO+。
4 3
④可以是两种带电荷数相同的阴离子,如OH-、F-。
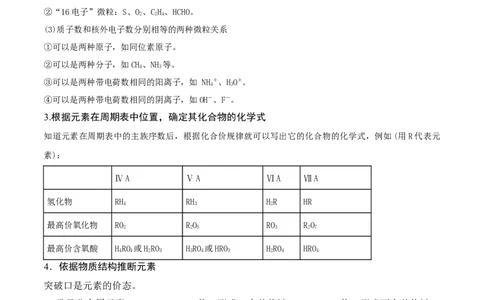
3.根据元素在周期表中位置,确定其化合物的化学式
知道元素在周期表中的主族序数后,根据化合价规律就可以写出它的化合物的化学式,例如(用R代表元
素):
ⅣA ⅤA ⅥA ⅦA
氢化物 RH RH HR HR
4 3 2
最高价氧化物 RO RO RO RO
2 2 5 3 2 7
最高价含氧酸 HRO 或HRO HRO 或HRO HRO HRO
4 4 2 3 3 4 3 2 4 4
4.依据物质结构推断元素
突破口是元素的价态。
(1)常见非金属元素。H、Cl、F:一价,形成一个共价键;O、S:二价,形成两个共价键;
N、P:三价,形成三个共价键;C、Si:四价,形成四个共价键。
(2)常见金属元素。K、Na、Li:形成+1价阳离子;Ca、Mg:形成+2价阳离子。
(二)依据元素周期表结构片段推断元素
残缺元素周期表型推断题一般给出两种信息:一是给出局部的元素周期表,展示出几种
不同元素的相对位置;二是给出某种元素的位置特征、原子结构特征或由该元素形成的单质
或化合物的特殊性质。解答此类题目时,要先根据给出的某种元素的特殊结构或性质,确定该元素在周期表中的位置,然后以此为“坐标原点”,根据其他元素与该元素的位置关系,
进而确定其他未知的元素。
1.元素周期表中短周期特殊结构的应用
(1)元素周期表中第1周期只有两种元素H和He,H元素所在的第ⅠA族为元素周期表的左侧
边界,第ⅠA族左侧无元素分布。
(2)He为0族元素,0族元素为元素周期表的右侧边界,0族元素右侧没有元素分布。
利用这个关系可以确定元素所在的周期和族。
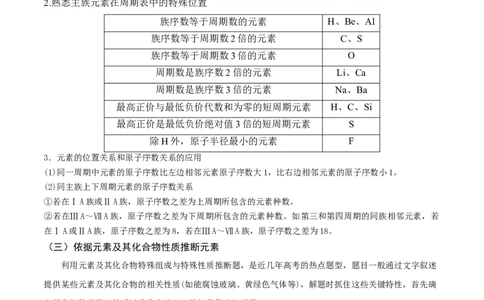
2.熟悉主族元素在周期表中的特殊位置
族序数等于周期数的元素 H、Be、Al
族序数等于周期数2倍的元素 C、S
族序数等于周期数3倍的元素 O
周期数是族序数2倍的元素 Li、Ca
周期数是族序数3倍的元素 Na、Ba
最高正价与最低负价代数和为零的短周期元素 H、C、Si
最高正价是最低负价绝对值3倍的短周期元素 S
除H外,原子半径最小的元素 F
3.元素的位置关系和原子序数关系的应用
(1)同一周期中元素的原子序数比左边相邻元素原子序数大1,比右边相邻元素的原子序数小1。
(2)同主族上下周期元素的原子序数关系
①若在ⅠA族或ⅡA族,原子序数之差为上周期所包含的元素种数。
②若在ⅢA~ⅦA族,原子序数之差为下周期所包含的元素种数。如第三和第四周期的同族相邻元素,若
在ⅠA或ⅡA族,原子序数之差为8,若在ⅢA~ⅦA族,原子序数之差为18。
(三)依据元素及其化合物性质推断元素
利用元素及其化合物特殊组成与特殊性质推断题,是近几年高考的热点题型,题目一般通过文字叙述
提供某些元素及其化合物的相关性质(如能腐蚀玻璃、黄绿色气体等),解题时抓住这些关键特性,首先确
定其为何种元素,然后以此为突破口,推知其他未知元素。
1.元素的特性
(1)形成化合物种类最多的元素或单质是自然界中硬度最大的物质的元素或气态氢化物中氢的质量分数最
大的元素:C
(2)空气中含量最多的元素或气态氢化物的水溶液呈碱性的元素:N
(3)元素的气态氢化物和它的最高价氧化物对应水化物起化合反应的元素:N。
(4)地壳中含量最多的元素或氢化物的沸点最高的元素或氢化物在通常情况下呈液态的元素:O
(5)最活泼的非金属元素、无正价的元素、无含氧酸的非金属元素、无氧酸(气态氢化物)可腐蚀玻璃的元素、气态氢化物最稳定的元素或阴离子的还原性最弱的元素:F。
(6)最活泼的金属元素或最高价氧化物对应水化物碱性最强的元素或阳离子的氧化性最弱的元素:Cs
(7)单质最易着火的非金属元素:P
(8)焰色反应呈黄色的元素:Na
(9)焰色反应呈紫色(透过蓝色钴玻璃)的元素:K
(10)单质密度最小的元素:H
(11)单质密度最小的金属元素:Li
(12)常温下单质呈液态的非金属元素:Br
(13)常温下单质呈液态的金属元素:Hg
(14)最高价氧化物及其水化物既能与强酸反应,又能与强碱反应的元素:Be、Al
(15)元素的气态氢化物和它的最高价氧化物对应水化物发生氧化还原反应的元素:S
(16)常见的一种元素存在几种单质的元素:C、P、O、S
(17)元素的单质在常温下能与水较快反应放出气体的短周期元素:Li、Na、F。
2.化合物的特性
(1)AlO、Al(OH) 的两性:既能与强酸反应又能与强碱反应。
2 3 3
(2)SO、HClO、NaO、HO 的漂白性。
2 2 2 2 2
(3)HClO 为酸性最强的无机含氧酸。
4
(4)HF是HX中唯一的弱酸,唯一能与SiO 反应的酸。
2
(5)NH 是中学阶段唯一的碱性气体。
3
(6)HSiO 是无机酸中唯一的难溶酸。
2 3
(7)HO、HO 是两种常见的无色液体。
2 2 2
【典例剖析】
高频考点1 考查依据原子结构或物质结构的推断元素
例1.(2021·河北保定市·高三二模)W、X、Y、Z为原子序数依次减小的短周期主族元素,已知W与Y位
于相邻主族,W、Y、Z的最外层电子数之和等于X的最外层电子数;由四种元素形成某化合物的结构如图。
下列叙述正确的是
A.X与Z既可形成10电子分子也可形成18电子分子
B.简单离子半径:X>W
C.Y的最高价氧化物对应水化物为强酸
D.该化合物中各元素原子最外层均满足8电子稳定结构
【解析】根据该化合物的结构可知W元素可以形成+2价阳离子,应为第IIA族元素,其原子序数最大,原子序数比其小的主族元素至少有3种,所以W应为第三周期元素,为Mg元素;X可以形成2个共价键,应
为第ⅥA族元素,所以X为O元素,Z可以形成1个共价键,原子序数小于O,则Z为H元素,所以Y元素
最外层电子数为6-1-2=3,所以Y为B元素。A.X为O元素,Z为H元素,二者可以形成10电子分子HO,
2
也可形成18电子分子HO, A正确;B.O2-和Mg2+电子层结构相同,但O2-核电荷数更小,半径更大,故B
2 2
正确;C.B元素的最高价氧化的水化物为HBO,为弱酸,故C错误;D.H元素最外层不满足8电子稳定
3 3
结构,故D错误。故答案为AB。
【答案】AB
【名师归纳】(1)掌握元素原子的4个关系式:①质子数=原子序数;②电子层数=周期序数;③最外层电子数=
主族序数;④最低负价=主族序数-8。
(2)熟练掌握元素周期表中的一些特殊规律:①各周期所能容纳元素种数;②稀有气体元素的原子序数及在
周期表中的位置;③同族上下相邻元素原子序数的关系。
【变式训练】(2021·宁夏银川市·高三模拟)已知W、X、Y、Z、L为原子序数依次递增的短周期主族元
素,其中W和Y,X和Z分别位于同主族,化合物M结构如图所示,则下列叙述正确的是
A.W和X形成的化合物只含共价键
B.简单离子半径:Z>L>Y>X>W
C.根据结构可推测化合物M可用作漂白剂
D.X、Z、L形成的简单氢化物中L的沸点最高
【解析】已知W、X、Y、Z、L为原子序数依次递增,X和Z位于同主族,且X形成两个共价键,所以X是O,
Z是S,Z、L为原子序数依次递增的短周期主族元素,则L是Cl,W和Y同主族,且Y+,W、X、Y、Z、L为
原子序数依次递增,所以Y是Na,W是H或者Li;即W、X、Y、Z、L分别是H(Li)、O、Na、S、Cl。A.X
是O,若W是H,则形成的化合物是HO和HO,只含共价键;若X是Li,则形成的化合物是LiO,含有离
2 2 2 2
子键,故A错误;B..电子层数越多,半径越大,电子层结构相同,核电荷数越大离子半径越小;简单离
子半径是 ,即Z>L>X>Y>W,故B错误;C..根据结构可推测化合物M中含有过氧键-
O-O-,有强氧化性可用作漂白剂,故C正确;D..X、Z、L形成的简单氢化物是HO、HS、HCl,水分子间
2 2
存在氢键,所以水的沸点最高,故D错误;故答案为:C。
【答案】C
高频考点2 考查依据元素周期表结构片段的推断元素
例2.(2021·陕西西安市·高三二模)现有短周期主族元素X、Y、Z、W,其中X、Y、Z在元素周期表中的相对位置关系如图,且X、Y、Z的原子序数之和为32,W原子的最外层电子数是其次外层电子数的2倍。
下列说法错误的是
X Z
Y
A.化合物WY 中所有原子的最外层均达到8电子稳定结构
2
B.原子半径:Y>Z
C.X、Z 、W简单氢化物的沸点:Z>X>W
D.X的氧化物对应水化物为强酸
【解析】现有短周期主族元素X、Y、Z、W,W原子的最外层电子数是其次外层电子数的2倍,则W的核外
电子排布为2、4,W为C。其中X、Y、Z在元素周期表中的相对位置关系如图,设X的原子序数为a, X、
Y、Z的原子序数之和为32,则a+a+2+a+9=32,得a=7,则X为N,Z为F,Y为S;A. 化合物WY 即CS 中
2 2
所有原子的最外层均达到8电子稳定结构,A正确;B. 同周期主族元素,从左到右原子半径逐渐减小;
元素位于同主族时,核电荷数越大,电子层数越多,原子半径越大,则原子半径:Y>Z,B正确;C. X、
Z 、W简单氢化物分别为氨气、氟化氢和甲烷,氨气和氟化氢分子间存在氢键,氟化氢标况下为液体,甲
烷分子间存在分子间作用力,则沸点:Z>X>W,C正确;D. X的最高价氧化物对应水化物即硝酸为强酸,
当化合价不为最高价时,例如亚硝酸是弱酸,D错误;答案选D。
【答案】D
【方法归纳】直接相邻的“┳”型、“┻”型、“╋”型原子序数关系
(1)
(2)
(3)
(4)
【变式训练】(2021·湖南永州市·高三三模)如表所示为元素周期表的一部分,其中X、Y、Z、W为短周
期元素,T的单质常温下为液体。下列说法错误的是A.X、Y的单质均存在同素异形体
B.Y、Z的简单氢化物的稳定性依次递增
C.R的单质可用于制造半导体材料
D.Y、Z、W元素简单阴离子的半径大小:Y>Z>W
【详解】T的单质常温下为液体,应为Br元素,由元素在周期表中的位置可知Z为F元素、W为Cl元素、
Y为O元素、X为P元素,R为Ge元素。A.P对应的同素异形体有红磷、白磷等,O对应的同素异形体由氧
气、臭氧等,故A正确;B.同周期元素从左到右元素的非金属性增强,元素的非金属性越强,对应的氢化
物越稳定,故Y、Z的简单氢化物的稳定性依次递增,故B正确;C.Ge和Si位于同一主族,为重要的半导
体材料,故C正确;D.Y、Z、W元素简单阴离子分别为O2-、F-、Cl-,核外电子排布相同的离子,根据
“序大径小”规律,简单阴离子的半径大小:Cl-> O2-> F-,故D错误;答案选D。
【答案】D
高频考点3 考查依据元素及其化合物性质的推断元素
例3.(2021·江西新余市·高三二模)X、Y、Z、W是原子序数依次增大的短周期元素,Y与W同主族,X
和Z的质子数之和为Y和W的质子数之和的一半。甲、乙、丙、丁是由这些元素组成的二元化合物,甲和
丁的组成元素相同且常温下均为液体,其中含甲3%的溶液是医院常用的一种消毒剂,化合物N是具有漂白
性的气体。上述物质间的转化关系如图所示(部分反应物和生成物及部分反应条件省略)。下列说法错误的
是
A.图中催化剂在一定条件下与铝粉混合可能发生铝热反应
B.由Y与Z元素形成的某常见化合物中,阴、阳离子个数比为1:2
C.沸点:丁>丙,是因为丁分子间存在氢键
D.丙与N能发生氧化还原反应,氧化剂和还原剂的物质的量之比为2:1
【答案】D
【解析】甲和丁的组成元素相同且常温下均为液体,其中含甲3%的溶液是医院常用的一种消毒剂,可推测
甲是HO,丁是HO,化合物N是具有漂白性的气体,可推测其是SO,根据物质间的转化关系则可推测M是
2 2 2 2氧气,丙是HS,则乙是硫化物。甲、乙、丙、丁是由这些元素组成的二元化合物,故X、Y、Z、W四种元
2
素中,由于X的原子序数最小,则X是H元素,Y与W同主族,则Y是氧元素,W是S元素,X和Z的质子数
之和为Y和W的质子数之和的一半,则Z是Na元素,则乙是NaS。A.经分析甲是HO,能使HO 分解的催
2 2 2 2 2
化剂种类很多,MnO 就是其中之一,MnO 在一定条件下与铝粉混合就能发生铝热反应,故A正确;B.经分
2 2
析Y是O元素,Z是Na,Y与Z元素形成的某常见化合物是NaO, 其阴、阳离子个数比为1:2,故B正确;
2
C.经分析丁是HO,丙是HS,沸点:HO>HS,是因为HO分子间存在氢键,故C正确;D.经分析丙HS,
2 2 2 2 2 2
N是SO,HS与SO 反应的化学方程式是2HS+ SO=3S↓+2HO,根据化学方程式中元素化合价变化情况,可
2 2 2 2 2 2
知HS是还原剂,SO 是氧化剂,则氧化剂和还原剂的物质的量之比为1:2,故D错误;本题答案D。
2 2
【归纳总结】常见元素及其化合物的特性
(1)形成化合物种类最多的元素、某一种单质是自然界中硬度最大的物质的元素或气态氢化物中氢的质量
分数最大的元素:C。
(2)空气中含量最多的元素或气态氢化物的水溶液呈碱性的元素:N。
(3)地壳中含量最多的元素或简单氢化物在常温下呈液态的元素:O。
(4)具有漂白性的物质:氯水、二氧化硫、过氧化钠、双氧水(HO)。
2 2
(5)最活泼的非金属元素、无正价的元素、无含氧酸的非金属元素、无氧酸(气态氢化物)可腐蚀玻璃的元
素、气态氢化物最稳定的元素或阴离子的还原性最弱的元素:F。
(6)单质密度最小的非金属元素:H;单质密度最小的金属元素:Li。
(7)常温下单质呈液态的非金属元素:Br;常温下单质呈液态的金属元素:Hg。
(8)最高价氧化物及其水化物既能与强酸反应,又能与强碱反应的元素:Al。
(9)元素的气态氢化物和它的最高价氧化物对应水化物起化合反应的元素:N。
(10)元素的单质在常温下能与水较快反应放出气体的短周期元素:Li、Na、F。
【变式训练】(2021·河北邯郸市·高三三模)X、Y、Z、W为原子序数递增的四种短周期元素,其中Z为
金属元素,其单质与水反应后溶液能使酚酞试液变为浅红色,X、W为同一主族元素,Y是地壳中含量最高
的元素。甲、乙、丙分别为X、Z、W形成的最高价氧化物。下列判断不正确的是
A.W位于元素周期表第三周期ⅣA族
B.原子半径:r(Z)˃r(W)>r(Y)>r(X)
C.丁为CO,反应③为工业制粗硅的原理
D.X、W简单氢化物的沸点: X < W【解析】X、Y、Z、W为原子序数递增的四种短周期元素,Y是地壳中含量最高的元素,则Y为O元素;其
中Z为金属元素,其单质与水反应后溶液能使酚酞试液变为浅红色,则Z与水反应的产物应是弱碱,则Z
为Mg,乙为MgO,甲可以和Mg反应得到MgO和X的单质,则X应为C,甲为CO,符合“X的单质在O 点燃
2 2
生成甲”,X、W为同一主族元素,且W也为短周期元素,所以W为Si元素,丙为SiO,C与SiO 高温反应
2 2
生成Si和CO,即丁是CO。A.W为Si元素,原子序数为14,位于第三周期ⅣA族,A正确;B.电子层数
越多原子半径越大,电子层数相同,核电荷数越小半径越大,所以原子半径从大到小顺序为:Mg>Si>C
>O,即r(Z)>r(W)>r(X)>r(Y),B错误;C.根据分析可知丁为CO,反应③为C与二氧化硅的反应,生成
硅和CO,为工业制粗硅的原理,C正确;D.X与W分别为C元素和Si元素,其简单氢化物均为分子构成,
因为CH 的相对分子质量较SiH 的小,分子间的范德华力较SiH 的小,所以其沸点相对较低,即X < W,D
4 4 4
正确;综上所述答案为B。
【答案】B
高频考点4 考查结合化学计算的推断元素
例4.(2020·山东泰安市·高三调研)化合物M由两种位于第四周期的过渡金属元素和一种位于第三周
期的非金属元素组成,一定条件下M存在如图所示转化。已知:固体Y中两种金属元素的化合价分别为
+2、+3。下列有关推断错误的是( )
A.气体X能使品红溶液、酸性高锰酸钾溶液、含酚酞的碳酸钠溶液褪色
B.溴水吸收气体X的离子方程式为Br+2HO+SO2HBr+2H++SO
2 2 2
C.根据上述数据推知,M的化学式为CuFeS
2
D.向KNO 和稀盐酸的混合溶液中加入少量固体Z,固体Z全部溶解
3
【解析】M在空气中灼烧,产生刺激性气味的气体X,气体X和溴水反应后的溶液与氯化钡反应生成的沉淀
是硫酸钡,硫酸钡的物质的量是 ,所以M中含有S元素,且物质的量是0.2mol,气体
X是二氧化硫;固体Y是金属氧化物,被CO还原为金属Z,红色固体R难溶于硫酸,所以R是Cu,铜的质
量是6.4g,固体Y中两种金属元素的化合价分别为+2、+3,则另一种金属为+3价,设另一种金属为T ,氧化物的化学式是 根据元素守恒,T元素的质量是 ; 的
质量是 ,设T元素的相对分子质量是a,则 ,a=56g/mol,所以
T是铁元素。A.气体X是二氧化硫,二氧化硫能使品红溶液、酸性高锰酸钾溶液、含酚酞的碳酸钠溶液褪
色,故A正确;B.溴水和二氧化硫反应生成硫酸和氢溴酸,反应的离子方程式为Br+2HO+SO=2Br-+4H+
2 2 2
+SO ,故B错误;C.根据上述数据推知,18.4g M含有Fe元素的物质的量是 、Cu元
素的物质的量是 、S元素的物质的量是0.2mol,M的化学式为CuFeS,故C正确;D.
2
固体Z是铁、铜的混合物,铁、铜都能溶液稀硝酸,向KNO 和稀盐酸的混合溶液中加入少量固体Z,固体Z
3
全部溶解,故D正确;选B。
【答案】B
【变式训练】(2020·辽宁大连市·高三二模)短周期主族元素X、Y、Z、R的原子序数依次增大,X是宇
宙中含量最多的元素,Y原子最外层电子数等于内层电子数的2倍。向100 mL XR的水溶液中缓缓通入RZ
2 2
气体,溶液pH与RZ 体积关系如图。下列说法正确的是( )
2
A.XR溶液的浓度为0.03 mol∙L−1
2
B.最简单气态氢化物的稳定性:Y>Z>R
C.X、Y、Z三种元素形成的化合物一定易溶于水
D. RZ 分别通入到XR、Ba(NO) 溶液中,均会产生沉淀
2 2 3 2
【解析】短周期主族元素X、Y、Z、R的原子序数依次增大,X是宇宙中含量最多的元素,X为H,Y原子最
外层电子数等于内层电子数的2倍,Y为C,向100 mL XR的水溶液中缓缓通入RZ 气体,溶液pH与RZ 体
2 2 2
积关系如图,则说明是HS通入SO,则Z为O,R为S。A. 根据2HS + SO = 3S↓+ 2HO,加入SO 气体体
2 2 2 2 2 2积336mL即0.015mol,溶液pH =7,即消耗HS物质的量为0.03mol,因此XR溶液的浓度为
2 2
,故A错误。B. 非金属性越强,最简单气态氢化物的稳定性越强,即
稳定性HO>CH,故B错误;C. H、C、O三种元素形成的化合物,如果属于酯等,则不溶于水,故C错误;
2 4
D. SO 通入到HS有黄色沉淀生成,SO 通入到Ba(NO) 溶液中生成硫酸钡沉淀,故D正确。答案为D。
2 2 2 3 2
【答案】D