文档内容
微专题 16 镁及其化合物的性质与海水提取镁的
工艺流程
【知识点梳理】
1.镁的性质
(1)物理性质:具有银白色金属光泽的固体,密度、硬度均较小,熔点较低,有良好的导
电、传热和延展性。
(2)化学性质:
①与非金属反应
②与CO 反应:2Mg+CO=====2MgO+C
2 2
③与HO反应:Mg+2HO=====Mg(OH) +H↑
2 2 2 2
④与H+反应:Mg+2H+===Mg2++H↑
2
镁也可在氮气中燃烧,生成氮化镁(Mg N),氮化镁能与水剧烈反应生成Mg(OH) 沉淀并
3 2 2
放出氨气。
2.海水提镁①由MgCl ·6H O到无水MgCl ,必须在HCl气流中加热,以防MgCl 水解。
2 2 2 2
②因镁在高温下能与O 、N 、CO 等气体发生反应,故工业电解MgCl 得到的镁,应在
2 2 2 2
H 氛围中冷却。
2
3.用途
生产合金,冶金工业上用作还原剂和脱氧剂。
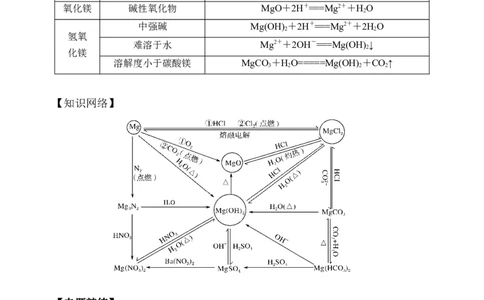
4.镁的重要化合物
物质 主要性质
氧化镁 碱性氧化物 MgO+2H+===Mg2++HO
2
中强碱 Mg(OH) +2H+===Mg2++2HO
2 2
氢氧
难溶于水 Mg2++2OH-===Mg(OH) ↓
2
化镁
溶解度小于碳酸镁 MgCO +HO=====Mg(OH) +CO↑
3 2 2 2
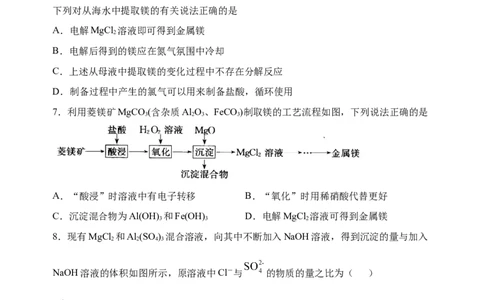
【知识网络】
【专题精练】
1.镁粉是焰火、闪光粉中不可缺少的原料,工业制造镁粉是将镁蒸气在气体中冷却,下
列不可作为冷却剂的是
①空气 ②CO ③Ar ④H ⑤N ⑥HO
2 2 2 2
A.①②⑤⑥ B.③④⑥ C.③⑥ D.③④
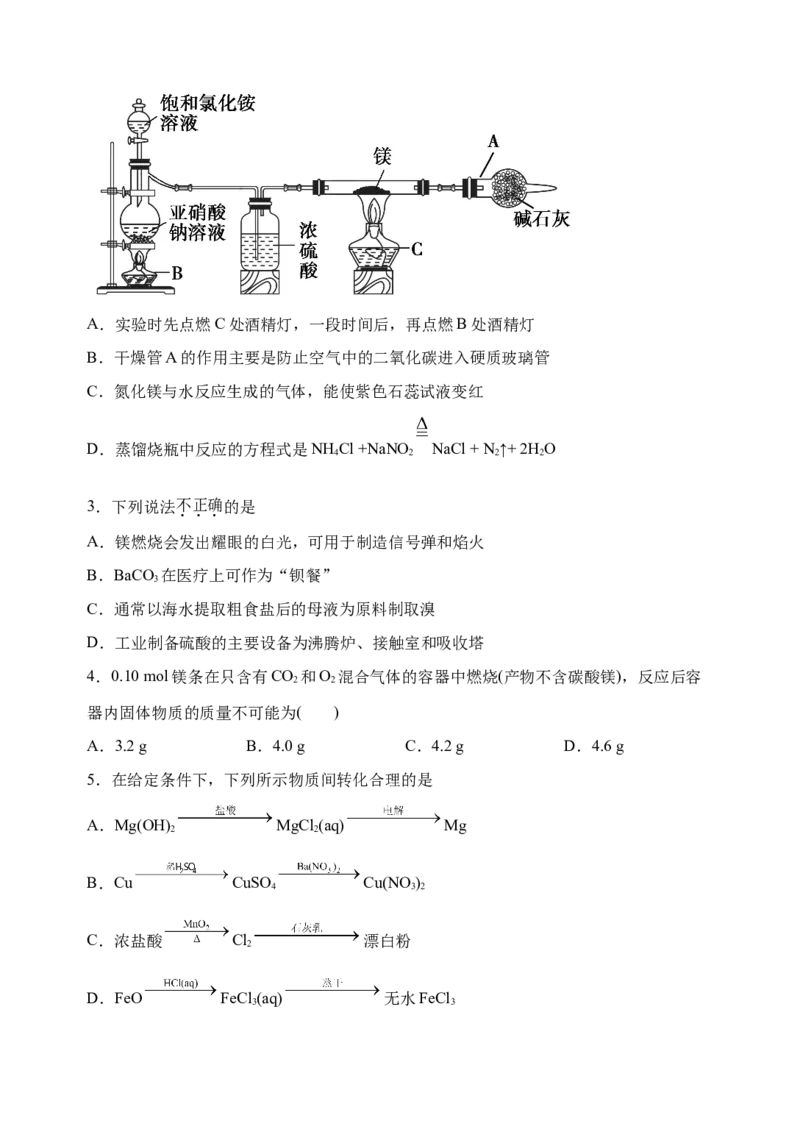
2.镁与氮气在加热条件下反应生成氮化镁,已知氮化镁遇水剧烈反应。某同学设计如图
装置制备氮化镁。下列说法正确的是A.实验时先点燃C处酒精灯,一段时间后,再点燃B处酒精灯
B.干燥管A的作用主要是防止空气中的二氧化碳进入硬质玻璃管
C.氮化镁与水反应生成的气体,能使紫色石蕊试液变红
D.蒸馏烧瓶中反应的方程式是NH Cl +NaNO NaCl + N ↑+ 2H O
4 2 2 2
3.下列说法不正确的是
A.镁燃烧会发出耀眼的白光,可用于制造信号弹和焰火
B.BaCO 在医疗上可作为“钡餐”
3
C.通常以海水提取粗食盐后的母液为原料制取溴
D.工业制备硫酸的主要设备为沸腾炉、接触室和吸收塔
4.0.10 mol镁条在只含有CO 和O 混合气体的容器中燃烧(产物不含碳酸镁),反应后容
2 2
器内固体物质的质量不可能为( )
A.3.2 g B.4.0 g C.4.2 g D.4.6 g
5.在给定条件下,下列所示物质间转化合理的是
A.Mg(OH) MgCl (aq) Mg
2 2
B.Cu CuSO Cu(NO )
4 3 2
C.浓盐酸 Cl 漂白粉
2
D.FeO FeCl (aq) 无水FeCl
3 36.从海水晒盐后的母液中提取镁,最基本的方法是往海水中加石灰乳,得到Mg(OH) 沉
2
淀,将沉淀分离后再加入盐酸变成MgCl 溶液;之后经结晶、过滤、干燥、电解,即可
2
得到金属镁(已知镁在热水中能反应生成氢气)。工艺流程如下:
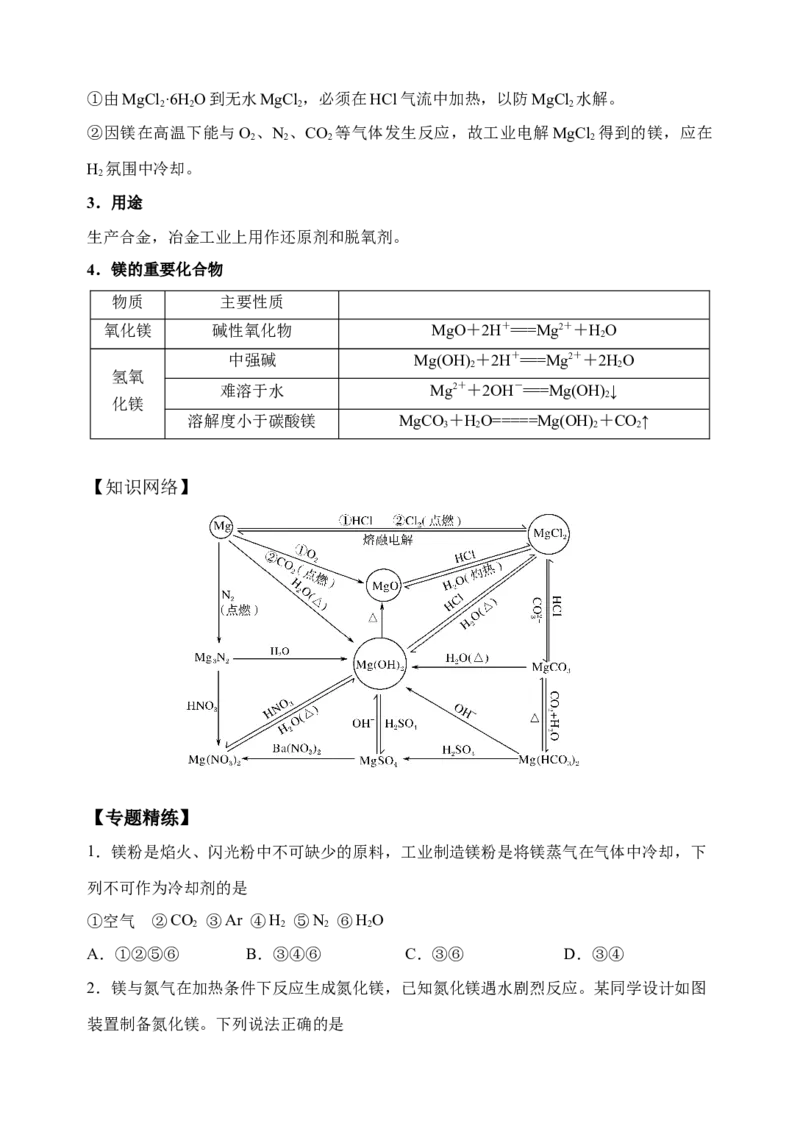
下列对从海水中提取镁的有关说法正确的是
A.电解MgCl 溶液即可得到金属镁
2
B.电解后得到的镁应在氮气氛围中冷却
C.上述从母液中提取镁的变化过程中不存在分解反应
D.制备过程中产生的氯气可以用来制备盐酸,循环使用
7.利用菱镁矿MgCO (含杂质Al O、FeCO)制取镁的工艺流程如图,下列说法正确的是
3 2 3 3
A.“酸浸”时溶液中有电子转移 B.“氧化”时用稀硝酸代替更好
C.沉淀混合物为Al(OH) 和Fe(OH) D.电解MgCl 溶液可得到金属镁
3 3 2
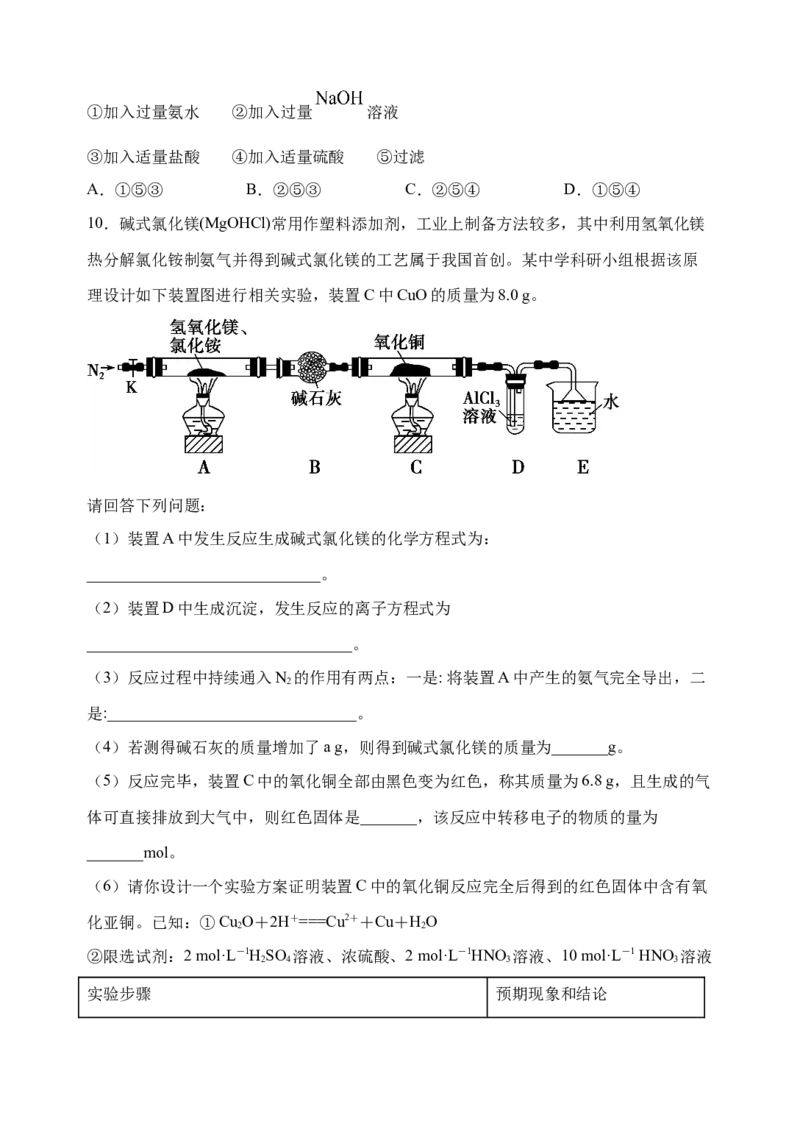
8.现有MgCl 和Al (SO ) 混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入
2 2 4 3
NaOH溶液的体积如图所示,原溶液中Cl-与 的物质的量之比为( )
A.1:3 B.2:3 C.6:1 D.3:1
9.欲从 溶液中除去少量 , 下列操作顺序正确的是①加入过量氨水 ②加入过量 溶液
③加入适量盐酸 ④加入适量硫酸 ⑤过滤
A.①⑤③ B.②⑤③ C.②⑤④ D.①⑤④
10.碱式氯化镁(MgOHCl)常用作塑料添加剂,工业上制备方法较多,其中利用氢氧化镁
热分解氯化铵制氨气并得到碱式氯化镁的工艺属于我国首创。某中学科研小组根据该原
理设计如下装置图进行相关实验,装置C中CuO的质量为8.0 g。
请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为:
_____________________________。
(2)装置D中生成沉淀,发生反应的离子方程式为
_________________________________。
(3)反应过程中持续通入N 的作用有两点:一是: 将装置A中产生的氨气完全导出,二
2
是:_______________________________。
(4)若测得碱石灰的质量增加了a g,则得到碱式氯化镁的质量为_______g。
(5)反应完毕,装置C中的氧化铜全部由黑色变为红色,称其质量为6.8 g,且生成的气
体可直接排放到大气中,则红色固体是_______,该反应中转移电子的物质的量为
_______mol。
(6)请你设计一个实验方案证明装置C中的氧化铜反应完全后得到的红色固体中含有氧
化亚铜。已知:①Cu O+2H+===Cu2++Cu+HO
2 2
②限选试剂:2 mol·L-1HSO 溶液、浓硫酸、2 mol·L-1HNO 溶液、10 mol·L-1 HNO 溶液
2 4 3 3
实验步骤 预期现象和结论步骤1:取反应后装置C中的少许固体于试管中
步骤2:____________ ____________
11.海水中蕴藏的元素高达80多种,是人类财富的重要集散地。如图是对海水资源的综
合利用的示意图。
请回答下列问题:
(1)地球上99%以上的溴元素存在于海洋中,资料显示海水中溴的含量约为 。
如图中制备溴涉及步骤I、Ⅱ、Ⅲ,写出步骤Ⅲ中反应的离子方程式:
____________________________。
(2)制备镁的工艺中,从卤水到 经历了 的过程,
生成 的过程看似多余,其实该过程的作用是_____________________。
(3)电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用
作镁蒸气的冷却剂的是_______(填字母序号)。
A.Ar B.CO C.O D.N
2 2 2