文档内容
押非选择题
有机化学综合题
考情统计 考向预测 备考策略
2023·辽宁卷,19 主要是有机物的分子式和结构 题目覆盖有机物主干基础知识,侧
2022·辽宁卷,19 简式、有机反应类型、反应条 重考查新信息获取、新旧知识的整
2021·辽宁卷,19 件、方程式的书写、同分异构 合应用能力。考查学生有序思维和
体、官能团的检验和鉴别以及 整合新旧知识解决有机问题的能
制备流程的设计等问题。 力。既考查了学生对教材中有机化
学基础知识的掌握,又考查了学生
有机化学知识的综合应用能力。
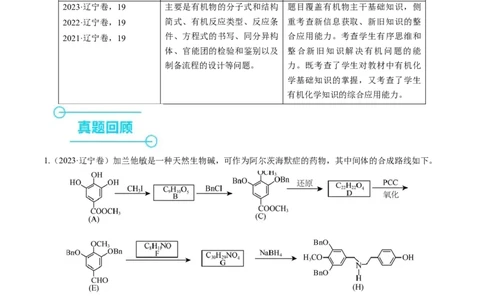
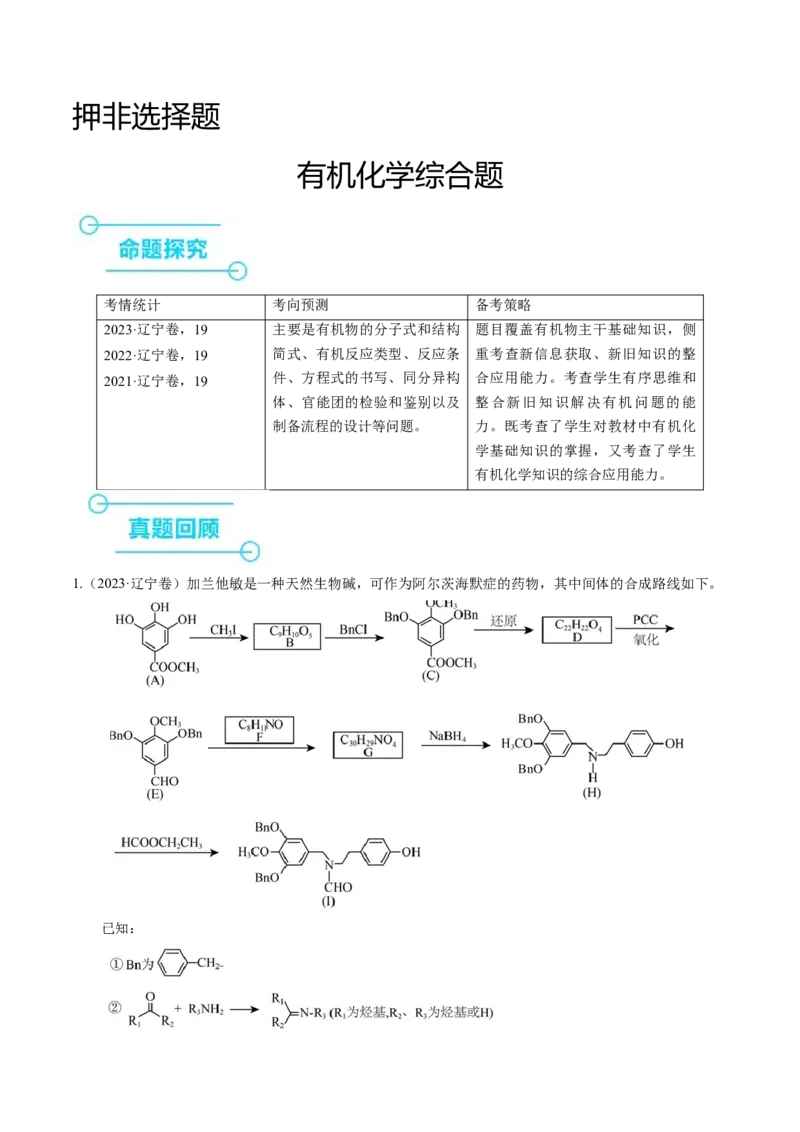
1.(2023·辽宁卷)加兰他敏是一种天然生物碱,可作为阿尔茨海默症的药物,其中间体的合成路线如下。
已知:回答下列问题:
(1)A中与卤代烃成醚活性高的羟基位于酯基的_______位(填“间”或“对”)。
(2)C发生酸性水解,新产生的官能团为羟基和_______(填名称)。
(3)用O 代替PCC完成D→E的转化,化学方程式为___________________________。
2
(4)F的同分异构体中,红外光谱显示有酚羟基、无N-H键的共有_______种。
(5)H→I的反应类型为_______。
(6)某药物中间体的合成路线如下(部分反应条件已略去),其中M和N的结构简式分别为_______和
________________。
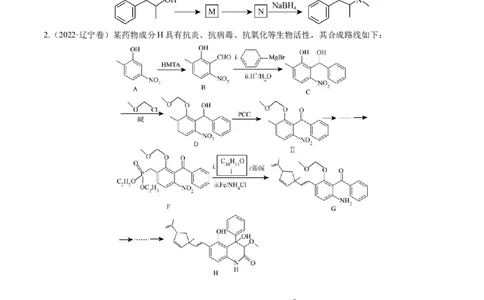
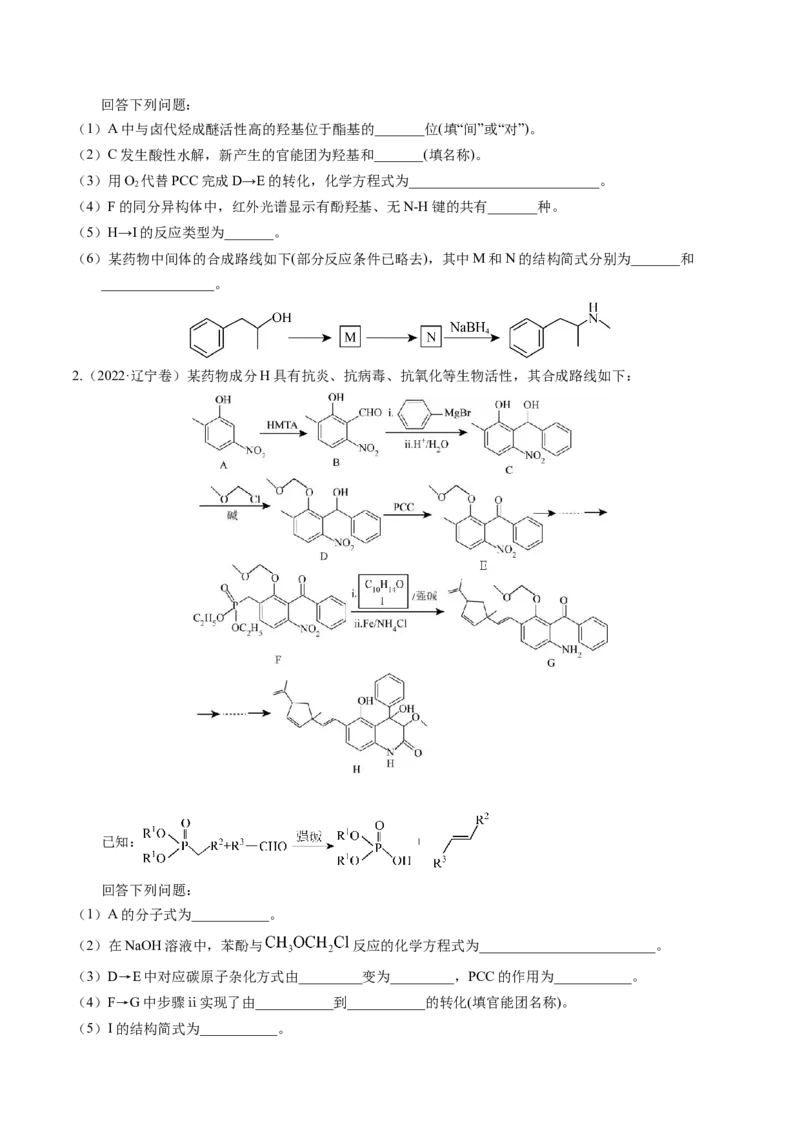
2.(2022·辽宁卷)某药物成分H具有抗炎、抗病毒、抗氧化等生物活性,其合成路线如下:
已知:
回答下列问题:
(1)A的分子式为___________。
(2)在NaOH溶液中,苯酚与 反应的化学方程式为_________________________。
(3)D→E中对应碳原子杂化方式由_________变为_________,PCC的作用为___________。
(4)F→G中步骤ⅱ实现了由___________到___________的转化(填官能团名称)。
(5)I的结构简式为___________。(6)化合物I的同分异构体满足以下条件的有_________种(不考虑立体异构);
i.含苯环且苯环上只有一个取代基
ii.红外光谱无醚键吸收峰
其中,苯环侧链上有3种不同化学环境的氢原子,且个数比为6∶2∶1的结构简式为___________(任写一
种)。
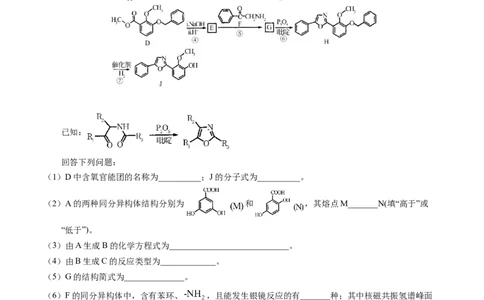
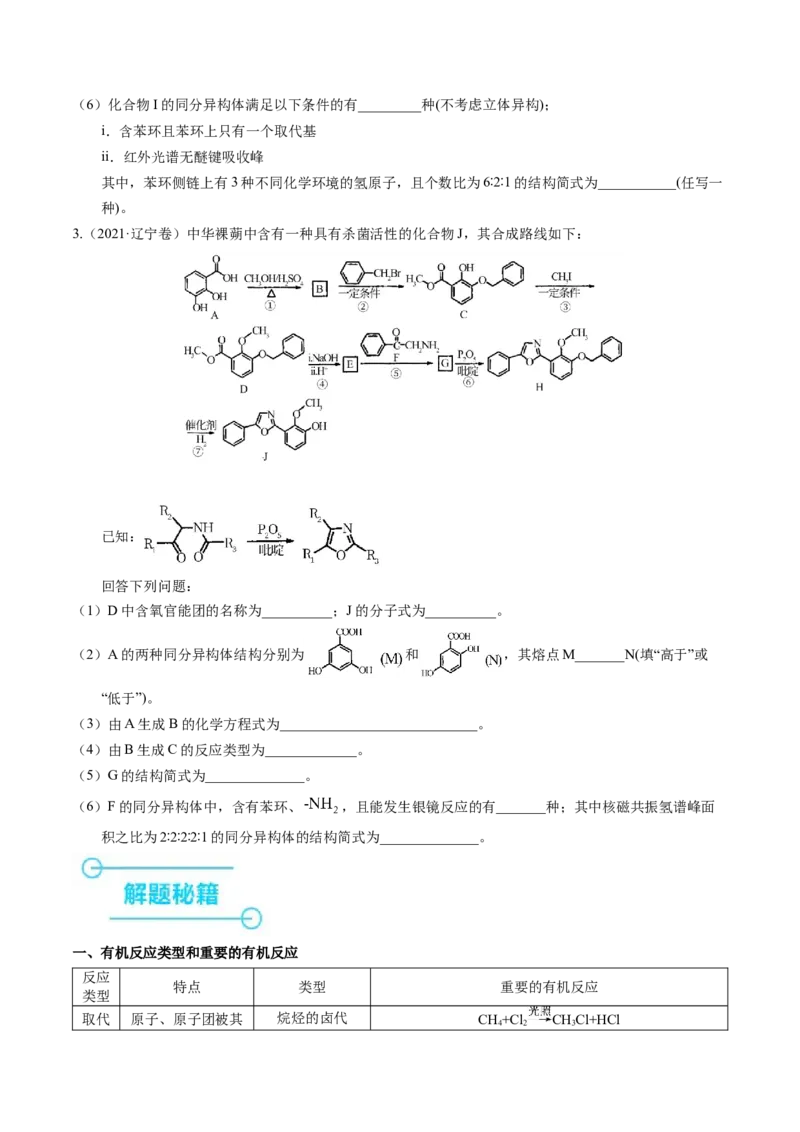
3.(2021·辽宁卷)中华裸蒴中含有一种具有杀菌活性的化合物J,其合成路线如下:
已知:
回答下列问题:
(1)D中含氧官能团的名称为__________;J的分子式为__________。
(2)A的两种同分异构体结构分别为 和 ,其熔点M_______N(填“高于”或
“低于”)。
(3)由A生成B的化学方程式为____________________________。
(4)由B生成C的反应类型为_____________。
(5)G的结构简式为______________。
(6)F的同分异构体中,含有苯环、 ,且能发生银镜反应的有_______种;其中核磁共振氢谱峰面
积之比为2∶2∶2∶2∶1的同分异构体的结构简式为______________。
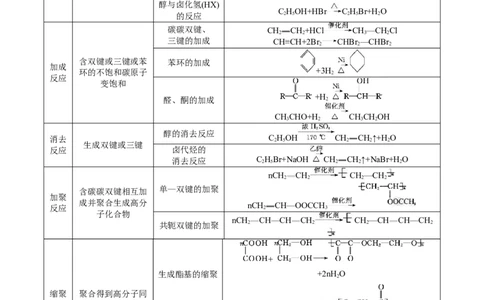
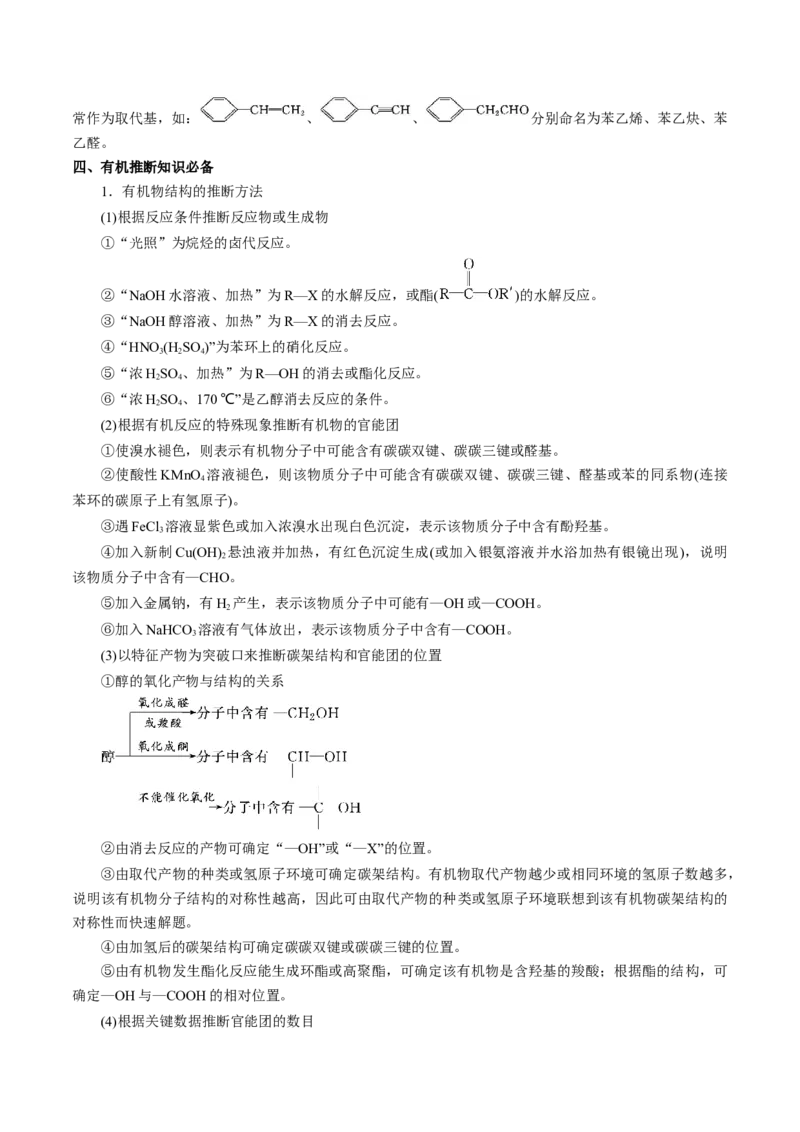
一、有机反应类型和重要的有机反应
反应
特点 类型 重要的有机反应
类型
取代 原子、原子团被其 烷烃的卤代 CH+Cl CHCl+HCl
4 2 3+Br +HBr
苯环上的取代 2
+HONO +H O
2 2
酯化反应
他原子、原子团所 CHCOOH+C HOH CHCOOC H+H O
反应 3 2 5 3 2 5 2
代替
卤代烃、酯的水
CHCHBr+NaOH CHCHOH+NaBr
3 2 3 2
解反应(双糖、
多糖、蛋白质水 CHCOOC H+H O CHCOOH+C HOH
3 2 5 2 3 2 5
解)
CHCOOC H+NaOH CHCOONa+C HOH
3 2 5 3 2 5
醇与卤化氢(HX)
C HOH+HBr C HBr+H O
的反应 2 5 2 5 2
碳碳双键、 CH CH+HCl CH—CHCl
2 2 3 2
三键的加成 CH≡CH+2Br CHBr —CHBr
2 2 2
含双键或三键或苯 苯环的加成
加成
环的不饱和碳原子 +3H 2
反应
变饱和
+H
醛、酮的加成 2
CHCHO+H CHCHOH
3 2 3 2
醇的消去反应
消去 C 2 H 5 OH CH 2 CH 2 ↑+H 2 O
生成双键或三键
反应 卤代烃的
消去反应 C 2 H 5 Br+NaOH CH 2 CH 2 ↑+NaBr+H 2 O
nCH CH CH—CH
2 2 2 2
含碳碳双键相互加 单—双键的加聚
加聚
成并聚合生成高分
nCH CH—OOCCH
反应 2 3
子化合物
nCH CH—CH CH CH—CH CH—CH
共轭双键的加聚 2 2 2 2
+
生成酯基的缩聚 +2nH O
2
缩聚 聚合得到高分子同
nHO—CH —COOH +nH O
反应 时生成小分子 2 2
氨基酸的缩聚
nHN—CH —COOH +nH O
2 2 2
酚醛树脂的生成
nC HOH+nHCHO C H(OH)CH +nH O
6 5 6 3 2 2
有机 2C 2 H 5 OH+O 2 2CH 3 CHO+2H 2 O
“加氧”或“去 催化氧化
氧化
氢” 2CHCHO+O 2CHCOOH
3 2 3
反应
碳碳双键被
RCH CH R—COOH+CO
2 2KMnO 酸性
4
溶液氧化
+R″COOH
苯的同系物被
KMnO
4
(H+)氧化
CHCHO+2Cu(OH) +NaOH CHCOONa+Cu O↓+3HO
3 2 3 2 2
醛基的氧化
CHCHO+2Ag(NH )OH CHCOONH+2Ag↓+3NH+H
3 3 2 3 4 3
O
2
醛、酮的还原
CHCHO+H CHCHOH
有机 3 2 3 2
“加氢”或
还原
硝基被还原
“去氧”
反应
为氨基
二、有机反应化学方程式的书写的注意事项
(1) 反应箭头和配平:书写有机反应化学方程式时应注意,反应物和产物之间用“―→”连接,有机物
用结构简式表示,并遵循原子守恒进行配平。
(2) 反应条件:有机物反应条件不同,所得产物不同。
有机反应 反应条件 说明
浓硫酸、170℃ C HOH――→CH===CH ↑+HO
2 5 2 2 2
醇的脱水
浓硫酸、140℃ 2C HOH――→C HOC H+HO
2 5 2 5 2 5 2
强碱的水溶液、加热 CHCHBr+NaOH――→C HOH+NaBr
3 2 2 5
卤代烃
强碱的醇溶液、加热 CHCHBr+NaOH――→CH===CH ↑+NaBr+HO
3 2 2 2 2
(3) 须用中文标明的有机反应。如:
(C H O)+nHO――→nC H O
6 10 5 n 2 6 12 6
淀粉 葡萄糖
C H O――→2C HOH+2CO↑
6 12 6 2 5 2
葡萄糖
三、有机物的命名方法
(1)明确多官能团化合物中官能团的优先顺序:羧酸>酯>醛>酮>醇>胺。
如:CH(OH)CHCHO命名为3-羟基丙醛。
2 2
(2)掌握基本的命名方法
①对于烷烃:确定最长碳链为主链,命名为某“烷”;标明支链位置和数目。
②对于烯烃、炔烃、卤代烃、醛、酮、羧酸必须选含官能团的最长链为主链。
③酯用形成酯的羧酸与醇命名为某酸某酯。
④苯的同系物以苯环为母体命名为某苯,如: 命名为乙苯。而芳香族化合物,苯环常作为取代基,如: 、 、 分别命名为苯乙烯、苯乙炔、苯
乙醛。
四、有机推断知识必备
1.有机物结构的推断方法
(1)根据反应条件推断反应物或生成物
①“光照”为烷烃的卤代反应。
②“NaOH水溶液、加热”为R—X的水解反应,或酯( )的水解反应。
③“NaOH醇溶液、加热”为R—X的消去反应。
④“HNO(H SO )”为苯环上的硝化反应。
3 2 4
⑤“浓HSO 、加热”为R—OH的消去或酯化反应。
2 4
⑥“浓HSO 、170 ℃”是乙醇消去反应的条件。
2 4
(2)根据有机反应的特殊现象推断有机物的官能团
①使溴水褪色,则表示有机物分子中可能含有碳碳双键、碳碳三键或醛基。
②使酸性KMnO 溶液褪色,则该物质分子中可能含有碳碳双键、碳碳三键、醛基或苯的同系物(连接
4
苯环的碳原子上有氢原子)。
③遇FeCl 溶液显紫色或加入浓溴水出现白色沉淀,表示该物质分子中含有酚羟基。
3
④加入新制Cu(OH) 悬浊液并加热,有红色沉淀生成(或加入银氨溶液并水浴加热有银镜出现),说明
2
该物质分子中含有—CHO。
⑤加入金属钠,有H 产生,表示该物质分子中可能有—OH或—COOH。
2
⑥加入NaHCO 溶液有气体放出,表示该物质分子中含有—COOH。
3
(3)以特征产物为突破口来推断碳架结构和官能团的位置
①醇的氧化产物与结构的关系
②由消去反应的产物可确定“—OH”或“—X”的位置。
③由取代产物的种类或氢原子环境可确定碳架结构。有机物取代产物越少或相同环境的氢原子数越多,
说明该有机物分子结构的对称性越高,因此可由取代产物的种类或氢原子环境联想到该有机物碳架结构的
对称性而快速解题。
④由加氢后的碳架结构可确定碳碳双键或碳碳三键的位置。
⑤由有机物发生酯化反应能生成环酯或高聚酯,可确定该有机物是含羟基的羧酸;根据酯的结构,可
确定—OH与—COOH的相对位置。
(4)根据关键数据推断官能团的数目①—CHO;
②2—OH(醇、酚、羧酸)――→H;
2
③2—COOH――→CO,—COOH――→CO;
2 2
⑤RCHOH――→CHCOOCH R。
2 3 2
(M) (M+42)
r r
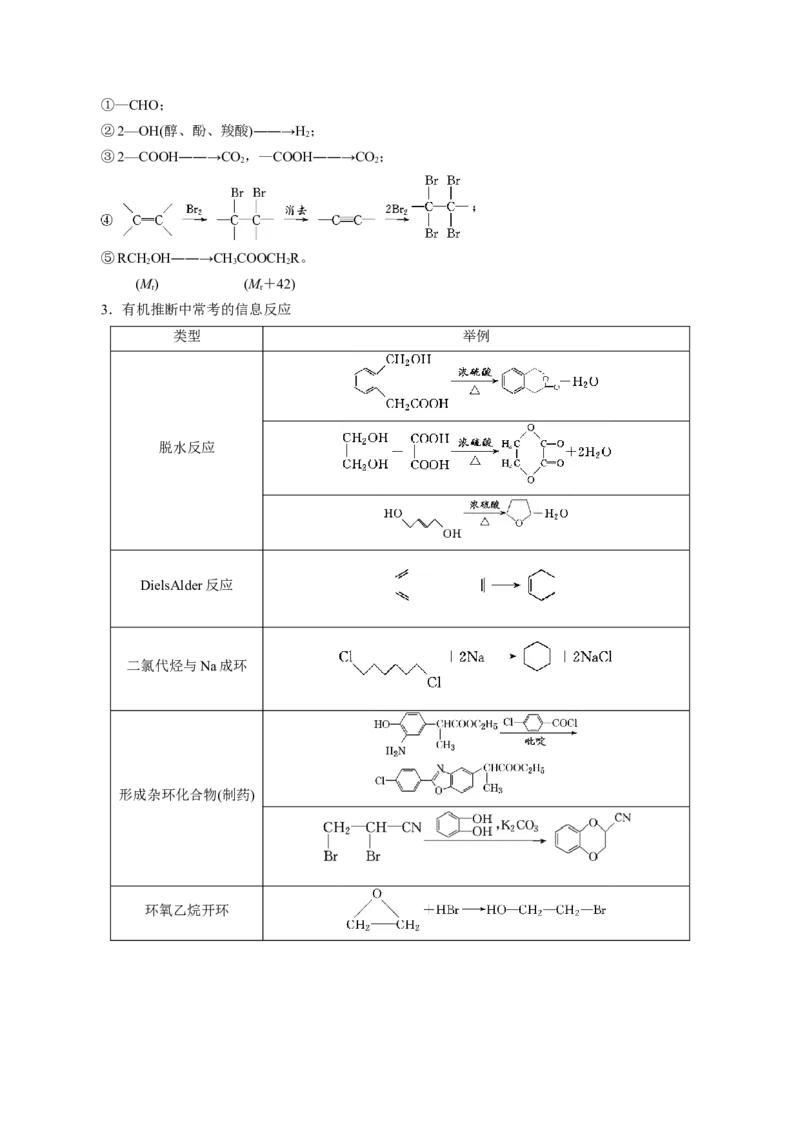
3.有机推断中常考的信息反应
类型 举例
脱水反应
DielsAlder反应
二氯代烃与Na成环
形成杂环化合物(制药)
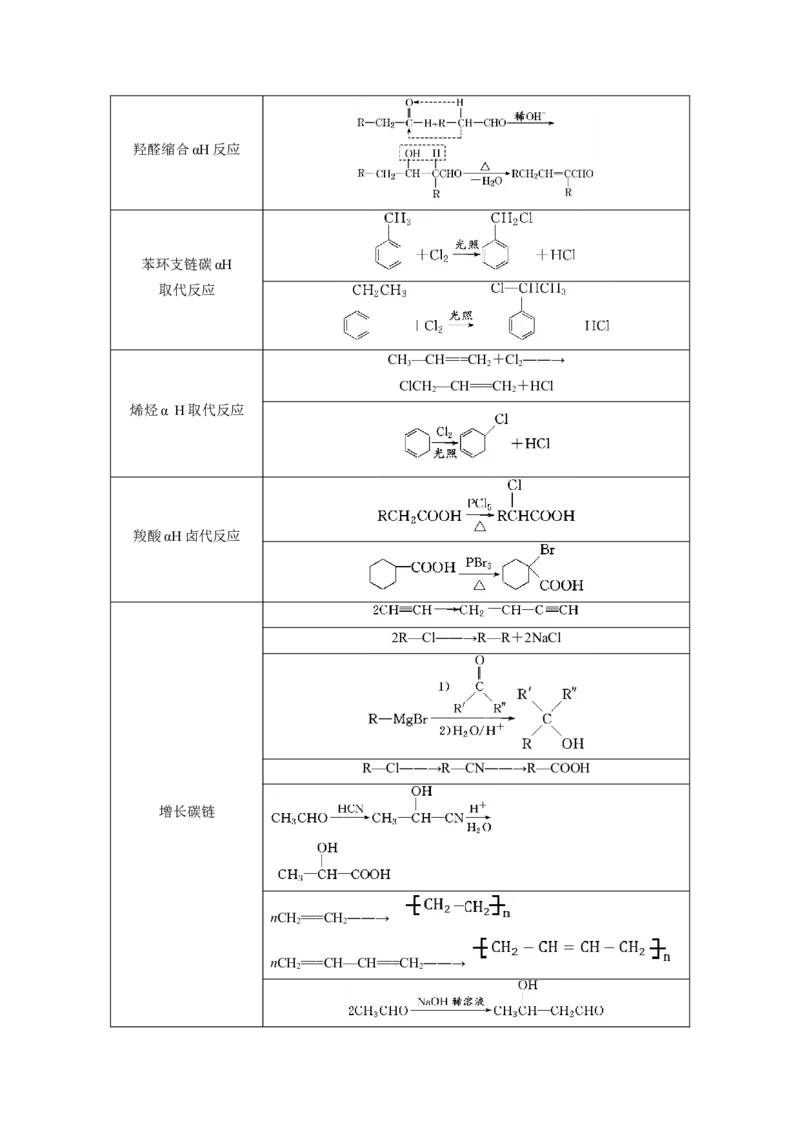
环氧乙烷开环羟醛缩合αH反应
苯环支链碳αH
取代反应
CH—CH===CH +Cl――→
3 2 2
ClCH —CH===CH +HCl
2 2
烯烃α H取代反应
羧酸αH卤代反应
2R—Cl――→R—R+2NaCl
R—Cl――→R—CN――→R—COOH
增长碳链
nCH===CH ――→
2 2
nCH===CH—CH===CH ――→
2 22R—C C—H――→R—C C—C C—R+H↑(Glaser反应)
2
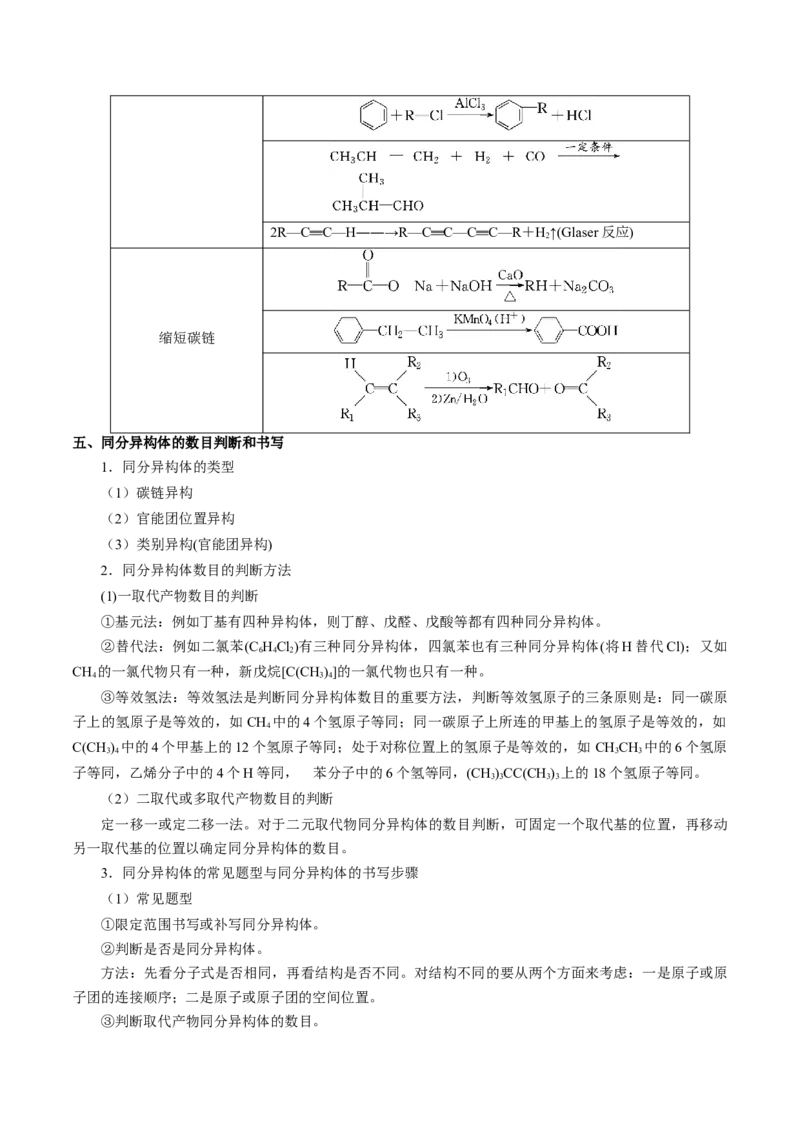
缩短碳链
五、同分异构体的数目判断和书写
1.同分异构体的类型
(1)碳链异构
(2)官能团位置异构
(3)类别异构(官能团异构)
2.同分异构体数目的判断方法
(1)一取代产物数目的判断
①基元法:例如丁基有四种异构体,则丁醇、戊醛、戊酸等都有四种同分异构体。
②替代法:例如二氯苯(C HCl)有三种同分异构体,四氯苯也有三种同分异构体(将H替代Cl);又如
6 4 2
CH 的一氯代物只有一种,新戊烷[C(CH)]的一氯代物也只有一种。
4 3 4
③等效氢法:等效氢法是判断同分异构体数目的重要方法,判断等效氢原子的三条原则是:同一碳原
子上的氢原子是等效的,如CH 中的4个氢原子等同;同一碳原子上所连的甲基上的氢原子是等效的,如
4
C(CH) 中的4个甲基上的12个氢原子等同;处于对称位置上的氢原子是等效的,如 CHCH 中的6个氢原
3 4 3 3
子等同,乙烯分子中的4个H等同, 苯分子中的6个氢等同,(CH)CC(CH) 上的18个氢原子等同。
3 3 3 3
(2)二取代或多取代产物数目的判断
定一移一或定二移一法。对于二元取代物同分异构体的数目判断,可固定一个取代基的位置,再移动
另一取代基的位置以确定同分异构体的数目。
3.同分异构体的常见题型与同分异构体的书写步骤
(1)常见题型
①限定范围书写或补写同分异构体。
②判断是否是同分异构体。
方法:先看分子式是否相同,再看结构是否不同。对结构不同的要从两个方面来考虑:一是原子或原
子团的连接顺序;二是原子或原子团的空间位置。
③判断取代产物同分异构体的数目。方法:分析有机物的结构特点,确定不同位置的氢原子种数,再确定取代产物同分异构体数目;或者
依据烃基的同分异构体数目进行判断。
(2)同分异构体的书写步骤
①先判断该有机物是否有类别异构。
②就每一类物质,先写出碳链异构体,再写出官能团的位置异构体。
③碳链异构体按“主链由长到短,支链由整到散,位置由心到边”的规律书写。
④检查是否有书写重复或书写遗漏,根据“碳四价”原理检查是否有书写错误。
(3)同分异构体的书写规律
①烷烃:烷烃只存在碳链异构,书写时应注意要全而不重复,具体规则如下:成直链,一条线;摘一
碳,挂中间;往边移,不到端;摘二碳,成乙基;二甲基,同、邻、间。
②具有官能团的有机物,一般书写的顺序:碳链异构→位置异构→官能团异构。
③芳香族化合物:取代基在苯环上的相对位置有邻、间、对3种。
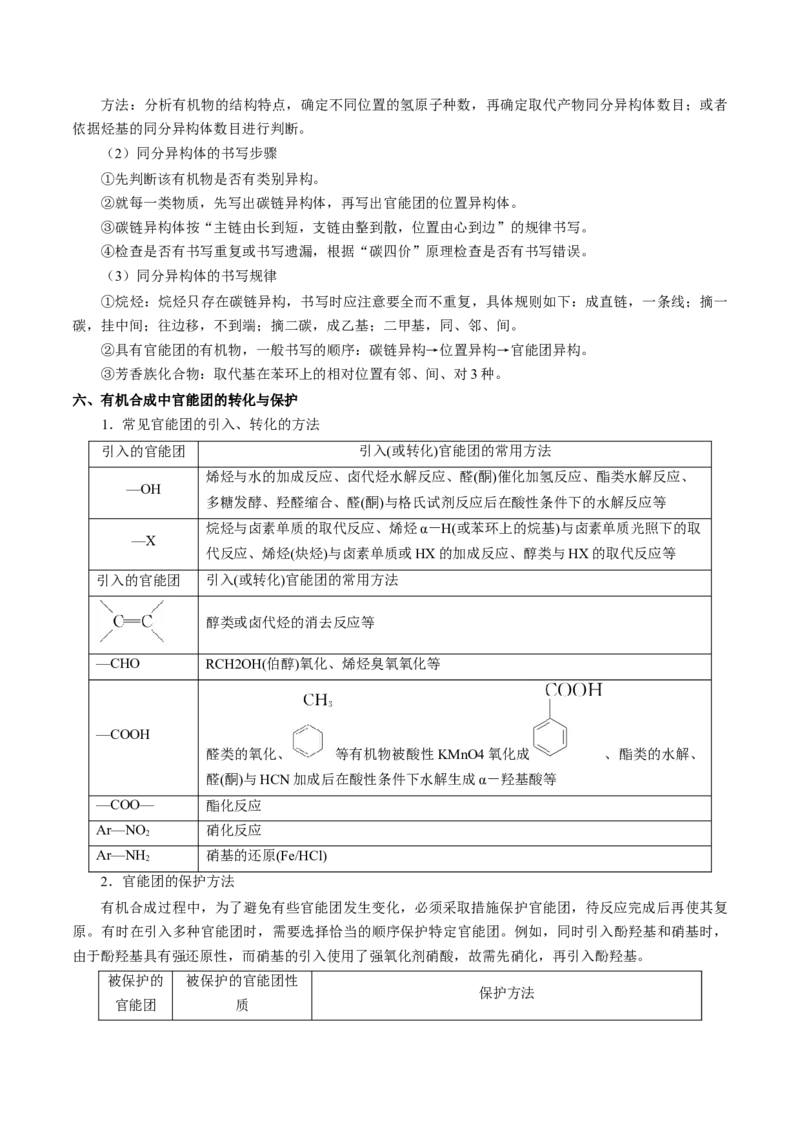
六、有机合成中官能团的转化与保护
1.常见官能团的引入、转化的方法
引入的官能团 引入(或转化)官能团的常用方法
烯烃与水的加成反应、卤代烃水解反应、醛(酮)催化加氢反应、酯类水解反应、
—OH
多糖发酵、羟醛缩合、醛(酮)与格氏试剂反应后在酸性条件下的水解反应等
烷烃与卤素单质的取代反应、烯烃α-H(或苯环上的烷基)与卤素单质光照下的取
—X
代反应、烯烃(炔烃)与卤素单质或HX的加成反应、醇类与HX的取代反应等
引入的官能团 引入(或转化)官能团的常用方法
醇类或卤代烃的消去反应等
—CHO RCH2OH(伯醇)氧化、烯烃臭氧氧化等
—COOH
醛类的氧化、 等有机物被酸性KMnO4氧化成 、酯类的水解、
醛(酮)与HCN加成后在酸性条件下水解生成α-羟基酸等
—COO— 酯化反应
Ar—NO 硝化反应
2
Ar—NH 硝基的还原(Fe/HCl)
2
2.官能团的保护方法
有机合成过程中,为了避免有些官能团发生变化,必须采取措施保护官能团,待反应完成后再使其复
原。有时在引入多种官能团时,需要选择恰当的顺序保护特定官能团。例如,同时引入酚羟基和硝基时,
由于酚羟基具有强还原性,而硝基的引入使用了强氧化剂硝酸,故需先硝化,再引入酚羟基。
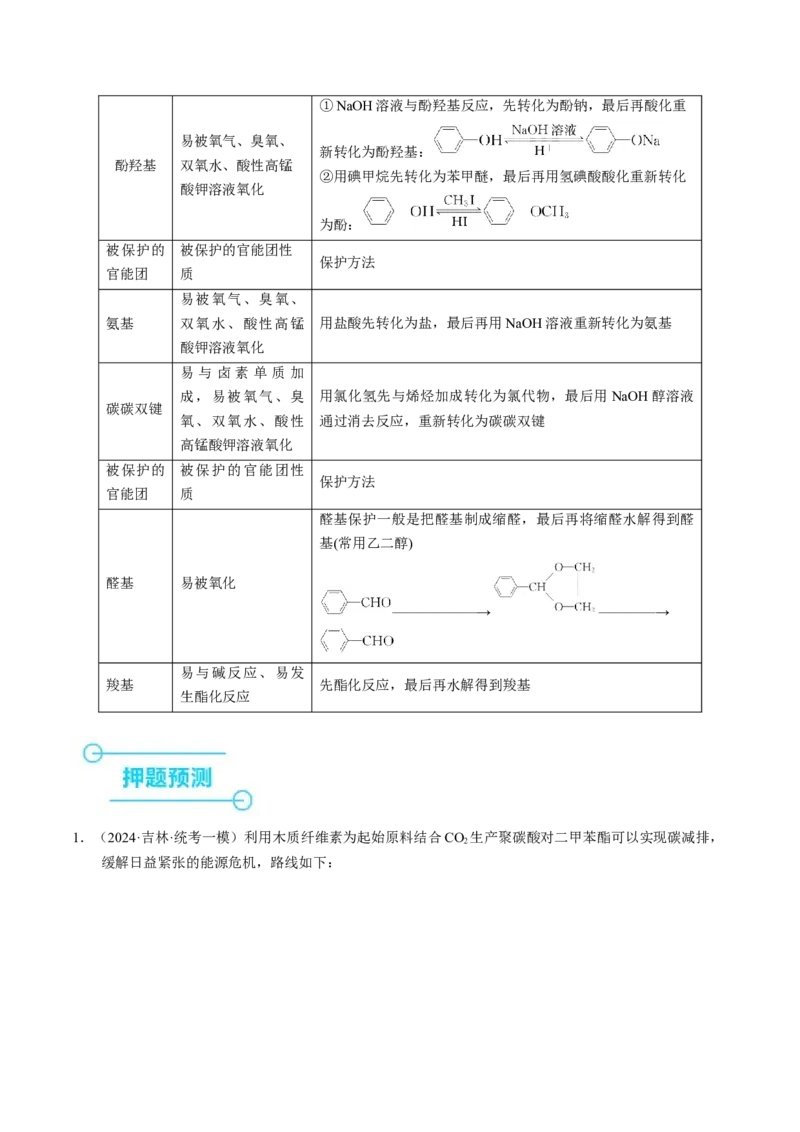
被保护的 被保护的官能团性
保护方法
官能团 质①NaOH溶液与酚羟基反应,先转化为酚钠,最后再酸化重
易被氧气、臭氧、
新转化为酚羟基:
酚羟基 双氧水、酸性高锰
②用碘甲烷先转化为苯甲醚,最后再用氢碘酸酸化重新转化
酸钾溶液氧化
为酚:
被保护的 被保护的官能团性
保护方法
官能团 质
易被氧气、臭氧、
氨基 双氧水、酸性高锰 用盐酸先转化为盐,最后再用NaOH溶液重新转化为氨基
酸钾溶液氧化
易 与 卤 素 单 质 加
成,易被氧气、臭 用氯化氢先与烯烃加成转化为氯代物,最后用NaOH醇溶液
碳碳双键
氧、双氧水、酸性 通过消去反应,重新转化为碳碳双键
高锰酸钾溶液氧化
被保护的 被保护的官能团性
保护方法
官能团 质
醛基保护一般是把醛基制成缩醛,最后再将缩醛水解得到醛
基(常用乙二醇)
醛基 易被氧化
——————→ ————→
易与碱反应、易发
羧基 先酯化反应,最后再水解得到羧基
生酯化反应
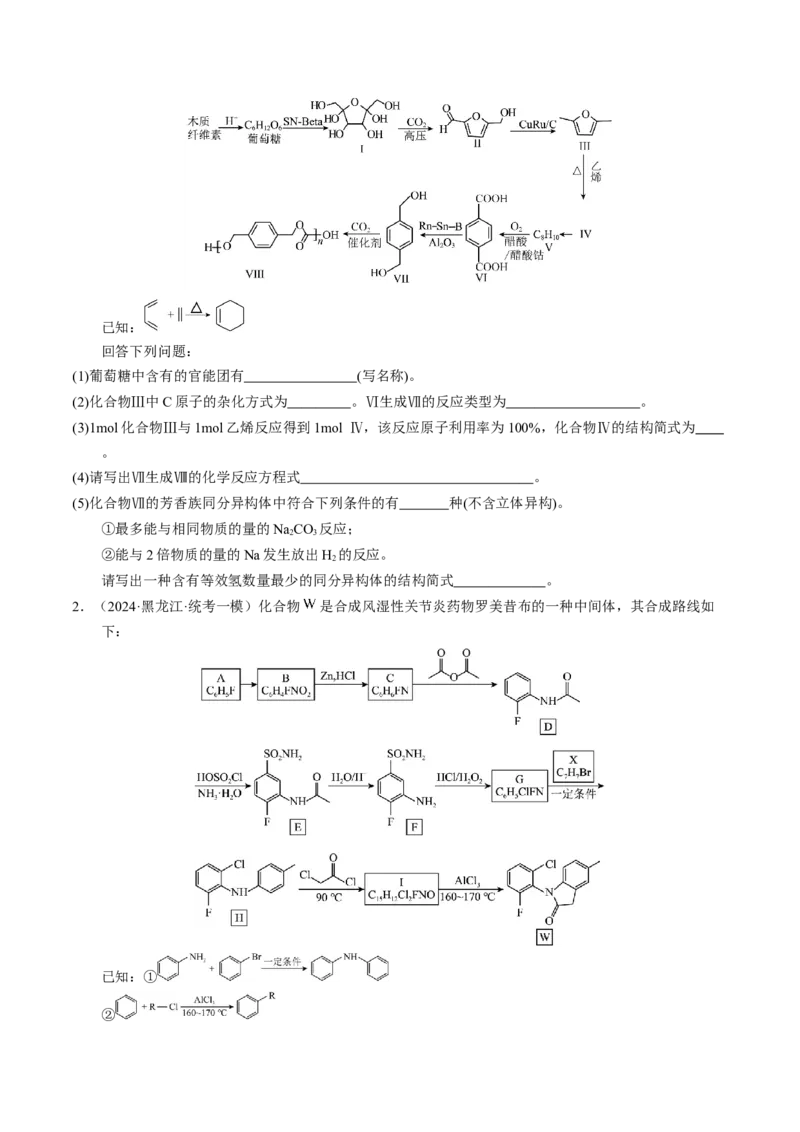
1.(2024·吉林·统考一模)利用木质纤维素为起始原料结合CO 生产聚碳酸对二甲苯酯可以实现碳减排,
2
缓解日益紧张的能源危机,路线如下:已知:
回答下列问题:
(1)葡萄糖中含有的官能团有 (写名称)。
(2)化合物Ⅲ中C原子的杂化方式为 。Ⅵ生成Ⅶ的反应类型为 。
(3)1mol化合物Ⅲ与1mol乙烯反应得到1mol Ⅳ,该反应原子利用率为100%,化合物Ⅳ的结构简式为
。
(4)请写出Ⅶ生成Ⅷ的化学反应方程式 。
(5)化合物Ⅶ的芳香族同分异构体中符合下列条件的有 种(不含立体异构)。
①最多能与相同物质的量的NaCO 反应;
2 3
②能与2倍物质的量的Na发生放出H 的反应。
2
请写出一种含有等效氢数量最少的同分异构体的结构简式 。
2.(2024·黑龙江·统考一模)化合物 是合成风湿性关节炎药物罗美昔布的一种中间体,其合成路线如
下:
已知:①
②回答下列问题:
(1)A中官能团名称为 ,D的化学式为 ,W结构中碳原子的杂化方式为
。
(2)由B生成C的反应类型为 。
(3)写出由G生成H的化学方程式 。
(4)写出I的结构简式 。
(5)D有多种同分异构体,同时满足下列条件的同分异构体有 种(不考虑立体异构)。
①苯环上有三个取代基②能发生银镜反应③在酸性条件下发生水解反应
3.(2024上·黑龙江牡丹江·高三一模)苯巴比妥曾作为催眠药或镇静药广泛应用于临床,其合成路线如下:
回答下列问题:
(1)A→B所使用的试剂及反应条件为 。
(2)D的化学名称为 ,E的含氧官能团名称为 。
(3)苯巴比妥的分子式为 。
(4)写出G生成H的化学方程式 。
(5)I的结构简式 。
(6)化合物E的同分异构体满足下列条件的共有 种。
①含有1个苯环
②能与饱和 反应产生
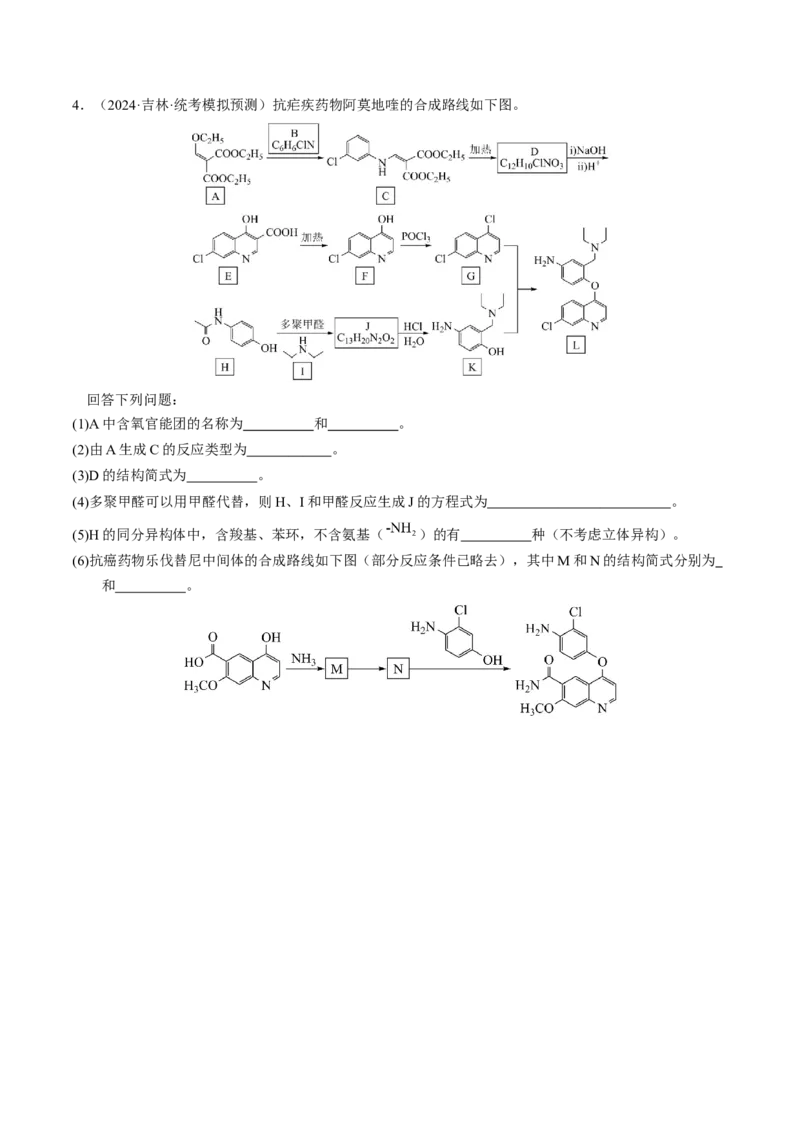
其中,核磁共振氢谱有四组峰,峰面积之比为2:2:2:1的结构简式为 。4.(2024·吉林·统考模拟预测)抗疟疾药物阿莫地喹的合成路线如下图。
回答下列问题:
(1)A中含氧官能团的名称为 和 。
(2)由A生成C的反应类型为 。
(3)D的结构简式为 。
(4)多聚甲醛可以用甲醛代替,则H、I和甲醛反应生成J的方程式为 。
(5)H的同分异构体中,含羧基、苯环,不含氨基( )的有 种(不考虑立体异构)。
(6)抗癌药物乐伐替尼中间体的合成路线如下图(部分反应条件已略去),其中M和N的结构简式分别为
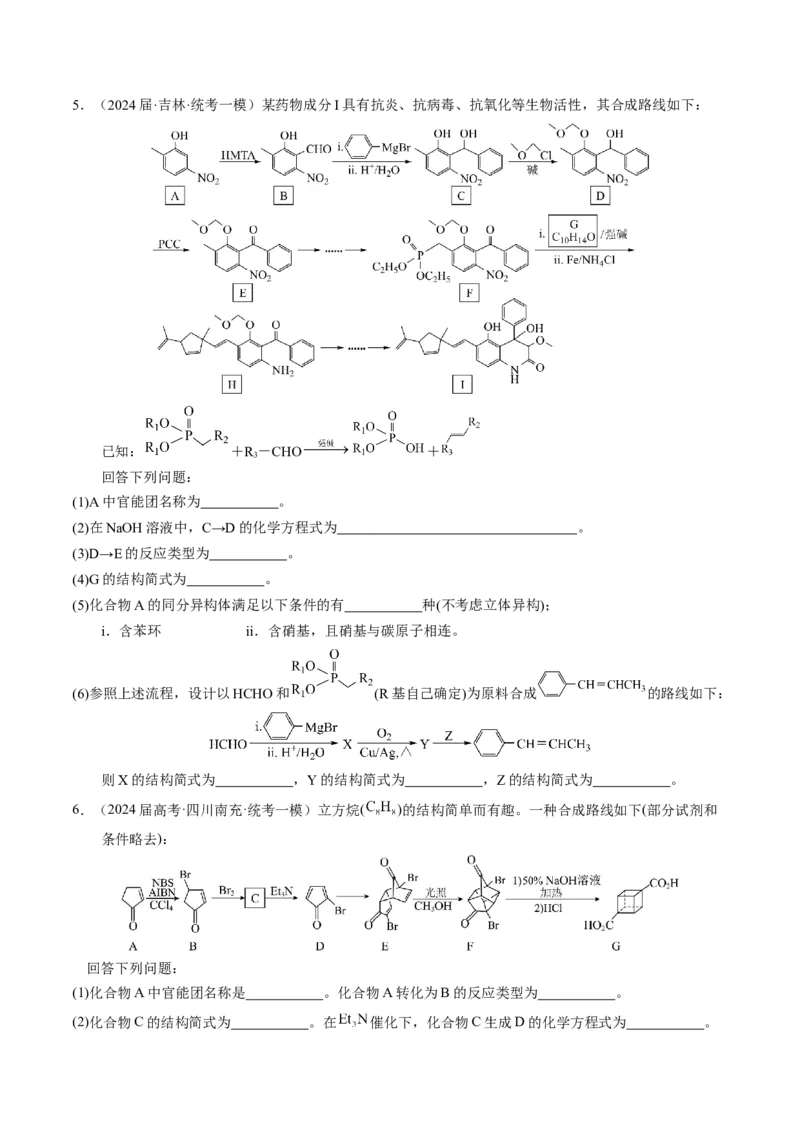
和 。5.(2024届·吉林·统考一模)某药物成分I具有抗炎、抗病毒、抗氧化等生物活性,其合成路线如下:
已知: +R -CHO +
3
回答下列问题:
(1)A中官能团名称为 。
(2)在NaOH溶液中,C→D的化学方程式为 。
(3)D→E的反应类型为 。
(4)G的结构简式为 。
(5)化合物A的同分异构体满足以下条件的有 种(不考虑立体异构);
i.含苯环 ii.含硝基,且硝基与碳原子相连。
(6)参照上述流程,设计以HCHO和 (R基自己确定)为原料合成 的路线如下:
则X的结构简式为 ,Y的结构简式为 ,Z的结构简式为 。
6.(2024届高考·四川南充·统考一模)立方烷( )的结构简单而有趣。一种合成路线如下(部分试剂和
条件略去):
回答下列问题:
(1)化合物A中官能团名称是 。化合物A转化为B的反应类型为 。
(2)化合物C的结构简式为 。在 催化下,化合物C生成D的化学方程式为 。(3)化合物D、F相对分子质量 和 的关系是 。
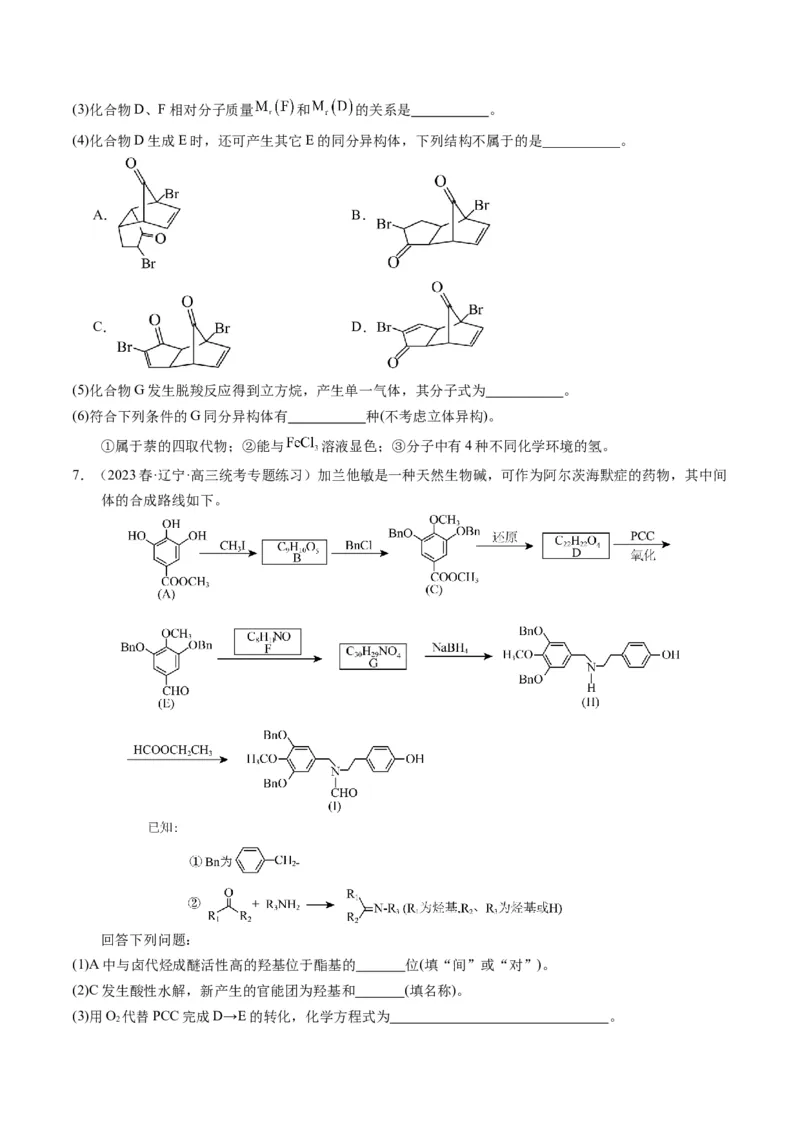
(4)化合物D生成E时,还可产生其它E的同分异构体,下列结构不属于的是___________。
A. B.
C. D.
(5)化合物G发生脱羧反应得到立方烷,产生单一气体,其分子式为 。
(6)符合下列条件的G同分异构体有 种(不考虑立体异构)。
①属于萘的四取代物;②能与 溶液显色;③分子中有4种不同化学环境的氢。
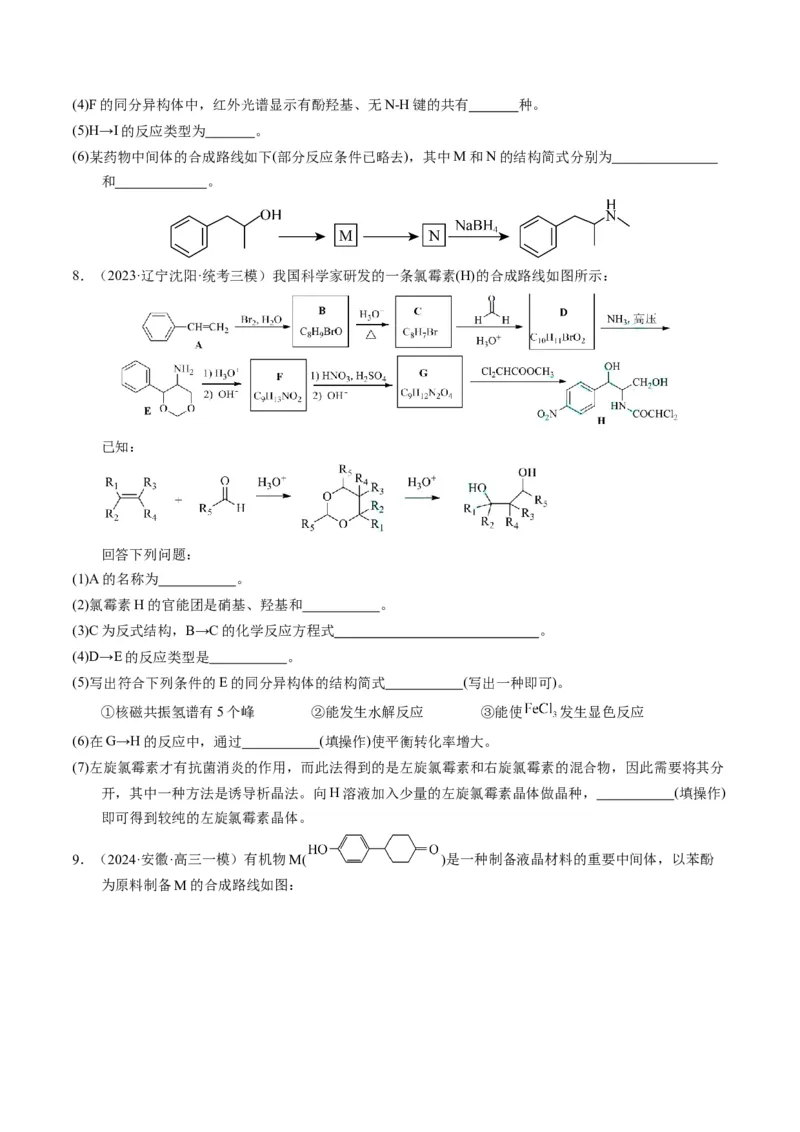
7.(2023春·辽宁·高三统考专题练习)加兰他敏是一种天然生物碱,可作为阿尔茨海默症的药物,其中间
体的合成路线如下。
回答下列问题:
(1)A中与卤代烃成醚活性高的羟基位于酯基的 位(填“间”或“对”)。
(2)C发生酸性水解,新产生的官能团为羟基和 (填名称)。
(3)用O 代替PCC完成D→E的转化,化学方程式为 。
2(4)F的同分异构体中,红外光谱显示有酚羟基、无N-H键的共有 种。
(5)H→I的反应类型为 。
(6)某药物中间体的合成路线如下(部分反应条件已略去),其中M和N的结构简式分别为
和 。
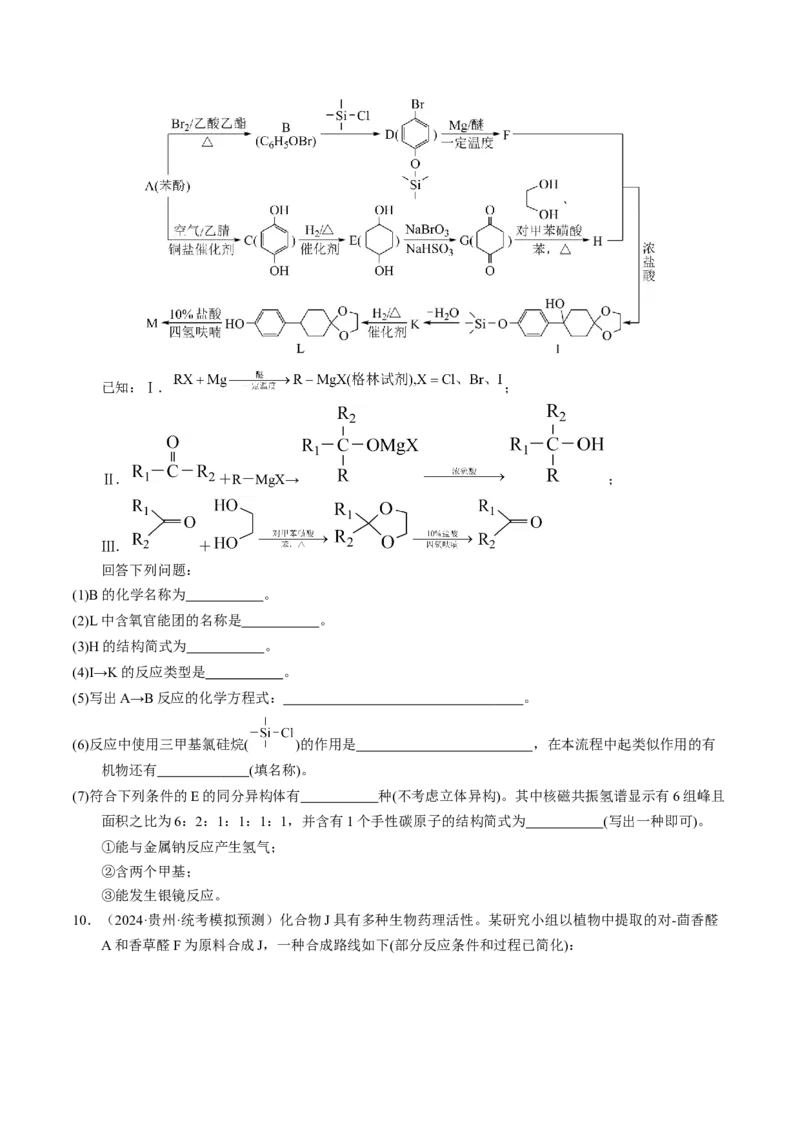
8.(2023·辽宁沈阳·统考三模)我国科学家研发的一条氯霉素(H)的合成路线如图所示:
已知:
回答下列问题:
(1)A的名称为 。
(2)氯霉素H的官能团是硝基、羟基和 。
(3)C为反式结构,B→C的化学反应方程式 。
(4)D→E的反应类型是 。
(5)写出符合下列条件的E的同分异构体的结构简式 (写出一种即可)。
①核磁共振氢谱有5个峰 ②能发生水解反应 ③能使 发生显色反应
(6)在G→H的反应中,通过 (填操作)使平衡转化率增大。
(7)左旋氯霉素才有抗菌消炎的作用,而此法得到的是左旋氯霉素和右旋氯霉素的混合物,因此需要将其分
开,其中一种方法是诱导析晶法。向H溶液加入少量的左旋氯霉素晶体做晶种, (填操作)
即可得到较纯的左旋氯霉素晶体。
9.(2024·安徽·高三一模)有机物M( )是一种制备液晶材料的重要中间体,以苯酚
为原料制备M的合成路线如图:已知:Ⅰ. ;
Ⅱ. +R-MgX→ ;
Ⅲ. +
回答下列问题:
(1)B的化学名称为 。
(2)L中含氧官能团的名称是 。
(3)H的结构简式为 。
(4)I→K的反应类型是 。
(5)写出A→B反应的化学方程式: 。
(6)反应中使用三甲基氯硅烷( )的作用是 ,在本流程中起类似作用的有
机物还有 (填名称)。
(7)符合下列条件的E的同分异构体有 种(不考虑立体异构)。其中核磁共振氢谱显示有6组峰且
面积之比为6:2:1:1:1:1,并含有1个手性碳原子的结构简式为 (写出一种即可)。
①能与金属钠反应产生氢气;
②含两个甲基;
③能发生银镜反应。
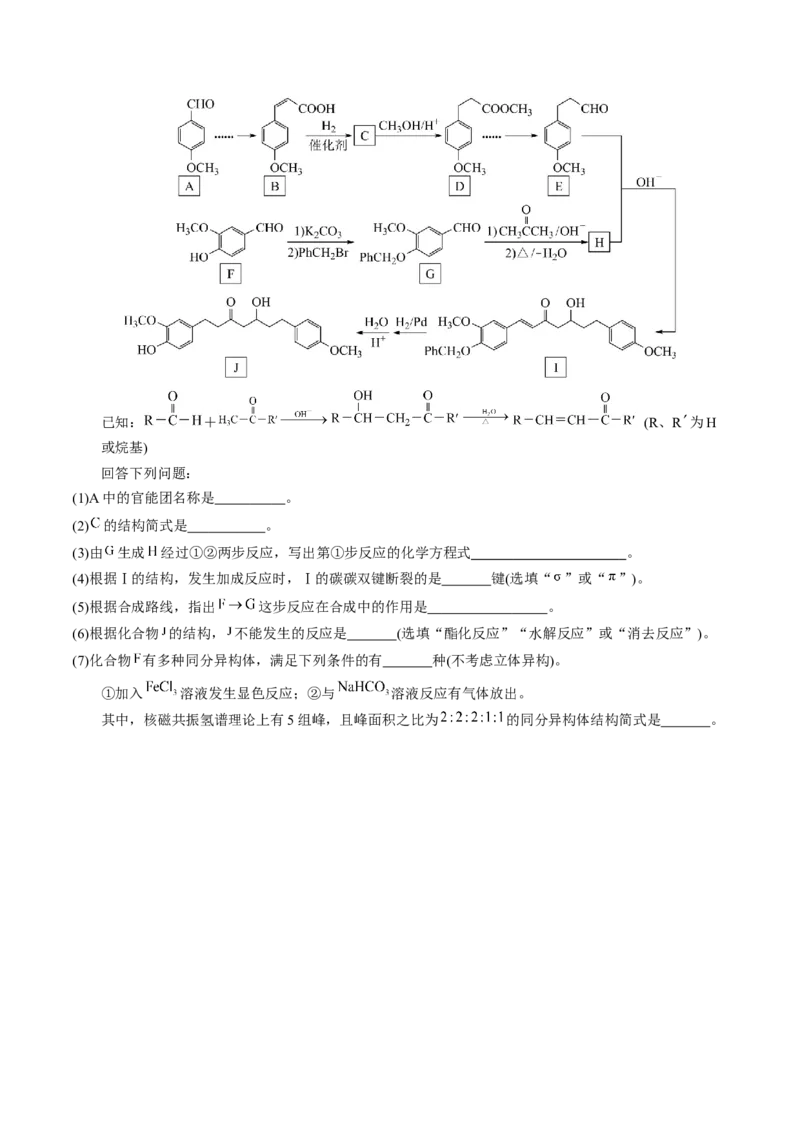
10.(2024·贵州·统考模拟预测)化合物J具有多种生物药理活性。某研究小组以植物中提取的对-茴香醛
A和香草醛F为原料合成J,一种合成路线如下(部分反应条件和过程已简化):已知: + (R、R 为H
或烷基)
回答下列问题:
(1)A中的官能团名称是 。
(2) 的结构简式是 。
(3)由 生成 经过①②两步反应,写出第①步反应的化学方程式 。
(4)根据Ⅰ的结构,发生加成反应时,Ⅰ的碳碳双键断裂的是 键(选填“ ”或“ ”)。
(5)根据合成路线,指出 这步反应在合成中的作用是 。
(6)根据化合物 的结构, 不能发生的反应是 (选填“酯化反应”“水解反应”或“消去反应”)。
(7)化合物 有多种同分异构体,满足下列条件的有 种(不考虑立体异构)。
①加入 溶液发生显色反应;②与 溶液反应有气体放出。
其中,核磁共振氢谱理论上有5组峰,且峰面积之比为 的同分异构体结构简式是 。