文档内容
热点 08 分子结构与性质
►命题趋势►解题策略►真题回眸►限时检测
考向一 化学键(σ键、π键、配位键等)
考向二 杂化方式和分子的空间构型
分子结构与性质
考向三 极性分子和非极性分子
考向四 分子的性质及应用
分子结构与性质是高中化学的重要内容,也是每年高考的热点之一,命题侧重结合新科技,新能源等
社会热点为背景,该部分主要考点是:
(1)杂化轨道理论和价层电子对互斥模型的应用,杂化类型及解释分子的空间构型;
(2)化学键的判断、σ键或π键数目的计算、配合物等内容;
(3)等电子原理的应用;
(3)极性分子和非极性分子的性质差异;
(4)分子间作用力和氢键对物质性质的影响等。
分子的立体结构和分子之间的作用力也是理解分子结构与性质关系的重要内容,常见题型为选择题和
填空题,本部分考查内容的规律性强,命题空间广阔,考查方式会向多方位、多层次发展。
预测2024年继续重点考查共价键的不同类型,特别是σ键、π键、配位键的判断,考查分子的空间构
型以及分子的杂化类型,特别是杂化类型的判断是高考重点,考察分子的性质,特别是熔沸点、水溶性、
键角大小的原因解释,复习时加以关注。
【策略1】熟悉化学键(σ键和π键)与大π键的判断方法
1.共价键
①分类
分类依据 类型
键 电子云“头碰头”重叠
形成共价键的原
子轨道重叠方式
键 电子云“肩并肩”重叠
形成共价键的电 极性键 共用电子对发生偏移子对是否偏移
非极性键 共用电子对不发生偏移
键 原子间有一对共用电子对
原子间共用电子
键 原子间有两对共用电子对
对的数目
键 原子间有三对共用电子对
②σ键和π键判断的一般规律
通过物质的结构式,可以快速有效地判断键的种类及数目,判断成键方式时,需掌握:
共价单键是σ键;
共价双键中含有个σ键,个π键;
共价三键中含有个σ键,个π键。
原子形成共价键时,优先形成σ键,σ键可以单独形成,π键不能单独形成。σ键形成过程中电子云重
叠程度比π键大,更稳定,故含有π键的分子发生化学反应时先断裂π键。
③共价键的键参数
概念
①键能越大,键长越短,分子越稳定。
键参数对分子性质
的影响
2.大π键的简介
大π键一般是三个或更多个原子间形成的,是未杂化轨道中原子轨道“肩并肩”
简介
重叠形成的π键表达式 Π,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数
对于多电子的粒子,若中心原子的杂化方式不是sp3杂化,中心原子与配位原子可
一般判断
能形成大π键
:Π; CH===CH—CH===CH :Π; NO:Π;
示例 2 2
SO :Π; O:Π; CO:Π
2 3
3.化学键对物质性质的影响
(1)对物理性质的影响
金刚石、晶体硅、石英、金刚砂等物质硬度大、熔点高,就是因为其中的共价键很强,破坏时需消耗
很多的能量。
NaCl等部分离子化合物,有很强的离子键,故熔点也较高。
(2)对化学性质的影响
N 分子中有很强的共价键,故在通常状况下,N 很稳定,HS、HI等分子中的共价键较弱,故它们受
2 2 2
热时易分解。
(3)物质熔化、溶解时化学键的变化
离子化合物的溶解或熔化过程:离子化合物溶于水或熔化后均电离出自由移动的阴、阳离子,离子键
被破坏。
共价化合物的溶解过程:
①有些共价化合物溶于水后,能与水反应,其分子内共价键被破坏,如CO 和SO 等。
2 2
②有些共价化合物溶于水后,与水分子作用形成水合离子,从而发生电离,形成阴、阳离子,其分子
内的共价键被破坏,如HCl、HSO 等。
2 4
③有些共价化合物溶于水后,其分子内的共价键不被破坏,如蔗糖(C H O )、酒精(C HOH)等。
12 22 11 2 5
【策略2】掌握配合物与超分子的概念及应用
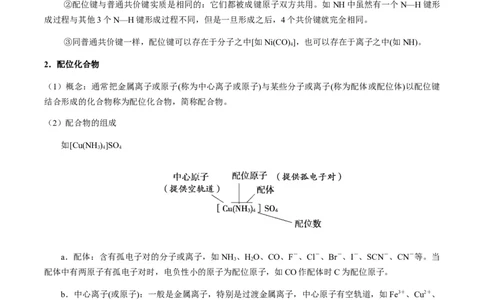
1.配位键
(1)概念:由一个原子单方面提供孤电子对,而另一个原子提供空轨道接受孤电子对形成的共价键,即
“电子对给予—接受”键,是一类特殊的共价键。
(2)表示方法:配位键可以用A→B来表示,其中A是提供孤电子对的原子,B是接受孤电子对的原子。例如: 中铜离子与水分子之间的化学键是由HO提供孤电子对给予Cu2+形
2
成的。
(3)配位键与共价键的关系
①形成过程不同:配位键实质上是一种特殊的共价键,在配位键中一方提供孤电子对,另一方提供空
轨道;普通共价键的共用电子对是由成键原子双方共同提供的。
②配位键与普通共价键实质是相同的:它们都被成键原子双方共用。如NH中虽然有一个N—H键形
成过程与其他3个N—H键形成过程不同,但是一旦形成之后,4个共价键就完全相同。
③同普通共价键一样,配位键可以存在于分子之中[如Ni(CO) ],也可以存在于离子之中(如NH)。
4
2.配位化合物
(1)概念:通常把金属离子或原子(称为中心离子或原子)与某些分子或离子(称为配体或配位体)以配位键
结合形成的化合物称为配位化合物,简称配合物。
(2)配合物的组成
如[Cu(NH )]SO
3 4 4
a.配体:含有孤电子对的分子或离子,如NH 、HO、CO、F-、Cl-、Br-、I-、SCN-、CN-等。当
3 2
配体中有两原子有孤电子对时,电负性小的原子为配位原子,如CO作配体时C为配位原子。
b.中心离子(或原子):一般是金属离子,特别是过渡金属离子,中心原子有空轨道,如Fe3+、Cu2+、
Zn2+、Ag+等。
c.配位数:直接同中心原子(或离子)配位的含有孤电子对的分子(或离子)的数目。中心原子(或离子)
的配位数一般为2、4、6、8等。
d.配合物在水溶液中电离成内界和外界两部分,
如 2Cl-,而内界微粒很难电离,因此,配合物
[Co(NH )Cl]Cl 内界中的Cl-不能被Ag+沉淀,只有外界的Cl-才能与硝酸银溶液反应产生沉淀。
3 5 23.配合物的生成实验探究
配合物形成时性质的改变:
①溶解度的改变:一些难溶于水的金属化合物形成配合物后,易溶解,如AgCl→[Ag(NH )]+。
3 2
②颜色的改变:当简单离子形成配合物时颜色会发生改变,如Fe(SCN) 的形成,利用此性质可检验铁
3
离子的存在。
③稳定性改变:形成配合物后,物质的稳定性增强。
(1)CuSO 溶液―――→Cu(OH) (蓝色沉淀)―――→[Cu(NH )]2+(深蓝色),其反应的离子方程式为
4 2 3 4
Cu2++2NH ·H O===Cu(OH) ↓+2NH,
3 2 2
Cu(OH) +4NH ===[Cu(NH)]2++2OH-。
2 3 3 4
(2)FeCl 溶液―――→Fe(SCN) (血红色),KSCN溶液检验Fe3+。
3 3
(3)NaCl溶液―――→AgCl(白色沉淀)――→[Ag(NH)]+,反应的离子方程式为
3 2
Cl-+Ag+===AgCl↓,
AgCl+2NH ===[Ag(NH )]++Cl-。
3 3 2
4.配合物的种类与应用
配合物种类繁多,如叶绿素、血红素和维生素B 都是配合物。如叶绿素中Mg2+为中心离子,大环有
12
机化合物作配体,配位原子为N。配合物在医药科学、化学催化剂、新型分子材料等领域应用广泛。
5.超分子
(1)定义:由两种或两种以上的分子通过分子间相互作用形成的分子聚集体。这里的分子也包含离子。
(2)特点:超分子这种分子聚集体,有的是有限的,有的是无限伸展的。
(3)应用
示例一:分离C 和C
60 70
示例二:冠醚识别碱金属离子:冠醚与合适的碱金属离子形成超分子。
(4)特征:超分子的两特征分别为分子识别和自组装。
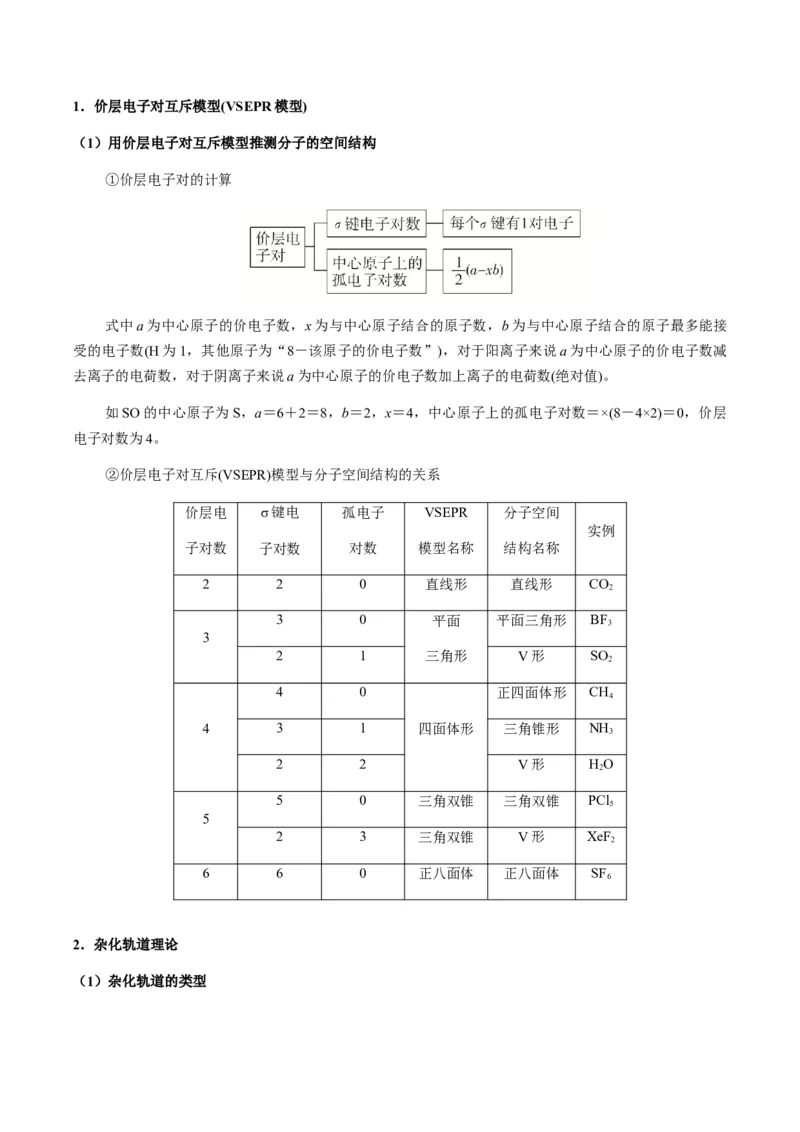
【策略3】熟练杂化方式与分子空间结构的判断方法1.价层电子对互斥模型(VSEPR模型)
(1)用价层电子对互斥模型推测分子的空间结构
①价层电子对的计算
式中a为中心原子的价电子数,x为与中心原子结合的原子数,b为与中心原子结合的原子最多能接
受的电子数(H为1,其他原子为“8-该原子的价电子数”),对于阳离子来说a为中心原子的价电子数减
去离子的电荷数,对于阴离子来说a为中心原子的价电子数加上离子的电荷数(绝对值)。
如SO的中心原子为S,a=6+2=8,b=2,x=4,中心原子上的孤电子对数=×(8-4×2)=0,价层
电子对数为4。
②价层电子对互斥(VSEPR)模型与分子空间结构的关系
价层电 σ键电 孤电子 VSEPR 分子空间
实例
子对数 子对数 对数 模型名称 结构名称
2 2 0 直线形 直线形 CO
2
3 0 平面 平面三角形 BF
3
3
2 1 三角形 V形 SO
2
4 0 正四面体形 CH
4
4 3 1 四面体形 三角锥形 NH
3
2 2 V形 HO
2
5 0 三角双锥 三角双锥 PCl
5
5
2 3 三角双锥 V形 XeF
2
6 6 0 正八面体 正八面体 SF
6
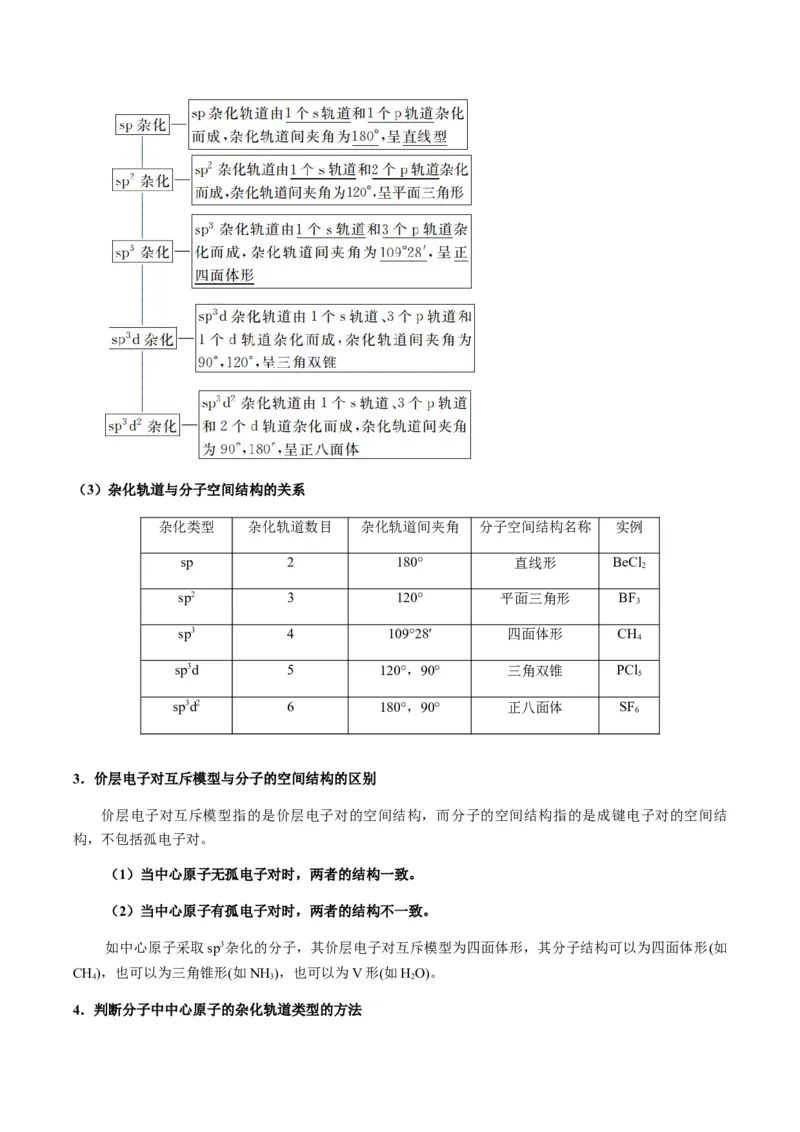
2.杂化轨道理论
(1)杂化轨道的类型(3)杂化轨道与分子空间结构的关系
杂化类型 杂化轨道数目 杂化轨道间夹角 分子空间结构名称 实例
sp 2 180° 直线形 BeCl
2
sp2 3 120° 平面三角形 BF
3
sp3 4 109°28′ 四面体形 CH
4
sp3d 5 120°,90° 三角双锥 PCl
5
sp3d2 6 180°,90° 正八面体 SF
6
3.价层电子对互斥模型与分子的空间结构的区别
价层电子对互斥模型指的是价层电子对的空间结构,而分子的空间结构指的是成键电子对的空间结
构,不包括孤电子对。
(1)当中心原子无孤电子对时,两者的结构一致。
(2)当中心原子有孤电子对时,两者的结构不一致。
如中心原子采取sp3杂化的分子,其价层电子对互斥模型为四面体形,其分子结构可以为四面体形(如
CH),也可以为三角锥形(如NH ),也可以为V形(如HO)。
4 3 2
4.判断分子中中心原子的杂化轨道类型的方法(1)根据分子的空间结构判断
①若分子的空间结构为正四面体形或三角锥形,则分子的中心原子发生sp3杂化。
②若分子的空间结构呈平面三角形,则分子的中心原子发生sp2杂化。
③若分子的空间结构呈直线形,则分子的中心原子发生sp杂化。
(2)根据键角判断
若键角为109°28′,则分子的中心原子发生 sp3杂化;若键角为120°,则分子的中心原子发生 sp2杂
化;若键角为180°,则分子的中心原子发生sp杂化。
(3)根据中心原子的价层电子对数判断
如中心原子的价层电子对数为4,是sp3杂化,为3是sp2杂化,为2,则是sp杂化。
(4)根据σ键数与孤电子对数(适用于结构式已知的粒子)
①含C有机物:2个σ—sp,3个σ—sp2,4个σ—sp3。
②含N化合物:2个σ—sp2,3个σ—sp3。
③含O(S)化合物:2个σ—sp3。
5.分子键角的大小比较
(1)杂化类型不同:sp>sp2>sp3。
(2)杂化类型相同
①孤电子对数越多,键角越小,如HOO—H…O>N—H…N。
特征 具有一定的方向性和饱和性。
分类 分子内氢键和分子间氢键。
分子间氢键使物质的熔、沸点升高,会对电离和溶解度等产生影响。同分异
构体中,形成分子间氢键的物质的熔沸点大于形成分子内氢键的物质。如对
物质性质
羟基苯甲醛(形成分子间氢键)的沸点高于邻羟基苯甲醛(形成分子内氢键)的
沸点。
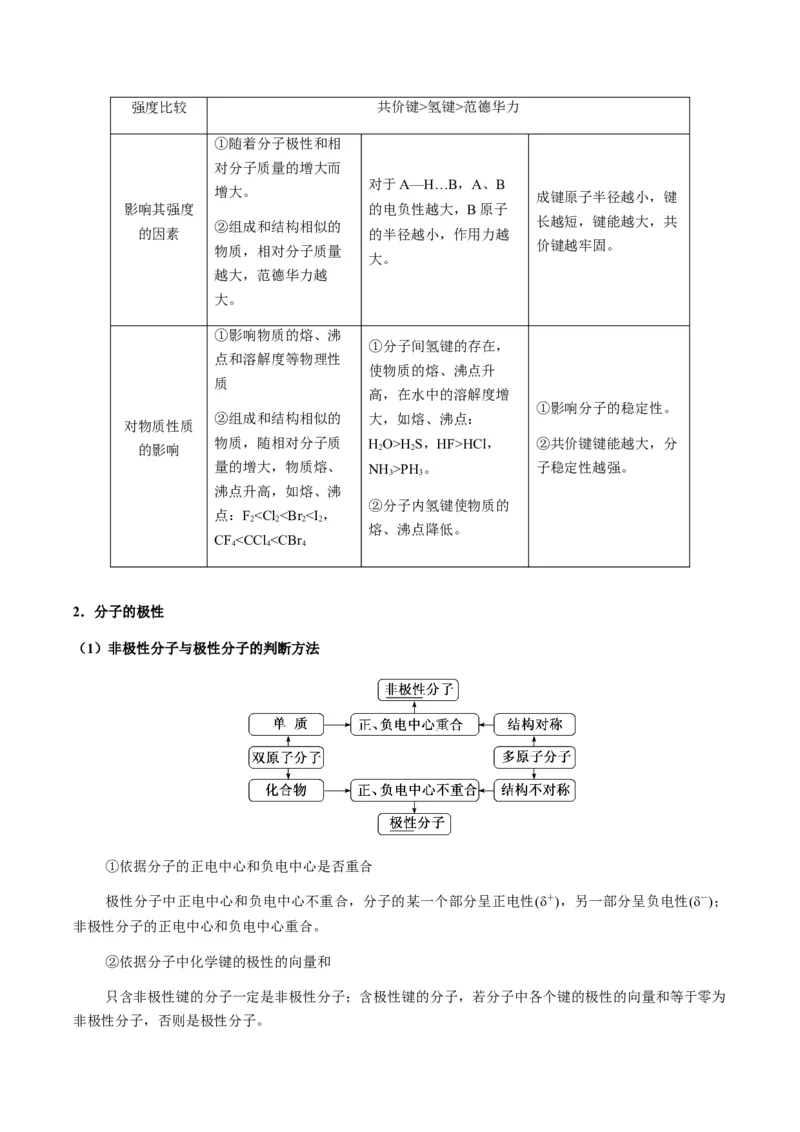
(3)范德华力、氢键和共价键的比较
范德华力 氢键 共价键
氢原子与氟、氮或氧原
子
作用粒子 分子 原子
(分子内,分子间)强度比较 共价键>氢键>范德华力
①随着分子极性和相
对分子质量的增大而
对于A—H…B,A、B
增大。
成键原子半径越小,键
影响其强度 的电负性越大,B原子
长越短,键能越大,共
②组成和结构相似的
的因素 的半径越小,作用力越
价键越牢固。
物质,相对分子质量
大。
越大,范德华力越
大。
①影响物质的熔、沸
①分子间氢键的存在,
点和溶解度等物理性
使物质的熔、沸点升
质
高,在水中的溶解度增
①影响分子的稳定性。
②组成和结构相似的 大,如熔、沸点:
对物质性质
物质,随相对分子质 HO>HS,HF>HCl, ②共价键键能越大,分
的影响 2 2
量的增大,物质熔、 NH >PH。 子稳定性越强。
3 3
沸点升高,如熔、沸
②分子内氢键使物质的
点:F三氯乙酸 性,使FC—的极性大于ClC—的极性,导致三氟乙酸的
3 3
羧基中的羟基的极性更大,更易电离出氢离子。
ClC—的极性>ClHC—的极性>ClH C—的极性,极性越
3 2 2
三氯乙酸>二氯乙酸>氯乙酸
强,羧基中的羟基的极性就越大,就越易电离出氢离子。
烃基是推电子基团,烃基越长推电子效应越大,使羧基中
甲酸>乙酸>丙酸
的羟基的极性越小,羧酸的酸性越弱。
键的极性对物质的化学性质有重要影响。例如,羧酸是一大类含羧基(—COOH)的有机酸,羧基可电
离出H+而呈酸性。羧酸的酸性可用pK 的大小来衡量,pK 越小,酸性越强。羧酸的酸性大小与其分子的
a a
组成和结构有关,如下表所示:
不同羧酸的pK
a
羧酸 pK
a
丙酸(C HCOOH) 4.88
2 5
乙酸(CHCOOH) 4.76
3
甲酸(HCOOH) 3.75
氯乙酸(CHClCOOH) 2.86
2
二氯乙酸(CHCl COOH) 1.29
2
三氯乙酸(CCl COOH) 0.65
3
三氟乙酸(CFCOOH) 0.23
3
(3)键的极性、分子空间结构与分子极性的关系
类型 实例 键的极性 空间结构 分子极性X H、N 非极性键 直线形 非极性分子
2 2 2
XY HCl、NO 极性键 直线形 极性分子
CO、CS 极性键 直线形 非极性分子
2 2
XY
2
SO 极性键 V形 极性分子
2
(X Y)
2
HO、HS 极性键 V形 极性分子
2 2
BF 极性键 平面正三角形 非极性分子
3
XY
3
NH 极性键 三角锥形 极性分子
3
XY CH、CCl 极性键 正四面体形 非极性分子
4 4 4
3.溶解性
(1)“相似相溶”的规律:
非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂。如果存在氢键,则溶剂与溶质之
间的氢键作用力越大,溶解性越好。
(2)随着溶质分子中憎水基个数的增大,溶质在水中的溶解度减小。如甲醇、乙醇和水能以任意比互
溶,而戊醇中的烃基较大,故在水中的溶解度明显减小。
(3)分子与HO反应,也能促进分子在水中的溶解,如SO 、NO 。
2 2 2
4.分子的手性
(1)手性异构体:具有完全相同的组成和原子排列的一对分子,如同左手和右手一样互为镜像,却在三
维空间里不能重叠,互称手性异构体。
(2)手性分子:具有手性异构体的分子。
(3)手性碳原子:在有机物分子中,连有四个不同基团或原子的碳原子。含有手性碳原子的分子是手性
分子,如 中*C为手性碳原子。
考向一 化学键(σ键、π键、配位键等)
1.(2023·辽宁·统考高考真题)下列化学用语或表述正确的是A.BeCl 的空间结构:V形 B.P 中的共价键类型:非极性键
2 4
C.基态Ni原子价电子排布式:3d10 D.顺—2—丁烯的结构简式:
2.(2023·河北·统考高考真题)物质的结构决定其性质。下列实例与解释不相符的是
选项 实例 解释
A 用 替代 填充探空气球更安全 的电子构型稳定,不易得失电子
B 与 形成配合物 中的B有空轨道接受 中N的孤电子对
C 碱金属中 的熔点最高 碱金属中 的价电子数最少,金属键最强
D 不存在稳定的 分子 N原子价层只有4个原子轨道,不能形成5个 键
A.A B.B C.C D.D
3.(2023·江苏·统考高考真题)氢元素及其化合物在自然界广泛存在且具有重要应用。 、 、 是
氢元素的3种核素,基态H原子 的核外电子排布,使得H既可以形成 又可以形成 ,还能形成
、 、 、 、 等重要化合物;水煤气法、电解水、光催化分解水都能获得 ,如水煤气
法制氢反应中, 与足量 反应生成 和 吸收131.3kJ的热量。 在金属冶
炼、新能源开发、碳中和等方面具有重要应用,如 在催化剂作用下与 反应可得到 。我国
科学家在氢气的制备和应用等方面都取得了重大成果。下列说法正确的是
A. 、 、 都属于氢元素
B. 和 的中心原子轨道杂化类型均为
C. 分子中的化学键均为极性共价键
D. 晶体中存在Ca与 之间的强烈相互作用
考向二 杂化方式和分子的空间构型
4.(2023·重庆·统考高考真题) 和 均可发生水解反应,其中 的水解机理示意图如下:下列说法正确的是
A. 和 均为极性分子 B. 和 中的 均为 杂化
C. 和 的水解反应机理相同 D. 和 均能与 形成氢键
5.(2023·湖北·统考高考真题)价层电子对互斥理论可以预测某些微粒的空间结构。下列说法正确的是
A. 和 的VSEPR模型均为四面体
B. 和 的空间构型均为平面三角形
C. 和 均为非极性分子
D. 与 的键角相等
6.(2023·海南·统考高考真题)下列有关元素单质或化合物的叙述正确的是
A. 分子呈正四面体,键角为
B.NaCl焰色试验为黄色,与Cl电子跃迁有关
C.Cu基态原子核外电子排布符合构造原理
D. 是由极性键构成的极性分子
7.(2023·北京·统考高考真题)硫代硫酸盐是一类具有应用前景的浸金试剂。硫代硫酸根 可看作
是 中的一个 原子被 原子取代的产物。
(3) 的空间结构是 。
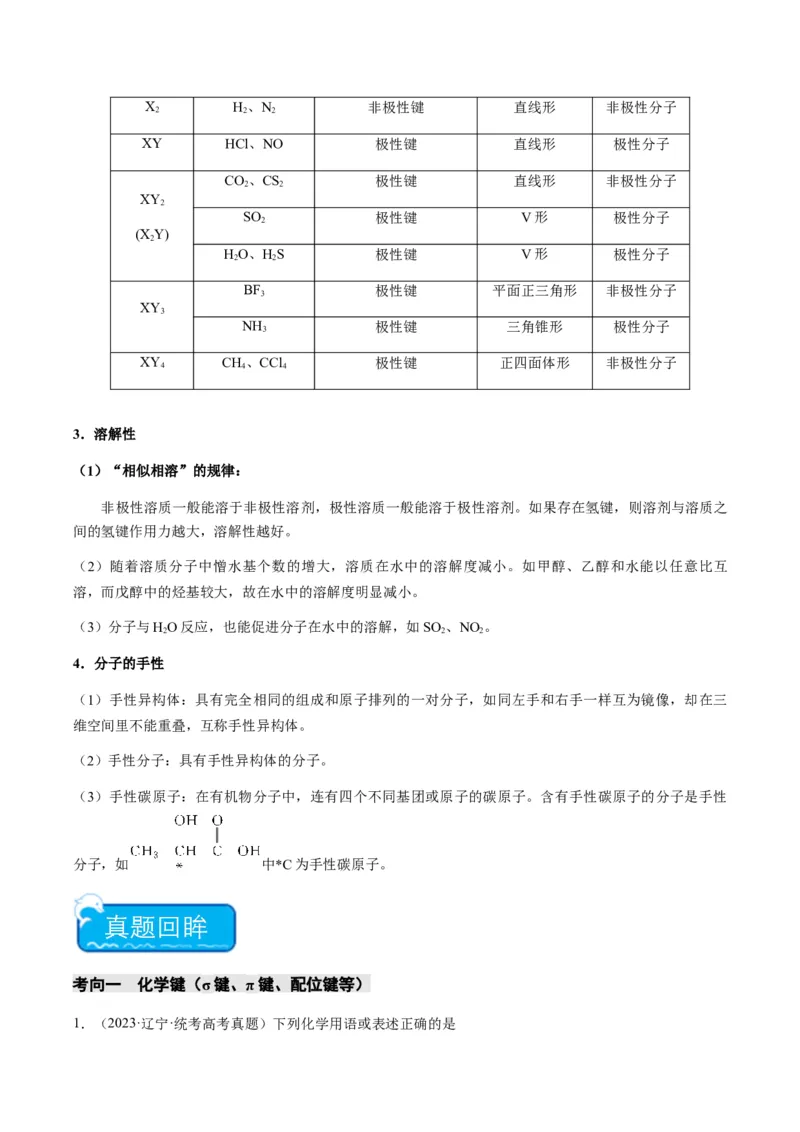
8.(2023·海南·统考高考真题)我国科学家发现一种钒配合物Ⅰ可以充当固氮反应的催化剂,反应过程中
经历的中间体包括Ⅱ和Ⅲ。( 代表单键、双键或叁键)
回答问题:
(1)配合物Ⅰ中钒的配位原子有4种,它们是 。
(2)配合物Ⅰ中,R′代表芳基, 空间结构呈角形,原因是 。
(3)配合物Ⅱ中,第一电离能最大的配位原子是 。
(4)配合物Ⅱ和Ⅲ中,钒的化合价分别为 和 ,配合物Ⅱ、Ⅲ和 三者中,两个氮原子间键长最长的是
。
考向三 极性分子和非极性分子
9.(2023·山东·统考高考真题)下列分子属于极性分子的是
A. B. C. D.
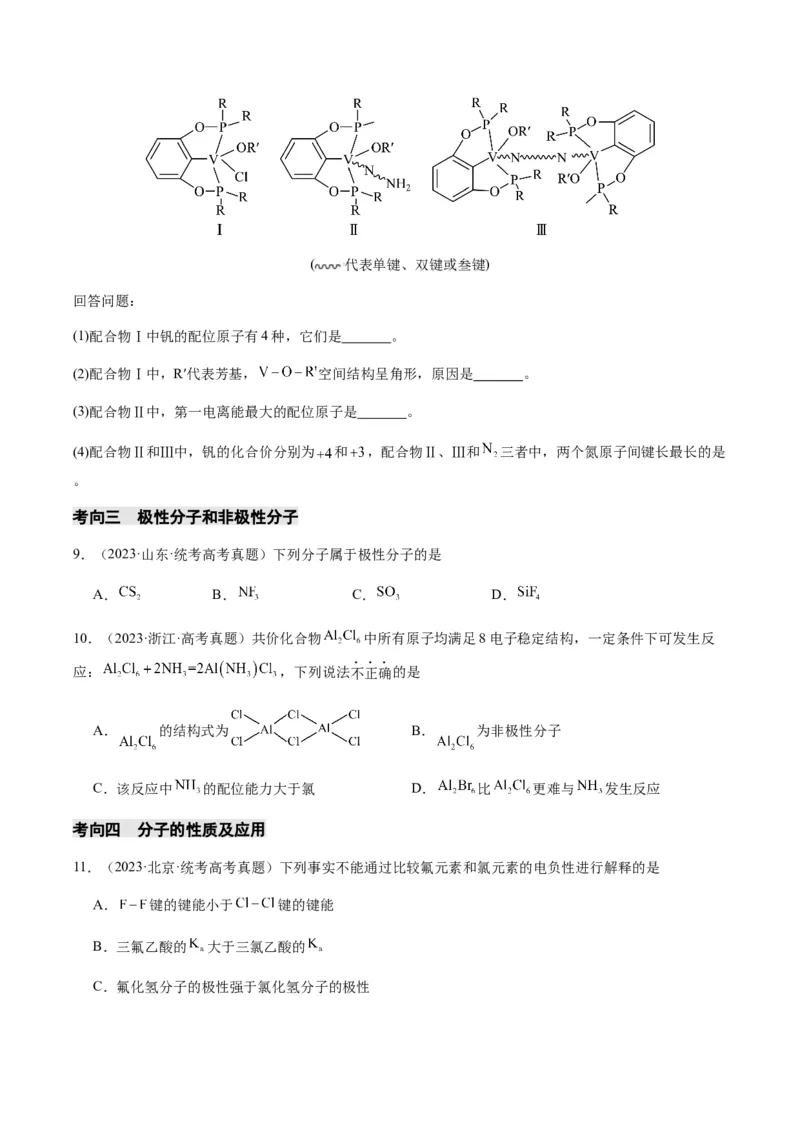
10.(2023·浙江·高考真题)共价化合物 中所有原子均满足8电子稳定结构,一定条件下可发生反
应: ,下列说法不正确的是
A. 的结构式为 B. 为非极性分子
C.该反应中 的配位能力大于氯 D. 比 更难与 发生反应
考向四 分子的性质及应用
11.(2023·北京·统考高考真题)下列事实不能通过比较氟元素和氯元素的电负性进行解释的是
A. 键的键能小于 键的键能
B.三氟乙酸的 大于三氯乙酸的
C.氟化氢分子的极性强于氯化氢分子的极性D.气态氟化氢中存在 ,而气态氯化氢中是 分子
12.(2023·湖南·统考高考真题)下列有关物质结构和性质的说法错误的是
A.含有手性碳原子的分子叫做手性分子
B.邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点
C.酰胺在酸或碱存在并加热的条件下可发生水解反应
D.冠醚(18-冠-6)的空穴与K+尺寸适配,两者能通过弱相互作用形成超分子
13.(2023·湖北·统考高考真题)物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
选项 性质差异 结构因素
A 沸点:正戊烷(36.1℃)高于新戊烷(9.5℃) 分子间作用力
B 熔点: (1040℃)远高于 (178℃升华) 晶体类型
C 酸性: ( )远强于 ( ) 羟基极性
D 溶解度(20℃): (29g)大于 (8g) 阴离子电荷
A.A B.B C.C D.D
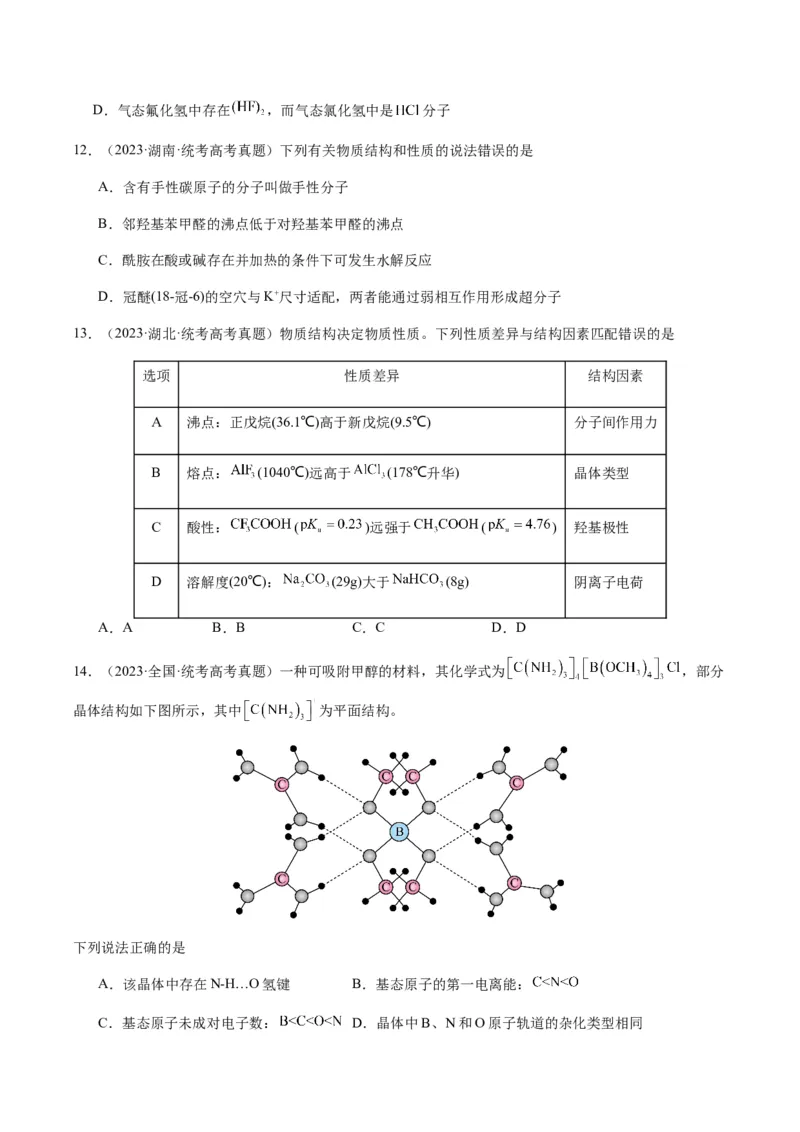
14.(2023·全国·统考高考真题)一种可吸附甲醇的材料,其化学式为 ,部分
晶体结构如下图所示,其中 为平面结构。
下列说法正确的是
A.该晶体中存在N-H…O氢键 B.基态原子的第一电离能:
C.基态原子未成对电子数: D.晶体中B、N和O原子轨道的杂化类型相同15.(2023·山东·统考高考真题)卤素可形成许多结构和性质特殊的化合物。回答下列问题:
(2) 中心原子为 , 中心原子为 ,二者均为 形结构,但 中存在大 键 。 中
原子的轨道杂化方式 ;为 键角 键角(填“>”“ <”或“=”)。比较 与
中 键的键长并说明原因 。
16.(2023·全国·统考高考真题)中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量
橄榄石矿物( )。回答下列问题:
(2)已知一些物质的熔点数据如下表:
物质 熔点/℃
800.7
与 均为第三周期元素, 熔点明显高于 ,原因是 。分析同族元素的氯
化物 、 、 熔点变化趋势及其原因 。 的空间结构为 ,其中 的轨
道杂化形式为 。
(建议用时:35分钟)
1.(2024·广西·校联考模拟预测)价层电子对互斥理论可以预测某些微粒的空间结构。下列说法错误的是
A.SO 和SO 的VSEPR模型均为平面三角形
2 3
B.PCl 、NCl 的空间构型都是三角锥形
3 3
C.BF 和NF 均为非极性分子
3 3
D.CO 与N 的键角相等
2
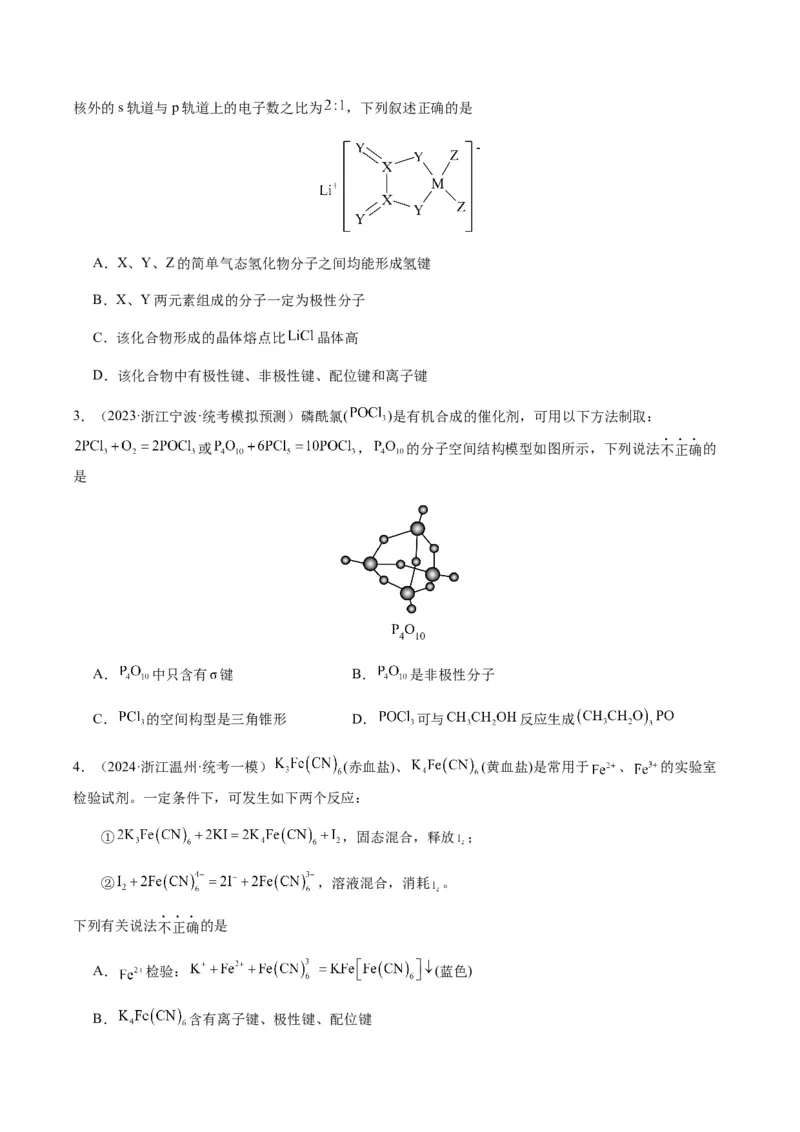
2.(2023·吉林长春·统考一模) 是一种新型的电解质锂盐,具有较高的电化学稳定性和电导率,
被广泛用于目前的锂电池中。 的结构如图所示,其中元素M、X、Y、Z位于同一短周期,X原子核外的s轨道与p轨道上的电子数之比为 ,下列叙述正确的是
A.X、Y、Z的简单气态氢化物分子之间均能形成氢键
B.X、Y两元素组成的分子一定为极性分子
C.该化合物形成的晶体熔点比 晶体高
D.该化合物中有极性键、非极性键、配位键和离子键
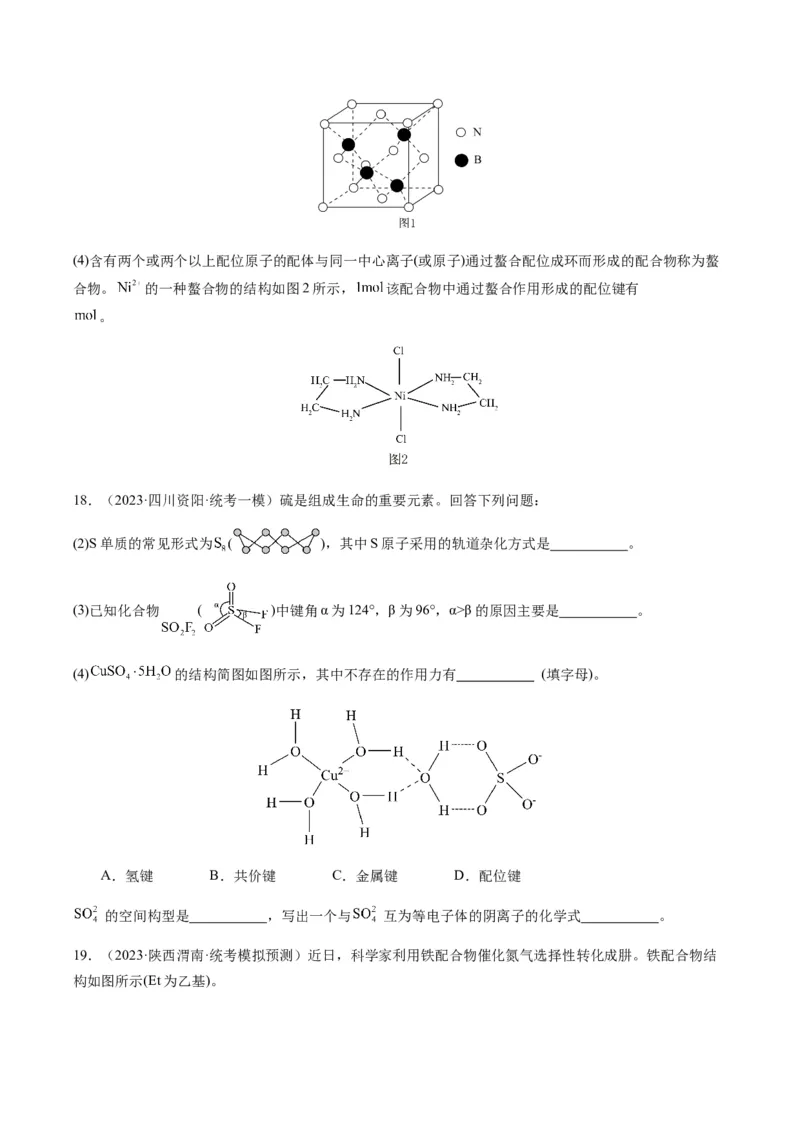
3.(2023·浙江宁波·统考模拟预测)磷酰氯( )是有机合成的催化剂,可用以下方法制取:
或 , 的分子空间结构模型如图所示,下列说法不正确的
是
A. 中只含有 键 B. 是非极性分子
C. 的空间构型是三角锥形 D. 可与 反应生成
4.(2024·浙江温州·统考一模) (赤血盐)、 (黄血盐)是常用于 、 的实验室
检验试剂。一定条件下,可发生如下两个反应:
① ,固态混合,释放 ;
② ,溶液混合,消耗 。
下列有关说法不正确的是
A. 检验: (蓝色)
B. 含有离子键、极性键、配位键C. 氧化性强于
D.两个反应方向不一致,原因可能是溶液中 与 的配位能力强于
5.(2024·广西北海·统考一模) (俗称铵铁蓝)是一种蓝色的无机颜料。下列有关该物质
的说法错误的是
A.电负性:
B.铵铁蓝中铁元素有两种化合价
C. 中 的键角比 中的 的键角大
D.铵铁蓝中的配体是 ,该配体中 键与 键的数目之比是
6.(2023·江苏南通·统考模拟预测)周期表中VIA族元素及其化合物应用广泛。 、 、 是氧元素
的3种核素,可以形0成多种重要的化合物。亚硫酰氯 为黄色液体,其结构式为(
),遇水发生水解。工业上可电解HSO 与 混合溶液制备过二硫酸铵 ,过二硫酸
2 4
铵与双氧水中都含有过氧键(-O-O-)。硝化法制硫酸的主要反应为:
。SO 和SO 都是酸性氧化物,是制备硫酸的中间产物。下列说法正确的是
2 3
A. 、 、 具有相同的中子数
B.亚硫酰氯空间构型为平面三角形
C.SO 、SO 的中心原子轨道杂化类型均为sp2
2 3
D.SO 晶体中存在S和O 之间的强烈作用
2 2
7.(2023·江苏南通·统考模拟预测)利用反应 可去除COCl 污染。下
2
列说法正确的是
A.NH 为非极性分子
3
B. 中只含共价键
C.NH Cl的电子式为
4D.基态N原子的轨道表示式:
8.(2023·江西·校联考模拟预测)下列分子属于极性分子的是
A.OF B.CS C.SiCl D.O
2 2 4 2
9.(2022·浙江·校联考一模)下列说法正确的是
A.氢键 中三原子共直线时,作用力最强
B.X射线衍射实验中,非晶体会呈现明锐的衍射峰
C. 中, 给出孤对电子, 提供空轨道
D.离子液体是一种常见的等离子体
10.(2023·辽宁大连·校考模拟预测)三硫化四磷( )是黄绿色针状晶体,易燃、有毒,分子结构如图所
示。下列有关 的说法中正确的是
A. 中仅P原子最外层均满足8电子稳定结构
B.键角:
C. 中P原子为 杂化,S原子为 杂化
D. 分子中含有6mol极性共价键
11.(2022·浙江·校联考一模)下列关于超分子和配合物的叙述不正确的是
A.[Cr(NH )(H O) Cl]2+中三价铬离子提供空轨道,N、O、Cl提供孤电子对与三价铬离子形成配位
3 3 2 2
键,其中心离子的配位数为6
B.配合物[TiCl(H O) ]Cl ·H O中存在离子键、共价键、配位键,若加入足量AgNO 溶液,所有Cl-均
2 5 2 2 3
被完全沉淀
C.超分子是两种或两种以上的分子通过分子间相互作用形成的分子聚集体,包括离子
D.人体细胞和细胞器的双分子膜体现了超分子的自组装的特征12.(2022·浙江金华·校联考模拟预测)下列关于物质结构或性质及解释都正确的是
选项 物质结构或性质 解释
A 电子云半径: 电子的能量高,在离核更远的区域出现的概率大
B 键角: 的电负性比 大,孤电子对对成键电子对的斥力比较大
C 熔点: 熔化时要断开化学键, 只需克服范德华力
D 稳定性: 分子间可以形成氢键, 没有氢键
A.A B.B C.C D.D
13.(2023·浙江杭州·校联考模拟预测)利用 、 和 反应制联氨( ),反应方程式为
,下列关于该反应的说法不正确的是
A. 与 的晶体类型不同
B.此反应过程中既有极性键、非极性键的断裂,也有极性键、非极性键的形成
C. 与 分子间易形成氢键,结构可表示为
D. 分子中 为吸电子基,导致N原子与 的配位能力减弱,等物质的量浓度的 和
的水溶液, 水溶液碱性较弱
14.(2023·湖南株洲·统考一模)已知吡啶( )中含有与苯类似的 大π键,下列有关叙述正确的是
A.吡啶中N原子的价层孤电子对占据sp杂化轨道
B.在水中的溶解度,吡啶远大于苯的原因只是相似相溶原理
C. 、 、 的碱性随N原子电子云密度的增大而增强,则其中碱
性最弱的是D. 与 互为同系物
15.(2023·四川眉山·校考一模)二茂铁( )分子式为 ,是具有导电性的有机配合物,其
衍生物一直是科学研究的前沿。
(2)羰基铁粉[ ]中铁元素的配位数是 ,配位原子为 。
(3)二茂铁的衍生物可和 等微粒产生静电作用,H、B、O和C的电负性由大到小的顺序为;
; 空间构型为 。 的键角比 的 (填“大”或“小”)
16.(2023·海南·模拟预测)N、P、 为第VA族元素,该族元素及其化合物在生产,生活中有广泛应
用。回答下列问题:
(2)已知: , 的空间结构为 , 原子的杂化类型为 ;
为正四面体结构,则1 中含 键。
(3)《本草纲目》中记载砒霜( )可入药,已知: 的熔点为312.3℃,沸点为465℃。古代采用
“升华法”提纯砒霜,砒霜升华时破坏的作用力有 ;
(4) 的键角为93.5°, 的键角为92.1°, 的键角大于 的键角的原因是 ;
17.(2023·四川成都·校考一模)硼、氮、磷、钴、镍等元素的化合物在现代农业、科技、国防中有着许
多独特的用途。
(2)钴位于元素周期表的 区,钴与 易形成正八面体形的 配离子,试推测
的空间构型有 种。
(3)制备氮化硼 的一种方法为 。立方氮化硼( )的晶胞如图1所
示,其晶体类型为 ,N的配位数为 。试用价层电子对互斥理论解释 的键角比
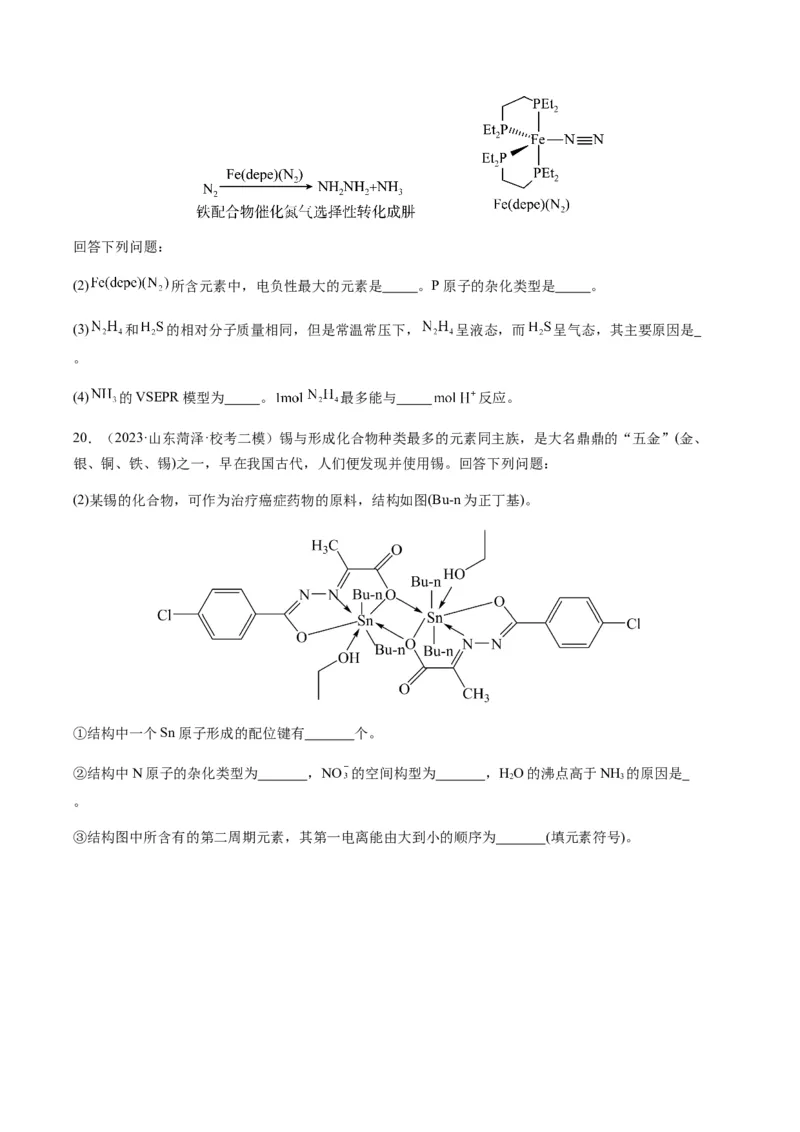
大的原因: 。(4)含有两个或两个以上配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物称为螯
合物。 的一种螯合物的结构如图2所示, 该配合物中通过螯合作用形成的配位键有
。
18.(2023·四川资阳·统考一模)硫是组成生命的重要元素。回答下列问题:
(2)S单质的常见形式为 ( ),其中S原子采用的轨道杂化方式是 。
(3)已知化合物 ( )中键角α为124°,β为96°,α>β的原因主要是 。
(4) 的结构简图如图所示,其中不存在的作用力有 (填字母)。
A.氢键 B.共价键 C.金属键 D.配位键
的空间构型是 ,写出一个与 互为等电子体的阴离子的化学式 。
19.(2023·陕西渭南·统考模拟预测)近日,科学家利用铁配合物催化氮气选择性转化成肼。铁配合物结
构如图所示(Et为乙基)。回答下列问题:
(2) 所含元素中,电负性最大的元素是 。P原子的杂化类型是 。
(3) 和 的相对分子质量相同,但是常温常压下, 呈液态,而 呈气态,其主要原因是
。
(4) 的VSEPR模型为 。 最多能与 反应。
20.(2023·山东菏泽·校考二模)锡与形成化合物种类最多的元素同主族,是大名鼎鼎的“五金”(金、
银、铜、铁、锡)之一,早在我国古代,人们便发现并使用锡。回答下列问题:
(2)某锡的化合物,可作为治疗癌症药物的原料,结构如图(Bu-n为正丁基)。
①结构中一个Sn原子形成的配位键有 个。
②结构中N原子的杂化类型为 ,NO 的空间构型为 ,HO的沸点高于NH 的原因是
2 3
。
③结构图中所含有的第二周期元素,其第一电离能由大到小的顺序为 (填元素符号)。