文档内容
高考解密11 常见非金属及其重要化合物
A 组 基础练
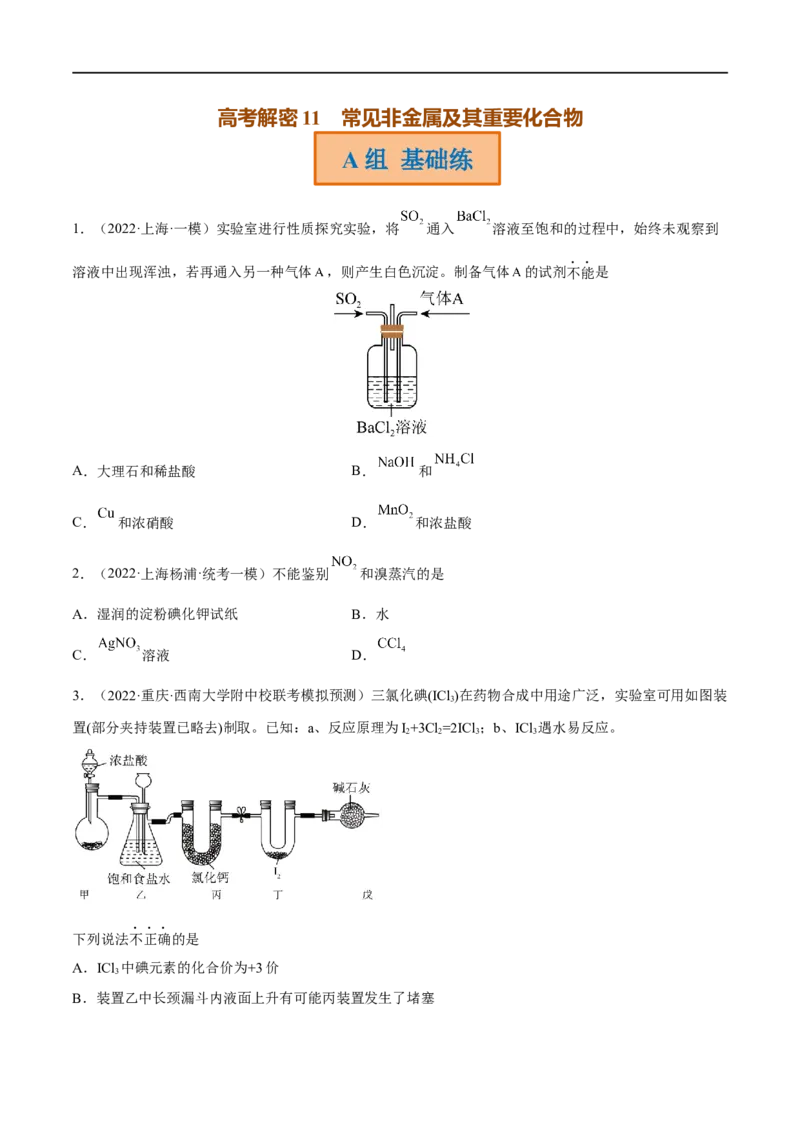
1.(2022·上海·一模)实验室进行性质探究实验,将 通入 溶液至饱和的过程中,始终未观察到
溶液中出现浑浊,若再通入另一种气体 ,则产生白色沉淀。制备气体 的试剂不能是
A.大理石和稀盐酸 B. 和
C. 和浓硝酸 D. 和浓盐酸
2.(2022·上海杨浦·统考一模)不能鉴别 和溴蒸汽的是
A.湿润的淀粉碘化钾试纸 B.水
C. 溶液 D.
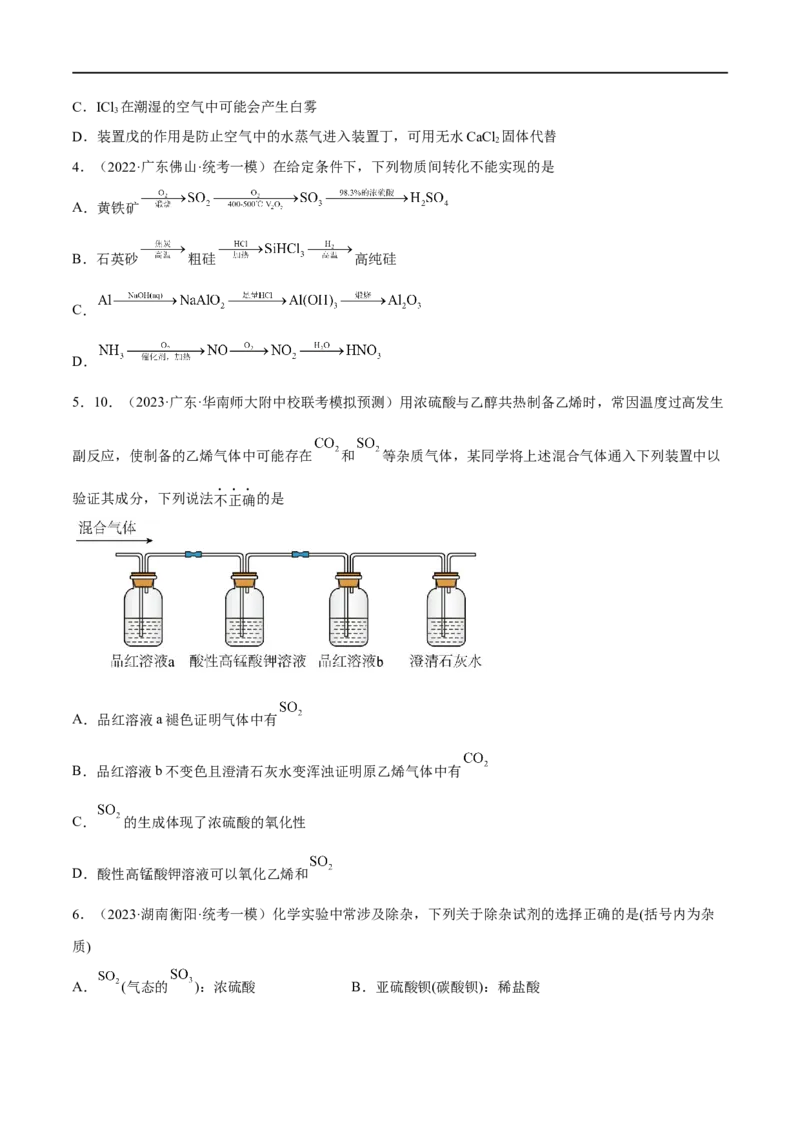
3.(2022·重庆·西南大学附中校联考模拟预测)三氯化碘(ICl )在药物合成中用途广泛,实验室可用如图装
3
置(部分夹持装置已略去)制取。已知:a、反应原理为I+3Cl=2ICl ;b、ICl 遇水易反应。
2 2 3 3
下列说法不正确的是
A.ICl 中碘元素的化合价为+3价
3
B.装置乙中长颈漏斗内液面上升有可能丙装置发生了堵塞C.ICl 在潮湿的空气中可能会产生白雾
3
D.装置戊的作用是防止空气中的水蒸气进入装置丁,可用无水CaCl 固体代替
2
4.(2022·广东佛山·统考一模)在给定条件下,下列物质间转化不能实现的是
A.黄铁矿
B.石英砂 粗硅 高纯硅
C.
D.
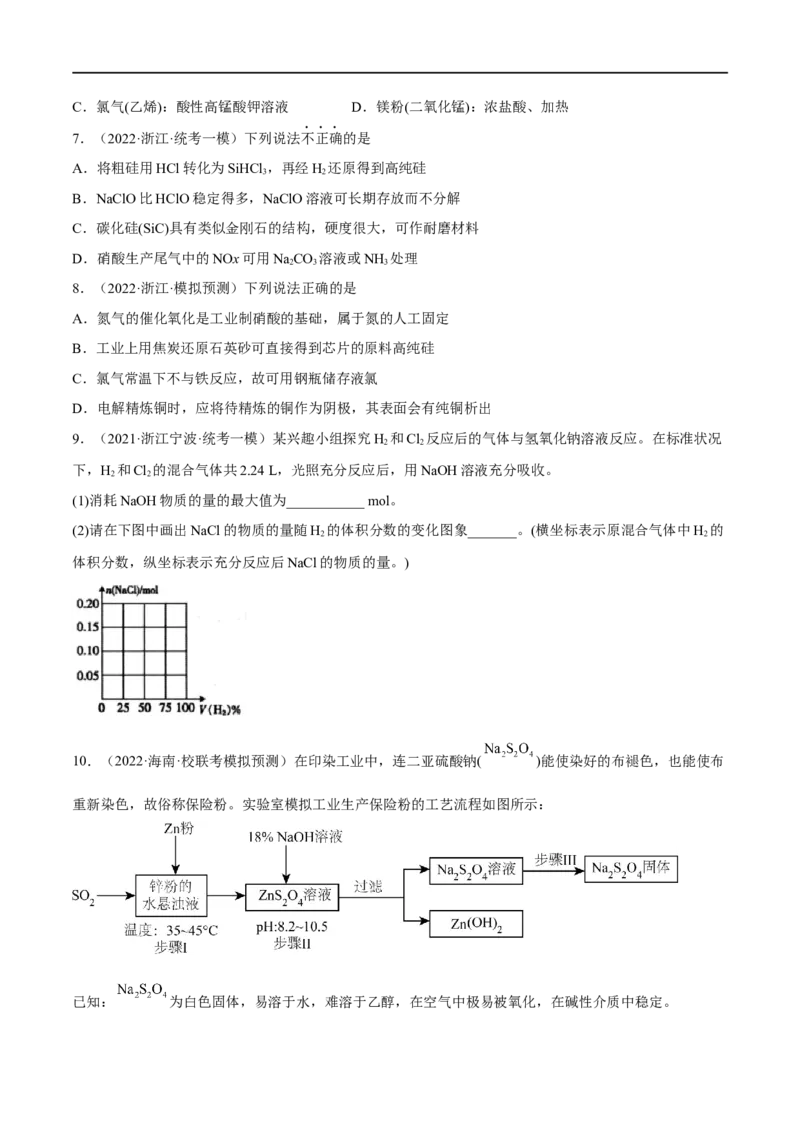
5.10.(2023·广东·华南师大附中校联考模拟预测)用浓硫酸与乙醇共热制备乙烯时,常因温度过高发生
副反应,使制备的乙烯气体中可能存在 和 等杂质气体,某同学将上述混合气体通入下列装置中以
验证其成分,下列说法不正确的是
A.品红溶液a褪色证明气体中有
B.品红溶液b不变色且澄清石灰水变浑浊证明原乙烯气体中有
C. 的生成体现了浓硫酸的氧化性
D.酸性高锰酸钾溶液可以氧化乙烯和
6.(2023·湖南衡阳·统考一模)化学实验中常涉及除杂,下列关于除杂试剂的选择正确的是(括号内为杂
质)
A. (气态的 ):浓硫酸 B.亚硫酸钡(碳酸钡):稀盐酸C.氯气(乙烯):酸性高锰酸钾溶液 D.镁粉(二氧化锰):浓盐酸、加热
7.(2022·浙江·统考一模)下列说法不正确的是
A.将粗硅用HCl转化为SiHCl ,再经H 还原得到高纯硅
3 2
B.NaClO比HClO稳定得多,NaClO溶液可长期存放而不分解
C.碳化硅(SiC)具有类似金刚石的结构,硬度很大,可作耐磨材料
D.硝酸生产尾气中的NOx可用NaCO 溶液或NH 处理
2 3 3
8.(2022·浙江·模拟预测)下列说法正确的是
A.氮气的催化氧化是工业制硝酸的基础,属于氮的人工固定
B.工业上用焦炭还原石英砂可直接得到芯片的原料高纯硅
C.氯气常温下不与铁反应,故可用钢瓶储存液氯
D.电解精炼铜时,应将待精炼的铜作为阴极,其表面会有纯铜析出
9.(2021·浙江宁波·统考一模)某兴趣小组探究H 和Cl 反应后的气体与氢氧化钠溶液反应。在标准状况
2 2
下,H 和Cl 的混合气体共2.24 L,光照充分反应后,用NaOH溶液充分吸收。
2 2
(1)消耗NaOH物质的量的最大值为___________ mol。
(2)请在下图中画出NaCl的物质的量随H 的体积分数的变化图象_______。(横坐标表示原混合气体中H 的
2 2
体积分数,纵坐标表示充分反应后NaCl的物质的量。)
10.(2022·海南·校联考模拟预测)在印染工业中,连二亚硫酸钠( )能使染好的布褪色,也能使布
重新染色,故俗称保险粉。实验室模拟工业生产保险粉的工艺流程如图所示:
已知: 为白色固体,易溶于水,难溶于乙醇,在空气中极易被氧化,在碱性介质中稳定。(1)工业上获得锌粉的方法为:将锌块加热熔化得到锌液,向锌液中不断鼓入 气体,冷却后可获得锌粉。
鼓入 气体的目的除了防止氧化外,还有__。
(2)在步骤I中,控制反应温度比较适宜的方法是___________加热(填“水浴”“油浴”或“砂浴”)。
(3)已知: 与 性质相似,当pH大于10.5时开始溶解,写出步骤II中碱性较强时
溶解的离子方程式:___________。
(4)已知:水溶液温度低于52℃时 以 形态结晶,碱性溶液中温度高于52℃时
脱水成无水盐。
步骤III的操作过程为:在无氧减压的环境中,将 碱性溶液于60℃左右蒸发至有大量晶体析出,
趁热过滤、洗涤、减压干燥。趁热过滤的目的是___________;操作中常选用无水乙醇洗涤,其优点是
___________、___________。
(5) 碱性溶液与 溶液反应有纳米银生成,该反应能用于 的纯度测定。若10mL
碱性溶液与20mL 溶液恰好完全反应,则该反应的离子方程式为
___________。
B 组 提升练
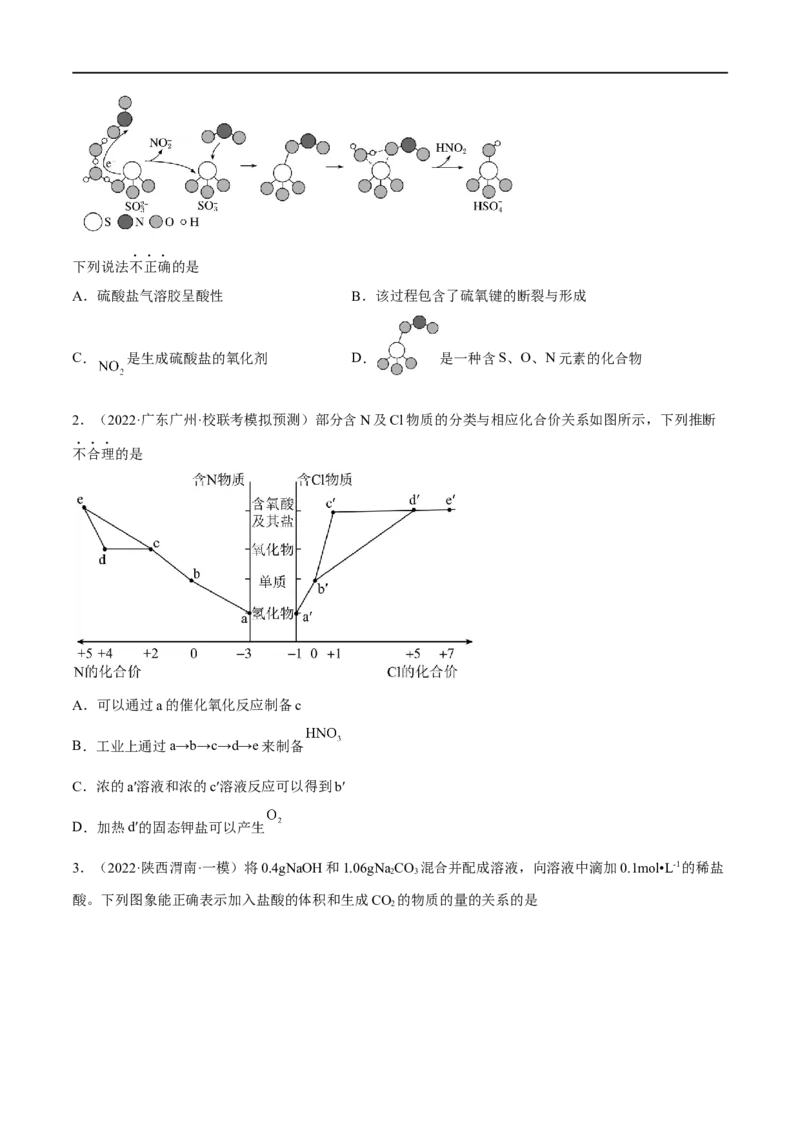
1.(2022·北京朝阳·和平街第一中学校考三模)硫酸盐(含 、 )气溶胶是 的成分之一。近期
科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如下:下列说法不正确的是
A.硫酸盐气溶胶呈酸性 B.该过程包含了硫氧键的断裂与形成
C. 是生成硫酸盐的氧化剂 D. 是一种含S、O、N元素的化合物
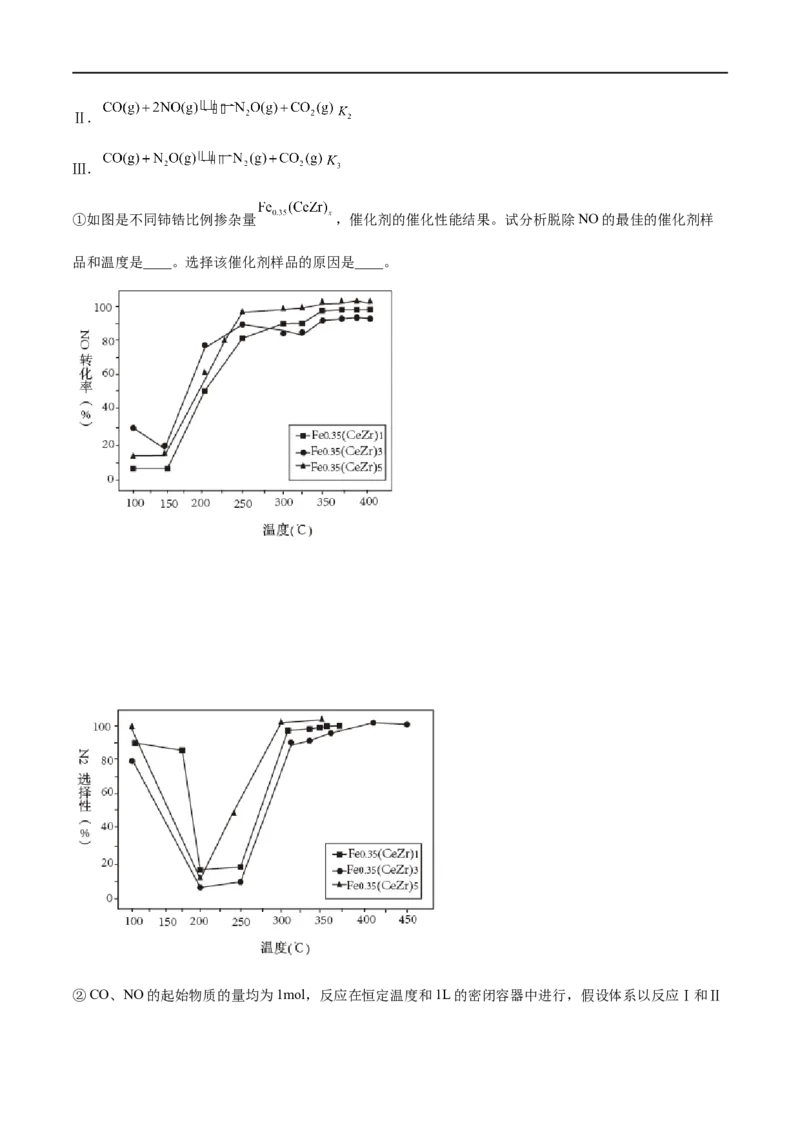
2.(2022·广东广州·校联考模拟预测)部分含N及Cl物质的分类与相应化合价关系如图所示,下列推断
不合理的是
A.可以通过a的催化氧化反应制备c
B.工业上通过a→b→c→d→e来制备
C.浓的a′溶液和浓的c′溶液反应可以得到b′
D.加热d′的固态钾盐可以产生
3.(2022·陕西渭南·一模)将0.4gNaOH和1.06gNa CO 混合并配成溶液,向溶液中滴加0.1mol•L-1的稀盐
2 3
酸。下列图象能正确表示加入盐酸的体积和生成CO 的物质的量的关系的是
2A. B.
C. D.
4.(2020·浙江·统考模拟预测)某课外兴趣小组成员为研究金属铜与强酸的反应 ,将6.4g铜粉分为两等
份,进行了如下实验,请完成有关计算。
(1)取其中一份铜粉投入200mL氢离子浓度为 1mol•L-1 硫酸和硝酸混合液中,微热使反应充分完成后,生
成一氧化氮气体448mL(标准状况)。则反应前混合溶液中硫酸的物质的量浓度为_________(写出计算过程)。
(2)用NaOH溶液吸收氮氧化物是防止NO 污染的一种方法。原理为2NO + 2NaOH=NaNO + NaNO +
2 2 3 2
HO,NO + NO + 2NaOH=2NaNO + H O。取另一份铜粉溶于过量的硝酸溶液,假设硝酸的还原产物只有
2 2 2 2
一氧化氮和二氧化氮,生成的混合气体能被amol NaOH溶液完全吸收,试讨论a的取值范围:_____。
5.(2021·浙江·统考模拟预测)氮氧化物 已经成为大气污染的主要污染源,其中NO的含量约占氮氧
化物总含量的90%,目前选择性催化还原技术是脱除 最普遍最有效的方法之一,请回答:
(1)实验室制取一氧化氮的化学方程式是_______。
(2)下列说法不正确的是_______。
A.上述反应的现象是铜片表面有无色气体产生,溶液由无色慢慢变蓝色
B.可通过排水法或排空气法收集一氧化氮
C.NO与 可与水反应,方程式为 ,可用以制硝酸
D.工业上,氨在钯或铂催化下被氧气氧化成一氧化氮
(3)在一定温度下,利用CO为还原剂在催化剂作用下将NO脱除并转化为 和 ,主要的反应方程式如
下:
Ⅰ.Ⅱ.
Ⅲ.
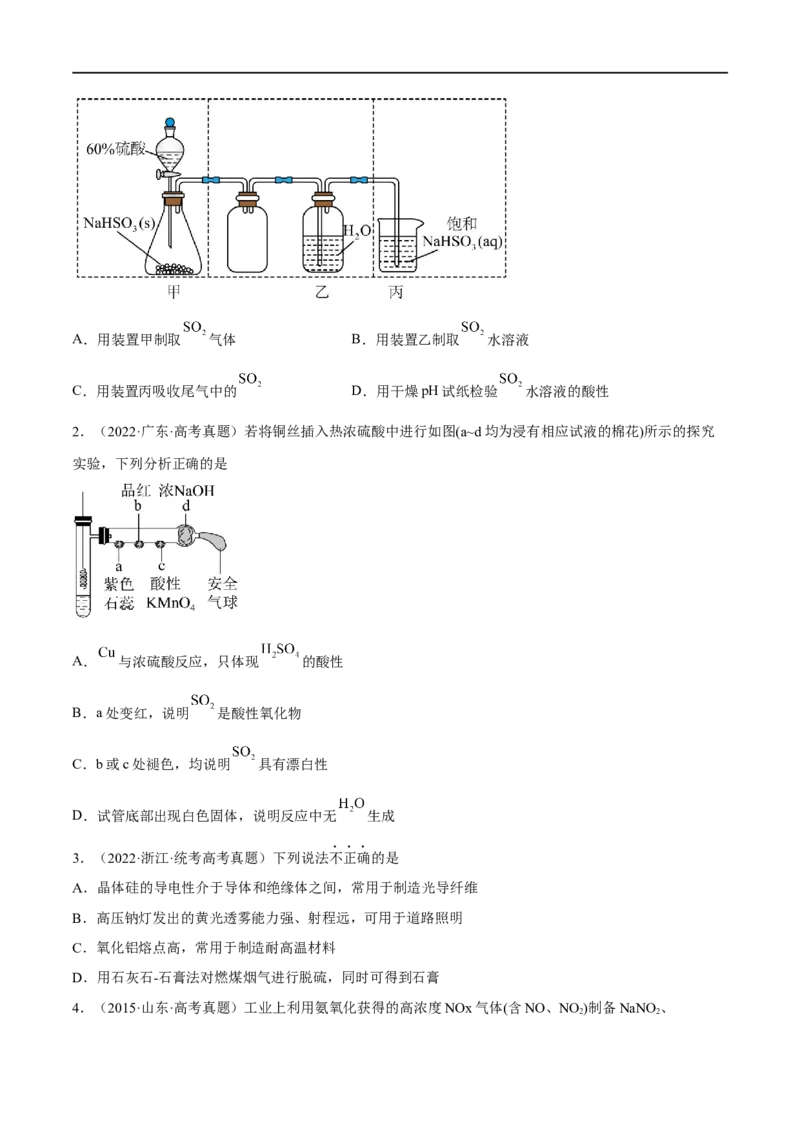
①如图是不同铈锆比例掺杂量 ,催化剂的催化性能结果。试分析脱除NO的最佳的催化剂样
品和温度是____。选择该催化剂样品的原因是____。
②CO、NO的起始物质的量均为1mol,反应在恒定温度和1L的密闭容器中进行,假设体系以反应Ⅰ和Ⅱ为主,达平衡时NO的转化率为80%, 的选择性为50%,则 ___。
(4)已知NO可直接分解: 。常温常压下,该反应的平衡常数为 ,NO是
可以分解的,但是实际上该反应是很难发生的,以碰撞理论说明原因:_______。
(5)工业上,在一定温度下,当 存在下用 催化去除NO,会发生如下主反应:
, 。下列说法不正确的是_______。
A.通入适量 有利于主反应的发生
B. 量过多会限制脱除NO的活性
C.当 通入过多会严重限制脱除NO的活性
D.气体组成中 时,发生
C 组 真题练
1.(2022·江苏·高考真题)实验室制取少量 水溶液并探究其酸性,下列实验装置和操作不能达到实验
目的的是A.用装置甲制取 气体 B.用装置乙制取 水溶液
C.用装置丙吸收尾气中的 D.用干燥pH试纸检验 水溶液的酸性
2.(2022·广东·高考真题)若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究
实验,下列分析正确的是
A. 与浓硫酸反应,只体现 的酸性
B.a处变红,说明 是酸性氧化物
C.b或c处褪色,均说明 具有漂白性
D.试管底部出现白色固体,说明反应中无 生成
3.(2022·浙江·统考高考真题)下列说法不正确的是
A.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
B.高压钠灯发出的黄光透雾能力强、射程远,可用于道路照明
C.氧化铝熔点高,常用于制造耐高温材料
D.用石灰石-石膏法对燃煤烟气进行脱硫,同时可得到石膏
4.(2015·山东·高考真题)工业上利用氨氧化获得的高浓度NOx气体(含NO、NO )制备NaNO 、
2 2NaNO ,工艺流程如下:
3
已知:NaCO+NO+NO =2NaNO +
2 3 2 2 CO2
(1)中和液所含溶质除NaNO 及少量NaCO 外,还有__________(填化学式)。
2 2 3
(2)中和液进行蒸发Ⅰ操作时,应控制水的蒸发量,避免浓度过大,目的是_______。蒸发Ⅰ产生的蒸气
中含有少量的NaNO 等有毒物质,不能直接排放,将其冷凝后用于流程中的_______(填操作名称)最合理。
2
(3)母液Ⅰ进行转化时加入稀HNO 的目的是_______。母液Ⅱ需回收利用,下列处理方法合理的是
3
________。
a.转入中和液 b.转入结晶Ⅰ操作
c.转入转化液 d.转入结晶Ⅱ操作
(4)若将NaNO 、NaNO 两种产品的物质的量之比设为2:1,则生产1.38吨NaNO 时,NaCO 的理论用
2 3 2 2 3
量为______吨(假定NaCO 恰好完全反应)。
2 3
5.(2021·浙江·统考高考真题)玻璃仪器内壁残留的硫单质可用热KOH溶液洗涤除去,发生如下反应:
3S+6KOH 2KS+KSO +3H O
2 2 3 2
(x-1)S+KS KS(x=2~6)
2 2 x
S+ K SO KSO
2 3 2 2 3
请计算:
(1)0.480 g硫单质与V mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成KS和KSO ,则V=______。
2 2 3
(2)2.560 g硫单质与60.0 mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成KS 和KSO,则x=______。
2 x 2 2 3
(写出计算过程)