文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(湖北专用)
黄金卷02
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 Li 7 Al 27
第Ⅰ卷
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.化学与科技、生活有密切的关系。下列叙述错误的是
A.航空航天工业中采用化学镀镍,电镀时镀件作阴极,镍作阳极
B.我国力争2060年前实现碳中和,用脱硫煤代替原煤作燃料有利于实现碳中和
C.“肾功能衰竭”的病人需要做“血液透析”,其原理与胶体的提纯有关
D.卡塔尔世界杯旗帜来自中国制造,其主要材质是透风性好、不易损坏的涤纶
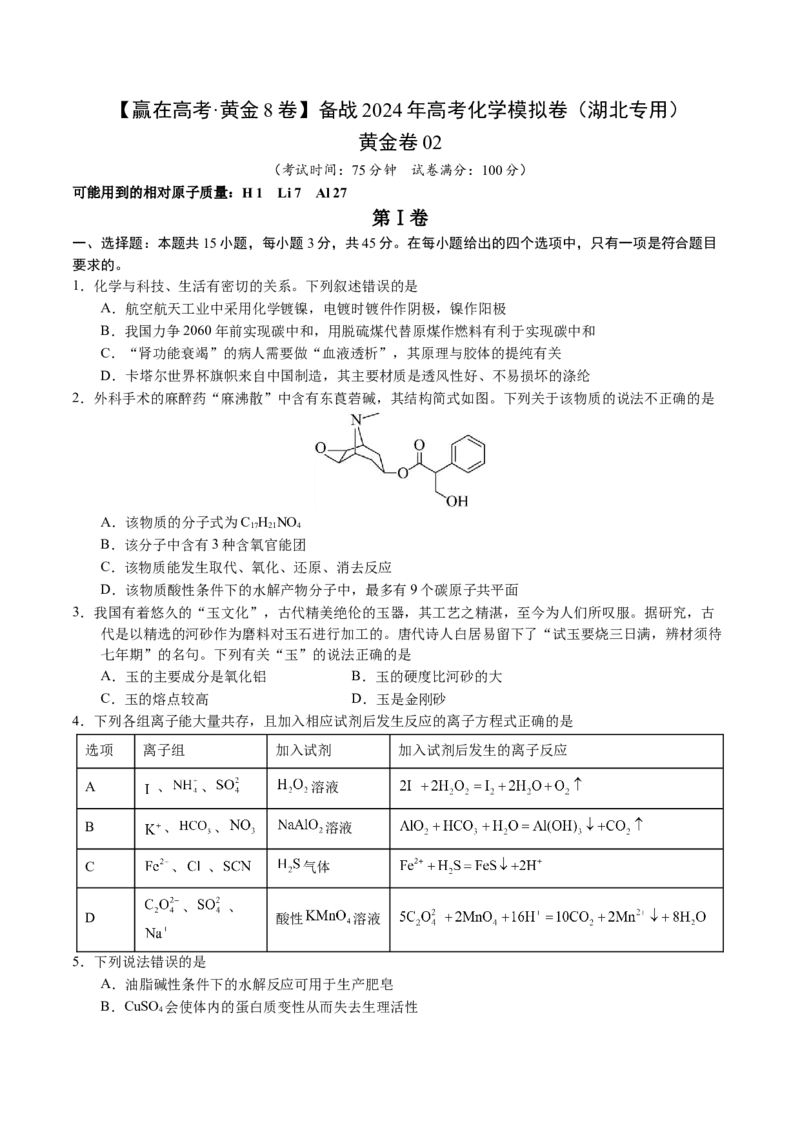
2.外科手术的麻醉药“麻沸散”中含有东莨菪碱,其结构简式如图。下列关于该物质的说法不正确的是
A.该物质的分子式为C H NO
17 21 4
B.该分子中含有3种含氧官能团
C.该物质能发生取代、氧化、还原、消去反应
D.该物质酸性条件下的水解产物分子中,最多有9个碳原子共平面
3.我国有着悠久的“玉文化”,古代精美绝伦的玉器,其工艺之精湛,至今为人们所叹服。据研究,古
代是以精选的河砂作为磨料对玉石进行加工的。唐代诗人白居易留下了“试玉要烧三日满,辨材须待
七年期”的名句。下列有关“玉”的说法正确的是
A.玉的主要成分是氧化铝 B.玉的硬度比河砂的大
C.玉的熔点较高 D.玉是金刚砂
4.下列各组离子能大量共存,且加入相应试剂后发生反应的离子方程式正确的是
选项 离子组 加入试剂 加入试剂后发生的离子反应
A 、 、 溶液
B 、 、 溶液
C 、 、 气体
、 、
D 酸性 溶液
5.下列说法错误的是
A.油脂碱性条件下的水解反应可用于生产肥皂
B.CuSO 会使体内的蛋白质变性从而失去生理活性
4C.纤维素在人体内可水解成葡萄糖,供人体组织的营养需要
D.葡萄糖能发生银镜反应
6.下列实验操作规范且能达到实验目的的是
A.用排水法收集 B.分离 C.验证酸性: D.加热
NO 胶体 制取无水
7.利用 、 和 反应制联氨( ),反应方程式为
,下列关于该反应的说法不正确的是
A. 与 的晶体类型不同
B.此反应过程中既有极性键、非极性键的断裂,也有极性键、非极性键的形成
C. 与 分子间易形成氢键,结构可表示为
D. 分子中 为吸电子基,导致N原子与 的配位能力减弱,等物质的量浓度的 和
的水溶液, 水溶液碱性较弱
8.已知反应(CH)S+I (CH)SI ,下列推测不合理的是
3 2 2 3 2 2
A.将(CH)SI 与淀粉溶液混合,溶液显蓝色
3 2 2
B.(CH)S的名称为二甲硫醚,常温下呈液态
3 2
C.(CH)SI 与水反应生成CH、HI和HSO
3 2 2 4 2 4
D.Cl 可与(CH)S反应生成(CH)SCl
2 3 2 3 2 4
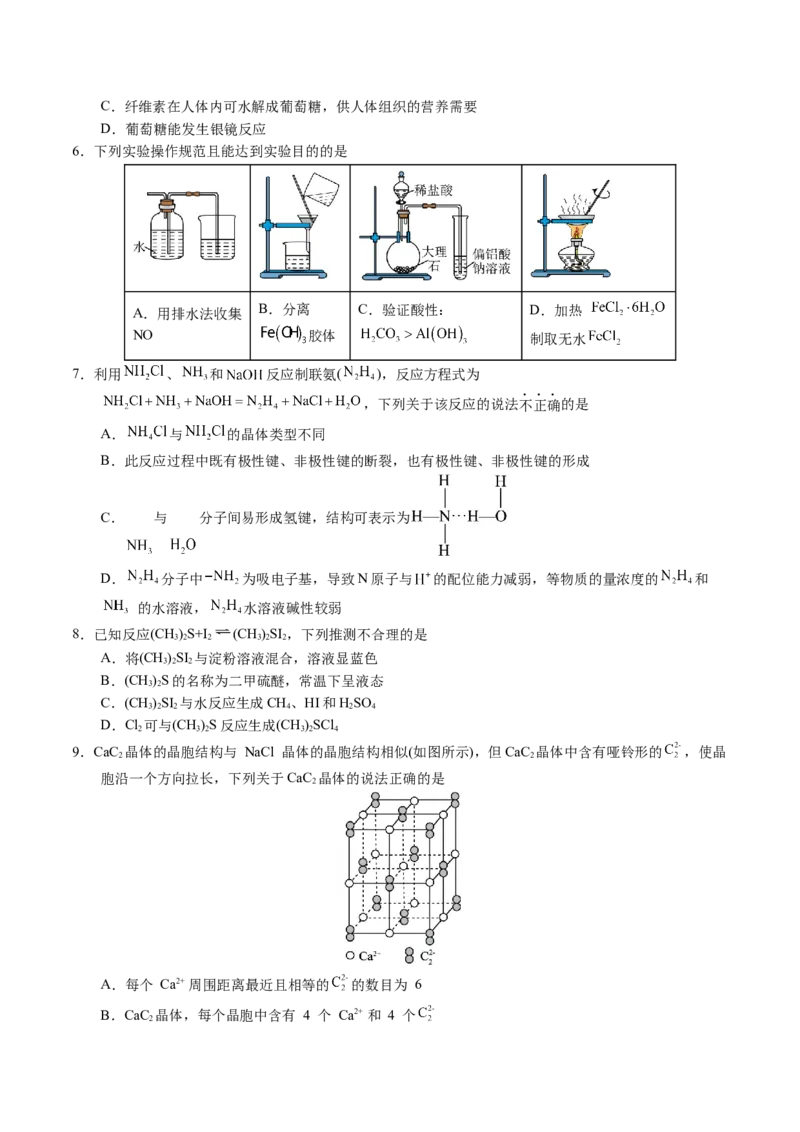
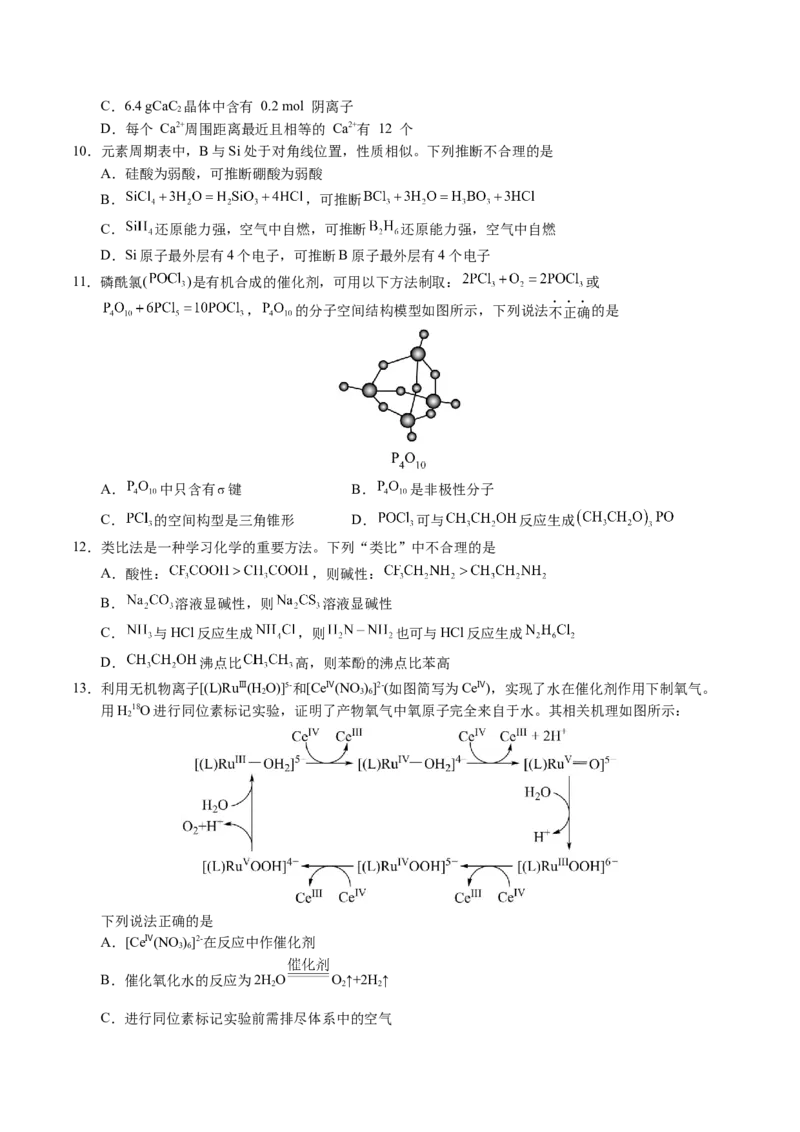
9.CaC 晶体的晶胞结构与 NaCl 晶体的晶胞结构相似(如图所示),但CaC 晶体中含有哑铃形的 ,使晶
2 2
胞沿一个方向拉长,下列关于CaC 晶体的说法正确的是
2
A.每个 Ca2+ 周围距离最近且相等的 的数目为 6
B.CaC 晶体,每个晶胞中含有 4 个 Ca2+ 和 4 个
2C.6.4 gCaC 晶体中含有 0.2 mol 阴离子
2
D.每个 Ca2+周围距离最近且相等的 Ca2+有 12 个
10.元素周期表中,B与Si处于对角线位置,性质相似。下列推断不合理的是
A.硅酸为弱酸,可推断硼酸为弱酸
B. ,可推断
C. 还原能力强,空气中自燃,可推断 还原能力强,空气中自燃
D.Si原子最外层有4个电子,可推断B原子最外层有4个电子
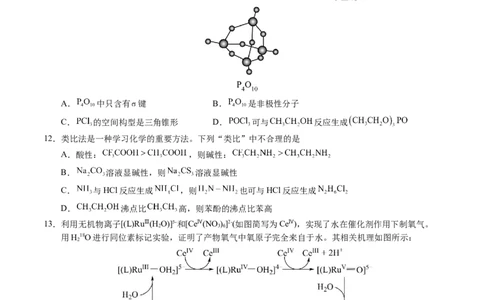
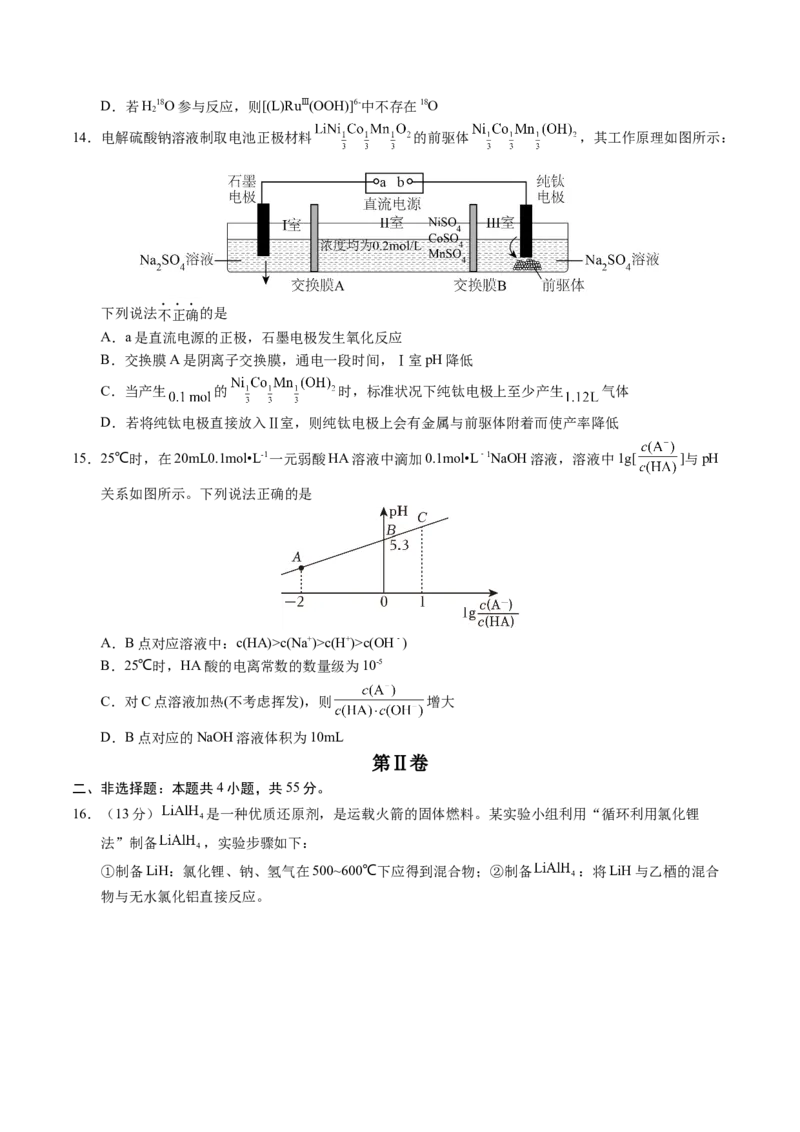
11.磷酰氯( )是有机合成的催化剂,可用以下方法制取: 或
, 的分子空间结构模型如图所示,下列说法不正确的是
A. 中只含有 键 B. 是非极性分子
C. 的空间构型是三角锥形 D. 可与 反应生成
12.类比法是一种学习化学的重要方法。下列“类比”中不合理的是
A.酸性: ,则碱性:
B. 溶液显碱性,则 溶液显碱性
C. 与HCl反应生成 ,则 也可与HCl反应生成
D. 沸点比 高,则苯酚的沸点比苯高
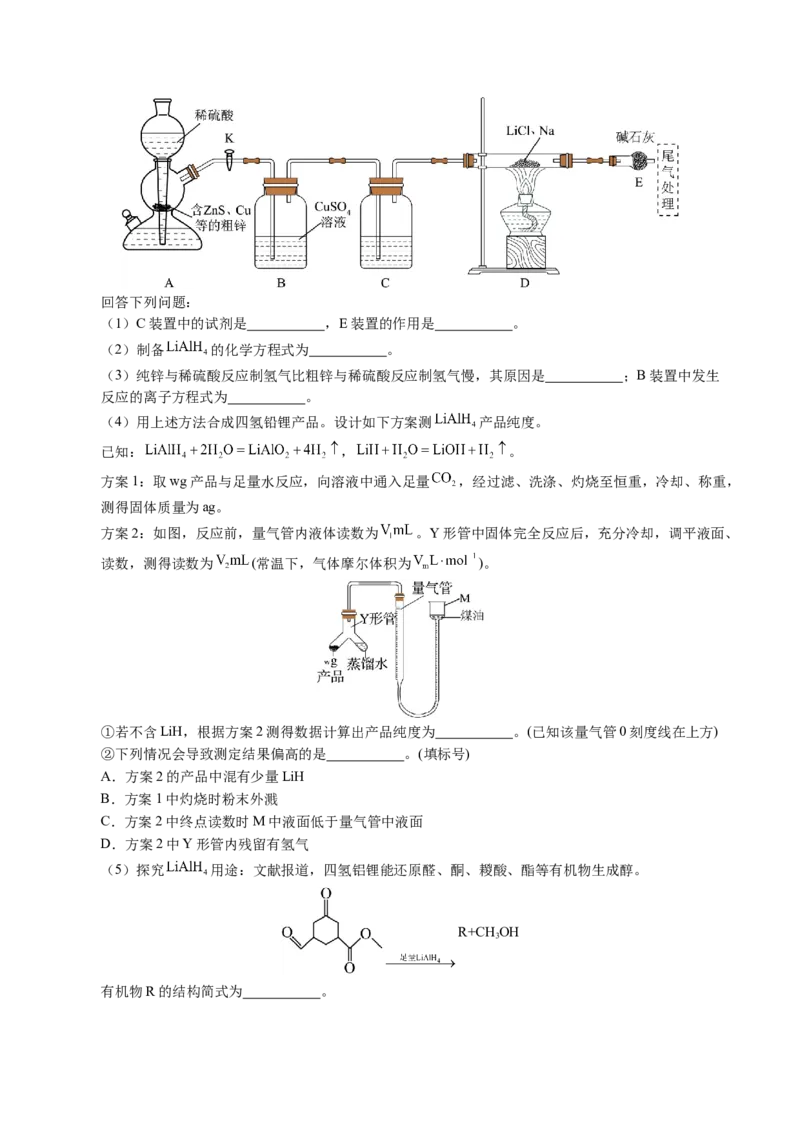
13.利用无机物离子[(L)RuⅢ(H O)]5-和[CeⅣ(NO )]2-(如图简写为CeⅣ),实现了水在催化剂作用下制氧气。
2 3 6
用H18O进行同位素标记实验,证明了产物氧气中氧原子完全来自于水。其相关机理如图所示:
2
下列说法正确的是
A.[CeⅣ(NO )]2-在反应中作催化剂
3 6
B.催化氧化水的反应为2HO O↑+2H ↑
2 2 2
C.进行同位素标记实验前需排尽体系中的空气D.若H18O参与反应,则[(L)RuⅢ(OOH)]6-中不存在18O
2
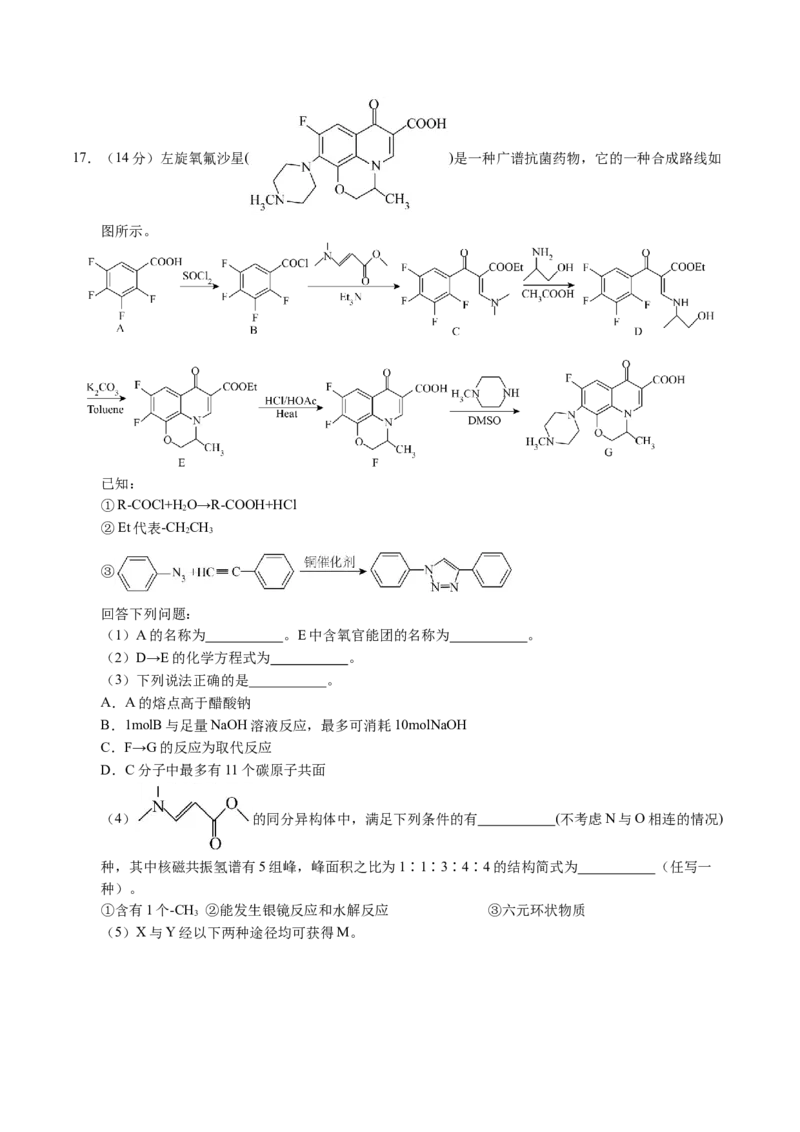
14.电解硫酸钠溶液制取电池正极材料 的前驱体 ,其工作原理如图所示:
下列说法不正确的是
A.a是直流电源的正极,石墨电极发生氧化反应
B.交换膜A是阴离子交换膜,通电一段时间,Ⅰ室pH降低
C.当产生 的 时,标准状况下纯钛电极上至少产生 气体
D.若将纯钛电极直接放入Ⅱ室,则纯钛电极上会有金属与前驱体附着而使产率降低
15.25℃时,在20mL0.1mol•L-1一元弱酸HA溶液中滴加0.1mol•L﹣1NaOH溶液,溶液中1g[ ]与pH
关系如图所示。下列说法正确的是
A.B点对应溶液中:c(HA)>c(Na+)>c(H+)>c(OH﹣)
B.25℃时,HA酸的电离常数的数量级为10-5
C.对C点溶液加热(不考虑挥发),则 增大
D.B点对应的NaOH溶液体积为10mL
第Ⅱ卷
二、非选择题:本题共4小题,共55分。
16.(13分) 是一种优质还原剂,是运载火箭的固体燃料。某实验小组利用“循环利用氯化锂
法”制备 ,实验步骤如下:
①制备LiH:氯化锂、钠、氢气在500~600℃下应得到混合物;②制备 :将LiH与乙梄的混合
物与无水氯化铝直接反应。回答下列问题:
(1)C装置中的试剂是 ,E装置的作用是 。
(2)制备 的化学方程式为 。
(3)纯锌与稀硫酸反应制氢气比粗锌与稀硫酸反应制氢气慢,其原因是 ;B装置中发生
反应的离子方程式为 。
(4)用上述方法合成四氢铅锂产品。设计如下方案测 产品纯度。
已知: , 。
方案1:取wg产品与足量水反应,向溶液中通入足量 ,经过滤、洗涤、灼烧至恒重,冷却、称重,
测得固体质量为ag。
方案2:如图,反应前,量气管内液体读数为 。Y形管中固体完全反应后,充分冷却,调平液面、
读数,测得读数为 (常温下,气体摩尔体积为 )。
①若不含LiH,根据方案2测得数据计算出产品纯度为 。(已知该量气管0刻度线在上方)
②下列情况会导致测定结果偏高的是 。(填标号)
A.方案2的产品中混有少量LiH
B.方案1中灼烧时粉末外溅
C.方案2中终点读数时M中液面低于量气管中液面
D.方案2中Y形管内残留有氢气
(5)探究 用途:文献报道,四氢铝锂能还原醛、酮、䎫酸、酯等有机物生成醇。
R+CH OH
3
有机物R的结构简式为 。17.(14分)左旋氧氟沙星( )是一种广谱抗菌药物,它的一种合成路线如
图所示。
已知:
①R-COCl+H O→R-COOH+HCl
2
②Et代表-CHCH
2 3
③
回答下列问题:
(1)A的名称为 。E中含氧官能团的名称为 。
(2)D→E的化学方程式为 。
(3)下列说法正确的是___________。
A.A的熔点高于醋酸钠
B.1molB与足量NaOH溶液反应,最多可消耗10molNaOH
C.F→G的反应为取代反应
D.C分子中最多有11个碳原子共面
(4) 的同分异构体中,满足下列条件的有 (不考虑N与O相连的情况)
种,其中核磁共振氢谱有5组峰,峰面积之比为1∶1∶3∶4∶4的结构简式为 (任写一
种)。
①含有1个-CH ②能发生银镜反应和水解反应 ③六元环状物质
3
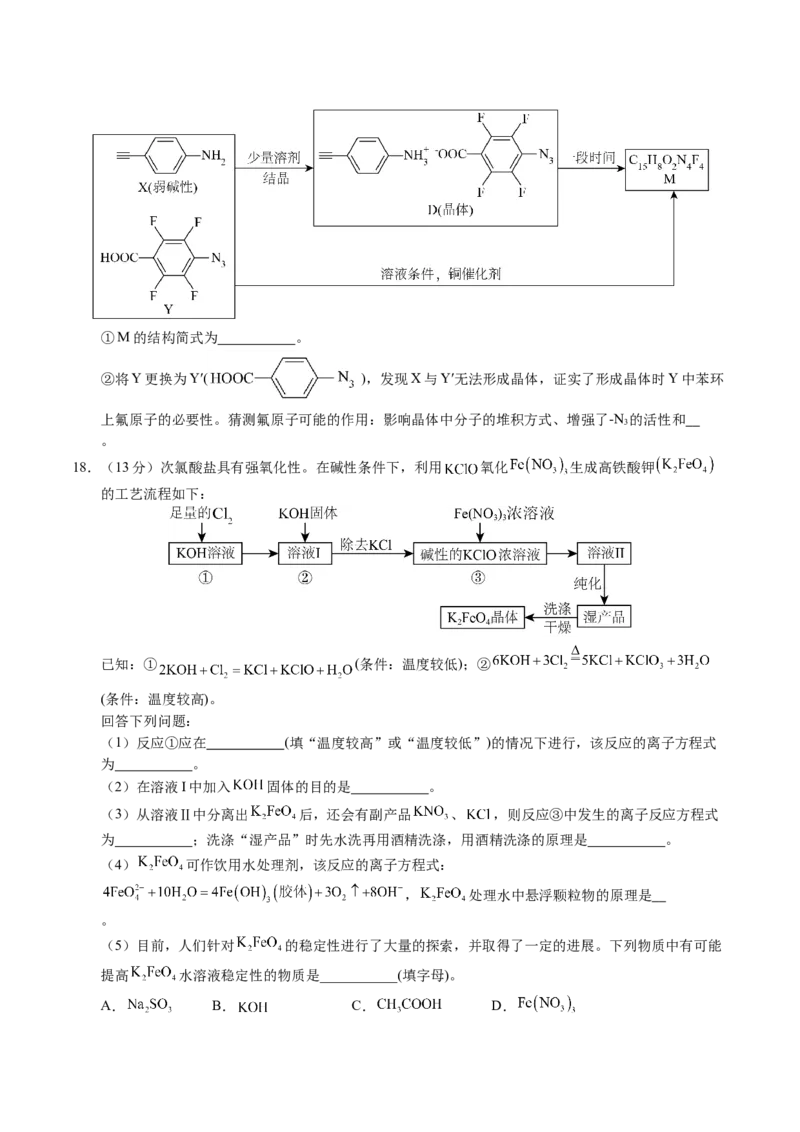
(5)X与Y经以下两种途径均可获得M。①M的结构简式为 。
②将Y更换为Y′( ),发现X与Y′无法形成晶体,证实了形成晶体时Y中苯环
上氟原子的必要性。猜测氟原子可能的作用:影响晶体中分子的堆积方式、增强了-N 的活性和
3
。
18.(13分)次氯酸盐具有强氧化性。在碱性条件下,利用 氧化 生成高铁酸钾
的工艺流程如下:
已知:① (条件:温度较低);②
(条件:温度较高)。
回答下列问题:
(1)反应①应在 (填“温度较高”或“温度较低”)的情况下进行,该反应的离子方程式
为 。
(2)在溶液I中加入 固体的目的是 。
(3)从溶液Ⅱ中分离出 后,还会有副产品 、 ,则反应③中发生的离子反应方程式
为 ;洗涤“湿产品”时先水洗再用酒精洗涤,用酒精洗涤的原理是 。
(4) 可作饮用水处理剂,该反应的离子方程式:
, 处理水中悬浮颗粒物的原理是
。
(5)目前,人们针对 的稳定性进行了大量的探索,并取得了一定的进展。下列物质中有可能
提高 水溶液稳定性的物质是___________(填字母)。
A. B. C. D.19.(15分)氮及其化合物在工农业生产中有着重要应用,减少氮的氧化物在大气中的排放是环境保护的
重要内容之一。
Ⅰ.一定条件下,用 催化还原可消除NO污染。
已知:
①
②
(1) 和 完全反应,每生成2.24L(标准状况)NO时,吸收8.9kJ的热量,则
;一定温度下,往一体积不变的密闭容
器中加入适量的 和NO,下列条件能判断该反应到达平衡状态的有 (填序号)。
A.混合气体的平均相对分子质量不变
B.
C.单位时间里有4n mol C—H断开同时有4n mol O—H断开
D.混合气体的压强不变
E.混合气体的密度不变
(2)将2mol NO(g)、1mol (g)和2mol He(g)通入反应器,在温度T、压强p条件下进行反应②和
。平衡时,若 、 与 三者的物质的量相等,则NO转化率为
,反应②平衡常数 (用含p的代数式表示)。
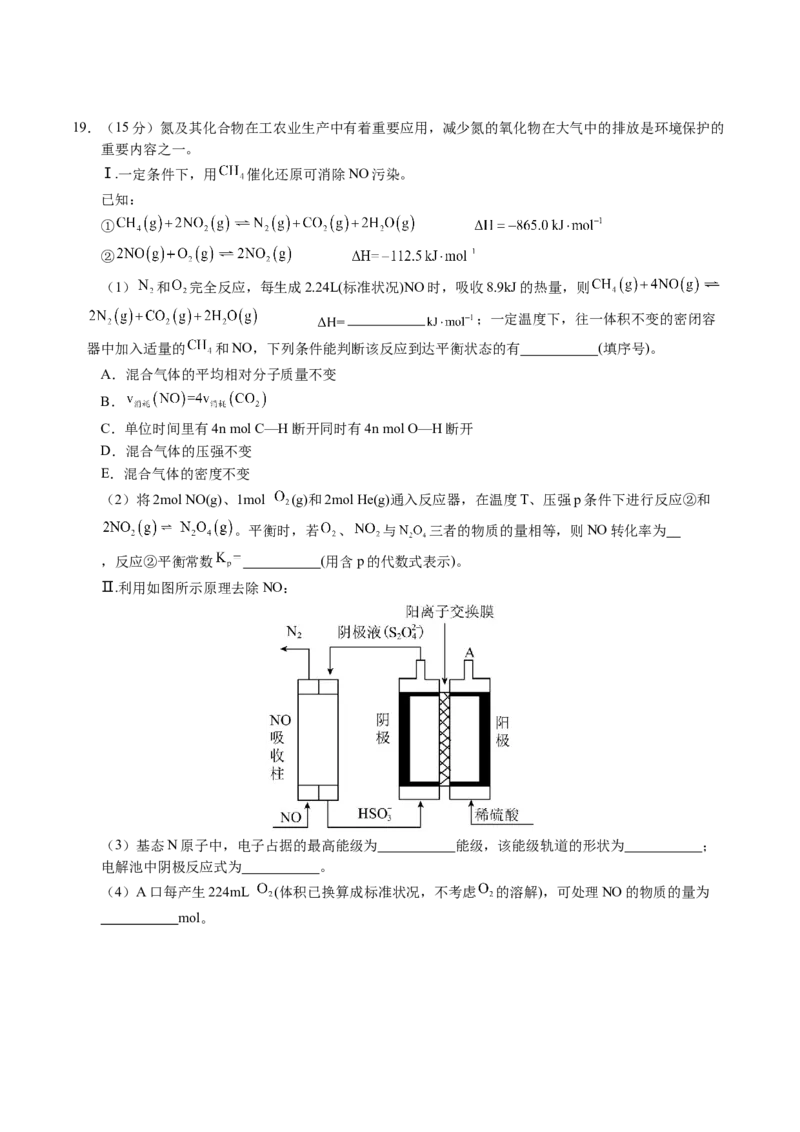
Ⅱ.利用如图所示原理去除NO:
(3)基态N原子中,电子占据的最高能级为 能级,该能级轨道的形状为 ;
电解池中阴极反应式为 。
(4)A口每产生224mL (体积已换算成标准状况,不考虑 的溶解),可处理NO的物质的量为
mol。