文档内容
2019 年普通高等学校招生全国统一考试
化学
注意事项:
1. 答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2. 回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在
本试卷上无效。
3. 考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:
一、选择题:本题共6小题,每小题2分,共12分,在每小题给出的四个选项中,只有一项
是符合题目要求的。
1. 某试剂瓶标签上安全标志如图,该试剂是
A. 氨水 B. 乙酸 C. 氢氧化钠 D. 硝酸
2. 我国古代典籍中有“石胆……浅碧色,烧之变白色者真”的记载,其中石胆是指
A. B.
C. D.
3. 反应C H(g) C H(g)+H(g) H>0,在一定条件下于密闭容器中达到平衡。下列各项措施中,不能
2 6 2 4 2
提高乙烷平衡转化率 的是 △
A. 增大容器容积 B. 升高反应温度
C. 分离出部分氢气 D. 等容下通入惰性气体
4. 下列各组化合物中不互为同分异构体的是
第1页 | 共7页A. B.
C. D.
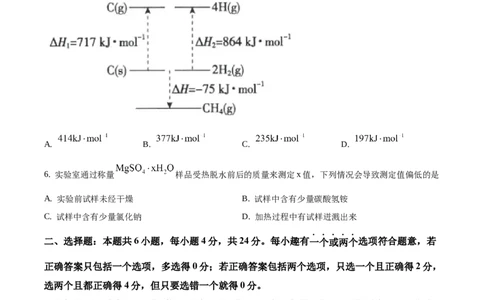
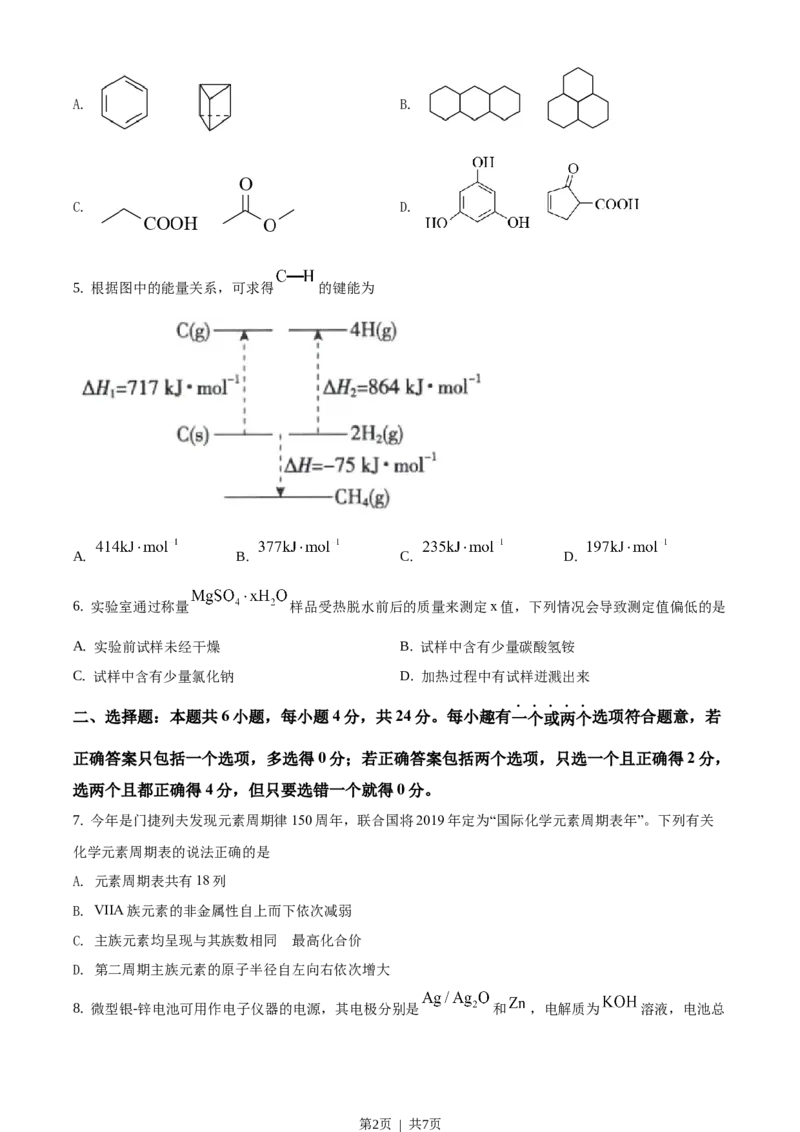
5. 根据图中的能量关系,可求得 的键能为
A. B. C. D.
6. 实验室通过称量 样品受热脱水前后的质量来测定x值,下列情况会导致测定值偏低的是
A. 实验前试样未经干燥 B. 试样中含有少量碳酸氢铵
C. 试样中含有少量氯化钠 D. 加热过程中有试样迸溅出来
二、选择题:本题共6小题,每小题4分,共24分。每小趣有一个或两个选项符合题意,若
正确答案只包括一个选项,多选得0分;若正确答案包括两个选项,只选一个且正确得2分,
选两个且都正确得4分,但只要选错一个就得0分。
7. 今年是门捷列夫发现元素周期律150周年,联合国将2019年定为“国际化学元素周期表年”。下列有关
化学元素周期表的说法正确的是
A. 元素周期表共有18列
B. VIIA族元素的非金属性自上而下依次减弱
C. 主族元素均呈现与其族数相同 的最高化合价
D. 第二周期主族元素的原子半径自左向右依次增大
8. 微型银-锌电池可用作电子仪器的电源,其电极分别是 和 ,电解质为 溶液,电池总
第2页 | 共7页反应为 ,下列说法正确的是
A. 电池工作过程中, 溶液浓度降低
B. 电池工作过程中,电解液中 向负极迁移
C. 负极发生反应
D. 正极发生反应
9. 一定温度下,AgCl(s) Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl-)的关系如图所示。下列说法正确的是
A. a、b、c三点对应的K 相等
sp
B. AgCl在c点的溶解度比b点的大
C. AgCl溶于水形成的饱和溶液中,c(Ag+)=c(Cl-)
D. b点的溶液中加入AgNO 固体,c(Ag+)沿曲线向c点方向变化
3
10. 下列说法正确的是
A. 和 都属于两性氧化物 B. 悬浊液和乳浊液的分散质均为液态
C. 和 中的金属都呈现两种价态 D. 葡萄糖溶液和淀粉溶液都具有丁达尔效应
11. 能正确表示下列反应的离子方程式为
A. 向FeBr 溶液中通入过量Cl:2Fe2++Cl=2Fe3++2Cl-
2 2 2
.
B 向碳酸钠溶液中通入少量CO:CO2-+CO +H O=2HCO -
2 3 2 2 3
C. 向碘化钾溶液中加入少量双氧水:3HO+I-=IO -+3H O
2 2 3 2
D. 向硫化钠溶液中通入过量SO :2S2-+5SO+2H O=3S↓+4HSO -
2 2 2 3
12. 下列化合物中,既能发生取代反应又能发生加成反应的有
A. CH -CH=CH B. CHCHCHOH
3 2 3 2 2
第3页 | 共7页C. D.
三、非选择题:共4分。每个试题考生都必须作答。
13. 自门捷列夫发现元素周期律以来,人类对自然的认识程度逐步加深,元素周期表中的成员数目不断增
加。回答下列问题:
(1)2016年 确认了四种新元素,其中一种为 ,中文名为“ ”。元素 可由反应: +
= +3 得到。该元素的质子数为______, 与 互为_________。
的
(2) 位于元素周期表中第 族,同族元素N 一种氢化物为NH NH ,写出该化合物分子的电子式
2 2
________________.该分子内存在的共价键类型有_______。
(3)该族中的另一元素P能呈现多种化合价,其中 价氧化物的分子式为______, 价简单含氧酸的分子
式为______。
14. 由 羟基丁酸生成 丁内酯的反应如下:HOCH CHCHCOOH +H O
2 2 2 2
在298K下, 羟基丁酸水溶液的初始浓度为 ,测得 丁内酯的浓度随时间变化的数据
如表所示。回答下列问题:
21 50 80 100 120 160 220
0.024 0.050 0.071 0.081 0.090 0.104 0.116 0.132
(1)该反应在50~80min内的平均反应速率为_____ 。
(2)120min时 羟基丁酸的转化率为______。
(3)298K时该反应的平衡常数 _____。
(4)为提高 羟基丁酸的平衡转化率,除适当控制反应温度外,还可采取的措施是______。
15. 无机酸有机酯在生产中具有广泛的应用,回答下列问题:
(1)硫酸氢乙酯( )可看作是硫酸与乙醇形成的单酯,工业上常通乙烯与浓硫酸反应制得,该反
应的化学方程式为_________,反应类型为__________,写出硫酸与乙醇形成的双酯—硫酸二乙酯(
第4页 | 共7页)的结构简式_____。
(2)磷酸三丁酯常作为稀土元素富集时的萃取剂,工业上常用正丁醇与三氯氧磷( )反应来制备,该反
应的化学方程式为__________,反应类型为________。写出正丁醇的任意一个醇类同分异构体的结构简式
___________。
16. 连二亚硫酸钠 ,俗称保险粉,易溶于水,常用于印染、纸张漂白等。回答下列问题:
(1) 中S的化合价为______。
(2)向锌粉的悬浮液中通入 ,制备 ,生成 ,反应中转移的电子数为____mol;向
溶液中加入适量 ,生成 并有沉淀产生,该反应的化学方程式为_________
(3) 电池具有高输出功率的优点。其正极为可吸附 的多孔碳电极,负极为金属锂,电解液为溶
解有 的碳酸丙烯酯-乙腈溶液。电池放电时,正极上发生的电极反应为 ,电池总
反应式为____________。该电池不可用水替代混合有机溶剂,其原因是_______________。
17. 干燥的二氧化碳和氨气反应可生成氨基甲酸铵固体,化学方程式为:
,在四氯化碳中通入二氧化碳和氨制备氨基甲酸铵的
实验装置如下图所示,回答下列问题:
(1)装置1用来制备二氧化碳气体:将块状石灰石放置在试管中的带孔塑料板上,漏斗中所加试剂为____;
装置2中所加试剂为____;
(2)装置4中试剂为固体NH Cl和Ca(OH) ,发生反应的化学方程式为________;试管口不能向上倾斜的原
4 2
因是__________。装置3中试剂为KOH,其作用为______________。
(3)反应时三颈瓶需用冷水浴冷却,其目的是_______________________。
四、选考题:共20分,请考生从第18、19题中任选一题作答。如果多做,则按所做的第一
第5页 | 共7页题计分。第18、19题的第Ⅰ题为选择题,在给出的四个选项中,有两个选项是符合题目要求
的,请将符合题目要求的选项标号填在答题卡相应位置:第Ⅱ题为非选择题,请在答题卡相
应位置作答并写明小题号。
18. 18-Ⅰ分子中只有两种不同化学环境的氢,且数目比为3:2的化合物( )
A. B. C. D.
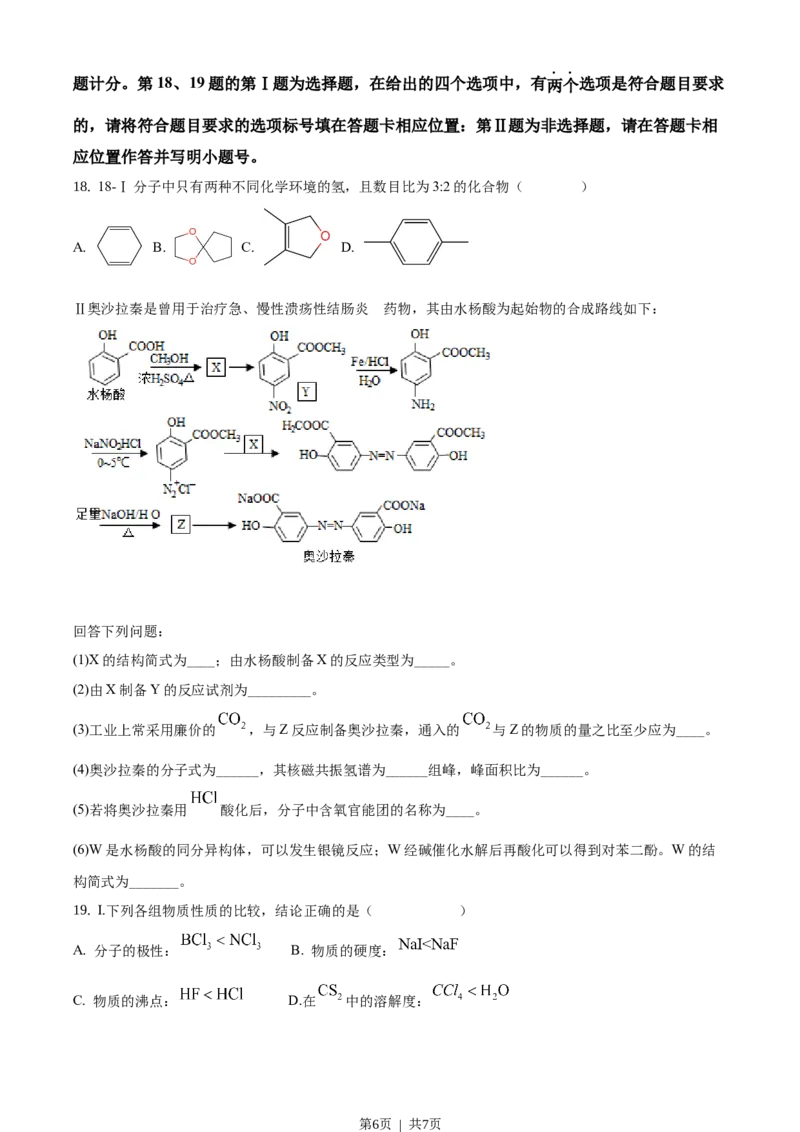
Ⅱ奥沙拉秦是曾用于治疗急、慢性溃疡性结肠炎 的药物,其由水杨酸为起始物的合成路线如下:
回答下列问题:
(1)X的结构简式为____;由水杨酸制备X的反应类型为_____。
(2)由X制备Y的反应试剂为_________。
(3)工业上常采用廉价的 ,与Z反应制备奥沙拉秦,通入的 与Z的物质的量之比至少应为____。
(4)奥沙拉秦的分子式为______,其核磁共振氢谱为______组峰,峰面积比为______。
(5)若将奥沙拉秦用 酸化后,分子中含氧官能团的名称为____。
(6)W是水杨酸的同分异构体,可以发生银镜反应;W经碱催化水解后再酸化可以得到对苯二酚。W的结
构简式为_______。
19. Ⅰ.下列各组物质性质的比较,结论正确的是( )
A. 分子的极性: B. 物质的硬度:
C. 物质的沸点: D.在 中的溶解度:
第6页 | 共7页Ⅱ.锰单质及其化合物应用十分广泛。回答下列问题:
(1) 位于元素周期表中第四周期____族,基态 原子核外未成对电子有_____个。
(2) 可与 反应生成 ,新生成的化学键为_____键。 分子的空间构型为
______,其中N原子的杂化轨道类型为_______。
(3)金属锰有多种晶型,其中 的结构为体心立方堆积,晶胞参数为a pm, 中锰的原子半径为
_____pm。已知阿伏加德罗常数的值为 , 的理论密度 ____ 。(列出计算式)
(4)已知锰的某种氧化物的晶胞如图所示,其中锰离子的化合价为____,其配位数为____。
第7页 | 共7页