文档内容
2012年贵州省毕节地区中考化学试卷
一、选择题(本题包括16小题,每小题3分,共48分.每题只有一个选项符合题意,请把该项
的序号按要求在答题卡上相应的位置填涂.)
1.(3分)今年四月,全省旅发大会在润天湖地,花海鹤乡的毕节试验区隆重召开,在开幕式
上的精彩表演中,发生化学变化的是( )
A.气球升空 B.歌舞表演 C.焰火表演 D.放飞白鸽
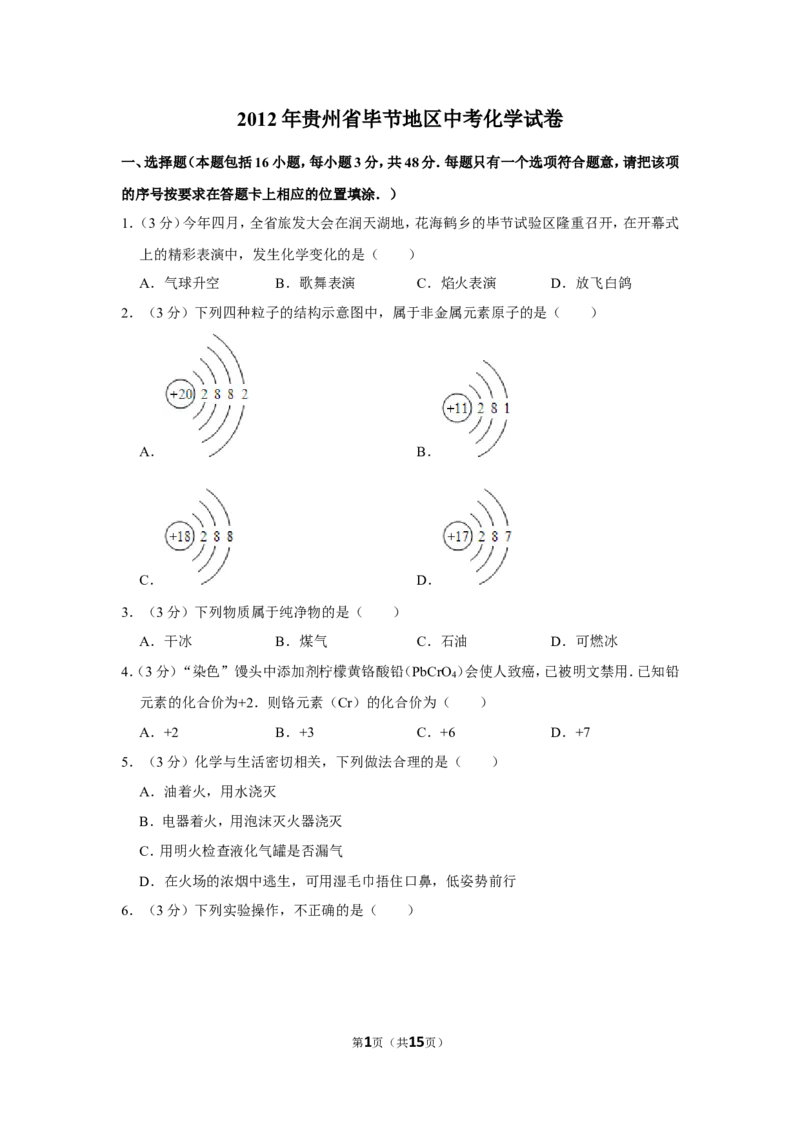
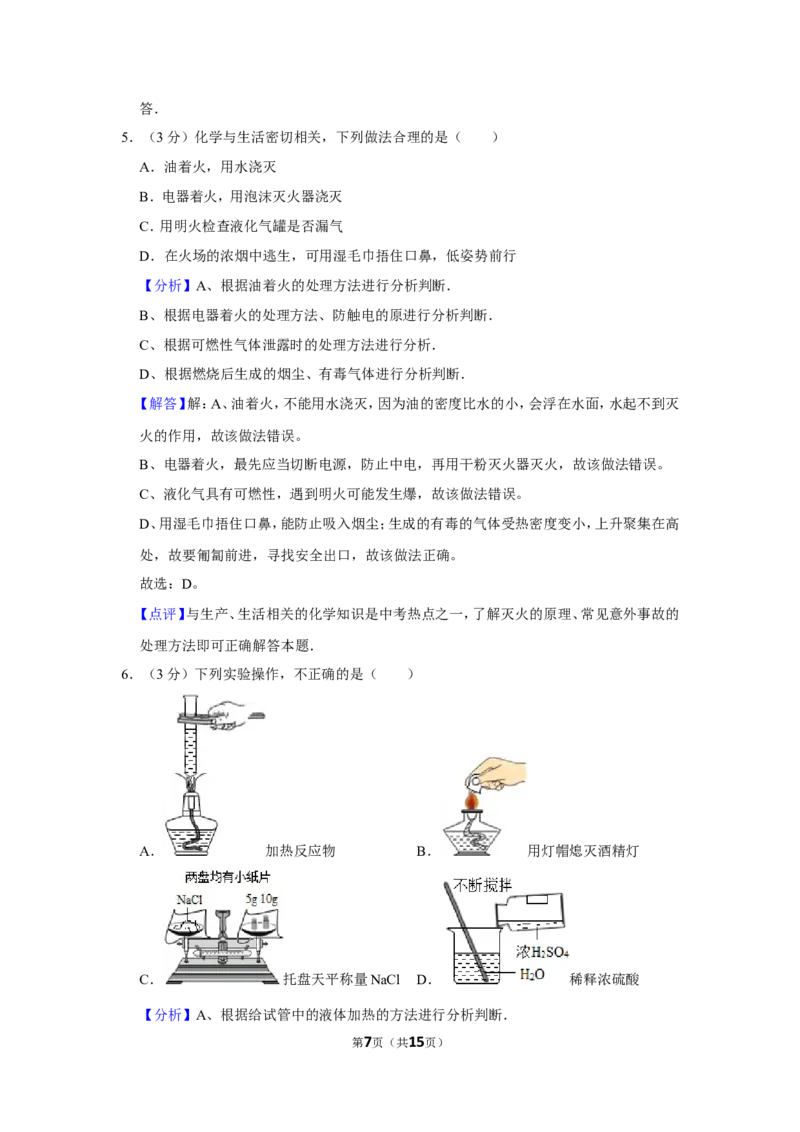
2.(3分)下列四种粒子的结构示意图中,属于非金属元素原子的是( )
A. B.
C. D.
3.(3分)下列物质属于纯净物的是( )
A.干冰 B.煤气 C.石油 D.可燃冰
4.(3分)“染色”馒头中添加剂柠檬黄铬酸铅(PbCrO )会使人致癌,已被明文禁用.已知铅
4
元素的化合价为+2.则铬元素(Cr)的化合价为( )
A.+2 B.+3 C.+6 D.+7
5.(3分)化学与生活密切相关,下列做法合理的是( )
A.油着火,用水浇灭
B.电器着火,用泡沫灭火器浇灭
C.用明火检查液化气罐是否漏气
D.在火场的浓烟中逃生,可用湿毛巾捂住口鼻,低姿势前行
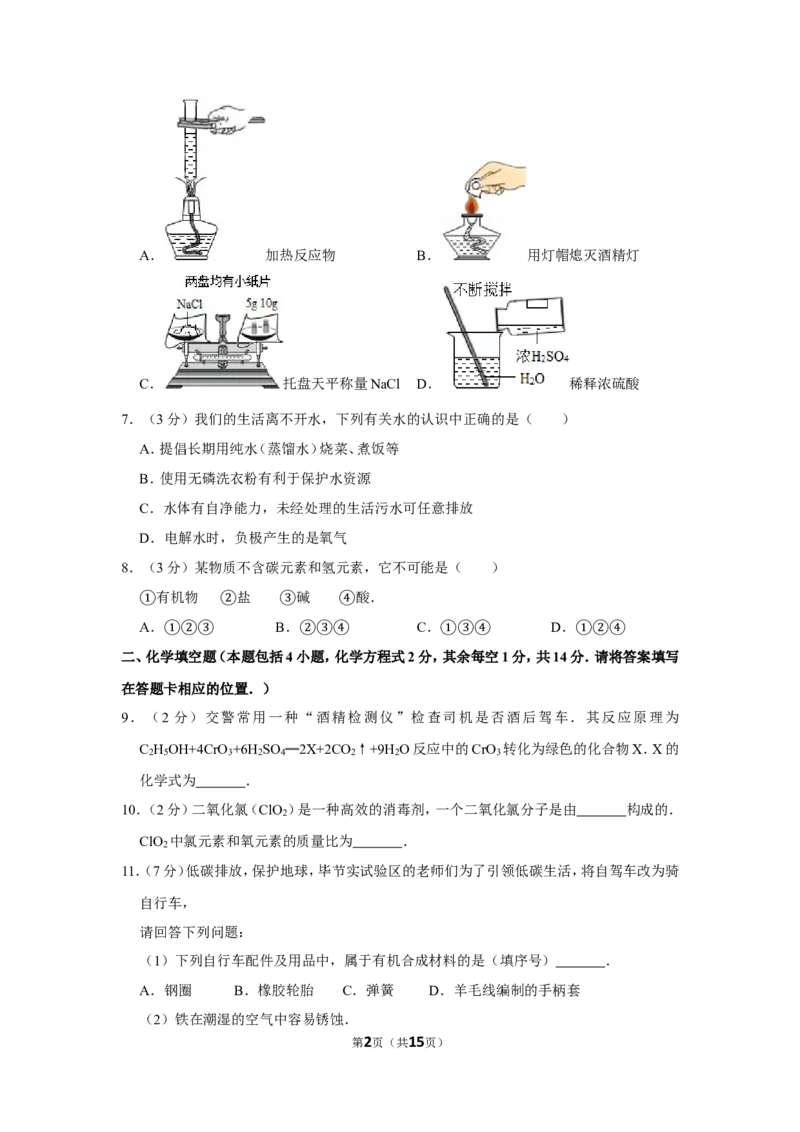
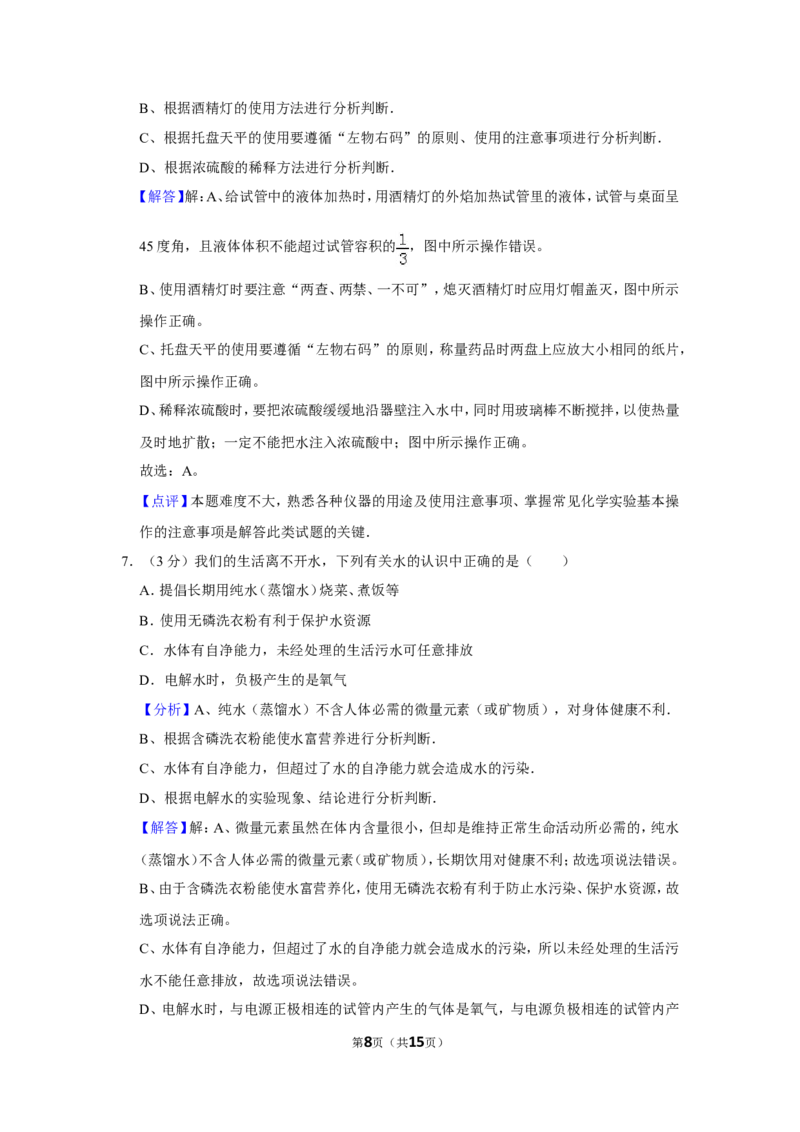
6.(3分)下列实验操作,不正确的是( )
第1页(共15页)A. 加热反应物 B. 用灯帽熄灭酒精灯
C. 托盘天平称量NaCl D. 稀释浓硫酸
7.(3分)我们的生活离不开水,下列有关水的认识中正确的是( )
A.提倡长期用纯水(蒸馏水)烧菜、煮饭等
B.使用无磷洗衣粉有利于保护水资源
C.水体有自净能力,未经处理的生活污水可任意排放
D.电解水时,负极产生的是氧气
8.(3分)某物质不含碳元素和氢元素,它不可能是( )
有机物 盐 碱 酸.
①A. ② B③. ④ C. D.
二、化学①填②空③题(本题包括4小②题③,④化学方程式2分,①其余③每④空1分,共14分①.②请将④答案填写
在答题卡相应的位置.)
9.(2 分)交警常用一种“酒精检测仪”检查司机是否酒后驾车.其反应原理为
C H OH+4CrO +6H SO ═2X+2CO ↑+9H O反应中的CrO 转化为绿色的化合物X.X的
2 5 3 2 4 2 2 3
化学式为 .
10.(2分)二氧化氯(ClO )是一种高效的消毒剂,一个二氧化氯分子是由 构成的.
2
ClO 中氯元素和氧元素的质量比为 .
2
11.(7分)低碳排放,保护地球,毕节实试验区的老师们为了引领低碳生活,将自驾车改为骑
自行车,
请回答下列问题:
(1)下列自行车配件及用品中,属于有机合成材料的是(填序号) .
A.钢圈 B.橡胶轮胎 C.弹簧 D.羊毛线编制的手柄套
(2)铁在潮湿的空气中容易锈蚀.
第2页(共15页)自行车的铁架表面喷漆,可以延缓自行车的绣蚀,其防绣原理是隔绝水和 .
①喷漆前需将铁制品放入稀盐酸中除锈(绣的主要成分是Fe
2
O
3
)观察到溶液变黄,有气
②泡溢出,反应的化学方程式是 , ,反应类型分别是 和 .
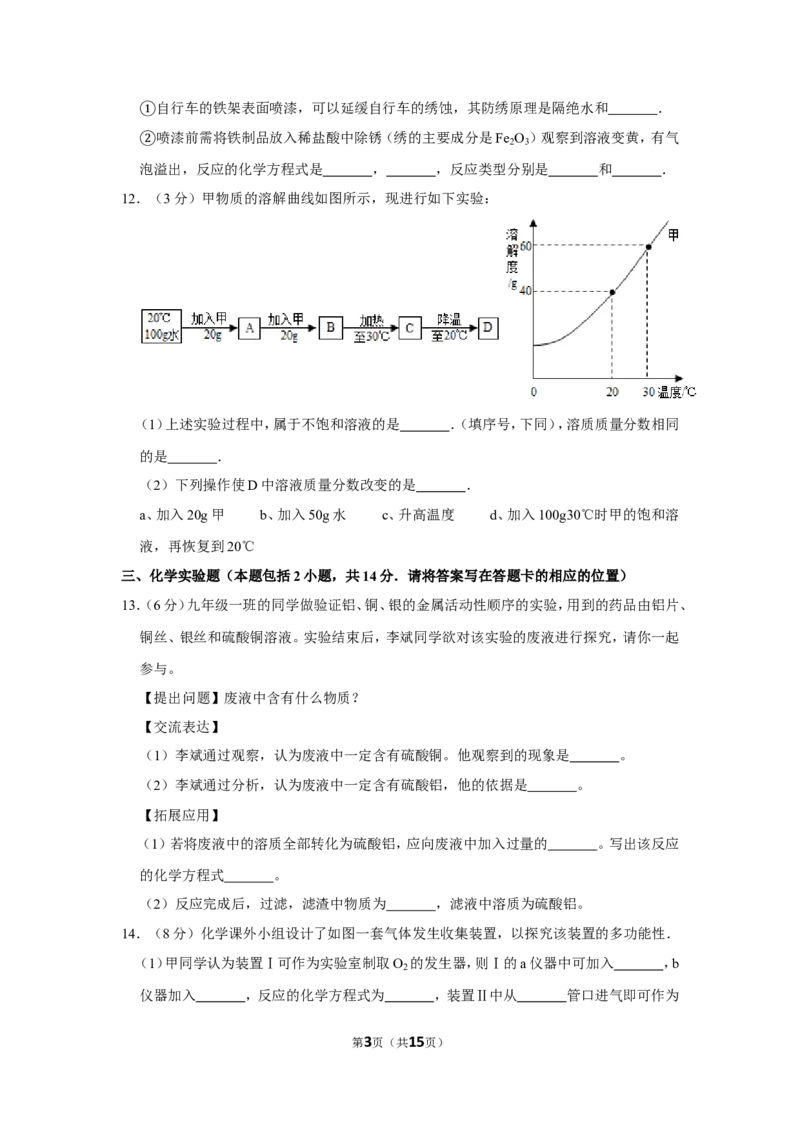
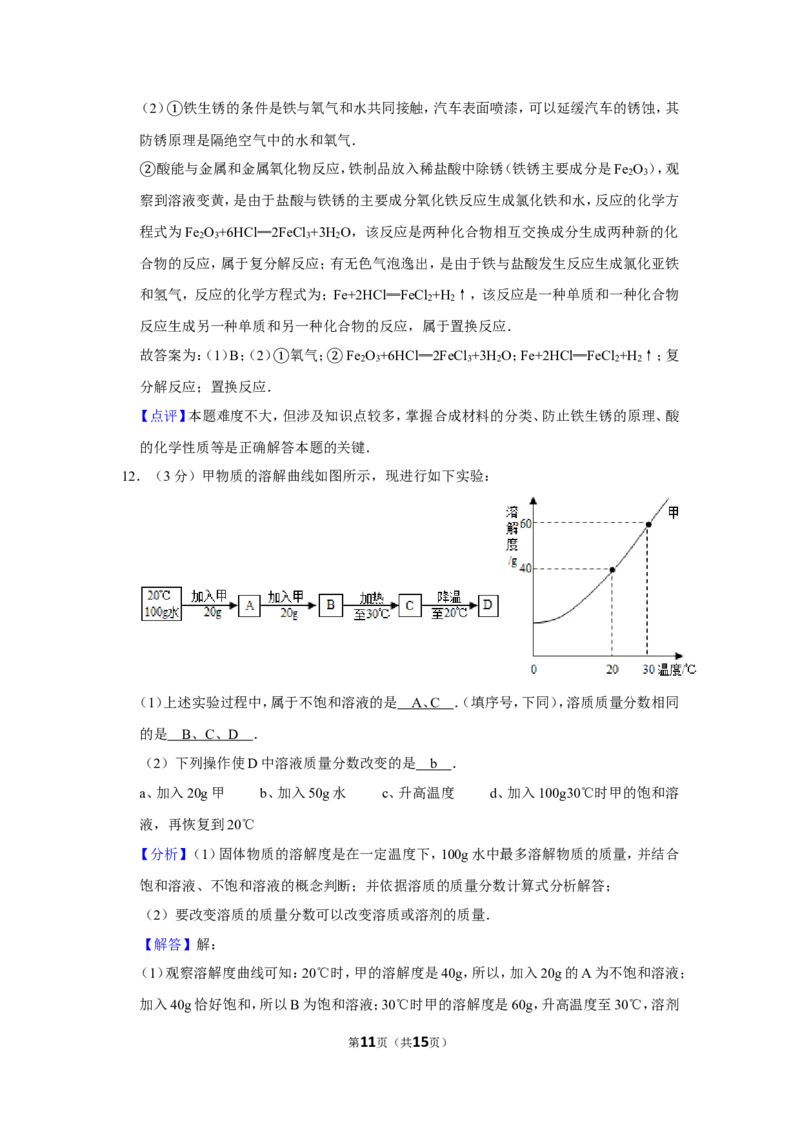
12.(3分)甲物质的溶解曲线如图所示,现进行如下实验:
(1)上述实验过程中,属于不饱和溶液的是 .(填序号,下同),溶质质量分数相同
的是 .
(2)下列操作使D中溶液质量分数改变的是 .
a、加入20g甲 b、加入50g水 c、升高温度 d、加入100g30℃时甲的饱和溶
液,再恢复到20℃
三、化学实验题(本题包括2小题,共14分.请将答案写在答题卡的相应的位置)
13.(6分)九年级一班的同学做验证铝、铜、银的金属活动性顺序的实验,用到的药品由铝片、
铜丝、银丝和硫酸铜溶液。实验结束后,李斌同学欲对该实验的废液进行探究,请你一起
参与。
【提出问题】废液中含有什么物质?
【交流表达】
(1)李斌通过观察,认为废液中一定含有硫酸铜。他观察到的现象是 。
(2)李斌通过分析,认为废液中一定含有硫酸铝,他的依据是 。
【拓展应用】
(1)若将废液中的溶质全部转化为硫酸铝,应向废液中加入过量的 。写出该反应
的化学方程式 。
(2)反应完成后,过滤,滤渣中物质为 ,滤液中溶质为硫酸铝。
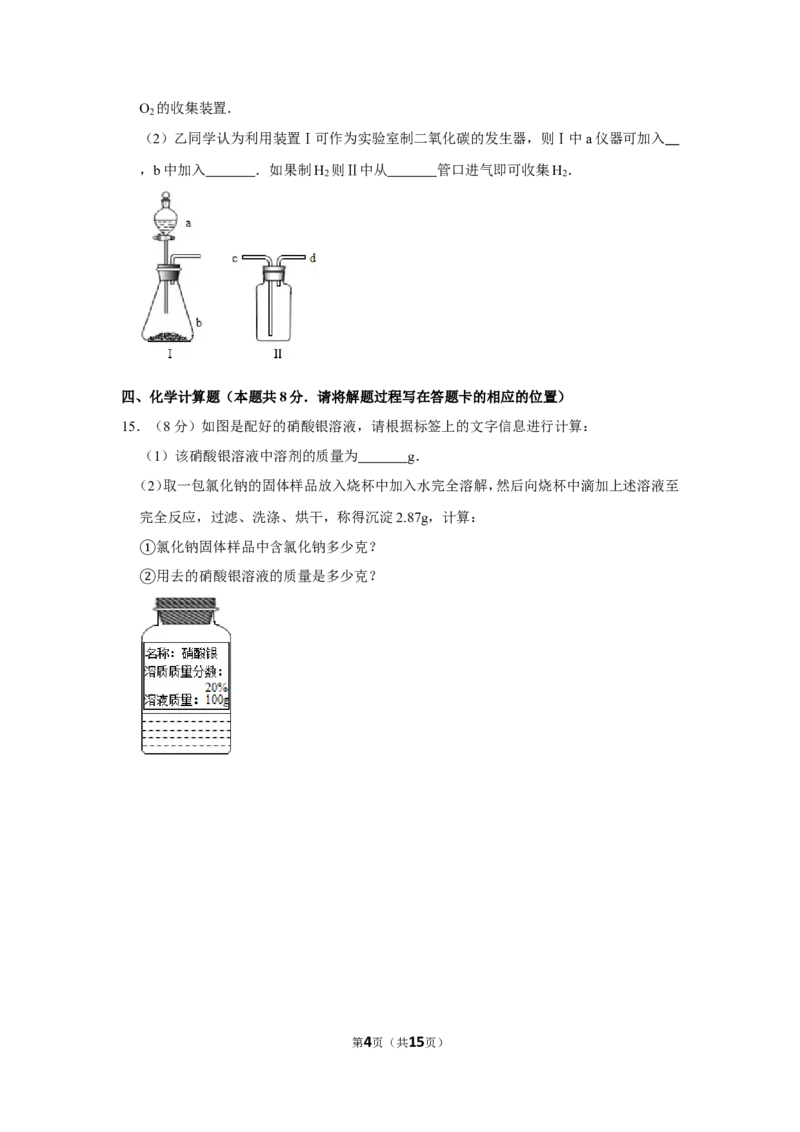
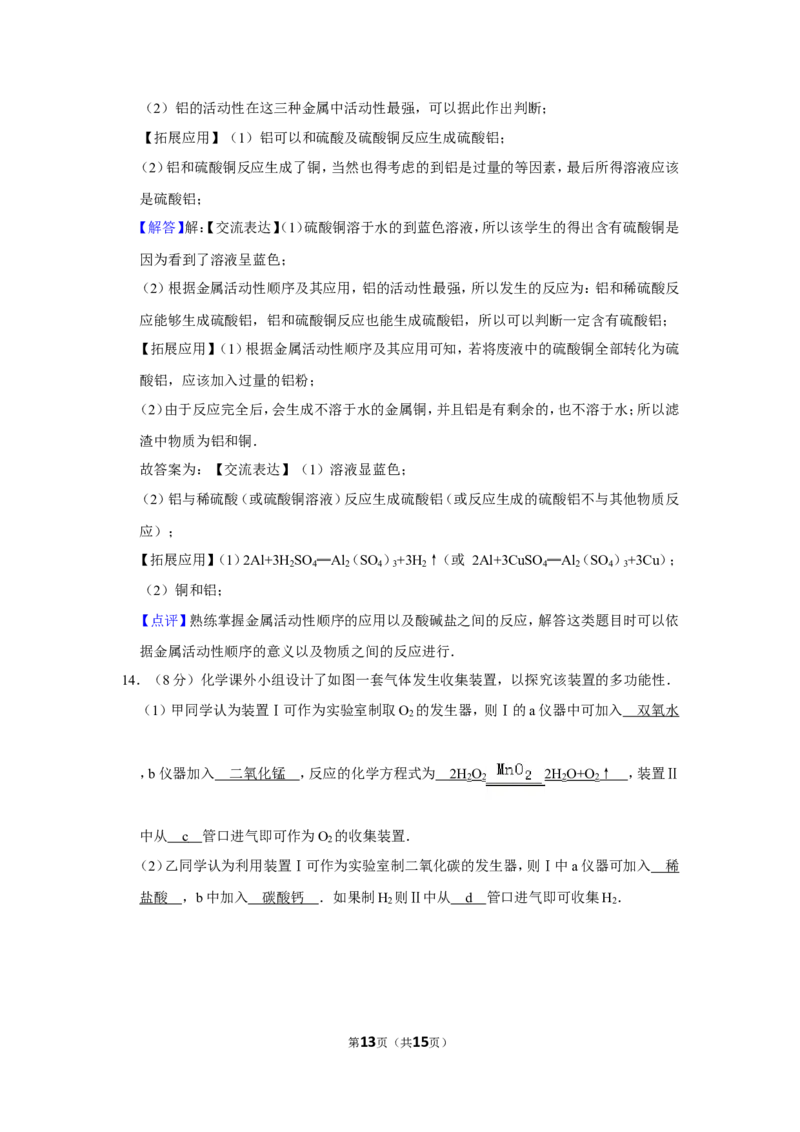
14.(8分)化学课外小组设计了如图一套气体发生收集装置,以探究该装置的多功能性.
(1)甲同学认为装置Ⅰ可作为实验室制取O 的发生器,则Ⅰ的a仪器中可加入 ,b
2
仪器加入 ,反应的化学方程式为 ,装置Ⅱ中从 管口进气即可作为
第3页(共15页)O 的收集装置.
2
(2)乙同学认为利用装置Ⅰ可作为实验室制二氧化碳的发生器,则Ⅰ中a仪器可加入
,b中加入 .如果制H 则Ⅱ中从 管口进气即可收集H .
2 2
四、化学计算题(本题共8分.请将解题过程写在答题卡的相应的位置)
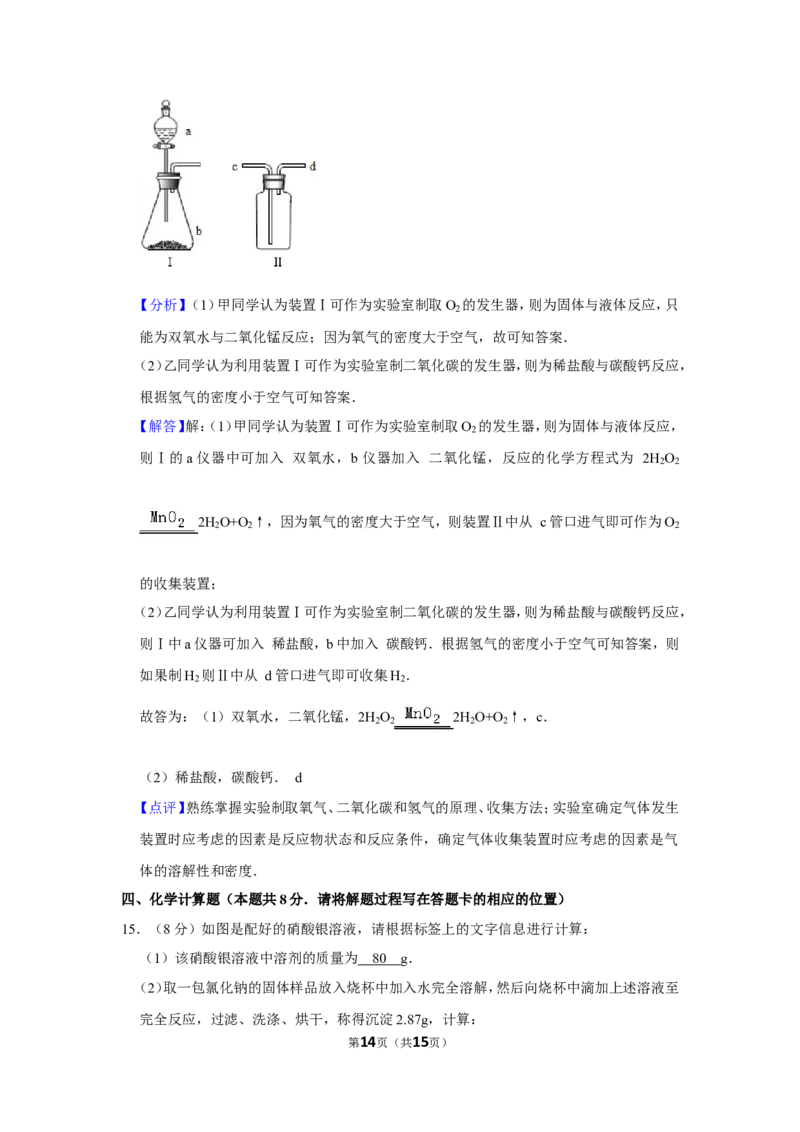
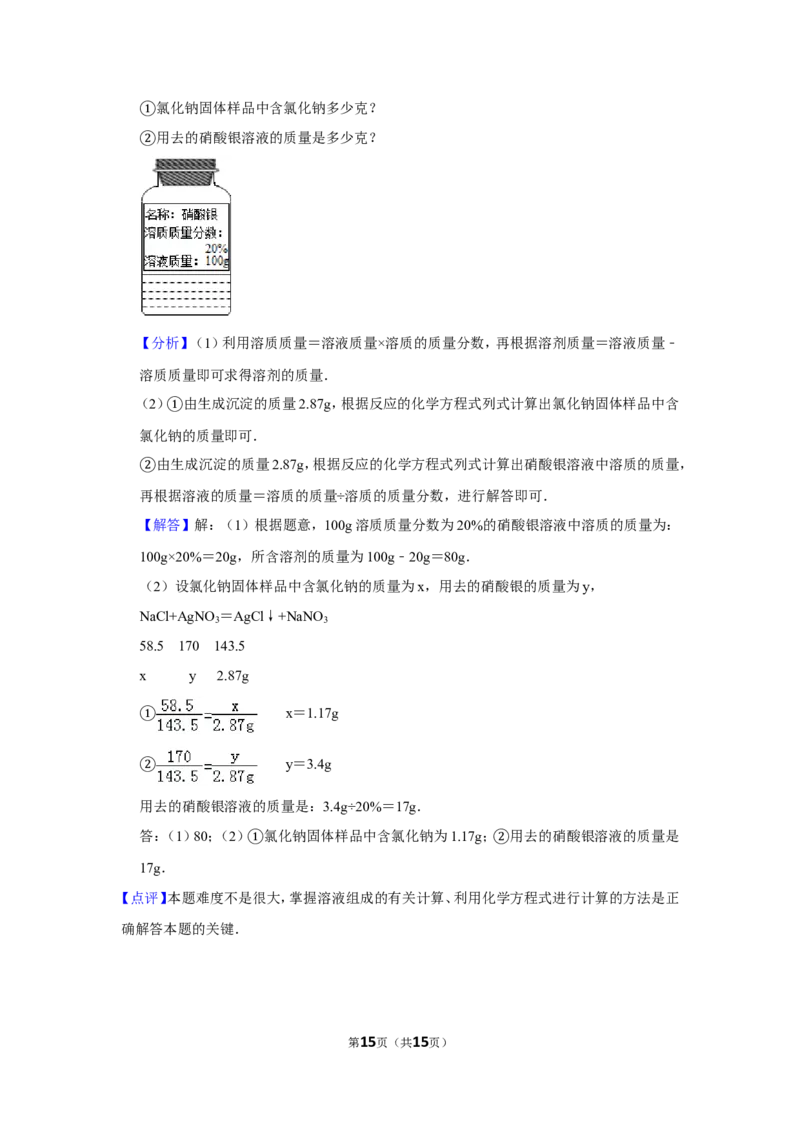
15.(8分)如图是配好的硝酸银溶液,请根据标签上的文字信息进行计算:
(1)该硝酸银溶液中溶剂的质量为 g.
(2)取一包氯化钠的固体样品放入烧杯中加入水完全溶解,然后向烧杯中滴加上述溶液至
完全反应,过滤、洗涤、烘干,称得沉淀2.87g,计算:
氯化钠固体样品中含氯化钠多少克?
①用去的硝酸银溶液的质量是多少克?
②
第4页(共15页)2012 年贵州省毕节地区中考化学试卷
参考答案与试题解析
一、选择题(本题包括16小题,每小题3分,共48分.每题只有一个选项符合题意,请把该项
的序号按要求在答题卡上相应的位置填涂.)
1.(3分)今年四月,全省旅发大会在润天湖地,花海鹤乡的毕节试验区隆重召开,在开幕式
上的精彩表演中,发生化学变化的是( )
A.气球升空 B.歌舞表演 C.焰火表演 D.放飞白鸽
【分析】化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学
变化与物理变化的本质区别是有无新物质生成,据此抓住化学变化和物理变化的区别结
合事实进行分析判断即可.
【解答】解:A、气球升空的过程中没有新物质生成,属于物理变化。
B、歌舞表演的过程中没有新物质生成,属于物理变化。
C、焰火表演的过程中发生了烟花的燃烧,有新物质二氧化碳等生成,属于化学变化。
D、放飞白鸽的过程中没有新物质生成,属于物理变化。
故选:C。
【点评】本题难度不大,解答时要分析变化过程中是否有新物质生成,这里的新物质是指
和变化前的物质是不同种的物质,若没有新物质生成属于物理变化,若有新物质生成属于
化学变化.
2.(3分)下列四种粒子的结构示意图中,属于非金属元素原子的是( )
A. B.
C. D.
【分析】原子结构示意图中,弧线上的数字表示该层上的电子数,离圆圈最远的弧线表示
第5页(共15页)最外层.若最外层电子数≥4,则一般为非金属元素,在化学反应中易得电子;若最外层电
子数<4,则一般为金属元素,在化学反应中易失去电子;若最外层电子数为8,则为稀有
气体元素的原子.
【解答】解:四种粒子质子数均等于核外电子数,均为原子。
A、最外层电子数为2,小于4,为金属元素,故选项错误。
B、最外层电子数是1,小于4,为金属元素,故选项错误。
C、最外层电子数是8,为稳定结构,是稀有气体元素,故选项错误。
D、最外层电子数是7,大于4,为非金属元素,故选项正确。
故选:D。
【点评】本题难度不大,考查学生对原子结构示意图及其意义的理解,明确原子结构示意
图中最外层电子数与元素种类的关系是解题的关键.
3.(3分)下列物质属于纯净物的是( )
A.干冰 B.煤气 C.石油 D.可燃冰
【分析】纯净物是由一种物质组成的物质,混合物是由多种物质组成的物质;据此结合常
见物质的组成成分逐项分析即可.
【解答】解:A、干冰是固态的二氧化碳,干冰中只含有一种物质,属于纯净物。
B、煤气的主要成分是一氧化碳,还含有氢气等成分,属于混合物。
C、石油中含有汽油、柴油、煤油等物质,属于混合物。
D、可燃冰的主要成分是甲烷的水合物,含有其它成分,属于混合物。
故选:A。
【点评】解答本题要充分理解纯净物和混合物的区别,要分析物质是由几种物质组成的,
如果只有一种物质组成就属于纯净物,如果有多种物质就属于混合物.
4.(3分)“染色”馒头中添加剂柠檬黄铬酸铅(PbCrO )会使人致癌,已被明文禁用.已知铅
4
元素的化合价为+2.则铬元素(Cr)的化合价为( )
A.+2 B.+3 C.+6 D.+7
【分析】根据在化合物中正负化合价代数和为零,结合柠檬黄铬酸铅(PbCrO )的化学式进
4
行解答本题.
【解答】解:铅元素的化合价为+2价,氧元素显﹣2价,设铬元素的化合价是x,根据在化合
物中正负化合价代数和为零,可得:(+2)+x+(﹣2)×4=0,则x=+6价。
故选:C。
【点评】本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解
第6页(共15页)答.
5.(3分)化学与生活密切相关,下列做法合理的是( )
A.油着火,用水浇灭
B.电器着火,用泡沫灭火器浇灭
C.用明火检查液化气罐是否漏气
D.在火场的浓烟中逃生,可用湿毛巾捂住口鼻,低姿势前行
【分析】A、根据油着火的处理方法进行分析判断.
B、根据电器着火的处理方法、防触电的原进行分析判断.
C、根据可燃性气体泄露时的处理方法进行分析.
D、根据燃烧后生成的烟尘、有毒气体进行分析判断.
【解答】解:A、油着火,不能用水浇灭,因为油的密度比水的小,会浮在水面,水起不到灭
火的作用,故该做法错误。
B、电器着火,最先应当切断电源,防止中电,再用干粉灭火器灭火,故该做法错误。
C、液化气具有可燃性,遇到明火可能发生爆,故该做法错误。
D、用湿毛巾捂住口鼻,能防止吸入烟尘;生成的有毒的气体受热密度变小,上升聚集在高
处,故要匍匐前进,寻找安全出口,故该做法正确。
故选:D。
【点评】与生产、生活相关的化学知识是中考热点之一,了解灭火的原理、常见意外事故的
处理方法即可正确解答本题.
6.(3分)下列实验操作,不正确的是( )
A. 加热反应物 B. 用灯帽熄灭酒精灯
C. 托盘天平称量NaCl D. 稀释浓硫酸
【分析】A、根据给试管中的液体加热的方法进行分析判断.
第7页(共15页)B、根据酒精灯的使用方法进行分析判断.
C、根据托盘天平的使用要遵循“左物右码”的原则、使用的注意事项进行分析判断.
D、根据浓硫酸的稀释方法进行分析判断.
【解答】解:A、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,试管与桌面呈
45度角,且液体体积不能超过试管容积的 ,图中所示操作错误。
B、使用酒精灯时要注意“两查、两禁、一不可”,熄灭酒精灯时应用灯帽盖灭,图中所示
操作正确。
C、托盘天平的使用要遵循“左物右码”的原则,称量药品时两盘上应放大小相同的纸片,
图中所示操作正确。
D、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量
及时地扩散;一定不能把水注入浓硫酸中;图中所示操作正确。
故选:A。
【点评】本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操
作的注意事项是解答此类试题的关键.
7.(3分)我们的生活离不开水,下列有关水的认识中正确的是( )
A.提倡长期用纯水(蒸馏水)烧菜、煮饭等
B.使用无磷洗衣粉有利于保护水资源
C.水体有自净能力,未经处理的生活污水可任意排放
D.电解水时,负极产生的是氧气
【分析】A、纯水(蒸馏水)不含人体必需的微量元素(或矿物质),对身体健康不利.
B、根据含磷洗衣粉能使水富营养进行分析判断.
C、水体有自净能力,但超过了水的自净能力就会造成水的污染.
D、根据电解水的实验现象、结论进行分析判断.
【解答】解:A、微量元素虽然在体内含量很小,但却是维持正常生命活动所必需的,纯水
(蒸馏水)不含人体必需的微量元素(或矿物质),长期饮用对健康不利;故选项说法错误。
B、由于含磷洗衣粉能使水富营养化,使用无磷洗衣粉有利于防止水污染、保护水资源,故
选项说法正确。
C、水体有自净能力,但超过了水的自净能力就会造成水的污染,所以未经处理的生活污
水不能任意排放,故选项说法错误。
D、电解水时,与电源正极相连的试管内产生的气体是氧气,与电源负极相连的试管内产
第8页(共15页)生的气体是氢气,故选项说法错误。
故选:B。
【点评】本题难度不大,了解化学元素与人体健康的关系、水的污染与防治措施、电解水的
实验现象、结论等即可正确解答本题.
8.(3分)某物质不含碳元素和氢元素,它不可能是( )
有机物 盐 碱 酸.
①A. ② B③. ④ C. D.
【分①析】②根③据含有碳元素的②化③合物④叫有机化合物,①简称③有④机物;酸是指在①电②离时④产生的阳
离子全部是氢离子的化合物;碱是指在电离时产生的阴离子全部是氢氧根离子的化合物;
盐是由金属离子(或铵根离子)和酸根离子组成的化合物;进行分析判断即可.
【解答】解:由题意,某物质不含碳元素和氢元素。
含有碳元素的化合物叫有机化合物,简称有机物,有机物在一定含有碳元素,故该物质
①不可能是有机物。
是由金属离子(或铵根离子)和酸根离子组成的化合物,盐中可能不含碳元素和氢元素,
②如NaCl,故该物质可能是盐。
碱是指在电离时产生的阴离子全部是氢氧根离子的化合物,碱中一定含有氢元素,故
③该物质不可能是碱。
酸是指在电离时产生的阳离子全部是氢离子的化合物,故酸中一定含有氢元素,故该
④物质不可能是酸。
故该物质不可能是 中的物质。
故选:C。 ①③④
【点评】本题难度不大,考查有机物、有机物、酸、碱、盐的概念,抓住有机物、酸、碱、盐的
特征是正确解答本题的关键.
二、化学填空题(本题包括4小题,化学方程式2分,其余每空1分,共14分.请将答案填写
在答题卡相应的位置.)
9.(2 分)交警常用一种“酒精检测仪”检查司机是否酒后驾车.其反应原理为
C H OH+4CrO +6H SO ═2X+2CO ↑+9H O反应中的CrO 转化为绿色的化合物X.X的
2 5 3 2 4 2 2 3
化学式为 C r ( SO ) .
2 4 3
【分析】由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推
断生成物X的化学式.
【解答】解:根据反应的化学方程式C H OH+4CrO +6H SO ═2X+2CO ↑+9H O,反应物
2 5 3 2 4 2 2
第9页(共15页)中碳、氢、氧(原子团之外的)、铬、硫酸根的个数分别为2、18、13、4、6,反应后的生成物中
碳、氢、氧、铬、硫酸根原子的个数分别为2、18、13、0、0,根据反应前后原子种类、数目不
变,则2X中含有4个铬原子、6个硫酸根,则每个X分子由2个铬原子和3个硫酸根构成,
则物质X的化学式为Cr (SO ) .
2 4 3
故答案为:Cr (SO ) .
2 4 3
【点评】本题难度不大,利用化学反应前后元素守恒、原子守恒来确定物质的化学式是解
题的关键.
10.(2分)二氧化氯(ClO )是一种高效的消毒剂,一个二氧化氯分子是由 1 个氯原子和 2
2
个氧原子 构成的.ClO 中氯元素和氧元素的质量比为 7 1 : 6 4 .
2
【分析】根据二氧化氯(ClO )化学式的含义、化合物中各元素质量比=各原子的相对原子
2
质量×原子个数之比,进行分析解答.
【解答】解:根据二氧化氯(ClO )的化学式可知,一个二氧化氯分子是由1个氯原子和2
2
个氧原子构成的;ClO 中氯元素和氧元素的质量比为35.5:(16×2)=71:64.
2
故答案为:1个氯原子和2个氧原子;71:64.
【点评】本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问
题、解决问题的能力.
11.(7分)低碳排放,保护地球,毕节实试验区的老师们为了引领低碳生活,将自驾车改为骑
自行车,
请回答下列问题:
(1)下列自行车配件及用品中,属于有机合成材料的是(填序号) B .
A.钢圈 B.橡胶轮胎 C.弹簧 D.羊毛线编制的手柄套
(2)铁在潮湿的空气中容易锈蚀.
自行车的铁架表面喷漆,可以延缓自行车的绣蚀,其防绣原理是隔绝水和 氧气 .
①喷漆前需将铁制品放入稀盐酸中除锈(绣的主要成分是Fe
2
O
3
)观察到溶液变黄,有气
②泡溢出,反应的化学方程式是 F e O +6HCl ═ 2FeCl +3H O , Fe+2HC l ═ FeC l +H ↑
2 3 3 2 2 2
,反应类型分别是 复分解反应 和 置换反应 .
【分析】(1)有机合成材料主要包括塑料、合成纤维、合成橡胶三大类.
(2) 根据防止铁生锈的原理进行分析解答.
根据①酸的化学性质、常见的基本反应类型进行分析解答.
【②解答】解:(1)钢圈、弹簧属于金属材料;橡胶轮胎是用合成橡胶制成的,属于合成材料;
羊毛线编制的手柄套属于天然材料.
第10页(共15页)(2) 铁生锈的条件是铁与氧气和水共同接触,汽车表面喷漆,可以延缓汽车的锈蚀,其
防锈①原理是隔绝空气中的水和氧气.
酸能与金属和金属氧化物反应,铁制品放入稀盐酸中除锈(铁锈主要成分是Fe O ),观
2 3
②察到溶液变黄,是由于盐酸与铁锈的主要成分氧化铁反应生成氯化铁和水,反应的化学方
程式为Fe O +6HCl═2FeCl +3H O,该反应是两种化合物相互交换成分生成两种新的化
2 3 3 2
合物的反应,属于复分解反应;有无色气泡逸出,是由于铁与盐酸发生反应生成氯化亚铁
和氢气,反应的化学方程式为;Fe+2HCl═FeCl +H ↑,该反应是一种单质和一种化合物
2 2
反应生成另一种单质和另一种化合物的反应,属于置换反应.
故答案为:(1)B;(2) 氧气; Fe O +6HCl═2FeCl +3H O;Fe+2HCl═FeCl +H ↑;复
2 3 3 2 2 2
分解反应;置换反应.① ②
【点评】本题难度不大,但涉及知识点较多,掌握合成材料的分类、防止铁生锈的原理、酸
的化学性质等是正确解答本题的关键.
12.(3分)甲物质的溶解曲线如图所示,现进行如下实验:
(1)上述实验过程中,属于不饱和溶液的是 A 、 C .(填序号,下同),溶质质量分数相同
的是 B 、 C 、 D .
(2)下列操作使D中溶液质量分数改变的是 b .
a、加入20g甲 b、加入50g水 c、升高温度 d、加入100g30℃时甲的饱和溶
液,再恢复到20℃
【分析】(1)固体物质的溶解度是在一定温度下,100g水中最多溶解物质的质量,并结合
饱和溶液、不饱和溶液的概念判断;并依据溶质的质量分数计算式分析解答;
(2)要改变溶质的质量分数可以改变溶质或溶剂的质量.
【解答】解:
(1)观察溶解度曲线可知:20℃时,甲的溶解度是40g,所以,加入20g的A为不饱和溶液;
加入40g恰好饱和,所以B为饱和溶液;30℃时甲的溶解度是60g,升高温度至30℃,溶剂
第11页(共15页)的质量不变,溶质的质量是40g,故C为不饱和溶液;再降低温度至20℃,溶液恰好饱和,
溶质40gA、C,溶剂的质量不变,综上所述,B、C、D的溶质质量分数相同;
故答案为:
A、C;B、C、D;
(2)溶质的质量分数= ×100%,所以改变溶质的质量分数可以改变溶质或溶
剂的质量;
a、D为20℃时的饱和溶液,所以加入20g甲不再溶解,故溶质的质量分数不变,错误;
b、加入50g水使溶液的质量增加,而溶质的质量不变,所以溶质的质量分数变小,正确;
c、甲物质的溶解度随温度的升高而增大,所以升高温度,溶质和溶剂的质量均不变,溶质
的质量分数不变,错误;
d、温度不变,甲的溶解度不变,其饱和溶液溶质的质量分数不变;30℃时甲的饱和溶液溶
质质量分数比20℃时大,而D已经是20℃时的饱和溶液,所以加入100g30℃时甲的饱和
溶液,再恢复到20℃,溶质的质量分数不变,故错误;
故选b.
【点评】本题考查了学生对于溶解度曲线的应用、溶液状态的判断、及溶液溶质质量分数
的分析判断,掌握相关知识并细心分析才能正确解答.
三、化学实验题(本题包括2小题,共14分.请将答案写在答题卡的相应的位置)
13.(6分)九年级一班的同学做验证铝、铜、银的金属活动性顺序的实验,用到的药品由铝片、
铜丝、银丝和硫酸铜溶液。实验结束后,李斌同学欲对该实验的废液进行探究,请你一起
参与。
【提出问题】废液中含有什么物质?
【交流表达】
(1)李斌通过观察,认为废液中一定含有硫酸铜。他观察到的现象是 溶液显蓝色 。
(2)李斌通过分析,认为废液中一定含有硫酸铝,他的依据是 铝与稀硫酸(或硫酸铜溶
液)反应生成硫酸铝(或反应生成的硫酸铝不与其他物质反应); 。
【拓展应用】
(1)若将废液中的溶质全部转化为硫酸铝,应向废液中加入过量的 铝 。写出该反应的
化学方程式 2Al+3H SO ═ A l( SO )+3H ↑(或 2Al+3CuSO ═ A l( SO ) +3Cu ) 。
2 4 2 4 3 2 4 2 4 3
(2)反应完成后,过滤,滤渣中物质为 铜和铝 ,滤液中溶质为硫酸铝。
【分析】【交流表达】(1)硫酸铜溶于水后显示特定的颜色,所以根据它的颜色来进行判断;
第12页(共15页)(2)铝的活动性在这三种金属中活动性最强,可以据此作出判断;
【拓展应用】(1)铝可以和硫酸及硫酸铜反应生成硫酸铝;
(2)铝和硫酸铜反应生成了铜,当然也得考虑的到铝是过量的等因素,最后所得溶液应该
是硫酸铝;
【解答】解:【交流表达】(1)硫酸铜溶于水的到蓝色溶液,所以该学生的得出含有硫酸铜是
因为看到了溶液呈蓝色;
(2)根据金属活动性顺序及其应用,铝的活动性最强,所以发生的反应为:铝和稀硫酸反
应能够生成硫酸铝,铝和硫酸铜反应也能生成硫酸铝,所以可以判断一定含有硫酸铝;
【拓展应用】(1)根据金属活动性顺序及其应用可知,若将废液中的硫酸铜全部转化为硫
酸铝,应该加入过量的铝粉;
(2)由于反应完全后,会生成不溶于水的金属铜,并且铝是有剩余的,也不溶于水;所以滤
渣中物质为铝和铜.
故答案为:【交流表达】(1)溶液显蓝色;
(2)铝与稀硫酸(或硫酸铜溶液)反应生成硫酸铝(或反应生成的硫酸铝不与其他物质反
应);
【拓展应用】(1)2Al+3H SO ═Al(SO )+3H ↑(或 2Al+3CuSO ═Al(SO )+3Cu);
2 4 2 4 3 2 4 2 4 3
(2)铜和铝;
【点评】熟练掌握金属活动性顺序的应用以及酸碱盐之间的反应,解答这类题目时可以依
据金属活动性顺序的意义以及物质之间的反应进行.
14.(8分)化学课外小组设计了如图一套气体发生收集装置,以探究该装置的多功能性.
(1)甲同学认为装置Ⅰ可作为实验室制取O 的发生器,则Ⅰ的a仪器中可加入 双氧水
2
,b仪器加入 二氧化锰 ,反应的化学方程式为 2H O 2H O+O ↑ ,装置Ⅱ
2 2 2 2
中从 c 管口进气即可作为O 的收集装置.
2
(2)乙同学认为利用装置Ⅰ可作为实验室制二氧化碳的发生器,则Ⅰ中a仪器可加入 稀
盐酸 ,b中加入 碳酸钙 .如果制H 则Ⅱ中从 d 管口进气即可收集H .
2 2
第13页(共15页)【分析】(1)甲同学认为装置Ⅰ可作为实验室制取O 的发生器,则为固体与液体反应,只
2
能为双氧水与二氧化锰反应;因为氧气的密度大于空气,故可知答案.
(2)乙同学认为利用装置Ⅰ可作为实验室制二氧化碳的发生器,则为稀盐酸与碳酸钙反应,
根据氢气的密度小于空气可知答案.
【解答】解:(1)甲同学认为装置Ⅰ可作为实验室制取O 的发生器,则为固体与液体反应,
2
则Ⅰ的a仪器中可加入 双氧水,b仪器加入 二氧化锰,反应的化学方程式为 2H O
2 2
2H O+O ↑,因为氧气的密度大于空气,则装置Ⅱ中从 c管口进气即可作为O
2 2 2
的收集装置;
(2)乙同学认为利用装置Ⅰ可作为实验室制二氧化碳的发生器,则为稀盐酸与碳酸钙反应,
则Ⅰ中a仪器可加入 稀盐酸,b中加入 碳酸钙.根据氢气的密度小于空气可知答案,则
如果制H 则Ⅱ中从 d管口进气即可收集H .
2 2
故答为:(1)双氧水,二氧化锰,2H O 2H O+O ↑,c.
2 2 2 2
(2)稀盐酸,碳酸钙. d
【点评】熟练掌握实验制取氧气、二氧化碳和氢气的原理、收集方法;实验室确定气体发生
装置时应考虑的因素是反应物状态和反应条件,确定气体收集装置时应考虑的因素是气
体的溶解性和密度.
四、化学计算题(本题共8分.请将解题过程写在答题卡的相应的位置)
15.(8分)如图是配好的硝酸银溶液,请根据标签上的文字信息进行计算:
(1)该硝酸银溶液中溶剂的质量为 8 0 g.
(2)取一包氯化钠的固体样品放入烧杯中加入水完全溶解,然后向烧杯中滴加上述溶液至
完全反应,过滤、洗涤、烘干,称得沉淀2.87g,计算:
第14页(共15页)氯化钠固体样品中含氯化钠多少克?
①用去的硝酸银溶液的质量是多少克?
②
【分析】(1)利用溶质质量=溶液质量×溶质的质量分数,再根据溶剂质量=溶液质量﹣
溶质质量即可求得溶剂的质量.
(2) 由生成沉淀的质量2.87g,根据反应的化学方程式列式计算出氯化钠固体样品中含
氯化①钠的质量即可.
由生成沉淀的质量2.87g,根据反应的化学方程式列式计算出硝酸银溶液中溶质的质量,
②再根据溶液的质量=溶质的质量÷溶质的质量分数,进行解答即可.
【解答】解:(1)根据题意,100g溶质质量分数为20%的硝酸银溶液中溶质的质量为:
100g×20%=20g,所含溶剂的质量为100g﹣20g=80g.
(2)设氯化钠固体样品中含氯化钠的质量为x,用去的硝酸银的质量为y,
NaCl+AgNO =AgCl↓+NaNO
3 3
58.5 170 143.5
x y 2.87g
x=1.17g
①
y=3.4g
②
用去的硝酸银溶液的质量是:3.4g÷20%=17g.
答:(1)80;(2) 氯化钠固体样品中含氯化钠为1.17g; 用去的硝酸银溶液的质量是
17g. ① ②
【点评】本题难度不是很大,掌握溶液组成的有关计算、利用化学方程式进行计算的方法是正
确解答本题的关键.
第15页(共15页)