文档内容
高途高中·化学
点睛卷
2024
海南省-------------------------------- 高途高中化学点睛卷 -----------------------------------
绝密 启用前
【高途】2024 年海南省普通高中学业水平选择性考试模拟测试卷
化 学
本试卷共7页,19小题,满分100分,考试用时90分钟
可能用到的相对原子质量: H—1 C—12 N—14 O—16 Na—23 Mg—24 S—32
Cl—35.5 Fe—56 Mn—55 Cr—52 Si—28
一、选择题:本题共 8小题,每小题2分,共 16分。每小题只有一个选项符合题目要求。
1.下列叙述错误的是
A.绿色化学的核心是如何对被污染的环境进行无毒无害的治理
B.“火树银花合,星桥铁锁开”中涉及化学能转化为热能和光能
C.刘长卿诗云“水声冰下咽,砂路雪中平”,固态冰转化为液态水需要吸热
D. “三月打雷麦谷堆”是指在雷电作用下N 最终转化成被作物吸收的化合态氮
2
2.下列化学用语表示正确的是
A.镁原子的结构示意图: B.2-丁烯的键线式:
C.邻羟基苯甲醛分子内氢键: D.乙烯的空间填充模型:
3.化学与生产、生活、科技及环境等密切相关下列说法正确的是
A.我国新一代长征七号运载火箭使用的是液氧煤油发动机,煤油主要由煤的干馏制得
B.固定太空电梯的缆绳材料最有可能是碳纳米管,碳纳米管与C 互为同素异形体
60
C.植物可以吸收利用空气中的NOx作为肥料,实现氮的固定
D.利用CO 合成了脂肪酸:实现了无机小分子向有机高分子的转变
2
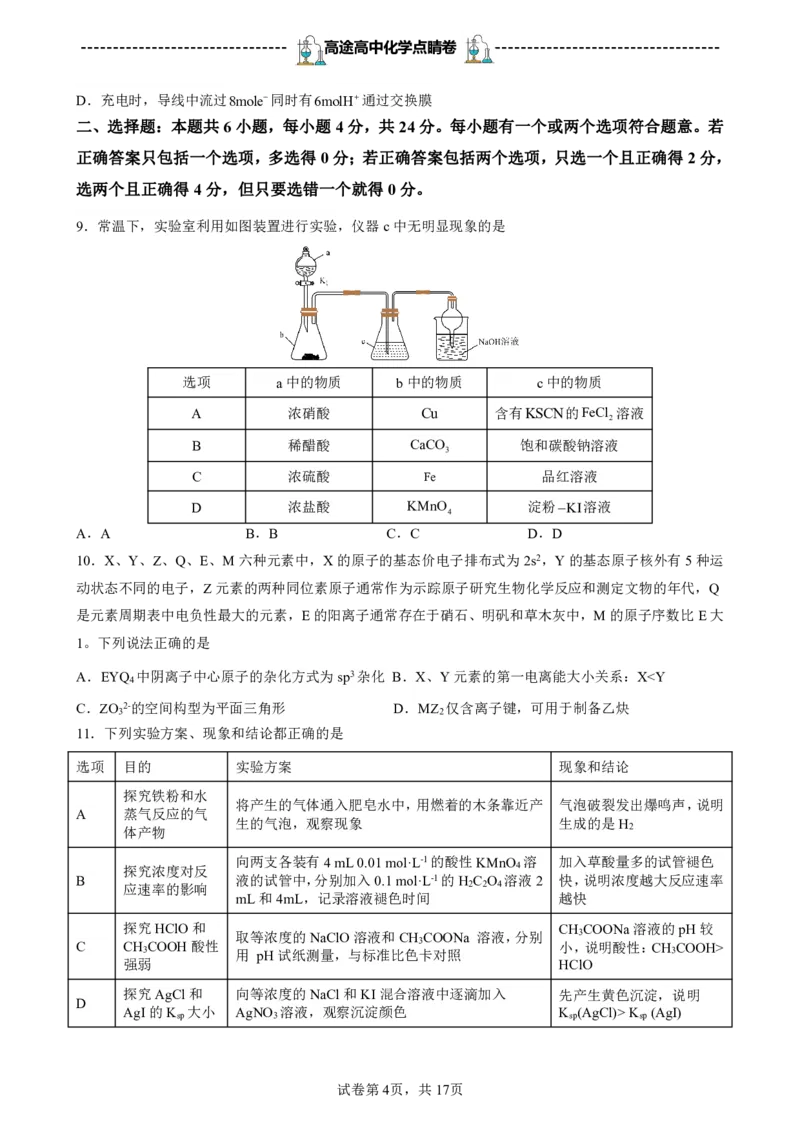
4.下列关于实验室制取气体的原理与装置正确的是
A.制取CO B.制取C H C.制取Cl D.制取NH
2 2 4 2 3
A.A B.B C.C D.D
试卷第2页,共17页-------------------------------- 高途高中化学点睛卷 -----------------------------------
5.对下列事实的解释不
.
正
.
确
.
的是
选项 事实 解释
A 稳定性:HF>HI HF分子间存在氢键,HI分子间不存在氢键
B 键角:NH+>H O 中心原子均采取sp3杂化,孤电子对有较大的斥力
4 2
C 熔点:石英>干冰 石英是共价晶体,干冰是分子晶体;共价键比分子间作用力强
酸性:CF COOH> F的电负性大于Cl,F-C的极性大于Cl-C,使F C-的极性大于Cl C
3 3 3
D
CCl COOH -的极性
3
A.A B.B C.C D.D
6.设N 为阿伏伽德罗常数的值,下列说法正确的是
A
A.18gH 18O中含有的中子数为10N
2 A
B.42g环己烷( )中含有σ键的数目为9 N
A
C.标准状况下,22.4LCHCl 中含有的分子数为N
3 A
D.6.0gSiO 与足量NaOH溶液反应,所得溶液中SiO2的个数为0.1N
2 3 A
7.对于反应2NO(g)+O (g)=2NO (g) ΔH=-116.4kJ·mol-1,下列说法正确的是
2 2
A.该反应能够自发的原因是ΔS>0
B.工业上使用合适的催化剂可提高NO 的生产效率
2
C.升高温度,该反应v 增大,v 减小,平衡向逆反应方向移动
(逆) (正)
D.2molNO(g)和1molO (g)中所含化学键能总和比2molNO (g)中大116.4kJ·mol-1
2 2
8.科研小组设计用电化学原理进行废水脱硫,放
.
电
.
时工作原理示意图如图所示。下列说法正确的是
A.放电时,负极电极的反应S24H O8e SO28H
2 4
B.放电时,H SO 溶液的浓度不断减小
2 4
C.充电时,阳极区需补充适量水以保持溶液浓度不变
试卷第3页,共17页-------------------------------- 高途高中化学点睛卷 -----------------------------------
D.充电时,导线中流过8mole同时有6molH通过交换膜
二、选择题:本题共 6小题,每小题 4分,共24分。每小题有一个或两个选项符合题意。若
正确答案只包括一个选项,多选得 0分;若正确答案包括两个选项,只选一个且正确得 2分,
选两个且正确得 4分,但只要选错一个就得 0分。
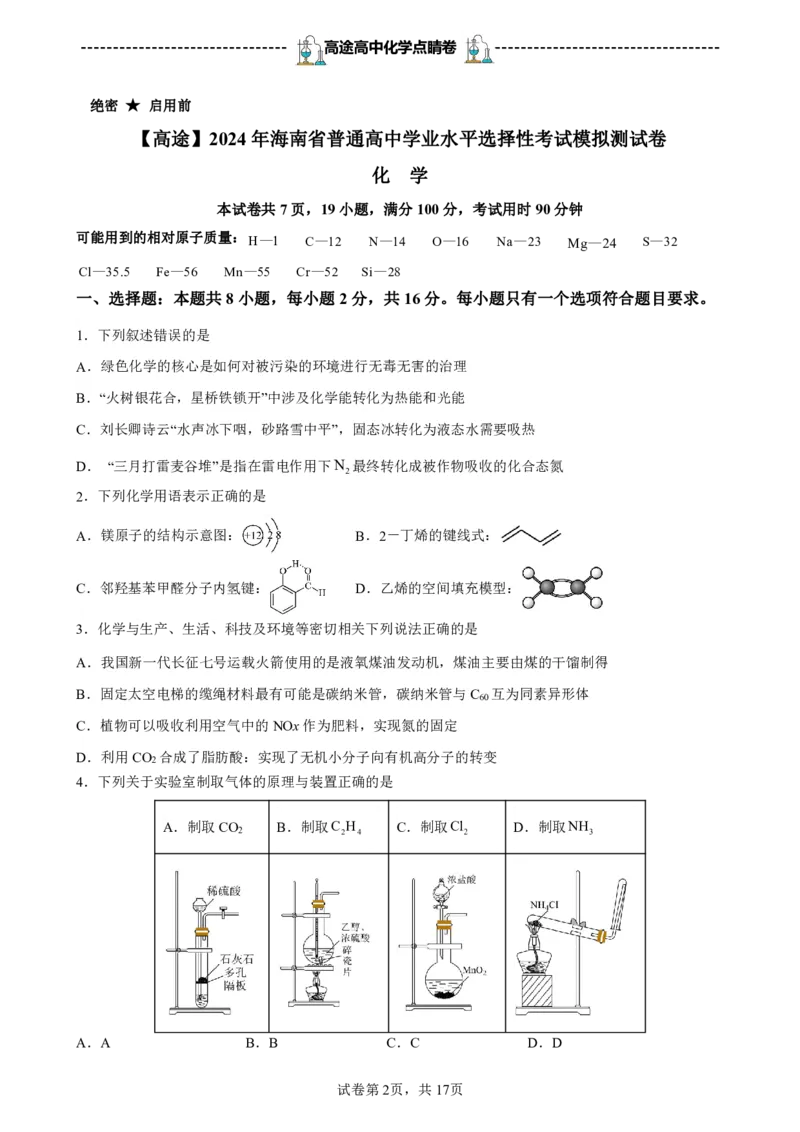
9.常温下,实验室利用如图装置进行实验,仪器c中无明显现象的是
选项 a中的物质 b中的物质 c中的物质
A 浓硝酸 Cu 含有KSCN的FeCl 溶液
2
B 稀醋酸 CaCO 饱和碳酸钠溶液
3
C 浓硫酸 Fe 品红溶液
D 浓盐酸 KMnO 淀粉KI溶液
4
A.A B.B C.C D.D
10.X、Y、Z、Q、E、M六种元素中,X的原子的基态价电子排布式为2s2,Y的基态原子核外有5种运
动状态不同的电子,Z元素的两种同位素原子通常作为示踪原子研究生物化学反应和测定文物的年代,Q
是元素周期表中电负性最大的元素,E的阳离子通常存在于硝石、明矾和草木灰中,M的原子序数比E大
1。下列说法正确的是
A.EYQ 中阴离子中心原子的杂化方式为sp3杂化 B.X、Y元素的第一电离能大小关系:X
强弱 HClO
探究AgCl和 向等浓度的NaCl和KI混合溶液中逐滴加入 先产生黄色沉淀,说明
D
AgI的K 大小 AgNO 溶液,观察沉淀颜色 K (AgCl)>K (AgI)
sp 3 sp sp
试卷第4页,共17页-------------------------------- 高途高中化学点睛卷 -----------------------------------
12.化合物Y是一种天然除草剂,其结构如图所示。下列说法错误的是
A.Y中含氧官能团有3种
B.1molY最多消耗4molNaOH
C.Y可发生取代、加成、消去反应
D.Y与足量H 加成后,产物分子中含5个手性碳原子
2
13.一定温度下,在2L的密闭容器中发生如下反应:As2Bg xCgΔH0,B、C的物质的量随
时间变化的关系如图1所示,达到平衡后在t 、t 、t 、t 时都只改变了一种条件,逆反应速率随时间变化
1 2 3 4
的关系如图2所示。
下列有关说法正确的是
A.x2,反应开始2min内,v
B
0.1mol/
Lmin
B.t 时改变的条件是降温,平衡逆向移动
1
C.t 时改变的条件可能是减小cA,平衡逆向移动
2
D.t 时可能是减小压强,平衡不移动;t 时可能是使用催化剂,cB不变
3 4
14.室温下,用0.05000mol·L-1稀硫酸滴定20.00mL某浓度的MOH溶液,混合溶液的pH随加入稀硫酸体
积的变化如图所示。下列说法正确的是
A.若反应在绝热容器中进行,a点对应的溶液温度最高
B.水的电离程度c>b>a
C.b点对应的溶液中,c(M+):c(MOH)=104:1
D.c点对应的溶液中,c(H+)=c(OH-)+c(M+)+c(MOH)
试卷第5页,共17页-------------------------------- 高途高中化学点睛卷 -----------------------------------
三、非选择题:本题共 5小题,共 60分。
15.(10分) 铬元素是一种重金属元素,工业上处理含铬废水并将其资源化的工艺有多种,其中两种工艺
如下图所示:
已知:①含铬废水中铬元素主要有3和6两种价态,6价铬在酸性环境中氧化性更强。
②CrO2H O2CrO22H。
2 7 2 4
回答下列问题:
(1)“还原”时,先加入H SO 酸化,再加入Na S O 固体,其发生反应的离子方程式为 ,若不加H SO
2 4 2 2 5 2 4
酸化,可能造成的后果是 。
(2)“中和”过程中,有大量气泡生成,写出中和时产生CrOH 的离子方程式: 。
3
(3)“过滤洗涤”时,证明沉淀已洗涤干净的操作为: 。
(4)“冶炼”时,该反应的能量主要转化形式为 。
(5)“氧化”时,发生反应的化学方程式为: 。
(6)已知K BaCrO 2.41010,利用氧化法除铬时,欲使废液中铬元素的含量不高于0.26mgL1,则此
sp 4
滤液中c
Ba2
的范围为 。
(7)与还原法相比,氧化法的优点为 。
16.(10分)温室气体的利用是当前环境和能源领域的研究热点,以下列两种方法为例,请回答问题。
I.哈伯合成氨在较高温度下以氢气做氢源,其使用的氢气可由天然气制备:
CH (g)H O(g)CO(g)3H (g)。下表列出了几种化学键的键能:
4 2 2
化学键 HH CH HO
键能kJ/mol 436 413 467 1072
(1)298K时,上述反应的ΔH kJ/mol。
(2)为提高CH 的平衡转化率,可采用的措施是___________。
4
A.使用合适的催化剂 B.采用较高的温度
C.采用较高的压强 D.恒温恒容增大甲烷和水蒸汽投料比
试卷第6页,共17页-------------------------------- 高途高中化学点睛卷 -----------------------------------
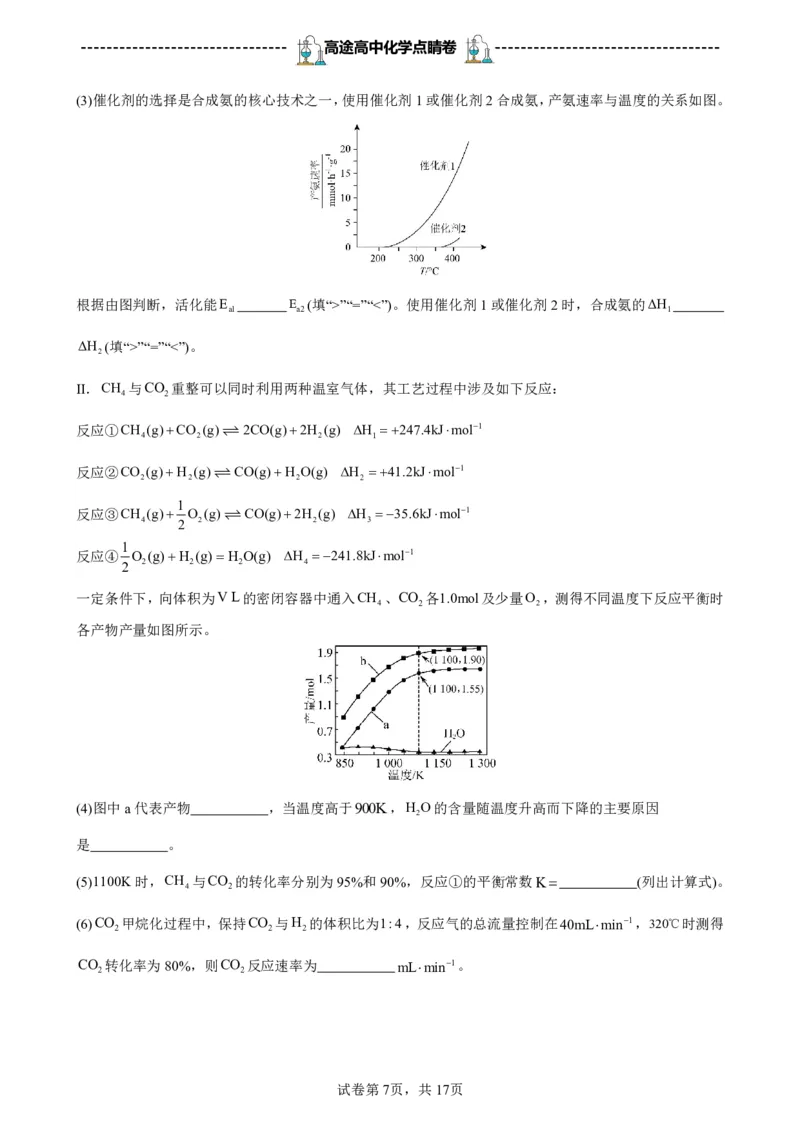
(3)催化剂的选择是合成氨的核心技术之一,使用催化剂1或催化剂2合成氨,产氨速率与温度的关系如图。
根据由图判断,活化能E E (填“>”“=”“<”)。使用催化剂1或催化剂2时,合成氨的ΔH
al a2 1
ΔH (填“>”“=”“<”)。
2
Ⅱ.CH 与CO 重整可以同时利用两种温室气体,其工艺过程中涉及如下反应:
4 2
反应①CH (g)CO (g)2CO(g)2H (g) H 247.4kJmol1
4 2 2 1
反应②CO (g)H (g)CO(g)H O(g) H 41.2kJmol1
2 2 2 2
1
反应③CH (g) O (g)CO(g)2H (g) H 35.6kJmol1
4 2 2 2 3
1
反应④ O (g)H (g)H O(g) H 241.8kJmol1
2 2 2 2 4
一定条件下,向体积为VL的密闭容器中通入CH 、CO 各1.0mol及少量O ,测得不同温度下反应平衡时
4 2 2
各产物产量如图所示。
(4)图中a代表产物 ,当温度高于900K,H O的含量随温度升高而下降的主要原因
2
是 。
(5)1100K时,CH 与CO 的转化率分别为95%和90%,反应①的平衡常数K (列出计算式)。
4 2
(6)CO 甲烷化过程中,保持CO 与H 的体积比为1:4,反应气的总流量控制在40mLmin1,320℃时测得
2 2 2
CO 转化率为80%,则CO 反应速率为 mLmin1。
2 2
试卷第7页,共17页-------------------------------- 高途高中化学点睛卷 -----------------------------------
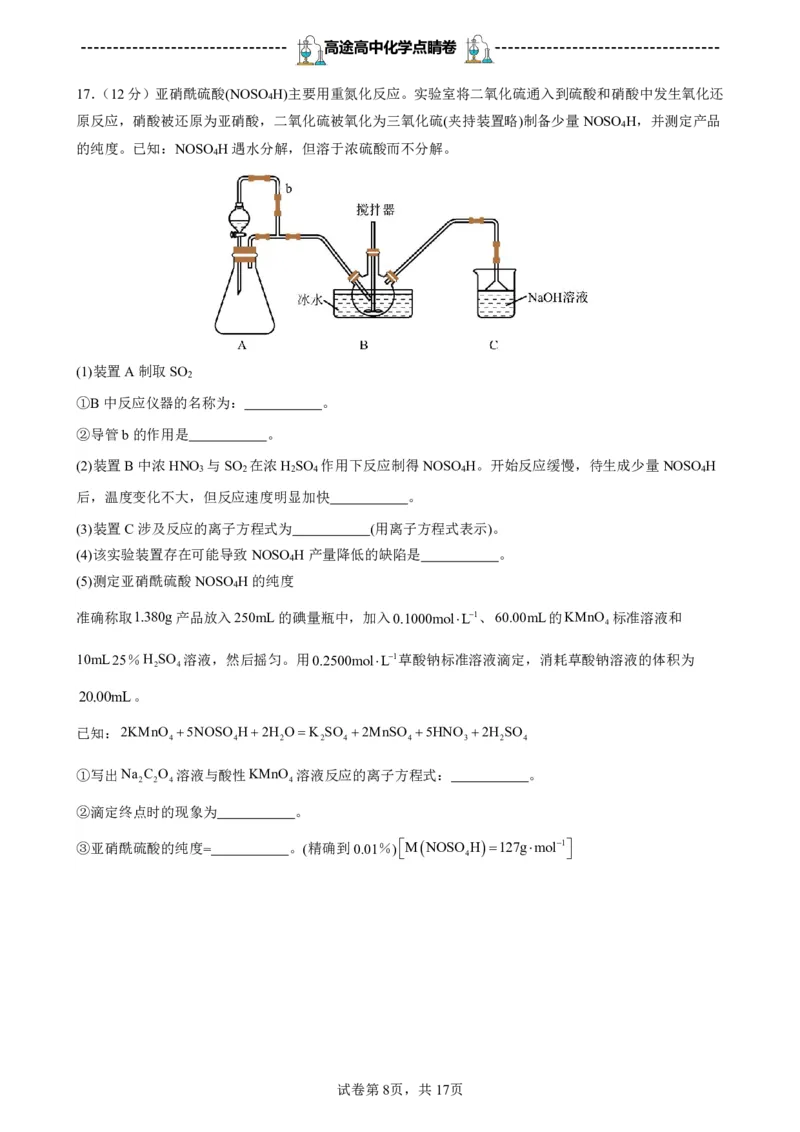
17.(12分)亚硝酰硫酸(NOSO H)主要用重氮化反应。实验室将二氧化硫通入到硫酸和硝酸中发生氧化还
4
原反应,硝酸被还原为亚硝酸,二氧化硫被氧化为三氧化硫(夹持装置略)制备少量NOSO H,并测定产品
4
的纯度。已知:NOSO H遇水分解,但溶于浓硫酸而不分解。
4
(1)装置A制取SO
2
①B中反应仪器的名称为: 。
②导管b的作用是 。
(2)装置B中浓HNO 与SO 在浓H SO 作用下反应制得NOSO H。开始反应缓慢,待生成少量NOSO H
3 2 2 4 4 4
后,温度变化不大,但反应速度明显加快 。
(3)装置C涉及反应的离子方程式为 (用离子方程式表示)。
(4)该实验装置存在可能导致NOSO H产量降低的缺陷是 。
4
(5)测定亚硝酰硫酸NOSO H的纯度
4
准确称取1.380g产品放入250mL的碘量瓶中,加入0.1000molL1、60.00mL的KMnO 标准溶液和
4
10mL25%H SO 溶液,然后摇匀。用0.2500molL1草酸钠标准溶液滴定,消耗草酸钠溶液的体积为
2 4
20.00mL。
已知:2KMnO 5NOSO H2H OK SO 2MnSO 5HNO 2H SO
4 4 2 2 4 4 3 2 4
①写出Na C O 溶液与酸性KMnO 溶液反应的离子方程式: 。
2 2 4 4
②滴定终点时的现象为 。
③亚硝酰硫酸的纯度= 。(精确到0.01%)
MNOSO
4
H127gmol1
试卷第8页,共17页-------------------------------- 高途高中化学点睛卷 -----------------------------------
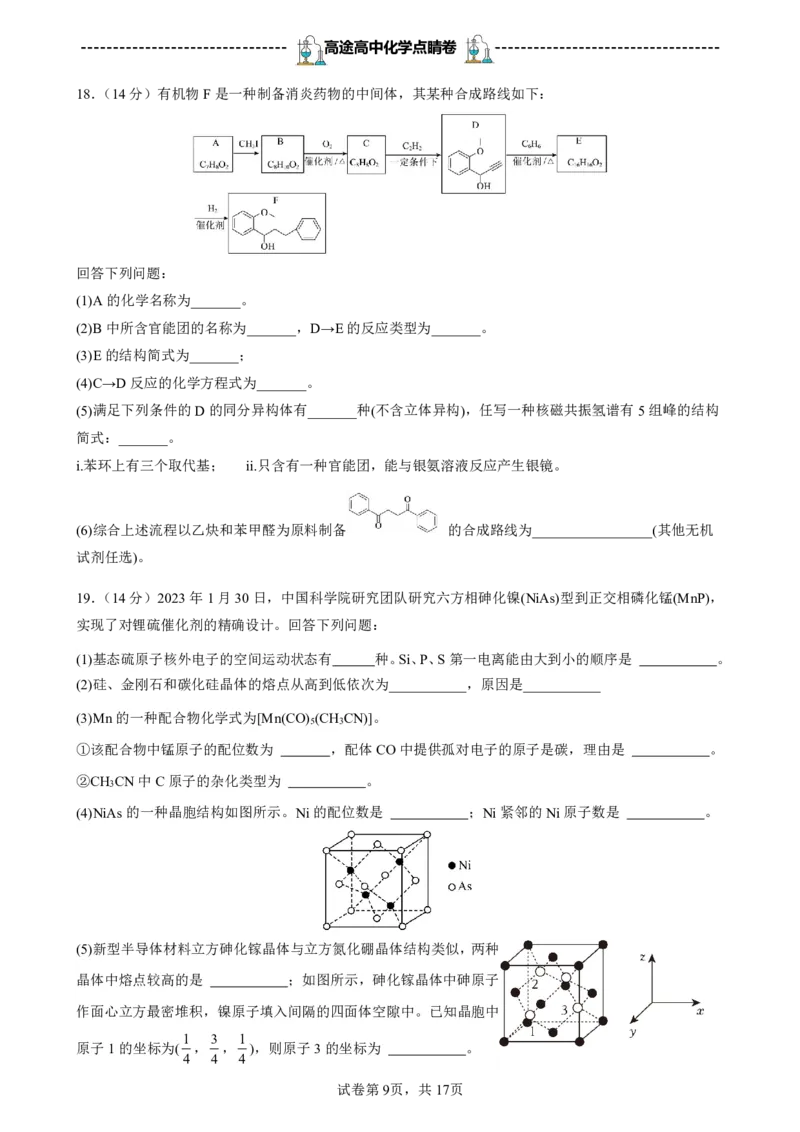
18.(14分)有机物F是一种制备消炎药物的中间体,其某种合成路线如下:
回答下列问题:
(1)A的化学名称为_______。
(2)B中所含官能团的名称为_______,D→E的反应类型为_______。
(3)E的结构简式为_______;
(4)C→D反应的化学方程式为_______。
(5)满足下列条件的D的同分异构体有_______种(不含立体异构),任写一种核磁共振氢谱有5组峰的结构
简式:_______。
i.苯环上有三个取代基; ii.只含有一种官能团,能与银氨溶液反应产生银镜。
(6)综合上述流程以乙炔和苯甲醛为原料制备 的合成路线为_________________(其他无机
试剂任选)。
19.(14分)2023年1月30日,中国科学院研究团队研究六方相砷化镍(NiAs)型到正交相磷化锰(MnP),
实现了对锂硫催化剂的精确设计。回答下列问题:
(1)基态硫原子核外电子的空间运动状态有 种。Si、P、S第一电离能由大到小的顺序是 。
(2)硅、金刚石和碳化硅晶体的熔点从高到低依次为___________,原因是___________
(3)Mn的一种配合物化学式为[Mn(CO) (CH CN)]。
5 3
①该配合物中锰原子的配位数为 ,配体CO中提供孤对电子的原子是碳,理由是 。
②CH CN中C原子的杂化类型为 。
3
(4)NiAs的一种晶胞结构如图所示。Ni的配位数是 ;Ni紧邻的Ni原子数是 。
(5)新型半导体材料立方砷化镓晶体与立方氮化硼晶体结构类似,两种
晶体中熔点较高的是 ;如图所示,砷化镓晶体中砷原子
作面心立方最密堆积,镍原子填入间隔的四面体空隙中。已知晶胞中
1 3 1
原子1的坐标为( , , ),则原子3的坐标为 。
4 4 4
试卷第9页,共17页-------------------------------- 高途高中化学点睛卷 -----------------------------------
【高途】2024 年海南省普通高中学业水平选择性考试模拟测试卷
化学参考答案
1.【答案】A
【详解】A.绿色化学的核心是利用化学原理和技术手段,减少或消除产品在生产和应用中涉及的有害化
学物质,实现从源头减少或消除环境污染,A项错误;
B.火树银花指的是灼热的铁水被打到半空中与氧气发生剧烈的氧化还原反应,这个过程中化学能转化成
了热能和光能,故B正确;
C.冰转化为水属于液化过程,需要吸热,故C正确;
D.雷电可以将空气中的N 转化为可以被作物吸收的化合态氮,故D正确;
2
答案选A。
2.【答案】C
【详解】A.Mg原子核外有12个电子,失去2个电子形成Mg2+,是10电子微粒,镁离子的结构示意图:
,A错误;
B.2-丁烯的键线式: ,B错误;
C.邻羟基苯甲醛分子内氢键: ,C正确;
D.乙烯的球棍模型: ,D错误;
故答案选C。
3.【答案】B
【详解】A.煤油是轻质石油产品的一类,由天然石油或人造石油经分馏或裂化而得,A错误;
B.碳纳米管与C 均为碳单质,互为同素异形体,B正确;
60
C.植物可以吸收利用空气中的NO 作为肥料,该过程是含N化合物之间的转化,不是氮气单质转化为氮
x
的化合物过程,不属于氮的固定,C错误;
D.脂肪酸不是有机高分子化合物,D错误;
故选B。
4.【答案】B
【详解】A.不能用稀硫酸和石灰石反应制取CO ,因为稀硫酸和CaCO 反应生成的CaSO 会包裹在石灰
2 3 4
石表面,使反应不能继续,A错误;
B.乙醇在浓硫酸的作用下,迅速升温到170℃,发生消去反应可制取C H ,B正确;
2 4
C.利用MnO 和浓盐酸共热反应制取Cl ,实验缺少加热装置,C错误;
2 2
D.不能通过加热氯化铵固体制取NH ,因为氯化铵加热分解为NH 和HCl,在试管口遇冷又会重新反应
3 3
生成氯化铵,D错误;
试卷第10页,共17页-------------------------------- 高途高中化学点睛卷 -----------------------------------
故选B。
5.【答案】A
【详解】A.氢化物的稳定性与键能大小有关,与氢键无关,则氟化氢的稳定性强于碘化氢是因为H-F键
键能比H-I大,故A错误;
B.铵根离子中的氮原子和水分子中的氧原子均采取sp3杂化,铵根离子中氮原子和水分子中氧原子的孤对
电子对数分别为0和2,孤对电子对数越多,对成键电子对的斥力越大,键角越小,所以铵根离子的键角
大于水分子,故B正确;
C.石英即二氧化硅,是共价晶体,干冰是分子晶体,共价键比分子间作用力强,所以石英的熔点高于干
冰,故C正确;
D.氟元素的电负性大于氯元素,F-C的极性大于Cl-C,使F C-的极性大于Cl C-的极性,对羧基的
3 3
吸电子能力大于Cl C-,所以CF COOH更易电离出氢离子,酸性强于CCl COOH,故D正确;
3 3 3
故选A。
6.【答案】B
m 18g
【详解】A.n 0.9mol,则中子数为9N ,A错误;
A
M 20g/mol
m 42g
B.n 0.5mol,1个环己烷中含有18个σ 键,则42g环己烷中含有σ键的数目为 9N ,B
A
M 84g/mol
正确;
C.标准状况下,CHCl 为液体,无法根据体积计算物质的量,C错误;
3
D.二氧化硅与氢氧化钠溶液反应生成硅酸钠和水,硅酸钠在溶液中发生水解反应,根据原子守恒,
m 6.0g
n Si 0.1mol,则SiO2个数小于0.1N ,故D错误;
M 60g/mol 3 A
故答案为:B。
7.【答案】B
【详解】A.根据自由能公式G=H-TS,当G0反应能够自发,该反应的 H<0, S<0,A错误;
B.催化剂可加快反应速率,缩短生产时间,从而可以提高NO 的生产效率,B△正确; △
2
C.升高温度,v 、v 增大,但平衡向吸热反应方向移动即逆反应方向移动,C错误;
(逆) (正)
D.根据2NOg+O g 2NO (g)ΔH 116.4kJ/mol-1, H<0,得到2molNO(g)和1molO (g)中所含化
2 2 2
学键能总和比2molNO (g)中所含化学键能总和小116.4kJ∙m △ ol−1,D错误。
2
故选B。
8.【答案】C
【详解】A.放电时,由题图得,Mn2+被氧化,故A错误;
B.放电时,正极区中的氢离子被还原生成氢气,负极区中的氢离子会透过质子交换膜流向正极区,硫酸
浓度不变,故B错误;
C.充电时,阳极区中的水被氧化,2H O-4e-=O ↑+4H+,需补充适量水来维持浓度,故C正确;
2 2
试卷第11页,共17页-------------------------------- 高途高中化学点睛卷 -----------------------------------
D.充电时,根据C中方程式,导线中流过8mol电子时,应有8mol氢离子穿过质子穿透膜,故D错误;
故本题选C。
9.【答案】C
【详解】A.浓硝酸与铜反应生成二氧化氮,二氧化氮与含有硫氰化钾的氯化亚铁溶液中的亚铁离子反应
生成能与硫氰酸根离子反应的铁离子,溶液会变为血红色,故A不符合题意;
B.稀硝酸与碳酸钙固体反应二氧化碳,二氧化碳能与饱和碳酸钠溶液反应生成碳酸氢钠沉淀,溶液会变
浑浊,故B不符合题意;
C.常温下,铁在浓硫酸中会发生钝化,致密的钝化膜阻碍反应的继续进行,不可能生成能使品红溶液褪
色的二氧化硫,所以品红溶液中无明显现象,故C符合题意;
D.浓盐酸与高锰酸钾固体反应生成氯气,氯气能与淀粉碘化钾溶液中的碘化钾反应生成单质碘,溶液会
变为蓝色,故D不符合题意;
故选C。
10.【答案】AC
【分析】X的原子的基态价电子排布式为2s2,则X为Be;Y的基态原子核外有5种运动状态不同的电子,
Y为B;Z元素的两种同位素原子通常作为示踪原子研究生物化学反应和测定文物的年代,Z为C;Q是
元素周期表中电负性最大的元素,为F;E的阳离子通常存在于硝石、明矾和草木灰中,E为K;M的原
子序数比E大1,M为Ca。
【详解】A.EYQ 即KBF ,阴离子中心B原子与F成4条化学键,杂化方式为sp3杂化,A说法正确;
4 4
B.X、Y分别为Be、B,元素的第一电离能大小关系:X>Y,B说法错误;
C.CO 2-的杂化方式为sp2,其空间构型为平面三角形,C说法正确;
3
D.MZ 即CaC ,既含离子键,又含共价键,可用于制备乙炔,D说法错误;
2 2
答案为AC。
11.【答案】AD
【详解】A.铁粉和水蒸气反应生成氢气和四氧化三铁,氢气可以燃烧,收集后,用燃着的木条靠近会有
爆鸣声,A正确;
B.草酸浓度相同,体积不同,且生成锰离子可作催化剂,不能探究浓度对反应速率的影响,B错误;
C.NaClO溶液具有漂白性,故不能用pH试纸测定NaClO溶液的pH,应该用pH计测定,C错误;
D.NaCl和KI浓度相同,向等浓度的NaCl和KI混合溶液中逐滴加入AgNO 溶液时,溶度积小的先形成
3
沉淀,AgI为黄色沉淀,故先产生黄色沉淀,说明K (AgCl)>K (AgI),D正确;
sp sp
故选AD。
12.【答案】CD
【详解】A.根据Y的结构简式可知,其中含有醚键,羟基,酯基,一种3种含氧官能团,A正确;
B.根据Y的结构简式可知,结构中含有的3个羟基和一个酯基都可以和氢氧化钠反应,故1molY最多消
耗4molNaOH,B正确;
C.根据Y的结构简式可知,其结构中的羟基位于苯环上,不能发生消去反应,C错误;
试卷第12页,共17页-------------------------------- 高途高中化学点睛卷 -----------------------------------
D.Y与足量H 加成后生成 ,一共7个手性碳,D错误;故选CD。
2
13.【答案】D
【详解】A.通过图1可知,2min达平衡, n(B)=0.3mol-0.1mol=0.2mol, n(C)=0.2mol,物质的量变化
△ 0.2m△ol
量之比等于化学计量数之比,故2:x=0.2mol:0.2mol,解得x=2,v(B)=
2L
=0.05mol/(L•min),故A错
2min
误;
B.正反应为放热反应,当降低温度,反应正向移动,正逆速率都减小,并且正反应速度降低的幅度小,
故B错误;
C.A为固体,浓度为常数,故C错误;
D.反应前后气体的物质的量不变,减小压强,同等程度降低速率,平衡不移动,使用催化剂,同等程度
加快反应速率,平衡不移动,故D正确;
故选D。
14.【答案】C
【详解】A.b点恰好完全反应,放热最多,故b点对应的溶液温度最高,故A错误;
B.b点的溶质为M SO ,水的电离程度最大,故B错误;
2 4
C.b点时溶质为M SO ,根据质子守恒可得c(H+)=c(OH-)+c(MOH),b点时pH=5,c(H+)=10-5mol/L,
2 4
c(OH-)=10-9mol/L,则c(MOH)=10-5mol/L-10-9mol/L≈10-5mol/L,c(M+)≈2c(SO2)=2×0.05mol/L=0.1mol/L,则
4
c(M+):c(MOH)=104:1,故C正确;
D.c点为M SO 和H SO 的混合物,且二者物质的量比为1:1,根据电荷守恒可知:
2 4 2 4
c(M+)+c(H+)=2c(SO2)+c(OH-);根据元素守恒可知:c(SO2)=c(M+)+c(MOH),由二者可推知质子守恒可得
4 4
c(H+)=c(OH-)+c(M+)+2c(MOH),故D错误;故选C。
15.(10分)【答案】(1)CrO2-+3S O2-+10H+=4Cr3++5H O+6SO2-;+6价铬不能完全被还原
2 7 2 5 2 4
(2)2Cr3++3CO2-+3H O=2Cr(OH) ↓+3CO ↑
3 2 3 2
(3)取最后一次洗涤液,向其中加入足量稀盐酸,再加入BaCl 溶液,没有白色沉淀生成
2
(4)化学能转化为热能
(5)2Cr(OH) +3NaClO+4NaOH=2Na CrO +3NaCl+5H O
3 2 4 2
(6)≥4.8×10-5mol L-1
(7)能耗低 ⋅
【分析】含铬废水先加入H
2
SO
4
酸化,再加入Na
2
S
2
O
5
固体,现发生转化2CrO2
4
-+2H+ Cr
2
O
7
2- +H
2
O,随
⇌
后发生反应CrO2-+3S O2-+10H+=4Cr3++5H O+6SO2-,加入碳酸钠调节,中和pH,发生反应
2 7 2 5 2 4
试卷第13页,共17页-------------------------------- 高途高中化学点睛卷 -----------------------------------
Cr3++CO2-+3H O=2Cr(OH) ↓+3CO ↑,过滤获得Cr(OH) ,经煅烧,得到氧化铬,加铝发生置换反应,获得
3 2 3 2 3
单质铬;下方流程:含铬废水加入氢氧化钠调节pH,发生反应Cr3++3OH-=Cr(OH) ↓,“氧化”时,发生反
3
应的化学方程式为2Cr(OH) +3NaClO+4NaOH=2Na CrO +3NaCl+5H O,加硝酸钡,利用沉淀溶解平衡,获
3 2 4 2
得BaCrO 沉淀,据此分析回答问题。
4
【详解】(1)已知+6价铬在溶液中存在如下平衡:2CrO2
4
-+2H+ Cr
2
O
7
2- +H
2
O,因此加入稀硫酸的目的是
⇌
将CrO2
4
-转化为Cr
2
O
7
2-,此时加入Na
2
S
2
O
5
固体,发生反应的离子方程式为
CrO2-+3S O2-+10H+=4Cr3++5H O+6SO2-,根据题意可知,+6价铬在酸性环境中氧化性更强,若不加H SO
2 7 2 5 2 4 2 4
酸化,可能造成的后果是+6价铬不能完全被还原
(2)“中和”时,加入Na CO 有大量气泡生成,由此可判断该气体为CO ,同时有沉淀生成,因此该反应
2 3 2
的离子方程式为2Cr3++3CO2-+3H O=2Cr(OH) ↓+3CO ↑
3 2 3 2
(3)“过滤洗涤”时,洗涤Cr(OH) 沉淀上的SO 2-等杂质离子,证明沉淀已洗涤干净的操作为取最后一次
3 4
洗涤液,向其中加入足量稀盐酸,再加入BaCl 溶液,没有白色沉淀生成
2
(4)“冶炼”时,发生反应为铝还原Cr O ,铝热反应放出大量热,因此能量主要转化形式为化学能转化为
2 3
热能
(5)加NaOH调节pH后,溶液中Cr3++3OH-=Cr(OH) ↓,“氧化”时,发生反应的化学方程式为
3
2Cr(OH) +3NaClO+4NaOH=2Na CrO +3NaCl+5H O;
3 2 4 2
0.26mg/L10-3g/mg
(6)若废液中c(CrO2-)= =5×10-6mol/L,根据
4 52g/mol
K BaCrO 2.41010
c(Ba2+)= s
c
p
CrO2-
4 =
5106
mol/L=4.8×10-5molL-1,因此溶液中c(Ba2+)≥4.8×10-5molL-1,故答案为:
4
⋅ ⋅
≥4.8×10-5mol L-1;
(7)与还原⋅法相比,氧化法的优点为能耗低,故答案为:能耗低。
16.(10分)【答案】(1)206
(2)B
(3)< =
1
(4)H 反应 O gH gH Og是放热反应,升高温度,平衡逆向移动,H O的含量减小
2 2 2 2 2 2
1.9021.552
(5)
0.050.10V2
(6)6.4
【详解】(1)化学反应的反应热=反应物键能之和-生成物键能之和,CH (g)+H O(g) CO(g)+3H (g)
4 2 2
ΔH=413kJ/mol×4+467kJ/mol×2-1072kJ/mol-436kJ/mol×3=+206kJ/mol;
试卷第14页,共17页-------------------------------- 高途高中化学点睛卷 -----------------------------------
(2)A.使用催化剂平衡不移动,甲烷转化率不变,A错误;
B.该反应为吸热反应,升高温度平衡正向移动,甲烷转化率增大,B正确;
C.该反应为气体分子数增大的反应,加压平衡逆向移动,甲烷转化率减小,C错误;
D.恒容恒容增大甲烷和水蒸汽投料比,则甲烷浓度增大的较多,此时水的转化率变大,甲烷的转化率减
小,D错误;故选B;
(3)使用催化剂可以通过降低反应活化能提高化学反应速率,图示中使用催化剂1的反应速率快,活化
能更低,因此E S>Si
(2)金刚石、碳化硅、硅
原子的半径越小,其形成共价键键能越大,硅、金刚石和碳化硅晶体均为共价晶体,键能:碳碳键>碳硅
键>硅硅键,共价晶体的熔点高低与共价键键能有关,故从高到低依次为金刚石、碳化硅、硅。
(3)6 C原子电负性比O原子小,更容易给出孤电子对 sp3、sp
(4) 4 12
试卷第17页,共17页-------------------------------- 高途高中化学点睛卷 -----------------------------------
3 1 1
(5) 立方氮化硼晶体 ( , , )
4 4 4
【详解】(1)基态硫原子核外电子排布为1s22s22p63s23p4,电子共占用9个原子轨道,核外电子空间运动
状态有9种;同一周期从左到右第一电离能呈增大的趋势,但第VA族元素的第一电离能大于同周期相邻
元素,所以Si、P、S第一电离能由大到小的顺序是P>S>Si;
(2)原子的电子层数越多,其半径越大,即碳的原子半径小于硅;原子的半径越小,其形成共价键键能
越大,硅、金刚石和碳化硅晶体均为共价晶体,键能:碳碳键>碳硅键>硅硅键,共价晶体的熔点高低与
共价键键能有关,故从高到低依次为金刚石、碳化硅、硅。
(3)Mn的一种配合物化学式为[Mn(CO) (CH CN)]。
5 3
①由配合物化学式可知,配体有5个CO、1个CH CN,该配合物中锰原子的配位数为6;电负性越小,
3
越容易给出孤电子对,C的电负性小于O,配体CO中提供孤对电子的原子是C。
②②CH CN中甲基中C原子形成4个σ键,﹣CN中C原子形成2个σ键,CH CN中C原子的杂化类型为
3 3
sp3、sp。
(4)根据NiAs的晶胞结构图,Ni与相连的4个As原子成键,Ni的配位数是4;Ni紧邻的Ni原子数是
12。
(5)立方砷化镓晶体与立方氮化硼晶体都是共价晶体,原子半径越小,键能越大,熔沸点高,故熔点较
1 3 1 3 1 1
高的是立方氮化硼晶体;晶胞中原子1的坐标为( , , ),则原子3的坐标为( , , )。
4 4 4 4 4 4
试卷第18页,共17页