文档内容
2025 届高三 2 月综合练习
化学
(满分:100分 考试时间:75分钟)
可能用到的相对原子质量:H—1 C—12 N—14 O—16 P—31 K—39 Fe—56
一、 单项选择题:本题共13小题,每小题3分,共39分。每小题只有一个选项最符合题
意。
1.中国古代文房四宝笔墨纸砚中,其主要化学成分不属于高分子的是
A.制毛笔用的狼毫 B.墨条 C.宣纸 D.竹砚
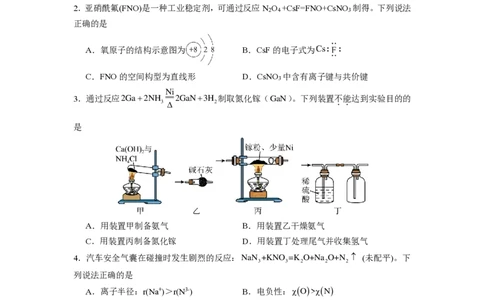
2.亚硝酰氟(FNO)是一种工业稳定剂,可通过反应N O +CsF=FNO+CsNO 制得。下列说法
2 4 3
正确的是
A.氧原子的结构示意图为 B.CsF的电子式为
C.FNO的空间构型为直线形 D.CsNO 中含有离子键与共价键
3
3.通过反应
2025届高三2月综合练习 化学 第1页,共8页
2 G a + 2 N H
3
N
i
2 G a N + 3 H
2
制取氮化镓( G a N )。下列装置不能达到实验目的的
..
是
A.用装置甲制备氨气 B.用装置乙干燥氨气
C.用装置丙制备氮化镓 D.用装置丁处理尾气并收集氢气
4.汽车安全气囊在碰撞时发生剧烈的反应: N a N
3
+ K N O
3
= K
2
O + N a
2
O + N
2
(未配平)。下
列说法正确的是
A.离子半径:r(Na+)>r(N3-) B.电负性:χ(O)>χ(N)
C.第一电离能:I (O)<I (Na) D.碱性:KOH<NaOH
1 1
5.下列物质的结构与性质或性质与用途不具有对应关系的是
A.HI晶体中范德华力较弱,HI分子稳定性较弱
B.浓硫酸具有吸水性,可用于干燥二氧化硫
C.甲醛水溶液可使蛋白质变性,福尔马林用于标本制作
D.ClO 具有强氧化性,可用于自来水消毒
2
{#{QQABLQIUggAAAABAAQhCQQFiCgOQkBACCYoOhBAcMAABwRNABAA=}#}阅读以下材料,完成6~7小题:
硫元素可形成多种化合物。
2025届高三2月综合练习 化学 第2页,共8页
H
2
S 、二硫化氢 ( H
2
S
2
) 均有弱酸性, H
2
S 的燃烧热为
5 1 8 k J / m o l 。硫化物可以除去废水中的重金属离子。Na S O 可以除去漂白液中的余氯
2 2 3
( C l
2
) ,
也可以与 I
2
反应生成氧化性较弱的 N a
2
S
4
O
6
。工业上煅烧黄铜矿(CuFeS )可得粗铜,再
2
通过电解精炼可得纯铜。
6.下列说法正确的是
A. H
2
S
2
为非极性分子
B.从物质结构的角度分析, S
4
O 2−6 的结构可能如图所示
C. H
2
S
2
沸点高于 H
2
S ,是因为 H
2
S
2
可形成分子间氢键
D.电解精炼粗铜,每转移0.2mol电子,阳极上溶解 0 .1 m o lC u
7.下列说法正确的是
A.H S燃烧的热化学方程式:
2
2 H
2
S ( g ) + 3 O
2
( g ) = 2 S O
2
( g ) + 2 H
2
O ( g ) Δ H = − 5 1 8 k J / m o l
B.使用 F e S 除去废水中汞离子: S 2 − + H g 2 + = H g S
C.实验室探究浓硫酸的性质: C u + 2 H
2
S O
4
(浓) CuSO +SO ↑+2H O
4 2 2
D.用 N a
2
S
2
O
3
除去余氯: N a
2
S
2
O
3
+ 4 C l
2
+ 5 H
2
O = 2 S O 24 − + 8 C l − + 2 N a + + 1 0 H +
8.间接电化学法处理NO的工作原理如图所示。
下列说法不正确的是
...
A.电极b与电源的正极相连
B.电极a的电极反应式:
2HSO−+2e− =S O2−+2OH−
3 2 4
C.电解一段时间后,b极区 N a
2
S O
4
的浓度增大
D.每处理标况下 1 1 .2 L N O ,理论上有 1 m o lH + 通过质子交换膜
9.“碳达峰·碳中和”是我国社会发展的重大战略之一,CH 还原CO 是实现“双碳”经济
4 2
的有效途径之一,相关主要反应有:
Ⅰ:CH (g)+CO (g)⇌ 2CO(g)+2H (g) ΔH =+247kJ/mol,K
4 2 2 1 1
Ⅱ:CO (g)+H (g)⇌ CO(g)+H O(g) ΔH =+41kJ/mol,K
2 2 2 2 2
下列说法正确的是
A.反应Ⅰ的平衡常数K =
1
c
c
( C
2 (
H
C
4O
)
)
c
c
( C
2 (
O
H
)
2)
2
B.反应Ⅱ的ΔS<0
C.有利于提高CO 平衡转化率的条件是高温低压
2
D.该工艺每转化0.2mol CO 可获得0.4molCO
2
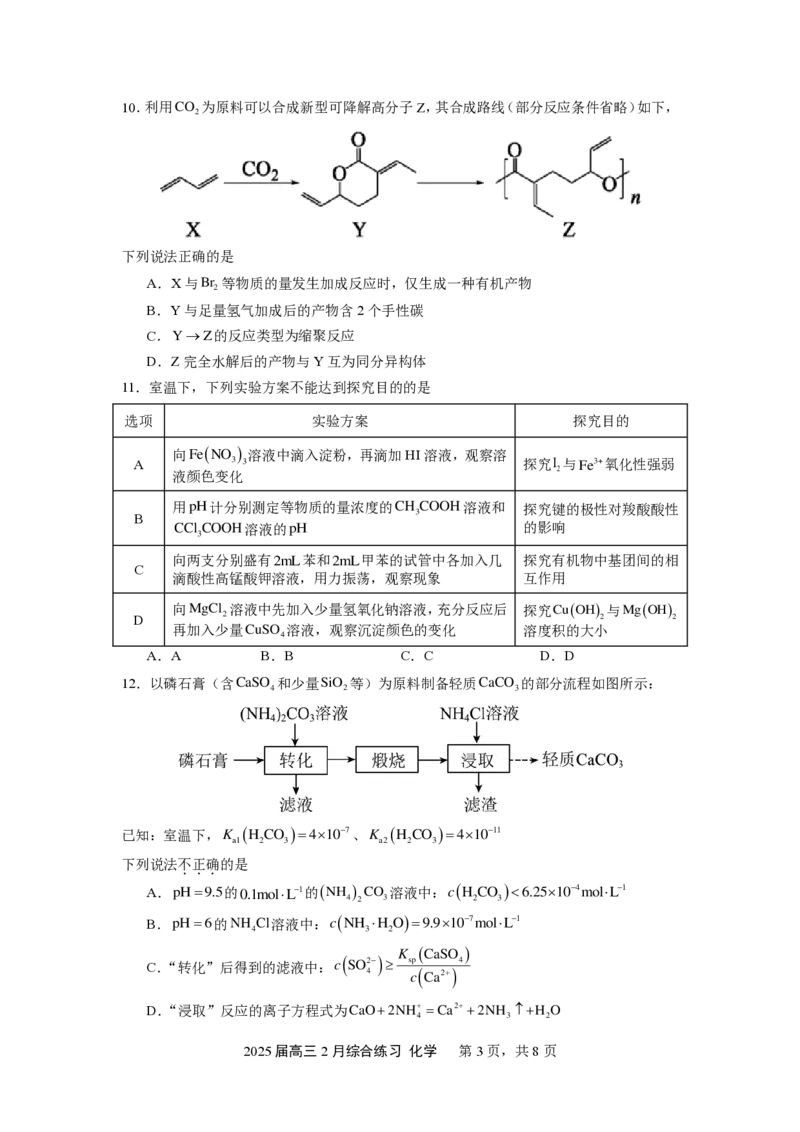
{#{QQABLQIUggAAAABAAQhCQQFiCgOQkBACCYoOhBAcMAABwRNABAA=}#}10.利用
2025届高三2月综合练习 化学 第3页,共8页
C O
2
为原料可以合成新型可降解高分子Z,其合成路线(部分反应条件省略)如下,
下列说法正确的是
A.X与Br 等物质的量发生加成反应时,仅生成一种有机产物
2
B.Y与足量氢气加成后的产物含2个手性碳
C. Y → Z 的反应类型为缩聚反应
D.Z完全水解后的产物与Y互为同分异构体
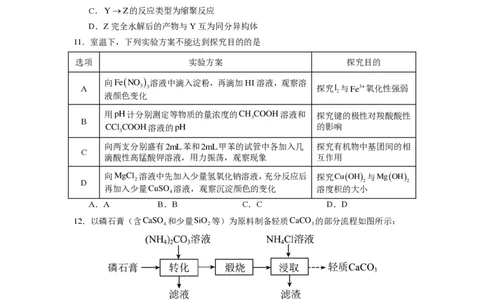
11.室温下,下列实验方案不能达到探究目的的是
选项 实验方案 探究目的
向
A
F e ( N O
3
)
3
溶液中滴入淀粉,再滴加HI溶液,观察溶
探究
液颜色变化
I
2
与Fe3+氧化性强弱
用
B
p H 计分别测定等物质的量浓度的 C H
3
C O O H 溶液和
C C l3 C O O H
探究键的极性对羧酸酸性
溶液的pH 的影响
向两支分别盛有
C
2 m L 苯和 2 m L 甲苯的试管中各加入几 探究有机物中基团间的相
滴酸性高锰酸钾溶液,用力振荡,观察现象 互作用
向
D
M g C l
2
溶液中先加入少量氢氧化钠溶液,充分反应后
再加入少量 C u S O
4
探究
溶液,观察沉淀颜色的变化
C u ( O H )
2
与 M g ( O H )
2
溶度积的大小
A.A B.B C.C D.D
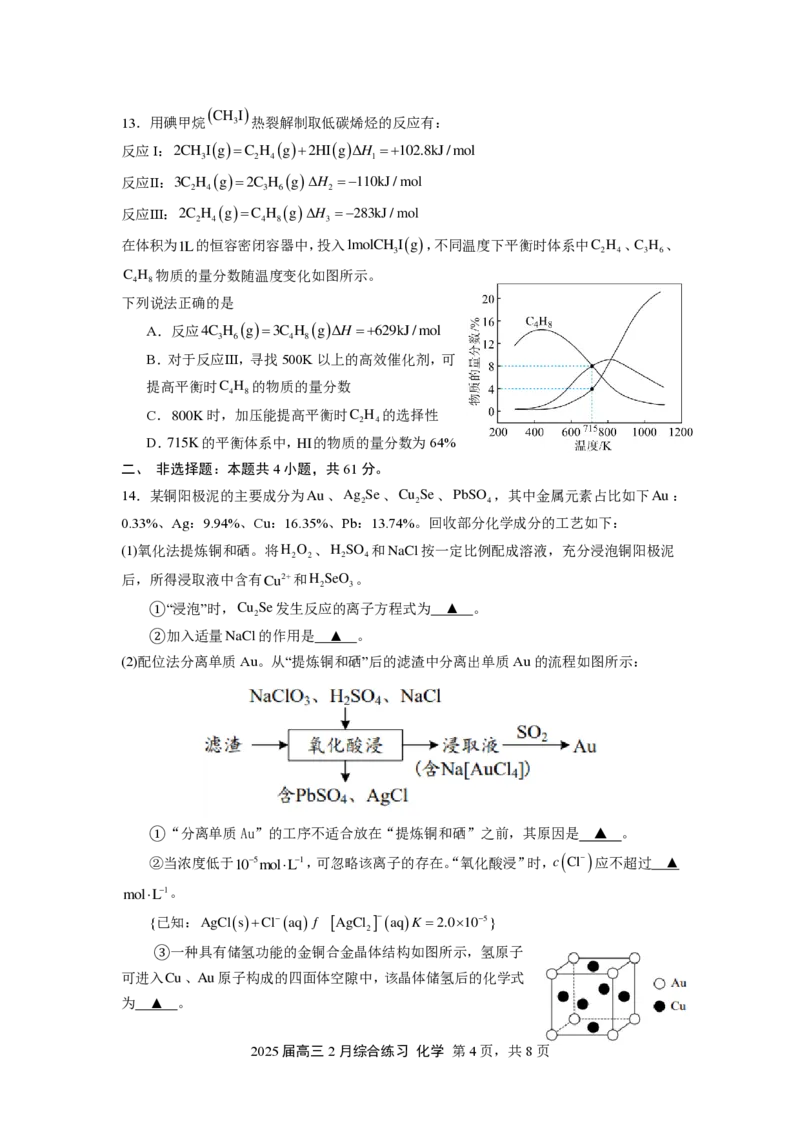
12.以磷石膏(含 C a S O
4
和少量 S iO
2
等)为原料制备轻质 C a C O
3
的部分流程如图所示:
已知:室温下, K
a1
( H
2
C O
3
) = 4 1 0 − 7 、K (H CO )=410−11
a2 2 3
下列说法不正确的是
...
A. p H = 9 .5 的0.1molL−1的(NH ) CO 溶液中:
4 2 3
c ( H
2
C O
3
) 6 .2 5 1 0 − 4 m o l L − 1
B.pH=6的NH Cl溶液中:c(NH H O)=9.910−7molL−1
4 3 2
K (CaSO )
C.“转化”后得到的滤液中:c ( SO2−) sp 4
4 c ( Ca2+)
D.“浸取”反应的离子方程式为CaO+2NH+ =Ca2++2NH +H O
4 3 2
{#{QQABLQIUggAAAABAAQhCQQFiCgOQkBACCYoOhBAcMAABwRNABAA=}#}13.用碘甲烷
2025届高三2月综合练习 化学 第4页,共8页
( C H
3
I )
热裂解制取低碳烯烃的反应有:
反应I: 2 C H
3
I ( g ) = C
2
H
4
( g ) + 2 H I ( g ) Δ H
1
= + 1 0 2 .8 k J / m o l
反应Ⅱ: 3 C
2
H
4
( g ) = 2 C
3
H
6
( g ) H
2
= − 1 1 0 k J / m o l
反应Ⅲ: 2 C
2
H
4
( g ) = C
4
H
8
( g ) H
3
= − 2 8 3 k J / m o l
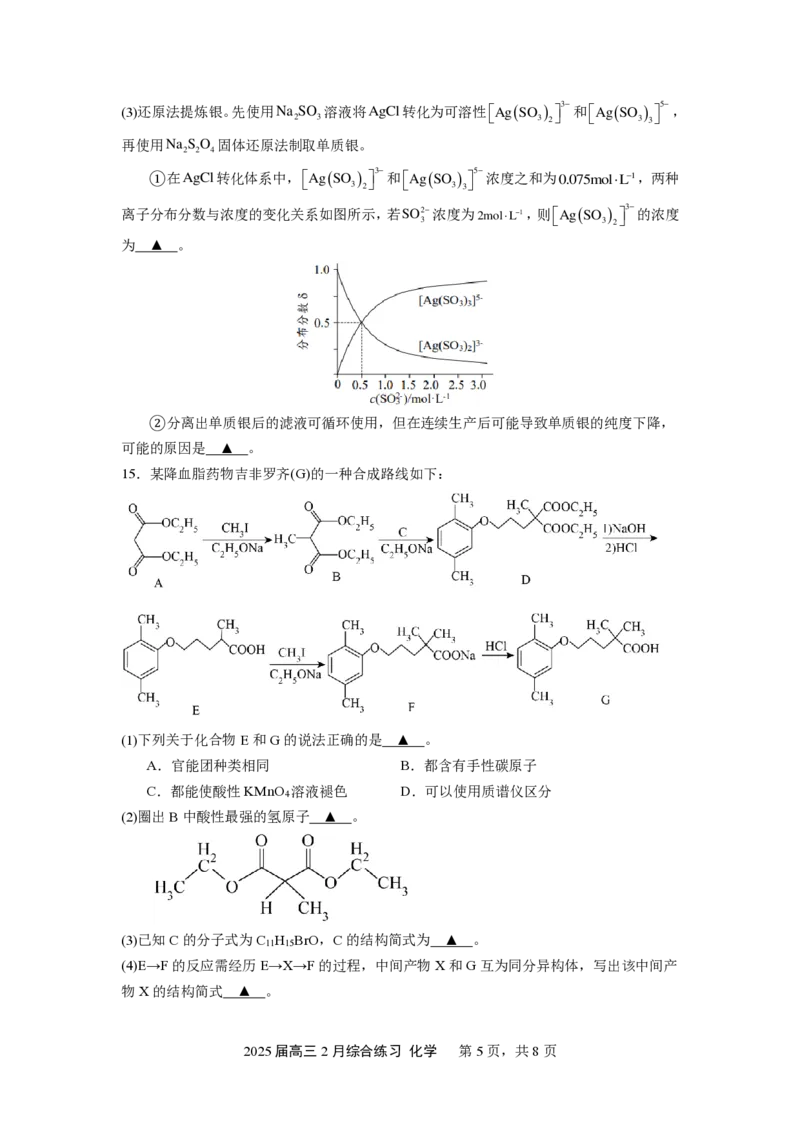
在体积为 1 L 的恒容密闭容器中,投入 1 m o lC H
3
I ( g ) ,不同温度下平衡时体系中C H 、C H 、
2 4 3 6
C
4
H
8
物质的量分数随温度变化如图所示。
下列说法正确的是
A.反应 4 C
3
H
6
( g ) = 3 C
4
H
8
( g ) Δ H = + 6 2 9 k J / m o l
B.对于反应Ⅲ,寻找500K以上的高效催化剂,可
提高平衡时 C
4
H
8
的物质的量分数
C. 8 0 0 K 时,加压能提高平衡时C H 的选择性
2 4
D. 7 1 5 K 的平衡体系中,HI的物质的量分数为64%
二、 非选择题:本题共4小题,共61分。
14.某铜阳极泥的主要成分为 A u 、 A g
2
S e 、 C u
2
S e 、 P b S O
4
,其中金属元素占比如下 A u :
0.33%、Ag:9.94%、Cu:16.35%、Pb:13.74%。回收部分化学成分的工艺如下:
(1)氧化法提炼铜和硒。将H O 、
2 2
H
2
S O
4
和 N a C l 按一定比例配成溶液,充分浸泡铜阳极泥
后,所得浸取液中含有 C u 2 + 和H SeO 。
2 3
①“浸泡”时, C u
2
S e 发生反应的离子方程式为 ▲ 。
②加入适量 N a C l 的作用是 ▲ 。
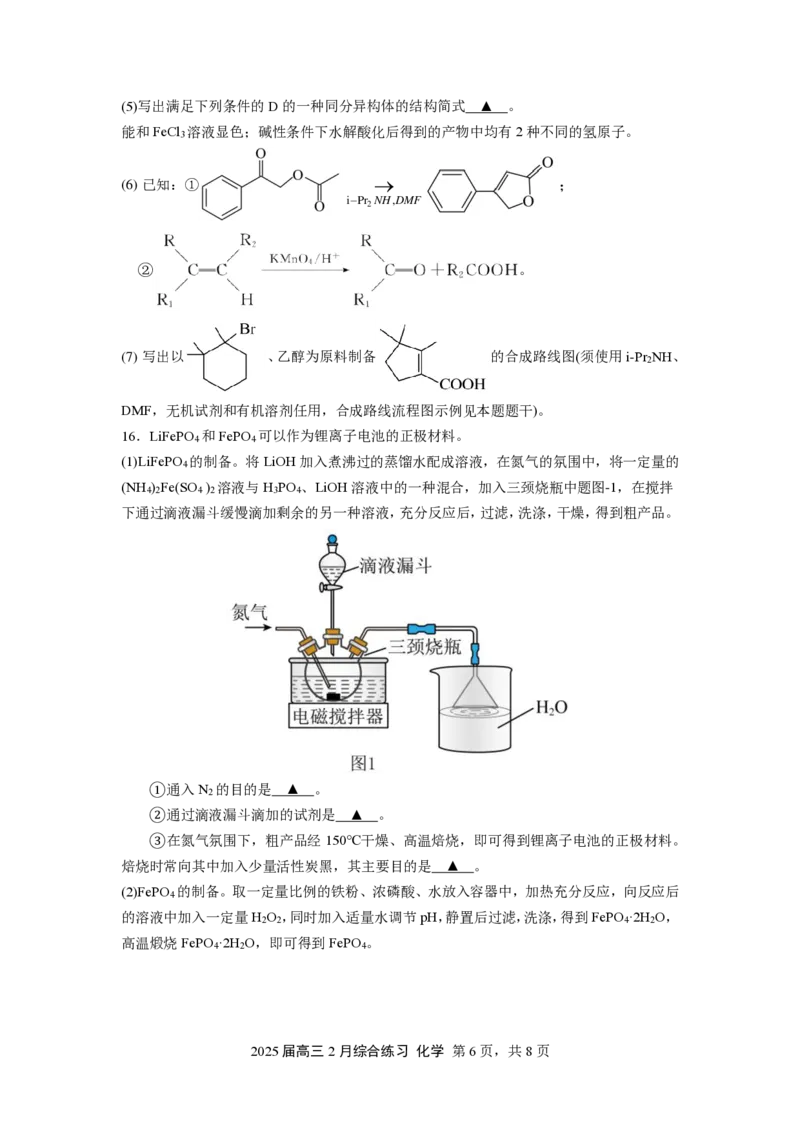
(2)配位法分离单质Au。从“提炼铜和硒”后的滤渣中分离出单质Au的流程如图所示:
①“分离单质Au”的工序不适合放在“提炼铜和硒”之前,其原因是 ▲ 。
②当浓度低于10−5molL−1,可忽略该离子的存在。“氧化酸浸”时, c ( C l − ) 应不超过 ▲
m o l L − 1 。
{已知: A g C l ( s ) + C l − ( a q ) ƒ A g C l
2
− ( a q ) K = 2 .0 1 0 − 5 }
③一种具有储氢功能的金铜合金晶体结构如图所示,氢原子
可进入Cu、Au原子构成的四面体空隙中,该晶体储氢后的化学式
为 ▲ 。
{#{QQABLQIUggAAAABAAQhCQQFiCgOQkBACCYoOhBAcMAABwRNABAA=}#}(3)还原法提炼银。先使用
2025届高三2月综合练习 化学 第5页,共8页
N a
2
S O
3
溶液将AgCl转化为可溶性 A g ( S O
3
)
2
3 − 和 A g ( S O
3
)
3
5 − ,
再使用 N a
2
S
2
O
4
固体还原法制取单质银。
①在AgCl转化体系中, A g ( S O
3
)
2
3 − 和 A g ( S O
3
)
3
5 − 浓度之和为0.075molL−1,两种
离子分布分数与浓度的变化关系如图所示,若 S O 23 − 浓度为 2 m o l L −1 ,则 A g ( S O
3
)
2
3 − 的浓度
为 ▲ 。
②分离出单质银后的滤液可循环使用,但在连续生产后可能导致单质银的纯度下降,
可能的原因是 ▲ 。
15.某降血脂药物吉非罗齐(G)的一种合成路线如下:
(1)下列关于化合物E和G的说法正确的是 ▲ 。
A.官能团种类相同 B.都含有手性碳原子
C.都能使酸性KMnO 溶液褪色 D.可以使用质谱仪区分
4
(2)圈出B中酸性最强的氢原子 ▲ 。
(3)已知C的分子式为C H BrO,C的结构简式为 ▲ 。
11 15
(4)E→F的反应需经历E→X→F的过程,中间产物X和G互为同分异构体,写出该中间产
物X的结构简式 ▲ 。
{#{QQABLQIUggAAAABAAQhCQQFiCgOQkBACCYoOhBAcMAABwRNABAA=}#}(5)写出满足下列条件的D的一种同分异构体的结构简式 ▲ 。
能和FeCl 溶液显色;碱性条件下水解酸化后得到的产物中均有2种不同的氢原子。
3
(6) 已知:①
2025届高三2月综合练习 化学 第6页,共8页
i− P r2
→N
H ,D M F
;
② 。
(7) 写出以 、乙醇为原料制备 的合成路线图(须使用i-Pr NH、
2
DMF,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
16.LiFePO 和FePO 可以作为锂离子电池的正极材料。
4 4
(1)LiFePO 的制备。将LiOH加入煮沸过的蒸馏水配成溶液,在氮气的氛围中,将一定量的
4
(NH ) Fe(SO ) 溶液与H PO 、LiOH溶液中的一种混合,加入三颈烧瓶中题图-1,在搅拌
4 2 4 2 3 4
下通过滴液漏斗缓慢滴加剩余的另一种溶液,充分反应后,过滤,洗涤,干燥,得到粗产品。
①通入N 的目的是 ▲ 。
2
②通过滴液漏斗滴加的试剂是 ▲ 。
③在氮气氛围下,粗产品经150℃干燥、高温焙烧,即可得到锂离子电池的正极材料。
焙烧时常向其中加入少量活性炭黑,其主要目的是 ▲ 。
(2)FePO 的制备。取一定量比例的铁粉、浓磷酸、水放入容器中,加热充分反应,向反应后
4
的溶液中加入一定量H O ,同时加入适量水调节pH,静置后过滤,洗涤,得到FePO ·2H O,
2 2 4 2
高温煅烧FePO ·2H O,即可得到FePO 。
4 2 4
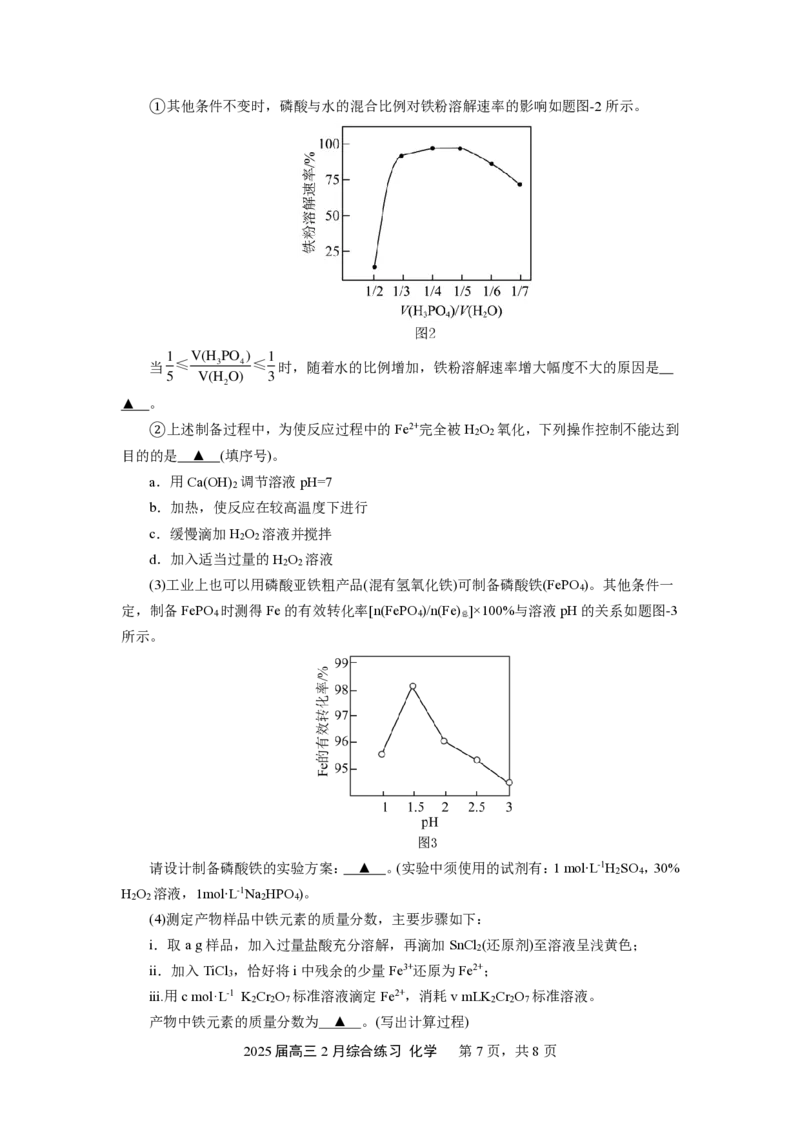
{#{QQABLQIUggAAAABAAQhCQQFiCgOQkBACCYoOhBAcMAABwRNABAA=}#}①其他条件不变时,磷酸与水的混合比例对铁粉溶解速率的影响如题图-2所示。
当
2025届高三2月综合练习 化学 第7页,共8页
1
5
≤
V (
V
H
(
3H
P
2
O
O
4)
)
≤
1
3
时,随着水的比例增加,铁粉溶解速率增大幅度不大的原因是
▲ 。
②上述制备过程中,为使反应过程中的Fe2+完全被H O 氧化,下列操作控制不能达到
2 2
目的的是 ▲ (填序号)。
a.用Ca(OH) 调节溶液pH=7
2
b.加热,使反应在较高温度下进行
c.缓慢滴加H O 溶液并搅拌
2 2
d.加入适当过量的H O 溶液
2 2
(3)工业上也可以用磷酸亚铁粗产品(混有氢氧化铁)可制备磷酸铁(FePO )。其他条件一
4
定,制备FePO 时测得Fe的有效转化率[n(FePO )/n(Fe) ]×100%与溶液pH的关系如题图-3
4 4 总
所示。
请设计制备磷酸铁的实验方案: ▲ 。(实验中须使用的试剂有:1 mol∙L-1H SO ,30%
2 4
H O 溶液,1mol∙L-1Na HPO )。
2 2 2 4
(4)测定产物样品中铁元素的质量分数,主要步骤如下:
i.取a g样品,加入过量盐酸充分溶解,再滴加SnCl (还原剂)至溶液呈浅黄色;
2
ii.加入TiCl ,恰好将i中残余的少量Fe3+还原为Fe2+;
3
ⅲ.用c mol·L-1 K Cr O 标准溶液滴定Fe2+,消耗v mLK Cr O 标准溶液。
2 2 7 2 2 7
产物中铁元素的质量分数为 ▲ 。(写出计算过程)
{#{QQABLQIUggAAAABAAQhCQQFiCgOQkBACCYoOhBAcMAABwRNABAA=}#}17. (15分)储能材料是当前研究的热点。
(1) AlH 易分解反应释氢,且可与固体氧化物混合作固体燃料推进剂。AlH 与Fe O 的反应
3 3 2 3
过程如下:
Ⅰ. AlH (s)===Al(s)+3H(g);ΔH=521.1 kJ·mol-1
3
Ⅱ. 6H(g)+Fe O (s)===2Fe(s)+3H O(g);ΔH=-1 209.2 kJ·mol-1
2 3 2
Ⅲ. 2Al(s)+Fe O (s)===Al O (s)+2Fe(s);ΔH=-851.5 kJ·mol-1
2 3 2 3
① LiAlH 和 AlCl 在无水乙醚中反应可以生成 AlH 和 LiCl,该反应的化学方程式为
4 3 3
▲ 。
② 反应2AlH (s)+2Fe O (s)===4Fe(s)+3H O(g)+Al O (s)的ΔH= ▲ 。
3 2 3 2 2 3
③ AlH 与普通铝粉相比,AlH 与Fe O 反应更容易引发的原因是 ▲ 。
3 3 2 3
(2) NaBH 是一种储氢材料,CoB 催化剂催化 NaBH 释氢的原理是 OH-使催化剂表面的
4 4
BH- 释放H-,催化剂表面的H-与H+结合生成H (Co容易吸附阴离子)。在CoB催化剂中
4 2
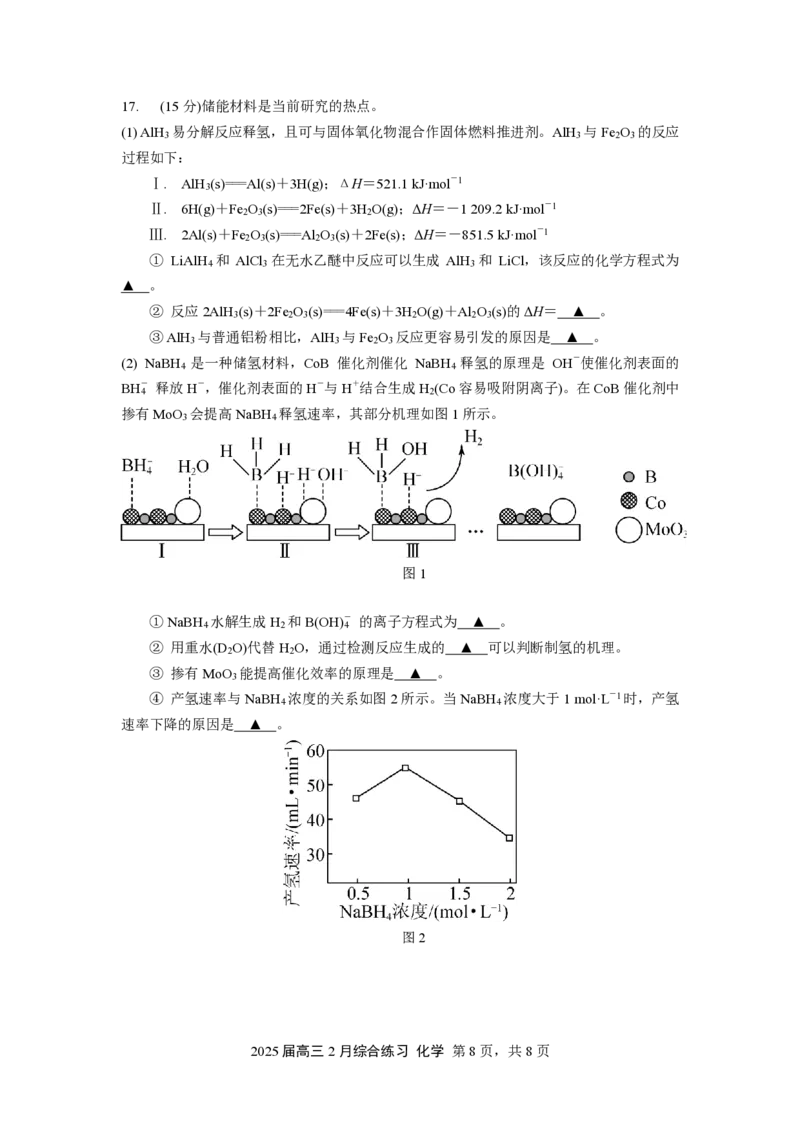
掺有MoO 会提高NaBH 释氢速率,其部分机理如图1所示。
3 4
图1
① NaBH 水解生成H 和B(OH)- 的离子方程式为 ▲ 。
4 2 4
② 用重水(D O)代替H O,通过检测反应生成的 ▲ 可以判断制氢的机理。
2 2
③ 掺有MoO 能提高催化效率的原理是 ▲ 。
3
④ 产氢速率与NaBH 浓度的关系如图2所示。当NaBH 浓度大于1 mol·L-1时,产氢
4 4
速率下降的原因是 ▲ 。
图2
2025届高三2月综合练习 化学 第8页,共8页
{#{QQABLQIUggAAAABAAQhCQQFiCgOQkBACCYoOhBAcMAABwRNABAA=}#}2025届高三下学期化学综合练习一
参考答案
题号 1 2 3 4 5 6 7 8 9 10
答案 B D D B A B C B C B
题号 11 12 13
答案 A C D
14.(15分)
(1)
答案第1页,共2页
C u
2
S e + 4 H
2
O
2
+ 4 H + = 2 C u 2 + + H
2
S e O
3
+ 5 H
2
O (2分)
使银元素转化为AgCl沉淀(2分)
(2) 单质金的含量较低,会被包裹在内部,在提取金之前要先脱铜(2分) 0.5(2分)
H
8
A u C u
3
(2分)
(3) 0 .0 1 5 m o l L − 1 (3分) Na SO 的浓度逐渐增大,会伴有晶体析出(2分)
2 3
15.(15分)
(1)ACD(3分)
(2) (1分)
(3) (2分)
(4) (2分)
(5) (2分)
{#{QQABLQIUggAAAABAAQhCQQFiCgOQkBACCYoOhBAcMAABwRNABAA=}#}(6)
(5分)
16.(16分)
(1)排除装置中的氧气,防止
答案第2页,共2页
F e 2 + 被氧化(2分) LiOH(2分)
改善成型后 L iF e P O
4
的导电性能(2分)
(2) ①当
1
5
≤
V (
V
H
(
3H
P
2
O
O
4)
)
≤
1
3
时,随着水的比例增加, H
3
P O
4
的浓度变稀,使c(H+)减小,
使反应速率减慢,同时反应放热能加快反应速率,前者对反应速率的影响略大于后者(2分)
②ab(2分)
(3) ③边搅拌边向磷酸亚铁粗产品中加入 1 m o l L − 1 H
2
S O
4
至完全溶解(1分),向溶液中加
入足量的 3 0 % H
2
O
2
溶液充分反应(1分),边搅拌边逐滴加入 1 m o l L − 1 N a
2
H P O
4
溶液至溶液 p H
约为 1 .5 (1分),充分反应至沉淀不再产生,过滤、洗涤、干燥(1分) (共4分) ④Cr O
2
27 −
+6Fe2++14H+=2Cr3++6Fe3++7H O
2
则由题可得如下转化关系: 6 F e 3 + : 6 F e 2 + : C r2 O 27 - ,Cr O
2
27 − 的物质的量为
c m o l/L V 1 0 − 3 L = 1 0 − 3 c V m o l ,则产物中铁元素的质量分数为
1 0 − 3 c V m o l
a
6
g
5 6 g / m o l
1 0 0 % =
3 3 .6
a
c V
% 。(2分)
17. (15分)
(1) ① 3LiAlH +AlCl ===4AlH +3LiCl(2分)
4 3 3
② -1 018.5 kJ·mol-1(2分)
③ AlH 分解得到活性 H 与 Fe O 反应大量放热引发铝热反应Ⅲ;AlH 分解得到Al更
3 2 3 3
容易与Fe O 反应(颗粒小、无氧化膜)(3分)
2 3
(2) ① BH- +4H O===B(OH)- +4H ↑(2分)
4 2 4 2
② HD、B(OD)- (2分)
4
③ MoO 促进H O的电离产生H+和OH-(2分)
3 2
④ BH- 浓度过大,吸附在Co上,减少H-的吸附(2分)
4
{#{QQABLQIUggAAAABAAQhCQQFiCgOQkBACCYoOhBAcMAABwRNABAA=}#}