文档内容
专题85 物质检验与鉴别
1.【2023年山东卷】鉴别浓度均为 的 、 三种溶液,仅用下列一种
方法不可行的是
A.测定溶液 B.滴加酚酞试剂
C.滴加 溶液 D.滴加饱和 溶液
【答案】C
【解析】A. 溶液显弱碱性, 溶液显强碱性, 溶液显酸性,则测定溶液 是可
以鉴别出来的,故A不符合题意;B. 溶液显弱碱性,滴入酚酞先变红后褪色, 溶液
显强碱性,滴入酚酞溶液,显红色, 溶液显酸性,滴入酚酞不变色,则滴加酚酞试剂是可
以鉴别出来的,故B不符合题意;C. 溶液滴入碘化钾溶液,发生氧化还原反应生成碘,液面
会由无色变成黄色,振荡后会变成无色,而 溶液, 溶液滴入碘化钾溶液后,因不
与两者反应而没有现象,则仅用滴加 溶液无法鉴别,则C符合题意;D.饱和 溶
液和 溶液不反应,和 溶液反应生成碳酸钡沉淀,和 溶液发生双水解反应生
成沉淀和气体,则滴入饱和 溶液是可以鉴别出来的,故D不符合题意;答案C。
2.(2021·海南真题)一次性鉴别等浓度的 、 、 三种溶液,下列方法不可行的是
A.测定 B.焰色试验
C.滴加 溶液 D.滴加饱和 溶液,微热
【答案】C
【解析】A. 溶液显中性, 溶液显酸性, 溶液显碱性,故可以用测定pH的方法鉴别,
故A正确;B. 的焰色试验中现象为透过蓝色钴玻璃为紫色, 的焰色试验中无现象,
的焰色试验中现象为黄色,故可以用焰色试验的方法鉴别,故B正确;C. 、 、
中只有 能与 反应有现象,故 和 不能鉴别,故C错误;D.2 +
CaCl2+2NH +2H O有刺激性气味气体产生, + =CaCO +2NaOH有白色沉
3 2 3
淀产生,而 不反应无现象,故可以鉴别,故D正确;故选C。
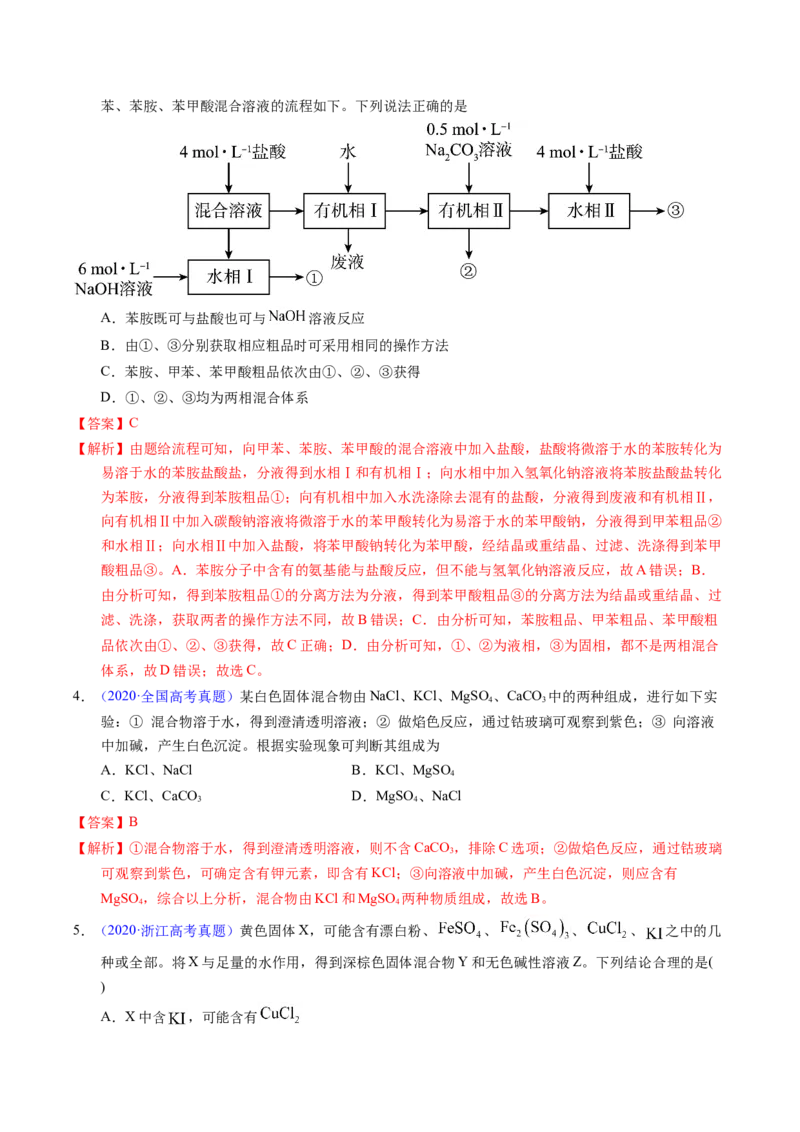
3.【2022年山东卷】已知苯胺(液体)、苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。实验室初步分离甲苯、苯胺、苯甲酸混合溶液的流程如下。下列说法正确的是
A.苯胺既可与盐酸也可与 溶液反应
B.由①、③分别获取相应粗品时可采用相同的操作方法
C.苯胺、甲苯、苯甲酸粗品依次由①、②、③获得
D.①、②、③均为两相混合体系
【答案】C
【解析】由题给流程可知,向甲苯、苯胺、苯甲酸的混合溶液中加入盐酸,盐酸将微溶于水的苯胺转化为
易溶于水的苯胺盐酸盐,分液得到水相Ⅰ和有机相Ⅰ;向水相中加入氢氧化钠溶液将苯胺盐酸盐转化
为苯胺,分液得到苯胺粗品①;向有机相中加入水洗涤除去混有的盐酸,分液得到废液和有机相Ⅱ,
向有机相Ⅱ中加入碳酸钠溶液将微溶于水的苯甲酸转化为易溶于水的苯甲酸钠,分液得到甲苯粗品②
和水相Ⅱ;向水相Ⅱ中加入盐酸,将苯甲酸钠转化为苯甲酸,经结晶或重结晶、过滤、洗涤得到苯甲
酸粗品③。A.苯胺分子中含有的氨基能与盐酸反应,但不能与氢氧化钠溶液反应,故A错误;B.
由分析可知,得到苯胺粗品①的分离方法为分液,得到苯甲酸粗品③的分离方法为结晶或重结晶、过
滤、洗涤,获取两者的操作方法不同,故B错误;C.由分析可知,苯胺粗品、甲苯粗品、苯甲酸粗
品依次由①、②、③获得,故C正确;D.由分析可知,①、②为液相,③为固相,都不是两相混合
体系,故D错误;故选C。
4.(2020·全国高考真题)某白色固体混合物由NaCl、KCl、MgSO 、CaCO 中的两种组成,进行如下实
4 3
验:① 混合物溶于水,得到澄清透明溶液;② 做焰色反应,通过钴玻璃可观察到紫色;③ 向溶液
中加碱,产生白色沉淀。根据实验现象可判断其组成为
A.KCl、NaCl B.KCl、MgSO
4
C.KCl、CaCO D.MgSO 、NaCl
3 4
【答案】B
【解析】①混合物溶于水,得到澄清透明溶液,则不含CaCO ,排除C选项;②做焰色反应,通过钴玻璃
3
可观察到紫色,可确定含有钾元素,即含有KCl;③向溶液中加碱,产生白色沉淀,则应含有
MgSO ,综合以上分析,混合物由KCl和MgSO 两种物质组成,故选B。
4 4
5.(2020·浙江高考真题)黄色固体X,可能含有漂白粉、 、 、 、 之中的几
种或全部。将X与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论合理的是(
)
A.X中含 ,可能含有B.X中含有漂白粉和
C.X中含有 ,Y中含有
D.用 酸化溶液Z,若有黄绿色气体放出,说明X中含有
【答案】C
【解析】固体X为黄色,则含有Fe (SO ),溶于水后,要使溶液Z为无色碱性,则一定含有漂白粉,且漂
2 4 3
白粉过量,得到深棕色固体混合物Y,则固体Y是Fe(OH) 和Cu(OH) 的混合物,X中一定含有
3 2
, 和 中含有其中一种或两种都含,据此解答。A.若X含有KI,则会与漂
白粉反应生成I,溶液不为无色,A不正确;B.由分析可知,不一定含有FeSO ,B不正确;C.由
2 4
分析可知, X含有CuCl ,Y含有Fe(OH) ,C正确;D.酸化后,产生黄绿色气体,为氯气,则发生
2 3
的发生反应的离子反应方程式为:Cl-+ClO-+2H+=Cl↑+H O,此时的Cl-有可能来自于漂白粉氧化FeSO
2 2 4
产生的Cl-,也有可能是漂白粉自身含有的,不能推导出含有CuCl ,D不正确;故选C。
2
6.(2019·浙江高考真题)白色固体混合物A,含有KCl、CaCO 、NaCO、NaSiO、CuSO 中的几种,
3 2 3 2 3 4
常温常压下进行如下实验。
下列推断不正确的是
A.无色溶液B的pH≥7
B.白色固体F的主要成分是HSiO
2 3
C.混合物A中有NaSiO、CuSO 和CaCO
2 3 4 3
D.在无色溶液B中加HNO 酸化,无沉淀;再滴加AgNO,若有白色沉淀生成,说明混合物A中有
3 3
KCl
【答案】C
【解析】白色固体混合物A加水得无色溶液B和固体C,B中肯定不含Cu2+,但结合固体C加过量硝酸,
产生蓝色溶液,说明A到B的过程中Cu2+转化为沉淀,A中必含有CuSO ,又结合固体C中加过量硝
4
酸后得到白色固体F,说明A中必含有NaSiO,而且固体C与硝酸反应可得无色气体,该气体只能
2 3
是CO,可能是CaCO 和硝酸反应,也可能是Cu2+和CO2-双水解得到的碱式碳酸铜与硝酸反应生成的,
2 3 3
因此,不能确定碳酸钙和碳酸钠是否一定存在,但两者至少存在一种。A.无色溶液B成分复杂,若
B中只含有KCl,则 pH=7;若含有NaCO 或硅酸钠或两者均有,则CO2-和硅酸根离子水解使溶液显
2 3 3
碱性,pH>7,故无色溶液pH≥7,正确;B.白色固体F难溶于硝酸,说明F为HSiO,正确;C.固
2 3
体C加入硝酸得无色气体,该气体只能是CO,可能是CaCO 生成的,也可能是NaCO 与硫酸铜反
2 3 2 3
应生成的碱式碳酸铜再与硝酸反应生成的CO,因此,固体C中不一定含有CaCO ,错误;D.检验
2 3
Cl-可用硝酸酸化的AgNO 溶液,所以证明A含有KCl,证明Cl-即可,正确。故答案选C。
3
7.(2019·上海高考真题)能证明亚硫酸钠样品部分变质的试剂是A.硝酸钡,稀硫酸 B.稀盐酸,氯化钡
C.稀硫酸,氯化钡 D.稀硝酸,氯化钡
【答案】B
【解析】在空气中,亚硫酸钠易被氧化成硫酸钠。证明亚硫酸钠样品部分变质,须检验样品中的亚硫酸根
和硫酸根。A.样品溶液中加入稀硫酸生成刺激性气味的气体,可证明有亚硫酸根,但引入硫酸根会
干扰硫酸根的检验。酸性溶液中,硝酸钡溶液中硝酸根会将亚硫酸根氧化为硫酸根,错误;B.样品
溶液中加入过量稀盐酸,生成刺激性气味的气体,可检出亚硫酸根。再滴入氯化钡溶液有白色沉淀生
成,证明有硫酸根离子,正确;C.样品溶液中加入稀硫酸,可检出亚硫酸根,但引入的硫酸根会干
扰硫酸根检验,错误;D.稀硝酸能将亚硫酸根氧化为硫酸根,干扰硫酸根检验,错误。本题选B。
8.(2019·海南高考真题)实验室通过称量 样品受热脱水前后的质量来测定x值,下列情
况会导致测定值偏低的是( )
A.实验前试样未经干燥 B.试样中含有少量碳酸氢铵
C.试样中含有少量氯化钠 D.加热过程中有试样迸溅出来
【答案】C
【解析】A.实验前试样未经干燥,加热后剩余固体质量偏少,导致结晶水含量偏高,A不符合题意;B.
试样中含有少量碳酸氢铵,碳酸氢铵受热分解成氨气、二氧化碳和水,加热分解后剩余固体质量偏少,
导致结晶水含量偏高,B不符合题意;C.试样中含有少量氯化钠,氯化钠受热不分解,加热分解后
剩余固体质量偏大,导致结晶水的含量偏低,C符合题意;D.加热过程中有试样迸溅出来,加热分
解后剩余固体质量偏少,会使结晶水的质量偏高,导致结晶水的含量偏高,D不符合题意;故合理选
项是C。
9.(2019·浙江高考真题)下列说法不正确的是
A.蒸馏时可通过加碎瓷片防暴沸
B.可用精密pH试纸区分pH=5.1和pH=5.6的两种NH Cl溶液
4
C.用加水后再分液的方法可将苯和四氯化碳分离
D.根据燃烧产生的气味,可区分棉纤绵和蛋白质纤维
【答案】C
【解析】A.加热液体至沸腾时,必须要在反应容器内加碎瓷片,防止暴沸,否则出现暴沸将会很危险,
正确;B.精密pH试纸可以将pH值精确到小数点后一位,所以可以区分pH=5.1和pH=5.6的两种
NH Cl溶液,正确;C.苯和四氯化碳互相溶解,均难溶于水,因而加水不影响苯和四氯化碳的互溶
4
体系,不可以分液,可采用蒸馏分离,错误;D.棉纤绵成分是纤维素,蛋白质纤维成分是蛋白质,
蛋白质燃烧时会产生烧焦羽毛的气味,因而可以用燃烧法区别,正确。故答案选C。
10.(2018·浙江高考真题)下列实验合理的是
A.用湿润的pH试纸测定CHCOONa溶液的pH
3
B.用蒸馏的方法分离乙醇(沸点为78.3℃)和苯(沸点为80.1℃)的混合物
C.用淀粉-KI试纸鉴别碘水和FeCl 溶液
3
D.用NaCO 溶液鉴别CaCl 溶液、NaCl溶液和稀硫酸
2 3 2【答案】D
【解析】A、用其他试纸时需要湿润,但是pH试纸是不需要湿润的,若湿润会稀释溶液,导致pH出现误
差,选项A不合理;B、蒸馏只能分离沸点相差较大的物质,乙醇和苯沸点相近,不能用蒸馏的方法
分离,选项B不合理;C、Fe3+和I-会发生氧化还原反应,生成I,也会使淀粉变蓝,两种物质的现象
2
一样,无法鉴别,选项C不合理;D、NaCO 和CaCl 会反应生成沉淀,NaCO 和NaCl不反应没有
2 3 2 2 3
明显现象,NaCO 和稀硫酸反应会产生气泡,可以鉴别,选项D合理。答案选D。
2 3
11.(2018·浙江高考真题)下列操作或试剂的选择不合理的是
A.可用蒸发结晶的方法从碘水中提取砷单质
B.可用灼烧法除去氧化制中混有的铜粉
C.可用硫酸鉴别碳酸钠、硅酸钠和硫酸钠
D.可用含氢氧化钠的氢氧化铜悬浊液鉴别乙醇、乙醛和乙酸
【答案】A
【解析】A.碘单质不易溶于水,易溶于有机溶液,一般使用萃取来提纯,错误;B.Cu与氧气反应生成
氧化铜,则灼烧可除去杂质,正确;C.硫酸与碳酸钠反应生成气体,与硅酸钠反应会有沉淀生成,
易于分辨,正确;D.乙醇、乙醛和乙酸分别与氢氧化钠的氢氧化铜悬浊液混合加热的现象为:无现
象、砖红色沉淀、蓝色溶液,现象不同可鉴别,正确。综上所述,本题正确答案为A。
12.(2017·浙江高考真题)下列方法(必要时可加热)不合理的是
A.用澄清石灰水鉴别CO和CO
2
B.用水鉴别苯和四氯化碳
C.用Ba(OH) 溶液鉴别NH Cl、(NH )SO 和KSO
2 4 4 2 4 2 4
D.用淀粉碘化钾试纸鉴别碘水和溴水
【答案】D
【解析】A.用澄清石灰水与CO不反应,与CO 能够反应生成碳酸钙沉淀,溶液变浑浊,能够鉴别,不
2
选;B.苯和四氯化碳均不溶于水,但苯的密度小于水,四氯化碳的密度大于水,能够鉴别,不选;
C.Ba(OH) 与NH Cl加热时有刺激性气味的气体放出,与(NH )SO 加热时生成白色沉淀和刺激性气
2 4 4 2 4
味的气体,与KSO 反应生成白色沉淀,现象各不相同,能够鉴别,不选;D.淀粉碘化钾试纸遇到
2 4
碘水和溴水均变成蓝色,现象相同,不能鉴别,选;故选D。
13.(2017·上海高考真题)下列各组物质中,能用酸性高锰酸钾溶液鉴别的是
A.乙烯、乙炔 B.苯、环己烷 C.己烯、苯 D.乙烷、丙烷
【答案】C
【解析】A.乙烯和乙炔都含有不饱和键,都能与酸性高锰酸钾发生氧化还原反应,不能鉴别,错误;B.
苯、环己烷与酸性高锰酸钾都不反应,不能鉴别,错误;C.己烯含有碳碳双键,可与酸性高锰酸钾
反应,苯与酸性高锰酸钾不反应,可鉴别,正确;D.乙烷、丙烷与酸性高锰酸钾都不反应,不能鉴
别,错误;故选C。
14.(2017·浙江高考真题)下列能使湿润的红色石蕊试剂变蓝的气体是
A.NH B.SO C.HCl D.CO
3 3 2【答案】A
【解析】A.NH 是碱性气体,能使湿润的红色石蕊试剂变蓝,A正确;B.SO 溶于水生成强酸硫酸,不
3 3
能能使湿润的红色石蕊试剂变蓝,B错误;C.HCl溶于水得到强酸盐酸,不能使湿润的红色石蕊试剂
变蓝,C错误;D.CO 是酸性氧化物,不能使湿润的红色石蕊试剂变蓝,D错误。答案选A。
2
15.(2016·全国高考真题)某白色粉末由两种物质组成,为鉴别其成分进行如下实验:
①取少量样品加入足量水仍有部分固体未溶解;再加入足量稀盐酸,有气泡产生,固体全部溶解;
②取少量样品加入足量稀硫酸有气泡产生,振荡后仍有固体存在。
该白色粉末可能为
A.NaHCO 、Al(OH) B.AgCl、NaHCO
3 3 3
C.NaSO 、BaCO D.NaCO、CuSO
2 3 3 2 3 4
【答案】C
【解析】A.NaHCO 、Al(OH) 中加入足量稀硫酸有气泡产生,生成硫酸钠、硫酸铝、二氧化碳和水,
3 3
最终无固体存在,错误;B.AgCl不溶于酸,固体不能全部溶解,错误;C.亚硫酸钠和碳酸钡溶于
水,碳酸钡不溶于水使部分固体不溶解,加入稀盐酸,碳酸钡与盐酸反应生成氯化钡、二氧化碳和水,
固体全部溶解,再将样品加入足量稀硫酸,稀硫酸和碳酸钡反应生成硫酸钡沉淀和二氧化碳和水,符
合题意,正确;D.NaCO、CuSO 中加热足量稀硫酸,振荡后无固体存在,错误;答案选C。
2 3 4
16.(2013·海南高考真题)下列鉴别方法不可行的是
A.用水鉴别乙醇、甲苯和溴苯
B.用燃烧法鉴别乙醇、苯和四氯化碳
C.用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯
D.用酸性高锰酸钾溶液鉴别苯、环已烯和环已烷
【答案】D
【解析】A.乙醇与水混溶,甲苯密度比水小,溴苯密度比水大,可加入水鉴别,可行;B.乙醇燃烧,火
焰明亮,无浓烟,苯燃烧有浓烟,四氯化碳不燃烧,现象各不相同,可鉴别,可行;C.乙醇易溶于
水,碳酸钠与乙酸反应生成二氧化碳气体,乙酸乙酯不溶于饱和碳酸钠溶液,溶液分层,可鉴别,可
行;D.甲苯、环己烯都可被酸性高锰酸钾氧化,不可行;故选D。
17.(2014·北京高考真题)下列说法正确的是( )
A.室温下,在水中的溶解度:丙三醇>苯酚>1-氯丁烷
B.用核磁共振氢谱不能区分HCOOCH 和HCOOCH CH
3 2 3
C.用NaCO 溶液不能区分CHCOOH和CHCOOCH CH
2 3 3 3 2 3
D.油脂在酸性或碱性条件下均能发生水解反应,且产物相同
【答案】A
【解析】A.含-OH越多,溶解性越大,卤代烃不溶于水,则室温下,在水中的溶解度:丙三醇>苯酚>
1-氯丁烷,A正确;B.HCOOCH 中两种H,HCOOCH CH 中有三种H,则用核磁共振氢谱能区分
3 2 3
HCOOCH 和HCOOCH CH,B错误;C.CHCOOH与碳酸钠溶液反应产生气泡,而NaCO 溶液与
3 2 3 3 2 3
CHCOOCH CH 会分层,因此可以用NaCO 溶液能区分CHCOOH和CHCOOCH CH,C错误;
3 2 3 2 3 3 3 2 3
D.油脂在酸性条件下水解产物为高级脂肪酸和甘油,碱性条件下水解产物为高级脂肪酸盐和甘油,水解产物不相同,D错误。答案选A。
18.(2011·全国高考真题)下列叙述错误的是
A.用金属钠可区分乙醇和乙醚
B.用高锰酸钾酸性溶液可区分己烷和3-己烯
C.用水可区分苯和溴苯
D.用新制的银氨溶液可区分甲酸甲酯和乙醛
【答案】D
【解析】A .乙醇含有-OH ,可与金属钠发生反应,而乙醚与钠不反应,可鉴别,正确;B .己烷为饱
和烃,与酸性高锰酸钾不反应,而己烯含有碳碳双键,可使酸性高锰酸钾褪色,可鉴别,正确;C .
苯的密度比水小,溴苯的密度比水大,可鉴别,正确;D .甲酸甲酯和乙醛都含有醛基,都可发生银
镜反应,不能鉴别,错误,答案选 D。
19.(2009·浙江高考真题)下列说法正确的是
A.仅用 溶液便可鉴别亚硝酸钠和食盐
B.重结晶时,溶液冷却速度越慢得到的晶体颗粒越大
C.乙酸与乙醇的混合溶液可用分液漏斗进行分离
D.用盐酸标准溶液滴定待测的氢氧化钠溶液时,水洗后的酸式滴定管未经标准润洗,则测定结果偏
低
【答案】B
【解析】A.亚硝酸银与氯化银均为不溶于水的化合物,但亚硝酸银溶于HNO,需另有HNO 才可以鉴别
3 3
亚硝酸钠和食盐,错误;B.冷却速度慢,则易析出晶体,越慢晶体析出越大,正确。C.乙醇和乙酸
是互溶的,不分层,所以无法用分液法分离,错误;D.未润洗酸式滴定管,相当稀释了盐酸,所用
标准HCl体积增大,则计算出的NaOH浓度偏大,错误。答案选B。
20.(2014·浙江高考真题)下列说法正确的是
A.金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理
B.用pH计、电导率仪(一种测量溶液导电能力的仪器)均可检测乙酸乙酯的水解程度
C.邻苯二甲酸氢钾可用于标定NaOH溶液的浓度,假如称量邻苯二甲酸氢钾时电子天平读数比实际
质量偏大,则测得的NaOH溶液浓度比实际浓度偏小
D.向某溶液中加入茚三酮试剂,加热煮沸后溶液若出现蓝色,则可判断该溶液含有蛋白质
【答案】B
【解析】A.金属汞一旦洒落在实验室地面或桌面,加硫磺粉处理,且金属汞不能深埋处理,易污染土壤
和地下水,错误;B.A.乙酸乙酯水解生成乙酸和乙醇,只有乙酸为电解质,且乙酸电离显酸性,则
乙酸浓度越大,酸性越强,导电能力也越强,所以用pH计、电导率仪(一种测量溶液导电能力的仪
器)均可监测乙酸乙酯的水解程度,B正确;C.邻苯二甲酸氢钾可用于标定NaOH溶液的浓度,假
如称量邻苯二甲酸氢钾时电子天平读数比实际质量偏大,即实际计量减小,滴定加入的体积偏大,故
则测得的NaOH溶液浓度比实际浓度偏大,C错误;D.茚三酮水合物稀溶液分别与@-氨基酸、多肽、
蛋白质一起加热生成蓝色物质,茚三铜试剂一般用于检验氨基酸,该溶液中可能有蛋白质,错误;故答案选B。
21.(2016·浙江高考真题)实验室有两瓶失去标签的溶液,其中一瓶是HSO ,另一瓶是蔗糖溶液。鉴别
2 4
时,下列选用的试纸或试剂不正确的是
A.pH试纸 B.KCl溶液 C.BaCl 溶液 D.NaCO 溶液
2 2 3
【答案】B
【解析】A.硫酸可使pH试纸变红色,可鉴别,A正确;B.二者与氯化钾都不反应,不能鉴别,B错误;
C.硫酸与氯化钡反应生成沉淀,能鉴别,C正确;D.碳酸钠与硫酸反应生成气体,可鉴别,D正确,
答案选B。
22.(2012·广东高考真题)下列实验能达到目的是( )
A.用溴水鉴别苯和正已烷
B.用BaCl 溶液鉴别SO 2﹣与SO 2﹣
2 4 3
C.用浓HNO 与Cu反应制备NO
3 2
D.将混有HCl的Cl 通入饱和NaHCO 溶液中除去HCl
2 3
【答案】C
【解析】A、两者密度都比水小,均发生萃取,溴水层褪色,不能鉴别,选项A错误;B、两者都有沉淀
生成,不能鉴别,选项B错误;C、浓硝酸具有强氧化性,可与Cu反应生成NO ,选项C正确;D、
2
两者均能与NaHCO 溶液反应,而且引入CO2,选项D错误。答案选C。
3
23.(2011·重庆高考真题)不能鉴别AgNO 、BaCl 、KSO 和Mg(NO) 四种溶液(不考虑他们间的相互
3 2 2 3 3 2
反应)的试剂是
A.盐酸、硫酸 B.盐酸、氢氧化钠溶液
C.氨水、硫酸 D.氨水、氢氧化钠溶液
【答案】D
【解析】取四种溶液少许,滴入盐酸生成白色沉淀的是AgNO,有气体生成的是KSO ;另取其他两种溶
3 2 3
液少许,滴入硫酸生成白色沉淀的是BaCl ,无明显现象的是Mg(NO),能鉴别;滴加盐酸后,另取
2 3 2
其他两种溶液少许,滴加氢氧化钠溶液生成白色沉淀的是Mg(NO),无明显现象的是BaCl ,也能鉴
3 2 2
别;取四种溶液少许,滴入氨水,先沉淀后沉淀消失的是AgNO,有白色沉淀生成的是Mg(NO);取
3 3 2
其他两种溶液少许,滴加硫酸后有白色沉淀生成的是BaCl ,有气体生成的是KSO ,可以鉴别;滴加
2 2 3
氨水后,取其他两种溶液少许,滴加氢氧化钠溶液时BaCl 和KSO 都无现象,不能鉴别。
2 2 3
24.(2014·重庆高考真题)下列实验可实现鉴别目的是( )
A.用KOH溶液鉴别SO (g)和SO
3 2
B.用湿润的碘化钾淀粉试纸鉴别Br (g)和NO
2 2
C.用CO 鉴别NaAlO 溶液和CHCOONa溶液
2 2 3
D.用BaCl 溶液鉴别AgNO 溶液和KSO 溶液
2 3 2 4
【答案】C
【解析】A.KOH溶液与SO (g)、SO 反应,没有明显现象,可用品红溶液检验,错误;B.Br (g)
3 2 2
和NO 都可氧化KI生成碘单质,可用硝酸银溶液或水鉴别,错误;C.二氧化碳与NaAlO 溶液反应
2 2生成氢氧化铝沉淀,可鉴别,正确;D.BaCl 溶液与AgNO 溶液和KSO 溶液反应都可生成沉淀,应
2 3 2 4
用盐酸或氯化钠溶液鉴别,错误.故选C.
25.(2010·上海高考真题)下列各组有机物只用一种试剂无法鉴别的是( )
A.乙醇、甲苯、硝基苯 B.苯、甲苯、环己烷
C.苯、苯酚、己烯 D.甲酸、乙醛、乙酸
【答案】B
【解析】A.乙醇与水混溶,甲苯与水混合分层后有机层在上层,硝基苯与水混合后有机层在下层,现象
不同,可鉴别,不选;B.苯、甲苯、环己烷均不溶于水,且密度均比水小,性质相似,一种试剂不
能鉴别,选;C.与溴水反应生成白色沉淀的为苯酚,使溴水褪色的为己烯,与溴水混合分层的为苯,
不选;D.甲酸、乙醛、乙酸分别与氢氧化铜悬浊液反应的现象为:砖红色沉淀和蓝色溶液、砖红色
沉淀、蓝色溶液,现象不同,可鉴别,不选;故答案为B。
26.(2007·北京高考真题)用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是
选项 操作及现象 溶液
A 通入CO,溶液变浑浊。再升高至65℃以上,溶液变澄清。 C HONa溶液
2 6 5
B 通入CO,溶液变浑浊。继续通CO 至过量,浑浊消失。 NaSiO 溶液
2 2 2 3
C 通入CO,溶液变浑浊。再加入品红溶液,红色褪去。 Ca(ClO) 溶液
2 2
通入CO,溶液变浑浊。继续通CO 至过量,浑浊消失。再加入足
2 2
D Ca(OH) 溶液
2
量NaOH溶液,又变浑浊。
【答案】B
【解析】A.苯酚钠和二氧化碳反应生成难溶性的苯酚和碳酸氢钠,但65℃以上苯酚易溶于水,导致溶液
变澄清,正确;B.NaSiO 溶液与CO 反应生成硅酸沉淀,继续通CO 至过量,浑浊不消失,错误;
2 3 2 2
C.Ca(ClO) 溶液与CO 反应生成HClO,HClO具有漂白性,可使品红溶液褪色,正确;D.Ca(OH)
2 2 2
溶液通入CO,生成碳酸钙沉淀,继续通CO 至过量生成碳酸氢钙,碳酸氢钙与NaOH反应又生成碳
2 2
酸钙沉淀,正确。
27.(2008·北京高考真题)下列各组物质的无色溶液,不用其他试剂即可鉴别的是( )
①KOH Na SO AlCl ②NaHCO Ba(OH) HSO ③HCl NaAlO NaHSO ④Ca(OH) NaCOBaCl
2 4 3 3 2 2 4 2 4 2 2 3 2
A.①② B.②③ C.①③④ D.①②④
【答案】A
【解析】不用其他试剂的鉴别通常用互滴的方法。①中NaSO 不与其他物质反应,首先可以鉴别出来,
2 4
KOH、AlCl 相互滴加顺序不同现象也不同,①可以不加试剂就可以鉴别;②将三种物质相互滴加,
3
当一种物质加入到另两种中均有白色沉淀的是Ba(OH) ,然后再把另外两种试剂分别滴加在白色沉淀
2
上,有气泡产生的试剂是HSO ,②可以鉴别;③HCl、NaHSO 两者都显强酸性,与NaAlO 溶液反
2 4 4 2
应的现象相同:产生白色沉淀,随着酸的增多,沉淀会逐渐溶解,③不能鉴别;④Ca(OH) 、BaCl 与
2 2
NaCO 产生白色沉淀,④不能鉴别。答案选A。
2 328.(2012·海南高考真题)两种盐的固体混合物:①加热时有气体产生,②加水溶解时有沉淀生成,且沉
淀溶于稀盐酸。满足上述条件的混合物是
A.BaCl 和(NH )SO B.AgNO 和NH Cl
2 4 2 4 3 4
C.FeCl 和NaHCO D.KCl和NaCO
3 3 2 3
【答案】AC
【解析】硫酸铵和氯化钡混合加热时会释放氨气,加水溶解会生成硫酸钡沉淀,A符合;氯化铵受热能放
出氨气,但生成的盐酸AgCl不溶于盐酸,B排除;碳酸氢钠受热放出二氧化碳气体,溶于水生成的
Fe(OH) 可溶于盐酸,C符合;氯化钾和碳酸钠混合溶于水不生成沉淀,D排除。
3