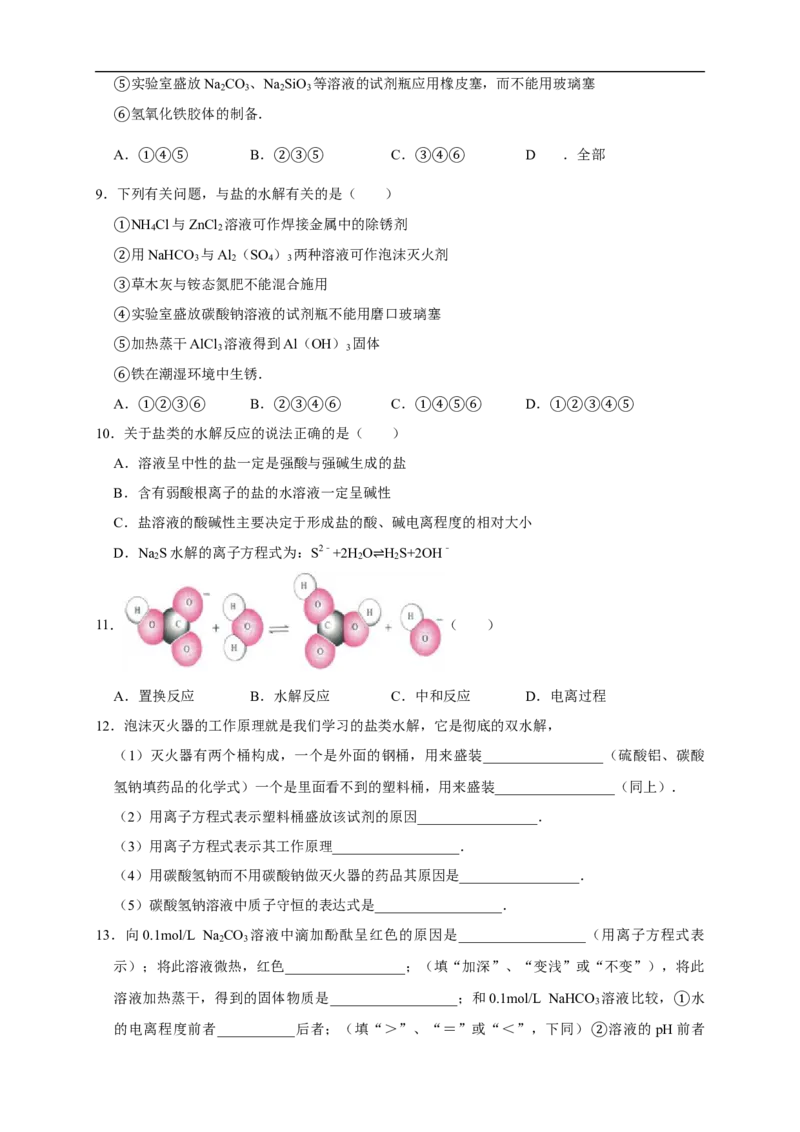文档内容
3.3.1 盐类的水解 练习(原卷版)
1.下列盐在水溶液中不能发生水解的是( )
A.NH NO B.CH COOK C.NaCl D.FeSO
4 3 3 4
2.下列各式表示水解反应的是( )
A.HCO ﹣+H O H O++CO 2﹣ B.HS﹣+H O H S+OH﹣
3 2 3 3 2 2
C.H PO ﹣+H O⇌HPO 2﹣+H O+ D.HCO ﹣+O⇌H﹣ H O+CO 2﹣
2 4 2 4 3 3 2 3
3.下列关于盐类水解⇌反应的应用说法正确的是( ) ⇌
A.可以用Cu除去CuCl 溶液中的杂质离子Fe3+
2
B.将FeCl 溶液蒸干并灼烧得到Fe O 固体
3 2 3
C.Al(NO ) 溶液与K S溶液混合后无明显现象
3 3 2
D.Mg粉投入到饱和NH Cl溶液中无明显现象
4
4.下列物质加入水中,因水解而使溶液呈酸性的是( )
A.CuCl B.NaHSO C.NaHCO D.SO
2 4 3 2
5.下面的问题中,与盐类水解有关的是( )
为保存FeCl 溶液,要在溶液中加入少量盐酸;
2
①实验室盛放Na
2
CO
3
、Na
2
SiO
3
等溶液的试剂瓶应用橡胶塞;
②在NH
4
Cl或AlCl
3
溶液中加入镁条会产生气泡;
③长期使用硫酸铵,土壤酸性增强.
④A.只有 B.只有 C.只有 D.全部
6.漂白粉在①溶④液中存在下列平衡体②系③:ClO﹣+H
2
O HCl③O+④OH﹣(正反应为吸热反应),以下措施
能增强漂白粉的漂白效果的是( ) ⇌
A.降低温度 B.加入大量的水
C.加入适量盐酸 D.加入适量烧碱溶液
7.下列反应不属于水解反应或水解方程式不正确的是 ( )
HCl+H O═H O++Cl﹣ ZnCl +2H O═Zn(OH) +2HCl Na CO +2H O H CO +2NaOH
2 3 2 2 2 2 3 2 2 3
①Al (CO ) +6H O 2②Al(OH) ↓+3H CO . ③ ⇌
2 3 3 2 3 2 3
④A. ⇌B. C. D.全部
8.下面①提②到的问题中,与盐的③水④解有关的是( )①②④
实验室配制AlCl 溶液时,应先把它溶在盐酸中,而后加水稀释
3
①草木灰与铵态氮肥不能混合施用
②蒸干AlCl
3
溶液得不到无水AlCl
3
③用MgO或碳酸镁除去MgCl
2
酸性溶液中的Fe3+
④实验室盛放Na CO 、Na SiO 等溶液的试剂瓶应用橡皮塞,而不能用玻璃塞
2 3 2 3
⑤氢氧化铁胶体的制备.
⑥
A. B. C. D .全部
①④⑤ ②③⑤ ③④⑥
9.下列有关问题,与盐的水解有关的是( )
NH Cl与ZnCl 溶液可作焊接金属中的除锈剂
4 2
①用NaHCO
3
与Al
2
(SO
4
)
3
两种溶液可作泡沫灭火剂
②草木灰与铵态氮肥不能混合施用
③实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
④加热蒸干AlCl
3
溶液得到Al(OH)
3
固体
⑤铁在潮湿环境中生锈.
⑥A. B. C. D.
10.关于①盐②类③的⑥水解反应的说②法③正确④的⑥是( ) ①④⑤⑥ ①②③④⑤
A.溶液呈中性的盐一定是强酸与强碱生成的盐
B.含有弱酸根离子的盐的水溶液一定呈碱性
C.盐溶液的酸碱性主要决定于形成盐的酸、碱电离程度的相对大小
D.Na S水解的离子方程式为:S2﹣+2H O H S+2OH﹣
2 2 2
⇌
11. ( )
A.置换反应 B.水解反应 C.中和反应 D.电离过程
12.泡沫灭火器的工作原理就是我们学习的盐类水解,它是彻底的双水解,
(1)灭火器有两个桶构成,一个是外面的钢桶,用来盛装_________________(硫酸铝、碳酸
氢钠填药品的化学式)一个是里面看不到的塑料桶,用来盛装_________________(同上).
(2)用离子方程式表示塑料桶盛放该试剂的原因_________________.
(3)用离子方程式表示其工作原理__________________.
(4)用碳酸氢钠而不用碳酸钠做灭火器的药品其原因是_________________.
(5)碳酸氢钠溶液中质子守恒的表达式是__________________.
13.向0.1mol/L Na CO 溶液中滴加酚酞呈红色的原因是__________________(用离子方程式表
2 3
示);将此溶液微热,红色_________________;(填“加深”、“变浅”或“不变”),将此
溶液加热蒸干,得到的固体物质是__________________;和0.1mol/L NaHCO 溶液比较, 水
3
的电离程度前者___________后者;(填“>”、“=”或“<”,下同) 溶液的pH①前者
②_________后者.
14.写出下列盐溶液水解的离子方程式
(1)次氯酸钠溶液_________________
(2)泡沫灭火器的水解原理_________________
(3)磷酸钠溶液_________________________________________________
(4)明矾净水水解原理_________________.
15.(1)在100℃时,PH=7呈_________________性.
(2)碳酸钠溶液呈碱性的原因,用离子方程式表示:________________.
(3)氯化铝溶液呈酸性的原因,用离子方程式表示:________________
(4)写电离方程式NaHCO _________________
3
(5)由氢气和氧气反应生成 1mol 水蒸气放热 241.8KJ,写出该反应的热化学方程式:
_________________.