文档内容
2024 年广州市普通高中毕业班冲刺训练题(二)
化学
本试卷共8页,20小题,满分100分。考试用时75分钟。
可能用到的相对原子质量: H 1 C 12 N 14 O 16 Ni 59
一、单项选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4
分。每小题只有一个选项符合题意。
1. 岭南文化源远流长,对社会的发展起着积极的推动作用。下列地方文化涉及的材料不属于有机高
分子化合物的是
选项 A B C D
地方
文化
顺德木制龙舟 石湾陶塑 广东剪纸 粤剧现代戏服
2. 回首百年征程,我国在科技领域不断创新和超越,向世界展示了一张张“中国名片”。下列说法正
确的是
A.华为麒麟芯片的主体材料属于金属晶体
B.首创了从二氧化碳到淀粉的合成,原料和产品均属于氧化物
C.“神舟十六号”返回舱外表的陶瓷材料具有耐高温、抗腐蚀功能
D.“天问一号”着陆火星,探测到火星陨石中含有的
化学试题 第 1 页 (共 10 页)
8 3 K r 和84Kr互为同系物
3. 化学与生活生产息息相关,下列相关说法正确的是
A.为防止月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶
B.基于界面效应的新型开关中含有碲元素和钛元素,两种元素均为过渡元素
C.燃料的脱硫、NO的催化转化都是减少温室效应的措施
D.氧化铁是质地疏松的红色固体,用做颜料为生活带来一抹红
4. 下列实验装置能达到实验目的的是
A.装置甲测定乙醇结构 B.装置乙制取少量CO
2
C.装置丙红磷燃烧测定空气中氧气的含量 D.装置丁提纯乙酸乙酯5. 化学与生活密切相关,下列说法正确的是
A.日常生活中所用的花生油、牛油、石蜡油分子中均含有酯基
B.用激光笔照射淀粉溶液、鸡蛋白溶液均能观察到丁达尔效应
C.泡沫灭火器中所用硫酸铝、碳酸氢钠溶于水后,溶液均显酸性
D.可以用麦芽糖吹糖人,麦芽糖属于多糖
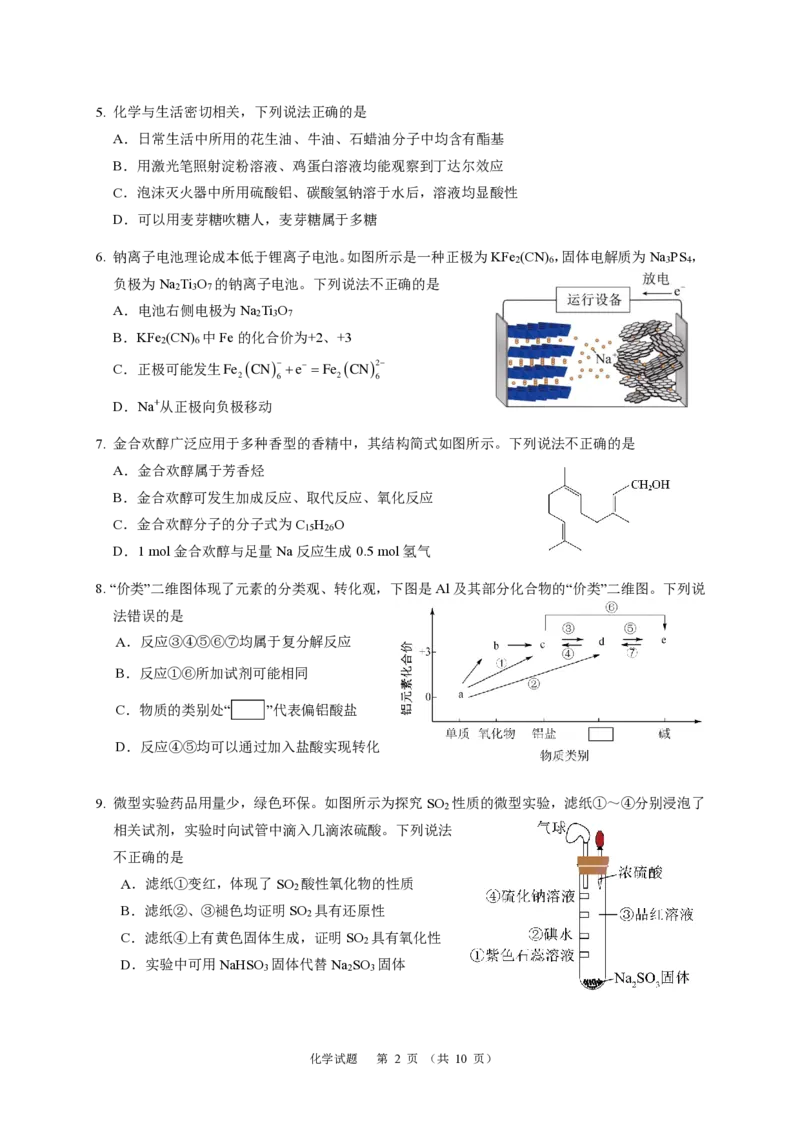
6. 钠离子电池理论成本低于锂离子电池。如图所示是一种正极为KFe (CN) ,固体电解质为Na PS ,
2 6 3 4
负极为Na Ti O 的钠离子电池。下列说法不正确的是
2 3 7
A.电池右侧电极为Na Ti O
2 3 7
B.KFe (CN) 中Fe的化合价为+2、+3
2 6
C.正极可能发生Fe (CN)−+e− =Fe (CN)2−
2 6 2 6
D.Na+从正极向负极移动
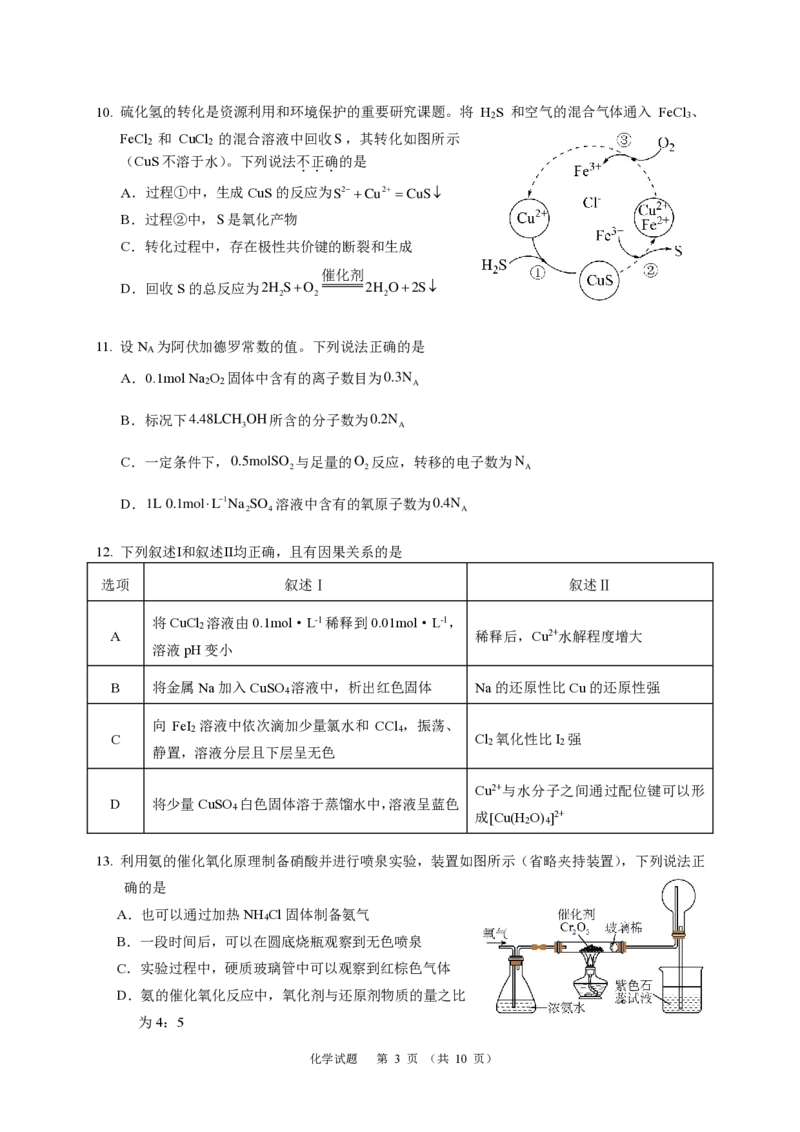
7. 金合欢醇广泛应用于多种香型的香精中,其结构简式如图所示。下列说法不正确的是
A.金合欢醇属于芳香烃
B.金合欢醇可发生加成反应、取代反应、氧化反应
C.金合欢醇分子的分子式为C H O
15 26
D.1 mol金合欢醇与足量Na反应生成0.5 mol氢气
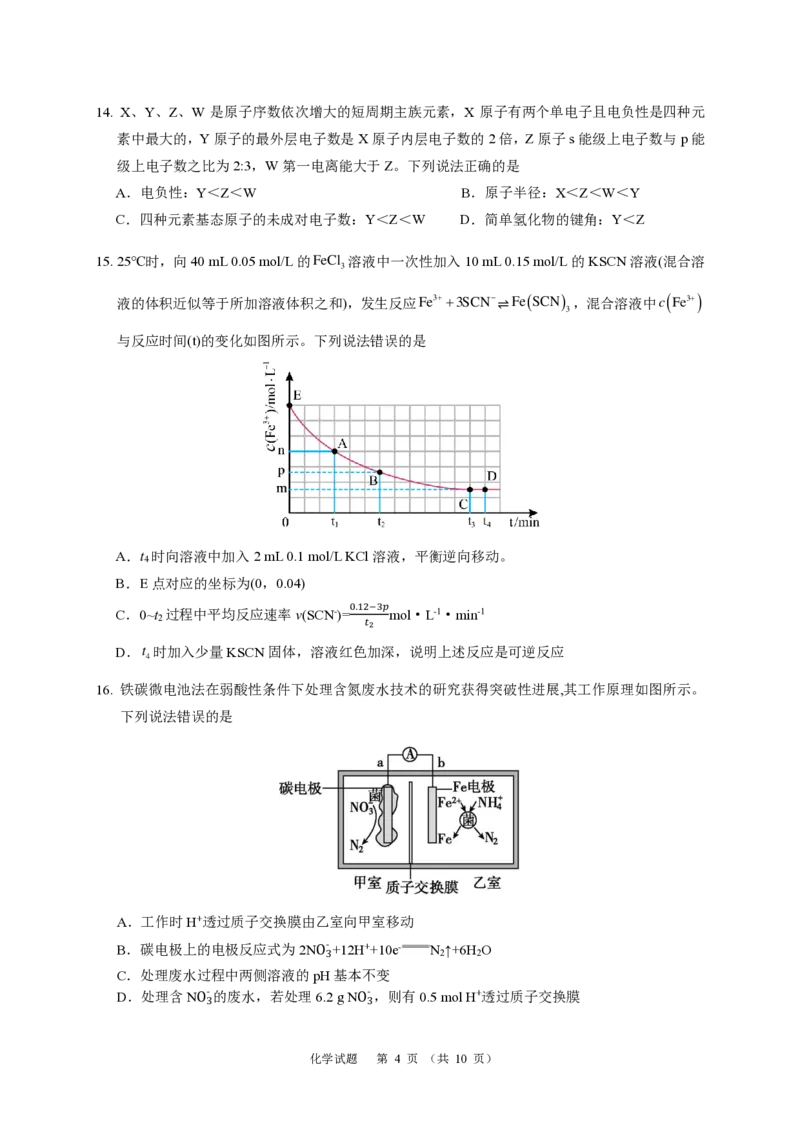
8. “价类”二维图体现了元素的分类观、转化观,下图是Al及其部分化合物的“价类”二维图。下列说
法错误的是
A.反应③④⑤⑥⑦均属于复分解反应
B.反应①⑥所加试剂可能相同
C.物质的类别处“ ”代表偏铝酸盐
D.反应④⑤均可以通过加入盐酸实现转化
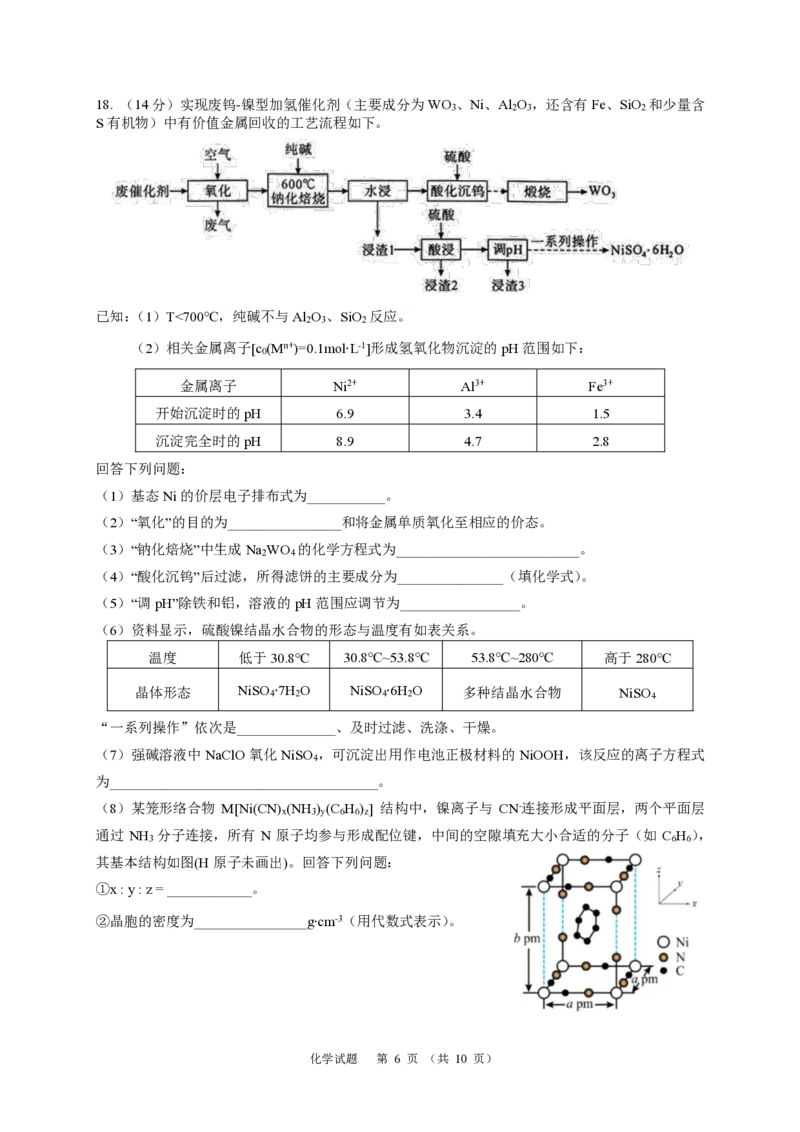
9. 微型实验药品用量少,绿色环保。如图所示为探究SO 性质的微型实验,滤纸①~④分别浸泡了
2
相关试剂,实验时向试管中滴入几滴浓硫酸。下列说法
不正确的是
A.滤纸①变红,体现了SO 酸性氧化物的性质
2
B.滤纸②、③褪色均证明SO 具有还原性
2
C.滤纸④上有黄色固体生成,证明SO 具有氧化性
2
D.实验中可用NaHSO 固体代替Na SO 固体
3 2 3
化学试题 第 2 页 (共 10 页)10. 硫化氢的转化是资源利用和环境保护的重要研究课题。将 H S 和空气的混合气体通入 FeCl 、
2 3
FeCl 和 CuCl 的混合溶液中回收
2 2
化学试题 第 3 页 (共 10 页)
S ,其转化如图所示
(CuS不溶于水)。下列说法不正确的是
...
A.过程①中,生成CuS的反应为 S 2 − + C u 2 + = C u S
B.过程②中,S是氧化产物
C.转化过程中,存在极性共价键的断裂和生成
D.回收S的总反应为 2 H
2
S + O
2
催 化 剂
2 H
2
O + 2 S
11. 设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.0.1mol Na O 固体中含有的离子数目为
2 2
0 .3 N
A
B.标况下 4 .4 8 L C H
3
O H 所含的分子数为 0 .2 N
A
C.一定条件下, 0 .5 m o lS O
2
与足量的O 反应,转移的电子数为
2
N
A
D. 1 L 0 .1 m o l L − 1 N a
2
S O
4
溶液中含有的氧原子数为 0 .4 N
A
12. 下列叙述Ⅰ和叙述Ⅱ均正确,且有因果关系的是
选项 叙述Ⅰ 叙述Ⅱ
将CuCl 溶液由0.1mol·L-1稀释到0.01mol·L-1,
2
A 稀释后,Cu2+水解程度增大
溶液pH变小
B 将金属Na加入CuSO 溶液中,析出红色固体 Na的还原性比Cu的还原性强
4
向 FeI 溶液中依次滴加少量氯水和 CCl ,振荡、
2 4
C Cl 氧化性比I 强
2 2
静置,溶液分层且下层呈无色
Cu2+与水分子之间通过配位键可以形
D 将少量CuSO 白色固体溶于蒸馏水中,溶液呈蓝色
4
成[Cu(H O) ]2+
2 4
13. 利用氨的催化氧化原理制备硝酸并进行喷泉实验,装置如图所示(省略夹持装置),下列说法正
确的是
A.也可以通过加热NH Cl固体制备氨气
4
B.一段时间后,可以在圆底烧瓶观察到无色喷泉
C.实验过程中,硬质玻璃管中可以观察到红棕色气体
D.氨的催化氧化反应中,氧化剂与还原剂物质的量之比
为4:514. X、Y、Z、W 是原子序数依次增大的短周期主族元素,X 原子有两个单电子且电负性是四种元
素中最大的,Y原子的最外层电子数是X原子内层电子数的2倍,Z原子s能级上电子数与p能
级上电子数之比为2:3,W第一电离能大于Z。下列说法正确的是
A.电负性:Y<Z<W B.原子半径:X<Z<W<Y
C.四种元素基态原子的未成对电子数:Y<Z<W D.简单氢化物的键角:Y<Z
15. 25℃时,向40 mL 0.05 mol/L的
化学试题 第 4 页 (共 10 页)
F e C l
3
溶液中一次性加入10 mL 0.15 mol/L的KSCN溶液(混合溶
液的体积近似等于所加溶液体积之和),发生反应 F e 3 + + 3 S C N − F e ( S C N )
3
⇌ F e 3 + + 3 S C N − F e ( S C N )
3
,混合溶液中 c ( F e 3 + )
与反应时间(t)的变化如图所示。下列说法错误的是
A.t 时向溶液中加入2 mL 0.1 mol/L KCl溶液,平衡逆向移动。
4
B.E点对应的坐标为(0,0.04)
0.12−3𝑝
C.0~t 过程中平均反应速率v(SCN-)= mol·L-1·min-1
2
𝑡2
D.t 时加入少量KSCN固体,溶液红色加深,说明上述反应是可逆反应
4
16. 铁碳微电池法在弱酸性条件下处理含氮废水技术的研究获得突破性进展,其工作原理如图所示。
下列说法错误的是
A.工作时H+透过质子交换膜由乙室向甲室移动
B.碳电极上的电极反应式为2NO- +12H++10e- N ↑+6H O
3 2 2
C.处理废水过程中两侧溶液的pH基本不变
D.处理含NO-的废水,若处理6.2 g NO-,则有0.5 mol H+透过质子交换膜
3 3二、非选择题:56分。
17. (14分)某小组在验证反应“Fe+2Ag+===Fe2++2Ag”的实验中检测到Fe3+,发现和探究过程如
下。
向硝酸酸化的0.05mol·L-1硝酸银溶液(pH≈2)中加入过量铁粉,搅拌后静置,烧杯底部有黑色固
体,溶液呈黄色。
(1)检验产物
①取出少量黑色固体,洗涤后,_____(填操作和现象),证明黑色固体中含有Ag。
②取上层清液,滴加K [Fe(CN) ]溶液,产生蓝色沉淀,说明溶液中含有__________。
3 6
(2)针对“溶液呈黄色”,甲认为溶液中有Fe3+,乙认为铁粉过量时不可能有Fe3+,乙依据的原理是
________(用离子方程式表示)。
针对两种观点继续实验:
①取上层清液,滴加KSCN溶液,溶液变红,证实了甲的猜测。同时发现有白色沉淀产生,且
溶液颜色变浅、沉淀量多少与取样时间有关,对比实验记录如下:
序号 取样时间/min 现象
ⅰ 3 产生大量白色沉淀;溶液呈红色
ⅱ 30 产生白色沉淀;较3min时量少;溶液红色较3min时加深
ⅲ 120 产生白色沉淀;较30min时量少;溶液红色较30min时变浅
(资料:Ag+与SCN-生成白色沉淀AgSCN)
②对Fe3+产生的原因作出如下假设:
假设a:可能是铁粉表面有氧化层,能产生Fe3+;
假设b:空气中存在O ,由于_____________(用离子方程式表示),可产生Fe3+;
2
假设c:酸性溶液中NO-具有氧化性,可产生Fe3+;
3
假设d:根据________现象,判断溶液中存在Ag+,可产生Fe3+。
③下列实验Ⅰ可证实假设a、b、c不是产生Fe3+的主要原因。实验Ⅱ可证实假设d成立。
实验Ⅰ:向硝酸酸化的________溶液(pH≈2)中加入过量铁粉,搅拌后静置,不同时间取上
层清液滴加KSCN溶液,3min时溶液呈浅红色,30min后溶液几乎无色。
实验Ⅱ:装置如图。其中甲溶液是________,操作及现象是______。
(3)根据实验现象,结合方程式推测实验ⅰ~ⅲ中Fe3+浓度变化的原因:________。
化学试题 第 5 页 (共 10 页)18. (14分)实现废钨-镍型加氢催化剂(主要成分为WO 、Ni、Al O ,还含有Fe、SiO 和少量含
3 2 3 2
S有机物)中有价值金属回收的工艺流程如下。
已知:(1)T<700℃,纯碱不与Al O 、SiO 反应。
2 3 2
(2)相关金属离子[c (Mn+)=0.1mol∙L-1]形成氢氧化物沉淀的pH范围如下:
0
金属离子 Ni2+ Al3+ Fe3+
开始沉淀时的pH 6.9 3.4 1.5
沉淀完全时的pH 8.9 4.7 2.8
回答下列问题:
(1)基态Ni的价层电子排布式为___________。
(2)“氧化”的目的为________________和将金属单质氧化至相应的价态。
(3)“钠化焙烧”中生成Na WO 的化学方程式为__________________________。
2 4
(4)“酸化沉钨”后过滤,所得滤饼的主要成分为_______________(填化学式)。
(5)“调pH”除铁和铝,溶液的pH范围应调节为_________________。
(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系。
温度 低于30.8℃ 30.8℃~53.8℃ 53.8℃~280℃ 高于280℃
晶体形态 NiSO 4 ∙7H 2 O NiSO 4 ∙6H 2 O 多种结晶水合物 NiSO 4
“一系列操作”依次是______________、及时过滤、洗涤、干燥。
(7)强碱溶液中NaClO氧化NiSO ,可沉淀出用作电池正极材料的NiOOH,该反应的离子方程式
4
为______________________________________。
(8)某笼形络合物 M[Ni(CN) (NH ) (C H ) ] 结构中,镍离子与 CN-连接形成平面层,两个平面层
x 3 y 6 6 z
通过 NH 分子连接,所有 N 原子均参与形成配位键,中间的空隙填充大小合适的分子(如 C H ),
3 6 6
其基本结构如图(H原子未画出)。回答下列问题:
①x : y : z = ____________。
②晶胞的密度为________________g∙cm-3(用代数式表示)。
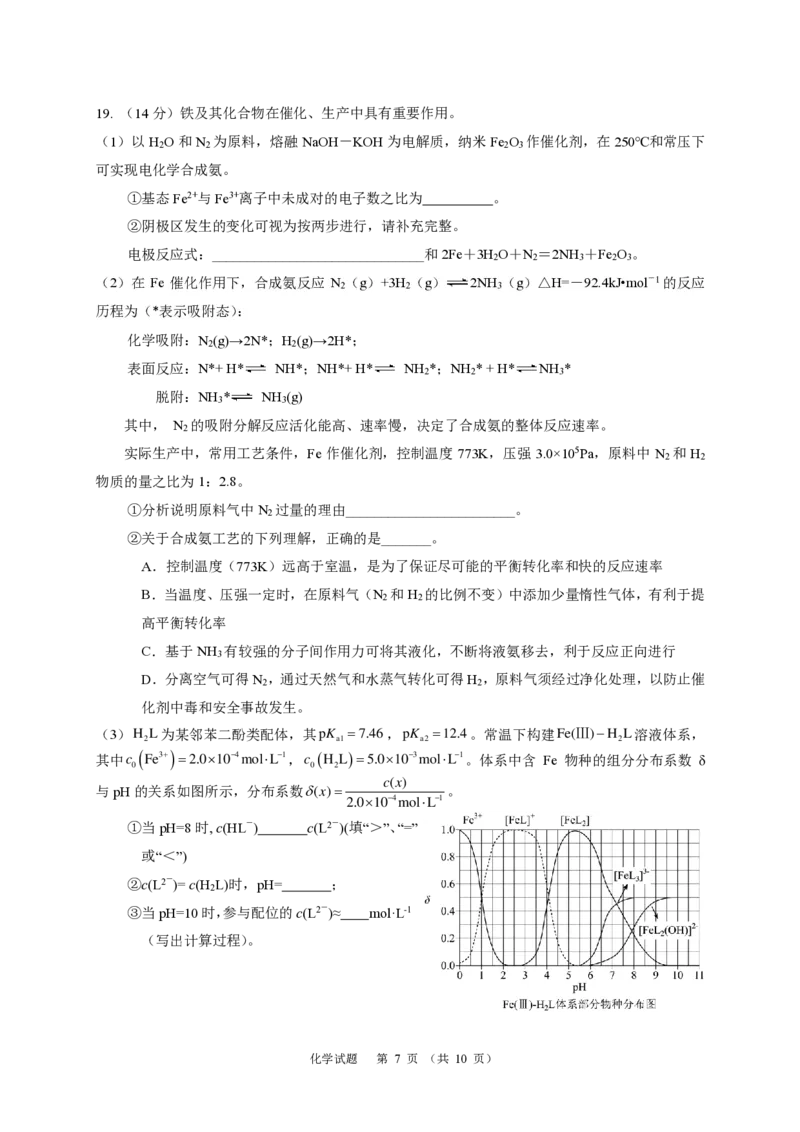
化学试题 第 6 页 (共 10 页)19. (14分)铁及其化合物在催化、生产中具有重要作用。
(1)以H O和N 为原料,熔融NaOH-KOH为电解质,纳米Fe O 作催化剂,在250℃和常压下
2 2 2 3
可实现电化学合成氨。
①基态Fe2+与Fe3+离子中未成对的电子数之比为 。
②阴极区发生的变化可视为按两步进行,请补充完整。
电极反应式:______________________________和2Fe+3H O+N =2NH +Fe O 。
2 2 3 2 3
(2)在 Fe 催化作用下,合成氨反应 N (g)+3H (g) 2NH (g)△H=-92.4kJ•mol-1的反应
2 2 3
历程为(*表示吸附态):
化学吸附:N (g)→2N*;H (g)→2H*;
2 2
表面反应:N*+ H* NH*;NH*+ H* NH *;NH * + H* NH *
2 2 3
脱附:NH * NH (g)
3 3
其中, N 的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。
2
实际生产中,常用工艺条件,Fe 作催化剂,控制温度 773K,压强 3.0×105Pa,原料中 N 和 H
2 2
物质的量之比为1:2.8。
①分析说明原料气中N 过量的理由________________________。
2
②关于合成氨工艺的下列理解,正确的是_______。
A.控制温度(773K)远高于室温,是为了保证尽可能的平衡转化率和快的反应速率
B.当温度、压强一定时,在原料气(N 和H 的比例不变)中添加少量惰性气体,有利于提
2 2
高平衡转化率
C.基于NH 有较强的分子间作用力可将其液化,不断将液氨移去,利于反应正向进行
3
D.分离空气可得N ,通过天然气和水蒸气转化可得H ,原料气须经过净化处理,以防止催
2 2
化剂中毒和安全事故发生。
(3)
化学试题 第 7 页 (共 10 页)
H
2
L 为某邻苯二酚类配体,其 p K
a1
= 7 .4 6 , p K
a 2
= 1 2 .4 。常温下构建 F e ( Ⅲ ) − H
2
L 溶液体系,
其中c ( Fe3+) =2.010−4molL−1,
0
c
0
( H
2
L ) = 5 .0 1 0 − 3 m o l L − 1 。体系中含 Fe 物种的组分分布系数 δ
与pH的关系如图所示,分布系数 ( x )
2 .0 1
c
0
( x )
4 m o l L 1
=
− −
。
①当pH=8时, c(HL-) c(L2-)(填“>”、“=”
或“<”)
②c(L2-)= c(H L)时,pH= ;
2
③当pH=10时,参与配位的c(L2-)≈ mol·L-1
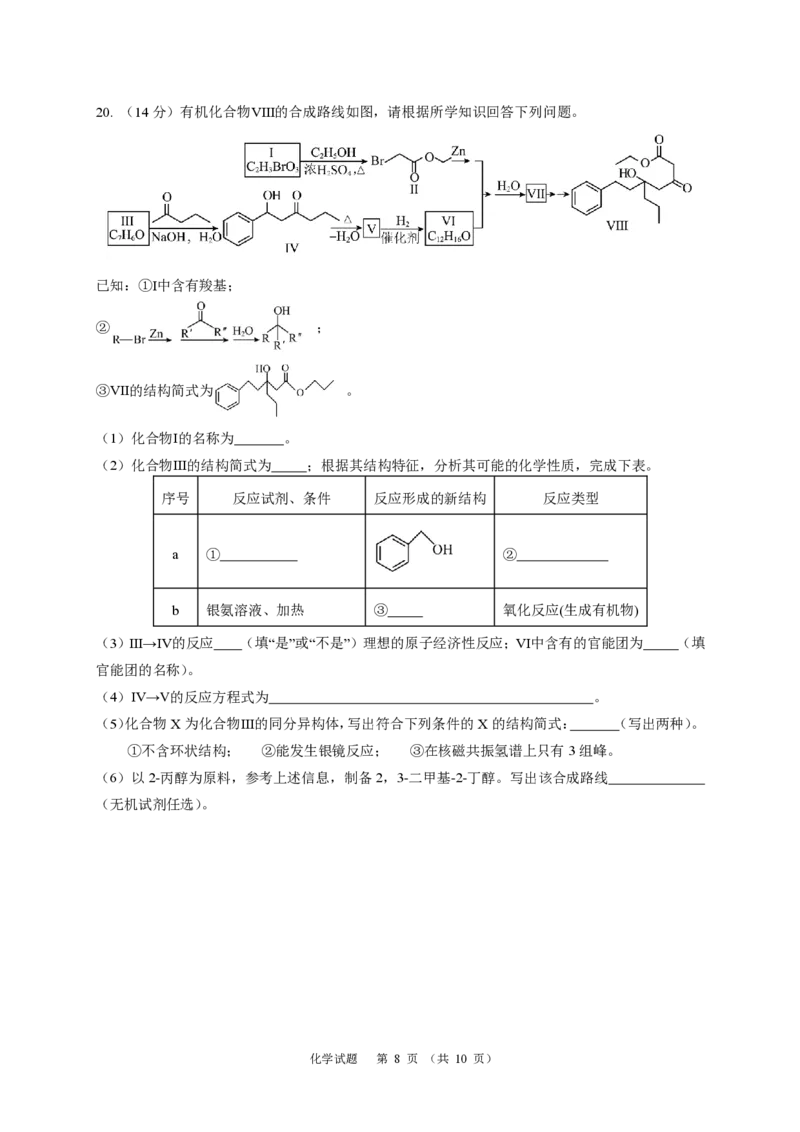
(写出计算过程)。20. (14分)有机化合物Ⅷ的合成路线如图,请根据所学知识回答下列问题。
已知:①Ⅰ中含有羧基;
② ;
③Ⅶ的结构简式为 。
(1)化合物Ⅰ的名称为 。
(2)化合物Ⅲ的结构简式为 ;根据其结构特征,分析其可能的化学性质,完成下表。
序号 反应试剂、条件 反应形成的新结构 反应类型
a ① ②
b 银氨溶液、加热 ③ 氧化反应(生成有机物)
(3)Ⅲ→Ⅳ的反应 (填“是”或“不是”)理想的原子经济性反应;Ⅵ中含有的官能团为 (填
官能团的名称)。
(4)Ⅳ→Ⅴ的反应方程式为 。
(5)化合物X为化合物Ⅲ的同分异构体,写出符合下列条件的X的结构简式: (写出两种)。
①不含环状结构; ②能发生银镜反应; ③在核磁共振氢谱上只有3组峰。
(6)以2-丙醇为原料,参考上述信息,制备2,3-二甲基-2-丁醇。写出该合成路线
(无机试剂任选)。
化学试题 第 8 页 (共 10 页)2024 年广州市普通高中毕业班化学冲刺训练题(二)
化学 参考答案
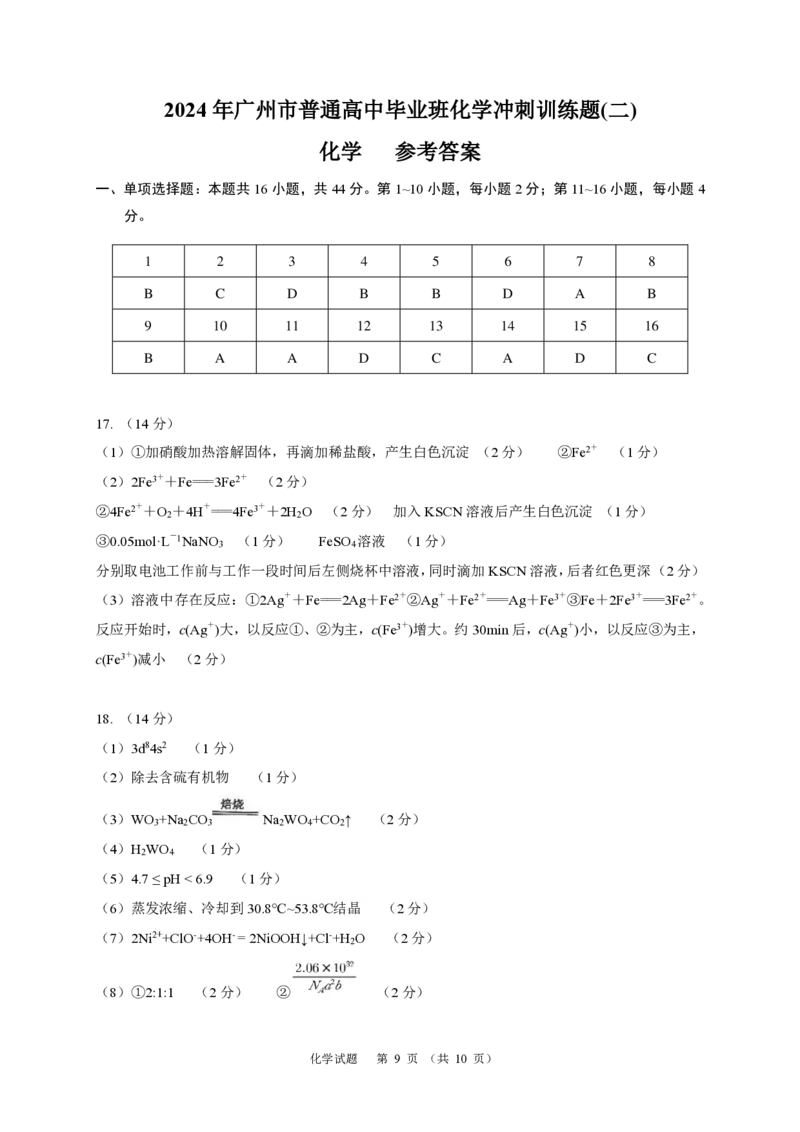
一、单项选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4
分。
1 2 3 4 5 6 7 8
B C D B B D A B
9 10 11 12 13 14 15 16
B A A D C A D C
17. (14分)
(1)①加硝酸加热溶解固体,再滴加稀盐酸,产生白色沉淀 (2分) ②Fe2+ (1分)
(2)2Fe3++Fe===3Fe2+ (2分)
②4Fe2++O +4H+===4Fe3++2H O (2分) 加入KSCN溶液后产生白色沉淀 (1分)
2 2
③0.05mol·L-1NaNO (1分) FeSO 溶液 (1分)
3 4
分别取电池工作前与工作一段时间后左侧烧杯中溶液,同时滴加KSCN溶液,后者红色更深 (2分)
(3)溶液中存在反应:①2Ag++Fe===2Ag+Fe2+②Ag++Fe2+===Ag+Fe3+③Fe+2Fe3+===3Fe2+。
反应开始时,c(Ag+)大,以反应①、②为主,c(Fe3+)增大。约30min后,c(Ag+)小,以反应③为主,
c(Fe3+)减小 (2分)
18. (14分)
(1)3d84s2 (1分)
(2)除去含硫有机物 (1分)
(3)WO +Na CO Na WO +CO ↑ (2分)
3 2 3 2 4 2
(4)H WO (1分)
2 4
(5)4.7 ≤ pH < 6.9 (1分)
(6)蒸发浓缩、冷却到30.8℃~53.8℃结晶 (2分)
(7)2Ni2++ClO-+4OH- = 2NiOOH↓+Cl-+H O (2分)
2
(8)①2:1:1 (2分) ② (2分)
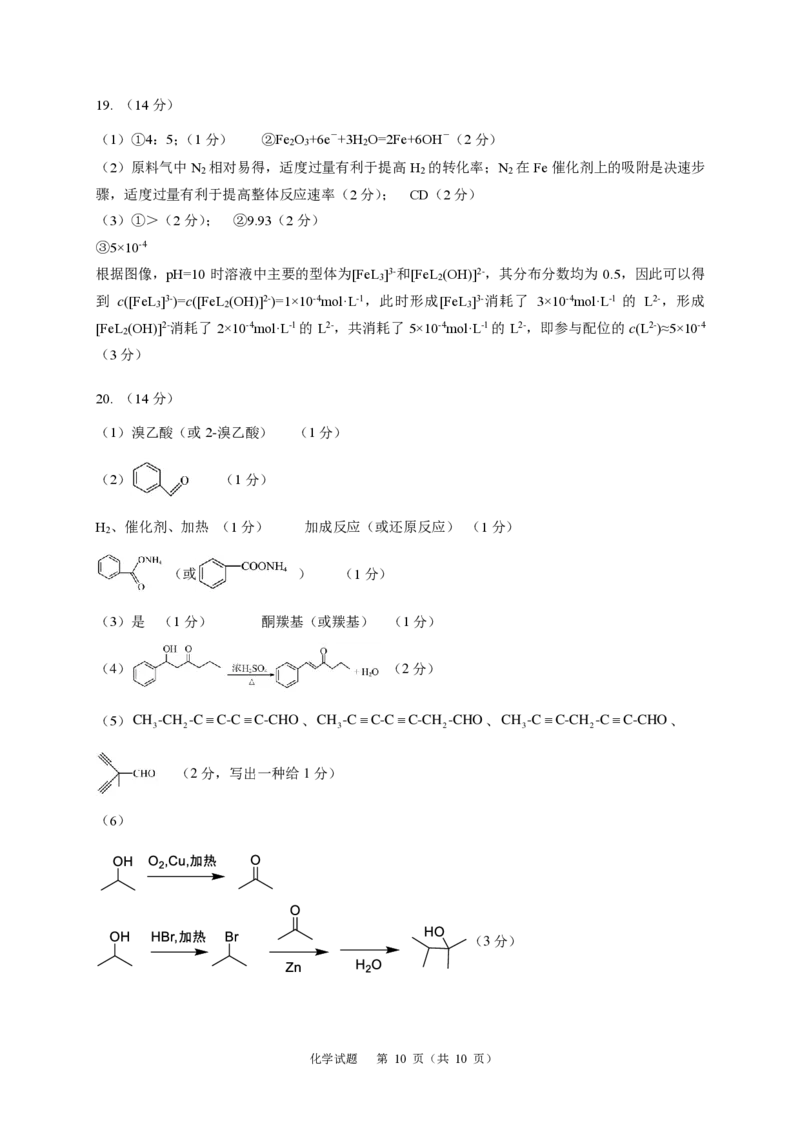
化学试题 第 9 页 (共 10 页)19. (14分)
(1)①4:5;(1分) ②Fe O +6e-+3H O=2Fe+6OH-(2分)
2 3 2
(2)原料气中N 相对易得,适度过量有利于提高H 的转化率;N 在Fe催化剂上的吸附是决速步
2 2 2
骤,适度过量有利于提高整体反应速率(2分); CD(2分)
(3)①>(2分); ②9.93(2分)
③5×10-4
根据图像,pH=10 时溶液中主要的型体为[FeL ]3-和[FeL (OH)]2-,其分布分数均为 0.5,因此可以得
3 2
到 c([FeL ]3-)=c([FeL (OH)]2-)=1×10-4mol·L-1,此时形成[FeL ]3-消耗了 3×10-4mol·L-1 的 L2-,形成
3 2 3
[FeL (OH)]2-消耗了 2×10-4mol·L-1的 L2-,共消耗了 5×10-4mol·L-1的 L2-,即参与配位的 c(L2-)≈5×10-4
2
(3分)
20. (14分)
(1)溴乙酸(或2-溴乙酸) (1分)
(2) (1分)
H 、催化剂、加热 (1分) 加成反应(或还原反应) (1分)
2
(或 ) (1分)
(3)是 (1分) 酮羰基(或羰基) (1分)
(4) (2分)
(5)
化学试题 第 10 页 (共 10 页)
C H
3
- C H
2
- C C - C C - C H O 、 C H
3
- C C - C C - C H
2
- C H O 、 C H
3
- C C - C H
2
- C C - C H O 、
(2分,写出一种给1分)
(6)
(3分)