文档内容
2023—2024学年下学期 A.用TiCl 制备TiO:TiCl +(x+2)H O(过量)=TiO ·xH O↓+4HCl
4 2 4 2 2 2
东北师大附中 高三年级( 化学 )科试卷 B.工业制硝酸:4NH +3O 2N+6H O
3 2 2 2
第六次模拟考试
C.侯式制碱法:CO+NH+H O+NaCl = NaHCO ↓+NHCl
2 3 2 3 4
满分:100分 考试时长:75分钟
D.工业制粗硅:SiO+2C Si+2CO↑
2
注意事项:
1.答题前考生需将姓名、班级填写在答题卡指定位置上,并粘贴好条形码。
4.下列所示装置或操作能达到实验目的的是
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如
需改动,用橡皮擦干净后,再选涂其它答案标号。
3.回答非选择题时,请使用0.5毫米黑色字迹签字笔将答案写在答题卡各题目的答题区域内,
超出答题区域或在草稿纸、本试卷上书写的答案无效。
4.保持卡面清洁,不要折叠、不要弄皱、弄破,不准使用涂改液、修正带、刮纸刀。
可能用到的相对原子质量:H-1 B-11 C-12 N-14 O-16 Na-23 Sc-45 V-51 Ga-70
A.图①:验证1-溴丁烷发生消去反应
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项符合
B.图②: 标准溶液滴定盐酸
题目要求。
C.图③:比较硫、碳、硅三种元素的非金属性强弱
1.化学与生产、生活、科技密切相关。下列说法错误的是
D.图④:蒸干 溶液获得 晶体
A.港珠澳大桥使用高性能富锌底漆是依据外加电流法防腐
B.“天和核心舱”电推进系统采用的氮化硼陶瓷属于新型无机非金属材料
C.屠呦呦用乙醚从青蒿中提取出对治疗疟疾有特效的青蒿素,该过程包括萃取操作 5. 用途广泛,利用 溶液与玻璃中 反应生产磨砂玻璃;利用反应:
D.农村推广风力发电、光伏发电有利于“碳达峰、碳中和” 3SiO+6C+2N Si N+6CO制备Si N 陶瓷。设 为阿伏加德罗常数的值。下列说法
2 2 3 4 3 4
不正确的是
2.烟气中的二氧化硫可用于处理含铬(Ⅵ)废水,其反应为:
A.1molSiO 中所含 键数目为4N
2 A
,下列化学用语正确的是
B.制备Si N 的反应中,生成 时转移电子数为
3 4
A. 元素位于周期表的ds区
C.2.8gN 与 的混合气体中所含质子数为1.4N
2 A
D.1L 的 溶液中所含H+数目为
B. 的 模型:
C.中子数为21的 核素符号:
D.用轨道表示式表示HO中O原子的杂化:
2
3.下列关于物质的工业制备涉及的相关反应中错误的是
6.卡维地洛类药物(丁)可用于治疗原发性高血压、有症状的充血性心力衰竭。以甲为原料合成丁
第六次模拟考试化学第试 1题 页 共 6 页
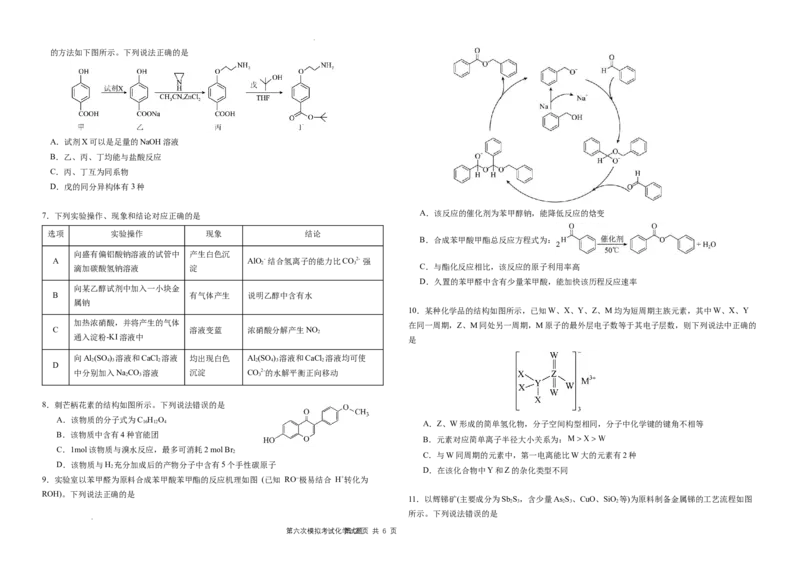
学学科科网网((北北京京))股股份份有有限限公公司司的方法如下图所示。下列说法正确的是
A.试剂X可以是足量的NaOH溶液
B.乙、丙、丁均能与盐酸反应
C.丙、丁互为同系物
D.戊的同分异构体有3种
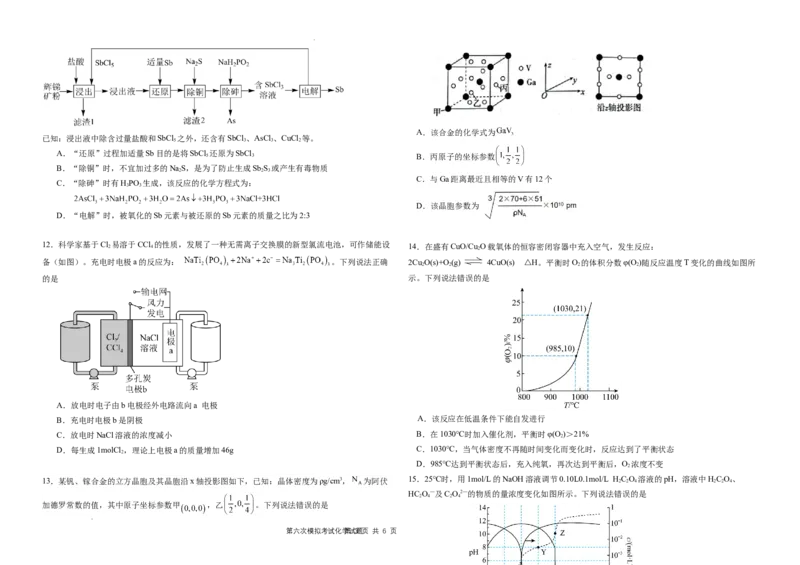
A.该反应的催化剂为苯甲醇钠,能降低反应的焓变
7.下列实验操作、现象和结论对应正确的是
选项 实验操作 现象 结论
B.合成苯甲酸甲酯总反应方程式为:
向盛有偏铝酸钠溶液的试管中 产生白色沉
A AlO- 结合氢离子的能力比CO2- 强
滴加碳酸氢钠溶液 淀 2 3 C.与酯化反应相比,该反应的原子利用率高
D.久置的苯甲醛中含有少量苯甲酸,能加快该历程反应速率
向某乙醇试剂中加入一小块金
B 有气体产生 说明乙醇中含有水
属钠
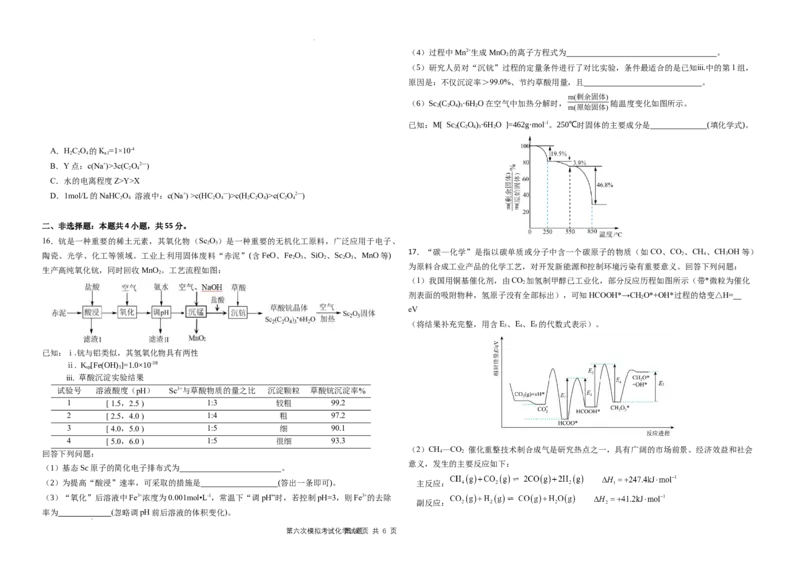
10.某种化学品的结构如图所示,已知W、X、Y、Z、M均为短周期主族元素,其中W、X、Y
加热浓硝酸,并将产生的气体
在同一周期,Z、M同处另一周期,M原子的最外层电子数等于其电子层数,则下列说法中正确的
C 溶液变蓝 浓硝酸分解产生NO
2
通入淀粉-KI溶液中
是
向Al (SO ) 溶液和CaCl 溶液 均出现白色 Al (SO ) 溶液和CaCl 溶液均可使
2 4 3 2 2 4 3 2
D
中分别加入NaCO 溶液 沉淀 CO2-的水解平衡正向移动
2 3 3
8.刺芒柄花素的结构如图所示。下列说法错误的是
A.该物质的分子式为C H O
16 12 4 A.Z、W形成的简单氢化物,分子空间构型相同,分子中化学键的键角不相等
B.该物质中含有4种官能团
B.元素对应简单离子半径大小关系为:
C.1mol该物质与溴水反应,最多可消耗2 mol Br
2 C.与W同周期的元素中,第一电离能比W大的元素有2种
D.该物质与H 充分加成后的产物分子中含有5个手性碳原子
2 D.在该化合物中Y和Z的杂化类型不同
9.实验室以苯甲醛为原料合成苯甲酸苯甲酯的反应机理如图 (已知 RO⁻极易结合 H+转化为
ROH)。下列说法正确的是
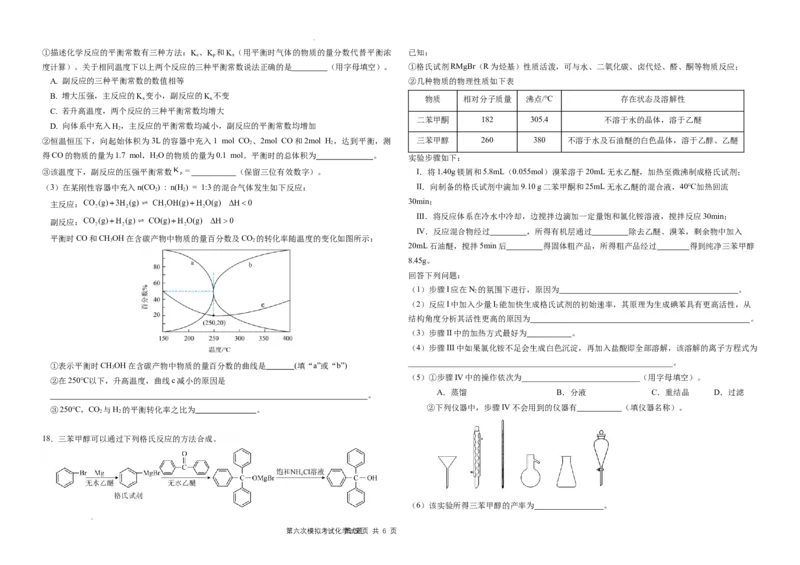
11.以辉锑矿(主要成分为Sb S,含少量As S、CuO、SiO 等)为原料制备金属锑的工艺流程如图
2 3 2 3 2
所示。下列说法错误的是
第六次模拟考试化学第试 2题 页 共 6 页
学学科科网网((北北京京))股股份份有有限限公公司司A.该合金的化学式为
已知:浸出液中除含过量盐酸和SbCl 之外,还含有SbCl 、AsCl 、CuCl 等。
5 3 3 2
A.“还原”过程加适量Sb目的是将SbCl 还原为SbCl
5 3 B.丙原子的坐标参数
B.“除铜”时,不宜加过多的NaS,是为了防止生成Sb S 或产生有毒物质
2 2 3
C.与Ga距离最近且相等的V有12个
C.“除砷”时有HPO 生成,该反应的化学方程式为:
3 3
D.该晶胞参数为
D.“电解”时,被氧化的Sb元素与被还原的Sb元素的质量之比为2:3
12.科学家基于Cl 2 易溶于CCl 4 的性质,发展了一种无需离子交换膜的新型氯流电池,可作储能设 14.在盛有CuO/Cu 2 O载氧体的恒容密闭容器中充入空气,发生反应:
备(如图)。充电时电极a的反应为: 。下列说法正确 2Cu O(s)+O (g) 4CuO(s) △H。平衡时O 的体积分数φ(O)随反应温度T变化的曲线如图所
2 2 2 2
的是 示。下列说法错误的是
A.放电时电子由b电极经外电路流向a 电极
B.充电时电极b是阴极 A.该反应在低温条件下能自发进行
C.放电时NaCl溶液的浓度减小 B.在1030℃时加入催化剂,平衡时φ(O)>21%
2
D.每生成1molCl ,理论上电极a的质量增加46g C.1030℃,当气体密度不再随时间变化而变化时,反应达到了平衡状态
2
D.985℃达到平衡状态后,充入纯氧,再次达到平衡后,O 浓度不变
2
13.某钒、镓合金的立方晶胞及其晶胞沿x轴投影图如下,已知:晶体密度为ρg/cm3, 为阿伏 15.25℃时,用1mol/L的NaOH溶液调节0.10L0.1mol/L H 2 C 2 O 4 溶液的pH,溶液中H 2 C 2 O 4 、
HC O—及C O2—的物质的量浓度变化如图所示。下列说法错误的是
2 4 2 4
加德罗常数的值,其中原子坐标参数甲 ,乙 。下列说法错误的是
第六次模拟考试化学第试 3题 页 共 6 页
学学科科网网((北北京京))股股份份有有限限公公司司(4)过程中Mn2+生成MnO 的离子方程式为 。
2
(5)研究人员对“沉钪”过程的定量条件进行了对比实验,条件最适合的是已知ⅲ.中的第1组,
原因是:不仅沉淀率>99.0%、节约草酸用量,且 。
m(剩余固体)
(6)Sc (C O)·6H O在空气中加热分解时, 随温度变化如图所示。
2 2 4 3 2 m(原始固体)
已知:M[ Sc (C O)·6H O ]=462g·mol-1。250℃时固体的主要成分是 (填化学式)。
2 2 4 3 2
A.HC O 的K =1×10-4
2 2 4 a1
B.Y点:c(Na+)>3c(C O2—)
2 4
C.水的电离程度Z>Y>X
D.1mol/L的NaHC O 溶液中:c(Na+) >c(HC O—)>c(H C O)>c(C O2—)
2 4 2 4 2 2 4 2 4
二、非选择题:本题共4小题,共55分。
16.钪是一种重要的稀土元素,其氧化物(Sc O )是一种重要的无机化工原料,广泛应用于电子、
2 3
17.“碳—化学”是指以碳单质或分子中含一个碳原子的物质(如CO、CO 、CH 、CHOH等)
陶瓷、光学、化工等领域。工业上利用固体废料“赤泥”(含FeO、Fe O 、SiO 、Sc O 、MnO等) 2 4 3
2 3 2 2 3
为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义。回答下列问题:
生产高纯氧化钪,同时回收MnO 。工艺流程如图:
2
(1)我国用铜基催化剂,由CO 加氢制甲醇已工业化,部分反应历程如图所示(带*微粒为催化
2
剂表面的吸附物种,氢原子没有全部标出),可知HCOOH*→CHO*+OH*过程的焓变△H=
2
eV
(将结果补充完整,用含E、E、E 的代数式表示)。
3 4 5
已知:ⅰ.钪与铝类似,其氢氧化物具有两性
ⅱ. K [Fe(OH) ]=1.0×10-38
sp 3
ⅲ. 草酸沉淀实验结果
试验号 溶液酸度(pH) Sc3+与草酸物质的量之比 沉淀颗粒 草酸钪沉淀率%
1 [ 1.5,2.5 ) 1:3 较粗 99.2
2 [ 2.5,4.0 ) 1:4 粗 97.2
3 [ 4.0,5.0 ) 1:5 细 90.1
4 [ 5.0,6.0 ) 1:5 很细 93.3
(2)CH—CO 催化重整技术制合成气是研究热点之一,具有广阔的市场前景、经济效益和社会
回答下列问题: 4 2
意义,发生的主要反应如下:
(1)基态Sc原子的简化电子排布式为 。
(2)为提高“酸浸”速率,可采取的措施是 (答出一条即可)。 主反应:
(3)“氧化”后溶液中Fe3+浓度为0.001mol•L-1,常温下“调pH”时,若控制pH=3,则Fe3+的去除
副反应:
率为 (忽略调pH前后溶液的体积变化)。
第六次模拟考试化学第试 4题 页 共 6 页
学学科科网网((北北京京))股股份份有有限限公公司司①描述化学反应的平衡常数有三种方法:K、K 和K (用平衡时气体的物质的量分数代替平衡浓 已知:
c p x
度计算)。关于相同温度下以上两个反应的三种平衡常数说法正确的是 (用字母填空)。 ①格氏试剂RMgBr(R为烃基)性质活泼,可与水、二氧化碳、卤代烃、醛、酮等物质反应;
A. 副反应的三种平衡常数的数值相等 ②几种物质的物理性质如下表
B. 增大压强,主反应的K 变小,副反应的K 不变
x x 物质 相对分子质量 沸点/℃ 存在状态及溶解性
C. 若升高温度,两个反应的三种平衡常数均增大
二苯甲酮 182 305.4 不溶于水的晶体,溶于乙醚
D. 向体系中充入H,主反应的平衡常数均减小,副反应的平衡常数均增加
2
②恒温恒压下,向起始体积为3L的容器中充入1 mol CO 、2mol CO和2mol H ,达到平衡,测 三苯甲醇 260 380 不溶于水及石油醚的白色晶体,溶于乙醇、乙醚
2 2
得CO的物质的量为1.7 mol,H 2 O的物质的量为0.1 mol。平衡时的总体积为 。 实验步骤如下:
③该温度下,副反应的压强平衡常数 (保留三位有效数字)。 I.将1.40g镁屑和5.8mL(0.055mol)溴苯溶于20mL无水乙醚,加热至微沸制成格氏试剂;
(3)在某刚性容器中充入n(CO) : n(H) = 1:3的混合气体发生如下反应: II.向制备的格氏试剂中滴加9.10 g二苯甲酮和25mL无水乙醚的混合液,40℃加热回流
2 2
30min;
主反应:
III.将反应体系在冷水中冷却,边搅拌边滴加一定量饱和氯化铵溶液,搅拌反应30min;
副反应:
IV.反应混合物经过 ,所得有机层通过 除去乙醚、溴苯,剩余物中加入
平衡时CO和CHOH在含碳产物中物质的量百分数及CO 的转化率随温度的变化如图所示:
3 2
20mL石油醚,搅拌5min后 得固体粗产品,所得粗产品经过 得到纯净三苯甲醇
8.45g。
回答下列问题:
(1)步骤I应在N 的氛围下进行,原因为 。
2
(2)反应I中加入少量I 能加快生成格氏试剂的初始速率,其原理为生成碘苯具有更高活性,从
2
结构角度分析其活性更高的原因为 。
(3)步骤II中的加热方式最好为 。
(4)步骤III中如果氯化铵不足会生成白色沉淀,再加入盐酸即全部溶解,该溶解的离子方程式为
_________________________________________________________________。
①表示平衡时CHOH在含碳产物中物质的量百分数的曲线是 (填“a”或“b”)
3
(5)①步骤IV中的操作依次为_____________________________(用字母填空)。
②在250℃以下,升高温度,曲线c减小的原因是
A.蒸馏 B.分液 C.重结晶 D.过滤
。
③250℃,CO 与H 的平衡转化率之比为 。 ②下列仪器中,步骤IV不会用到的仪器有 (填仪器名称)。
2 2
18.三苯甲醇可以通过下列格氏反应的方法合成。
(6)该实验所得三苯甲醇的产率为 。
第六次模拟考试化学第试 5题 页 共 6 页
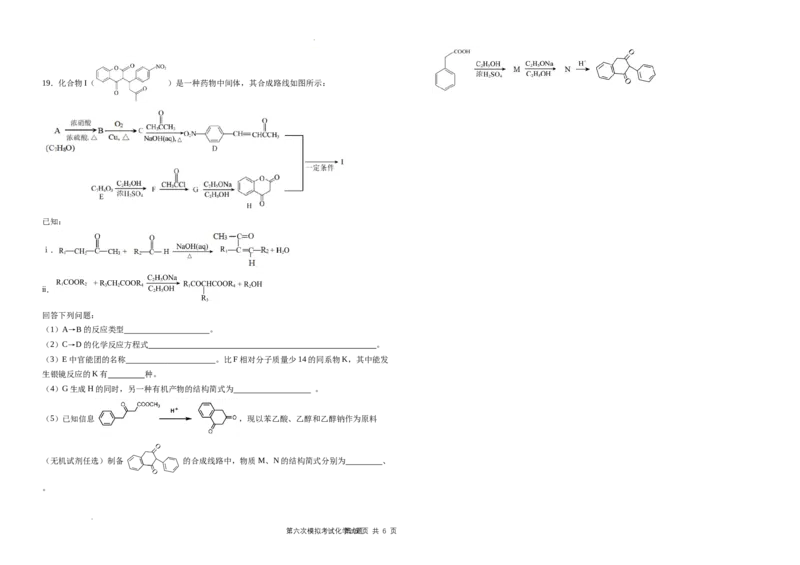
学学科科网网((北北京京))股股份份有有限限公公司司19.化合物I( )是一种药物中间体,其合成路线如图所示:
已知:
ⅰ.
ⅱ.
回答下列问题:
(1)A→B的反应类型 。
(2)C→D的化学反应方程式 。
(3)E中官能团的名称 。比F相对分子质量少14的同系物K,其中能发
生银镜反应的K有 种。
(4)G生成H的同时,另一种有机产物的结构简式为 。
(5)已知信息 ,现以苯乙酸、乙醇和乙醇钠作为原料
(无机试剂任选)制备 的合成线路中,物质M、N的结构简式分别为 、
。
第六次模拟考试化学第试 6题 页 共 6 页
学学科科网网((北北京京))股股份份有有限限公公司司