文档内容
人教版(2019)必修第一册第一章第一节 物质的分类及转
化课时训练一
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.文物是人类宝贵的历史文化遗产。按制作文物的主要材料分类,下列文物属于金属
文物的是
文
物
选 C.甲骨 D.竖线划纹黑
A.青铜亚长牛尊 B.虎形玉佩
项 片 陶尊
A.A B.B C.C D.D
2.2022年春节就要到了,一个名叫“福 氟 禄 氯 双全 醛 ”的物质 结构简式如
图 在学习化学的同学朋友圈中火了起来。该物质属于
A.混合物 B.无机物 C.有机物 D.卤代烃
3.下图中相邻两种物质均可归属为一类,下列分类正确的是
A.甲中两种物质水溶液都呈碱性 B.乙中两种物质都是碱性氧化物
C.丙中两种物质都是钠盐 D.丁中两种物质都是硫酸盐
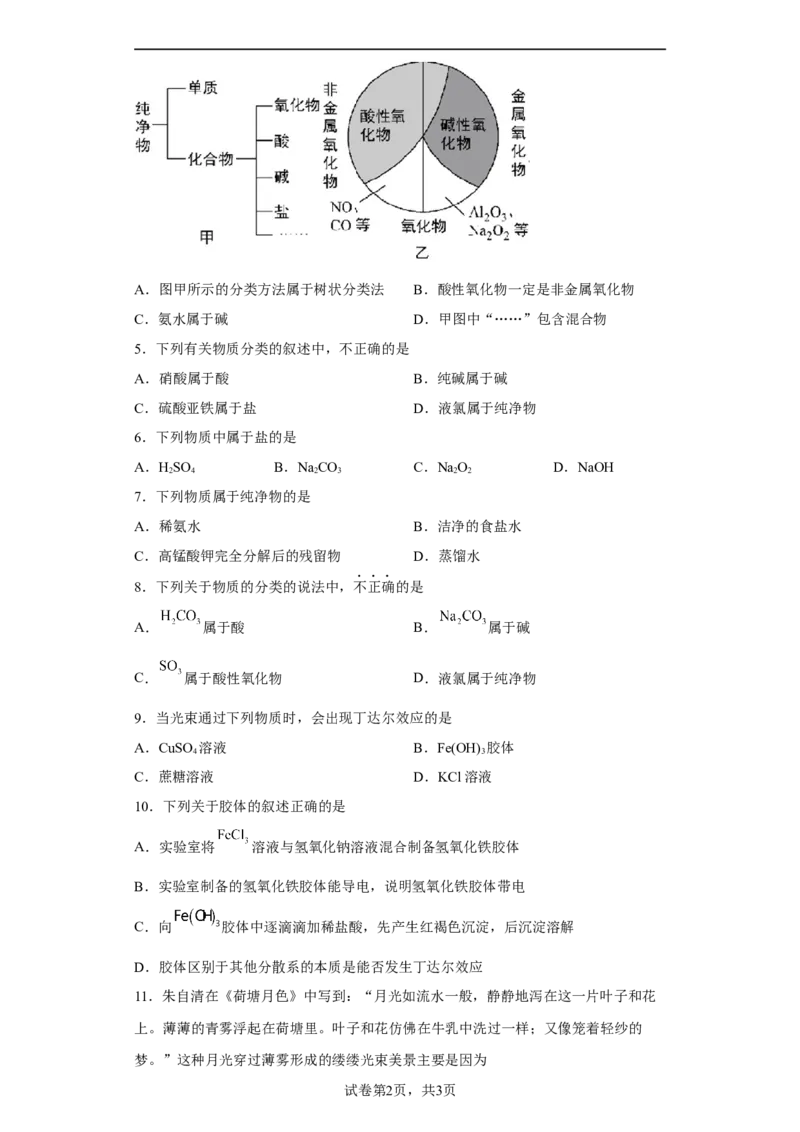
4.分类是一种重要的学习方法。物质的分类如图所示,下列说法中正确的是A.图甲所示的分类方法属于树状分类法 B.酸性氧化物一定是非金属氧化物
C.氨水属于碱 D.甲图中“……”包含混合物
5.下列有关物质分类的叙述中,不正确的是
A.硝酸属于酸 B.纯碱属于碱
C.硫酸亚铁属于盐 D.液氯属于纯净物
6.下列物质中属于盐的是
A.HSO B.NaCO C.NaO D.NaOH
2 4 2 3 2 2
7.下列物质属于纯净物的是
A.稀氨水 B.洁净的食盐水
C.高锰酸钾完全分解后的残留物 D.蒸馏水
8.下列关于物质的分类的说法中,不正确的是
A. 属于酸 B. 属于碱
C. 属于酸性氧化物 D.液氯属于纯净物
9.当光束通过下列物质时,会出现丁达尔效应的是
A.CuSO 溶液 B.Fe(OH) 胶体
4 3
C.蔗糖溶液 D.KCl溶液
10.下列关于胶体的叙述正确的是
A.实验室将 溶液与氢氧化钠溶液混合制备氢氧化铁胶体
B.实验室制备的氢氧化铁胶体能导电,说明氢氧化铁胶体带电
C.向 胶体中逐滴滴加稀盐酸,先产生红褐色沉淀,后沉淀溶解
D.胶体区别于其他分散系的本质是能否发生丁达尔效应
11.朱自清在《荷塘月色》中写到:“月光如流水一般,静静地泻在这一片叶子和花
上。薄薄的青雾浮起在荷塘里。叶子和花仿佛在牛乳中洗过一样;又像笼着轻纱的
梦。”这种月光穿过薄雾形成的缕缕光束美景主要是因为
试卷第2页,共3页A.光的折射 B.光与雾形成的丁达尔效应
C.小液滴的直径小于 D.光的反射
12.分散系1:食盐分散在水中形成无色透明溶液;分散系2:食盐分散在乙醇中形成
无色透明胶体。下列说法正确的是
A.两种分散系中分散质微粒直径相同
B.两种分散系均可用半透膜分离出NaCl
C.食盐在不同分散剂中可形成不同的分散系
D.能否产生丁达尔现象是两种分散系的本质区别
13.当光束通过下列物质时,不会出现丁达尔效应的是
A.云、雾 B.蔗糖溶液 C.有色玻璃 D. 胶体
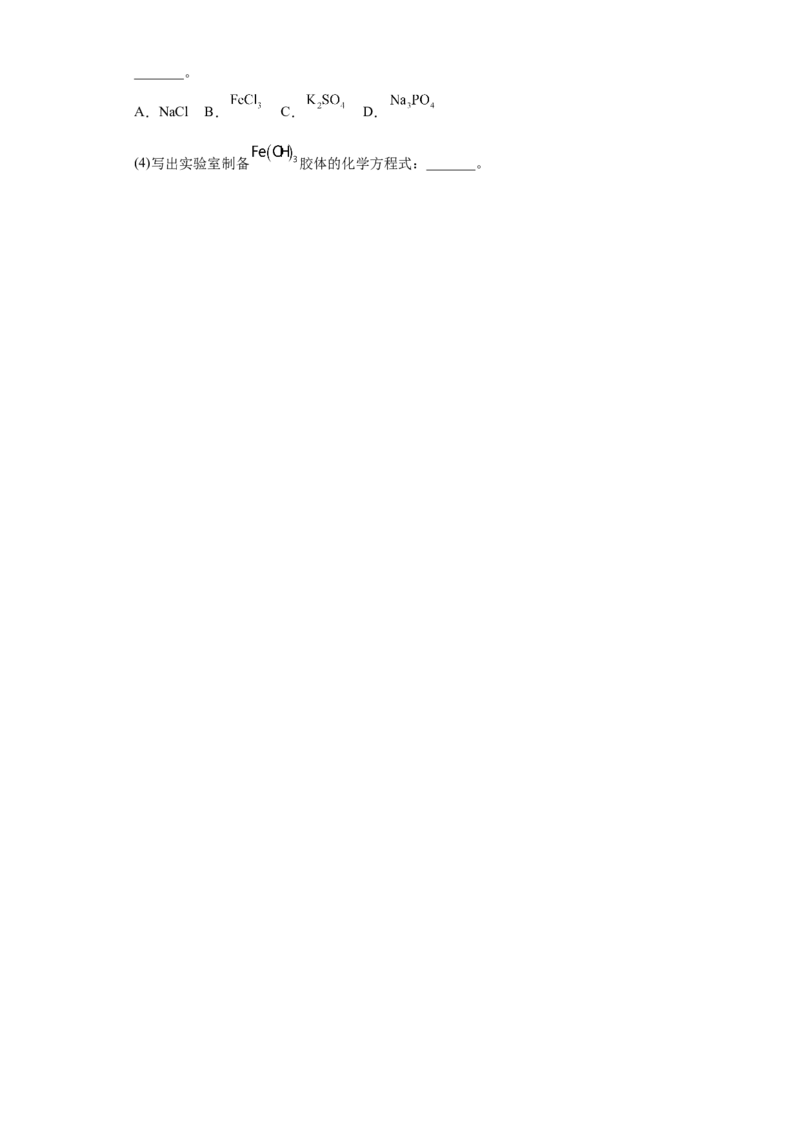
14.如图所示为实验室中制备胶体的一种方法。下列说法正确的是
A.该制备方法属于物理方法 B.烧杯中液体的颜色逐渐变浅
C.可用丁达尔效应判断是否制得胶体 D.加热能促使该分散系中的分散质粒子
直径减小
15.下列实验操作正确的是
A.蒸馏实验中温度计的水银球应插入液态混合物中
B.用酒精萃取碘水中的碘
C.分液时,使下层液体从下口流出之后,上层液体从上口倒出
D.将浓 溶液逐滴加到煮沸的 溶液制备 胶体
二、填空题
16.现有甲、乙、丙、丁四名同学分别进行Fe(OH) 胶体的制备实验。
3
甲同学:向1mol·L-1的FeCl 溶液中加少量NaOH溶液。
3
乙同学:直接加热饱和FeCl 溶液。
3
丙同学:向25mL沸水中逐滴加入5~6滴FeCl 饱和溶液,继续煮沸至溶液呈红褐色,
3
停止加热。试回答下列问题:(1)其中操作正确的同学是___________。
(2)证明有Fe(OH) 胶体生成的实验操作是___________。利用的胶体性质是
3
___________。
(3)在胶体中加入电解质或带有相反电荷的胶体粒子能使胶体粒子沉淀出来,丁同学利
用所制得Fe(OH) 胶体进行实验:
3
①将其装入U形管内,用石墨作电极,通电一段时间后发现阴极区附近的颜色逐渐变
深,这表明Fe(OH) 胶粒带___________(填“正”或“负”)电荷。
3
②向其中加入饱和NaSO 溶液,产生的现象是___________。
2 4
(4)丁同学在实验室进行了如图所示的实验。通过实验现象,据你推测X、Z烧杯中分
散质___________(填“相同”或“不同”),Y中产生的气体为___________。(填名称)
得到的红褐色透明液体主要成分是___________(填化学式)
17.铜器久置于空气中会和空气中的水蒸气、 、 作用产生“绿锈”,“绿锈”
俗称“铜绿”[化学式为 ],“铜绿”能跟酸反应生成铜盐和 、 。
某同学利用下述系列反应实现了“铜→铜绿→……→铜”的转化:
铜 铜绿 A Cu(OH) B Cu
2
(1)从三种不同分类标准回答,“铜绿”属于哪类物质:_______。
(2)请写出“铜绿”与盐酸反应的化学方程式:_______。
(3)写出④、⑤的化学方程式:
④_______、⑤_______。
(4)上述转化过程中属于化合反应的是_______,属于复分解反应的是_______,属于分
解反应的是_______。
(5)以Cu为原料,其他试剂自选,设计制备 的实验方案,并用流程图表示出来
_______。
18.回答下列问题:
(1)如图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了C HOH、CO、Fe O
2 5 2 2 3、
FeCl 、KOH,图中相连的物质均可归为一类,相交部分A、B、C、D为相应的分类标
3
试卷第4页,共3页准代号。
①相连的两种物质都是氧化物的是_______(填分类标准代号,下同)。
②图中相连的两种物质能够相互反应的是_______,所属的基本反应类型是_______反
应。
③上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,则该反应
的化学方程式为_______。
(2)分类方法应用广泛,属于同一类的物质具有相似性,在生活和学习中,使用分类的
方法处理问题可以做到举一反三,还可以达到由此及彼的效果。
都属于酸性氧化物,由 ,可得出 与NaOH反应的化
学方程式为_______。
(3)化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧
碱和纯碱。从物质的分类角度看,不恰当的一种物质是_______。
19.下列物质:①NaOH ②HNO ③KClO ④H O⑤ NaHCO ⑥CH
3 3 2 3 4
(1)属于酸的是_______;
(2)属于碱的是_______;
(3)属于盐的是_______;
(4)属于氧化物的是_______;
(5)有机物的是_______(填序号)
20.下列4组物质均有一种物质的类别与其他3种不同:
A.CaO、NaO、CO、CuO B.H、C、P、Cu
2 2 2
C.O、Fe、Cu、Zn D.HCO、HO、HSO 、HNO
2 2 3 2 2 4 3
(1)以上四组物质中与众不同的物质依次是(填化学式)A___________;B___________;
C___________;D___________。
(2)碱式碳酸铜可以看作是Cu(OH) 和CuCO 按照1∶1的比例组成的混合型化合物,写
2 3
出它与足量盐酸反应的化学方程式:___________。
三、实验题
21.现有甲、乙、丙三名同学分别进行Fe(OH) 胶体的制备实验。
3
I.甲同学向稀氯化铁溶液中加入少量的NaOH溶液;II.乙同学直接加热饱和FeCl 溶液;
3
III.丙同学向25mL沸水中逐滴加入5~6滴FeCl 饱和溶液;继续煮沸至溶液呈红褐色,
3
停止加热。 试回答下列问题:
(1)其中操作正确的同学是_______,写出此过程中的化学方程式:_______;
(2)证明有Fe(OH) 胶体生成的最简单实验操作是 _______;
3
(3)Fe(OH) 胶体能不能透过滤纸:_______ (填“能”或“不能”)。
3
(4)丁同学利用所制得的Fe(OH) 胶体进行下列实验:
3
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的
颜色逐渐变深,这表明Fe(OH) 胶粒带_______电荷。
3
②向其中加入饱和NaSO 溶液,产生的现象是_______;
2 4
③向所得Fe(OH) 胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为______;
3
继续滴加,沉淀最终消失且得棕黄色溶液,写出化学方程式_______;
④欲除去Fe(OH) 胶体中混有的NaCl,所用仪器物品是______;操作名称是______。
3
22.现有甲、乙、丙三名同学分别进行 胶体的制备实验。
甲同学:向 的氯化铁溶液中加入少量的NaOH溶液。
乙同学:直接加热饱和 溶液。
丙同学:向25mL沸水中逐滴加入5~6滴 饱和溶液;继续煮沸至溶液呈红褐色,
停止加热。
试回答下列问题:
(1)其中操作正确的同学是_______(填“甲”“乙”或“丙”)。
(2)证明有 胶体生成的实验操作是_______利用的胶体性质是_______。
(3)在胶体中加入电解质溶液或带有相反电荷的胶体粒子能使胶体粒子沉淀出来。丁同
学利用制得的 胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的
液体颜色逐渐变深,这表明 胶体微粒带_______(带“正”或“负”)电荷。
②实验证明,电解质的凝聚能力主要取决于与胶粒带相反电荷的离子所带的电荷数,
电荷数越大,凝聚力越大。向 胶体加入下列电解质时,其凝聚能力最强的为
试卷第6页,共3页_______。
A.NaCl B. C. D.
(4)写出实验室制备 胶体的化学方程式:_______。参考答案:
1.A
【详解】A.青铜主要由铜、锡含有少量铅的合金,属于金属文物,故A选;
B.玉佩主要成分为玉石,属于矿物质,为含硅化合物,不属于金属文物,故B不选;
C.胛骨片主要成分为动物骨骼,属于无机非金属文物,故C不选;
D.竖线划纹黑陶尊主要成分为硅酸盐等含硅化合物,不属于金属制品,故D不选;
故选A。
2.C
【详解】依据图中物质结构简式可知该物质含有C、H、O、F、Cl共5种元素,属于有机
物,故选C。
3.D
【详解】A.甲中NH 的水溶液呈碱性,但SO 的水溶液呈酸性,A不正确;
3 2
B.乙中NaO为碱性氧化物,但SO 为酸性氧化物,B不正确;
2 2
C.丙中两种物质,前者是钠的氧化物,后者是钠盐,C不正确;
D.丁中两种物质都是硫酸盐,前者是硫酸的钠盐,后者是硫酸的钾盐,D正确;
故选D。
4.A
【详解】A.树状分类法含义:对同一类事物按照某些属性进行分类的分类法,从甲图形
看应属于树状分类法,故A正确;
B.酸性氧化物不一定是非金属氧化物,如金属氧化物 为酸性氧化物,故B错误;
C.氨水为混合物,故C错误;
D.甲图中“……”是化合物的分类,不包含混合物,故D错误;
故答案为A。
5.B
【详解】A.硝酸属于无机酸,故A正确;
B.纯碱是碳酸钠,属于盐,故B错误;
C.硫酸亚铁属于硫酸盐或亚铁盐,故C正确;
D.液氯是液态Cl,属于纯净物,故D正确;
2
故答案选B。
6.B
【详解】A.HSO 在水中电离出的阳离子全部是H+,故HSO 属于酸,A不符合题意;
2 4 2 4B.NaCO 是水中电离出金属阳离子和酸根离子,故NaCO 属于盐,B符合题意;
2 3 2 3
C.NaO 由两种元素组成其中一种元素为氧元素为氧化物,C不符合题意;
2 2
D.NaOH在水中电离出的阴离子全部是OH-,属于碱,D不符合题意;
故选B。
7.D
【详解】A.稀氨水是氨气溶于水得到的水溶液,为混合物,故A错误;
B.食盐水为氯化钠的水溶液,为混合物,故B错误;
C.高锰酸钾受热分解生成锰酸钾、二氧化锰,残留物为混合物,故C错误;
D.蒸馏水只含水分子,为纯净物,故D正确;
故选:D。
8.B
【详解】A.水溶液中电离出的阳离子全部为氢离子的化合物为酸,HCO 属于酸,A正
2 3
确;
B.由金属阳离子或铵根离子与酸根离子构成的化合物叫做盐,则NaCO 属于盐不属于碱,
2 3
B错误;
C.与碱反应生成盐和水的氧化物叫酸性氧化物,SO 属于酸性氧化物,C正确;
3
D.液氯只含氯气分子,属于纯净物,D正确;
故选B。
9.A
【分析】丁达尔效应是胶体分散系特有的性质,分散质了粒子直径介于1−100nm的分散系,
属于胶体。
【详解】CuSO 溶液、蔗糖溶液、氯化钾溶液分散质粒子直径小于1nm,属于溶液,不能
4
产生丁达尔效应;Fe(OH) 胶体分散系分散质粒子直径介于1−100nm之间,属于胶体,能
3
产生丁达尔效应;
故答案选B。
【点睛】本题考查了胶体和其它分散系的本质区别和其特征性质,掌握基础是解题关键,
题目难度不大。
10.C
【详解】A.实验室将 溶液与沸水制备氢氧化铁胶体,选项A错误;
B.氢氧化铁胶体的胶粒带正电,胶体不带电,选项B错误;
答案第2页,共2页C.向 胶体中逐滴滴加稀盐酸,先发生胶体聚沉,后沉淀溶解,选项C正确;
D.分散系根据分散质粒子直径大小分为溶液、胶体和浊液,分散质粒子直径介于1~
100nm之间的分散系为胶体,故胶体区别于其他分散系的本质特征是分散质粒子的直径在
1nm~100nm之间,选项D错误;
答案选C。
11.B
【详解】A.折射是光从一种透明介质斜射入另一种透明介质时,传播方向发生变道化的
现象,而薄雾中只有空气一种介质,所以不是光的折射,A不正确;
B.雾分散到空气中属于胶体,光透过薄雾时产生丁达尔效应,B正确;
C.小液滴属于胶粒,其直径介于10-9~10-7m之间,C不正确;
D.胶粒直径比较小,不足以让光发生反射,光射到胶粒上,发生散射,D不正确;
故选B。
12.C
【详解】A.两种分散系中分散质微粒直径不相同,胶体中粒子直径在1~100nm、溶液中
粒子直径<1nm,故A错误;
B.分散系1是溶液,不能用半透膜分离出NaCl,故B错误;
C.根据题意,食盐在不同分散剂中可形成不同的分散系,故C正确;
D.分散质粒子直径不同是两种分散系的本质区别,故D错误;
选C。
13.B
【分析】当光束通过胶体分散系时会产生丁达尔效应,只要判断出分散系是胶体即可。
【详解】A.云、雾是胶体,有丁达尔效应,A不符合题意;
B.蔗糖溶液是溶液不是胶体,不会出现丁达尔效应,B符合题意;
C.有色玻璃是胶体,有丁达尔效应,C不符合题意;
D.Fe(OH) 胶体属于胶体,有丁达尔效应,D不符合题意;
3
故选B。
14.C
【详解】A.该制备方法有氢氧化铁生成,属于化学方法,故A错误;
B.烧杯中液体逐渐变为红褐色胶体,故B错误;
C.胶体能产生丁达尔效应,可用丁达尔效应判断是否制得胶体,故C正确;
D.加热可使胶体聚沉,加热能促使该分散系中的分散质粒子直径增大,故D错误;选C。
15.C
【详解】A.蒸馏实验中温度计的水银球应与蒸馏烧瓶的支管口相平,A错误;
B.酒精与水互溶,不能用于萃取碘水中的碘,B错误;
C.分液时为了避免污染,下层液体从下口流出,上层液体从上口倒出,C正确;
D.将浓 溶液逐滴加到煮沸的 溶液会得到 沉淀,D错误;
故选C。
16.(1)丙
(2) 用激光笔照射该透明液体,若出现明显的光路,则说明有Fe(OH) 胶体生成
3
丁达尔效应;
(3) 正 有红褐色沉淀生成
(4) 不同 二氧化碳 Fe(OH)
3
【详解】(1)甲同学向1mol·L-1氯化铁溶液中加入少量的NaOH溶液,会发生复分解反应
生成红褐色沉淀,乙同学直接加热饱和FeCl 溶液,三价铁会水解生成红褐色沉淀,制备氢
3
氧化铁胶体的方法:向25mL沸水中逐滴加入5~6滴FeCl 饱和溶液,继续煮沸至溶液呈红
3
褐色,停止加热,因此正确的同学是丙。
(2)胶体具有丁达尔效应,当光束通过胶体时,从侧面观察到一条光亮的“通路”,则证
明有胶体生成,因此证明有Fe(OH) 胶体生成的实验操作是用激光笔照射该透明液体,若
3
出现明显的光路,则说明有Fe(OH) 胶体生成,这是利用了胶体的丁达尔效应。
3
(3)①胶体具有电泳性质,电泳实验能证明胶粒带电,胶粒向负极移动,说明Fe(OH) 胶
3
粒带正电;
②胶体具有聚沉的性质,向胶体中加入可溶性的电解质、加热、搅拌等条件会使胶体聚沉,
所以向其中加入饱和NaSO 溶液,产生的现象是有红褐色沉淀生成。
2 4
(4)在X烧杯中分散系为FeCl 溶液,在Z烧杯中分散系为Fe(OH) 胶体,两者分散质不
3 3
同。前者不能产生丁达尔效应,后者可以产生丁达尔效应。产生的气体是二氧化碳,涉及
到的反应为:3CaCO +2FeCl +3H O=2Fe(OH) (胶体)+3CO ↑十3CaCl 。
3 3 2 3 2 2
17.(1)盐、铜盐、碱式盐(或碳酸盐)
(2)Cu (OH)CO+4HCl=2CuCl +CO ↑+3H O
2 2 3 2 2 2
答案第4页,共2页(3) Cu(OH) CuO+HO CuO+H Cu+H O
2 2 2 2
(4) ① ②③ ④
(5)
【详解】(1)铜绿化学式是Cu (OH) CO,电离产生金属阳离子和酸根阴离子,因此属于
2 2 3
盐;由于电离产生的金属阳离子是Cu2+,因此该物质属于铜盐;电离产生的阴离子除含有
外,还含有OH-,因此该盐又属于碱式盐;电离产生的酸根阴离子是 ,因此该盐
也属于碳酸盐,故“铜绿”属于盐、铜盐、碱式盐(或碳酸盐);
(2)铜绿与盐酸反应产生CuCl 、HO、CO,反应方程式为:
2 2 2
Cu (OH) CO+4HCl=2CuCl +CO ↑+3H O;
2 2 3 2 2 2
(3)反应④中Cu(OH) 受热分解产生CuO和水,反应方程式为Cu(OH) CuO+HO;反
2 2 2
应⑤是CuO与H 混合加热,反应产生Cu、HO,反应方程式为:CuO+H Cu+H O;
2 2 2 2
(4)反应①是Cu、O、CO、HO反应产生铜绿Cu (OH) CO,反应物是多种,生成物只
2 2 2 2 2 3
有一种,反应基本类型属于化合反应;
反应②是Cu (OH) CO 与HCl反应产生CuCl 、CO、HO。反应基本类型是复分解反应;
2 2 3 2 2 2
反应③是CuCl 与NaOH发生复分解反应产生Cu(OH) 沉淀和NaCl,反应类型为复分解反
2 2
应;
反应④是Cu(OH) 受热分解产生CuO和水,反应类型是分解反应;
2
反应⑤是CuO与H 在加热时反应产生Cu、HO,反应类型是置换反应;
2 2
故上述转化过程中属于化合反应的为①;属于复分解反应的为②③;属于分解反应的为④;
(5)Cu与O 加热反应产生CuO,CuO与HSO 反应产生CuSO 和水,则物质转化流程图
2 2 4 4
为: 。
18.(1) B D 复分解 Fe O+6HCl=2FeCl +3H O
2 3 3 2(2)2NaOH+SO =Na SO +H O
3 2 4 2
(3)纯碱即NaCO
2 3
【详解】(1)①氧化物是指由两种元素其中一种是氧元素的化合物,故CO 和Fe O 属于
2 2 3
氧化物,则组成相连的两种物质都是氧化物的是B,故答案为:B;
②已知C HOH与CO,CO 与Fe O,Fe O 与FeCl 均不反应,FeCl 与KOH能够反应生
2 5 2 2 2 3 2 3 3 3
成Fe(OH) 沉淀和KCl,图中相连的两种物质能够相互反应的是D,方程式为:
3
FeCl +3KOH=Fe(OH) ↓+3KCl,该反应所属的基本反应类型是复分解反应,故答案为:D;
3 3
复分解;
③上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,即Fe O 和HCl
2 3
反应生成FeCl 和HO,则该反应的化学方程式为Fe O+6HCl=2FeCl +3H O,故答案为:
3 2 2 3 3 2
Fe O+6HCl=2FeCl +3H O;
2 3 3 2
(2)由 ,即酸性氧化物和碱反应生成盐和水,故可得出
与NaOH反应的化学方程式为:2NaOH+SO =Na SO +H O,故答案为:
3 2 4 2
2NaOH+SO =Na SO +H O;
3 2 4 2
(3)酸是指在水溶液中电离出的阳离子全部为H+的化合物,故硝酸、硫酸和盐酸均属于
酸,而碱是指在水溶液中电离出的阴离子全部为OH-的化合物,故烧碱即NaOH属于碱,
而纯碱为NaCO 不是碱,而是盐,故从物质的分类角度看,不恰当的一种物质是纯碱即
2 3
NaCO,故答案为:纯碱即NaCO。
2 3 2 3
19.(1)②
(2)①
(3)③⑤
(4)④
(5)⑥
【分析】①NaOH是碱,②HNO 是酸,③KClO 是盐④HO是氧化物⑤ NaHCO 盐
3 3 2 3
⑥CH 是有机物
4
【详解】(1)②HNO 是酸,答案:②;
3
(2)①NaOH是碱,答案①;
答案第6页,共2页(3)③KClO 是盐,⑤ NaHCO 盐,答案:③⑤
3 3
(4)④HO是氧化物,答案:④;
2
(5)⑥CH 是有机物,答案:⑥;
4
20.(1) CO Cu O HO
2 2 2
(2)Cu (OH) CO+4HCl=2CuCl +3H O+CO↑
2 2 3 2 2 2
【解析】(1)
A中CaO、NaO、CuO均是金属氧化物、碱性氧化物,CO 是非金属氧化物,酸性氧化物,
2 2
与众不同的是CO;
2
B中H、C、P均是非金属单质,Cu是金属单质,与众不同的是Cu;
2
C中Fe、Cu、Zn均是金属单质,O 是非金属单质,与众不同的是O;
2 2
D中HCO、HSO 、HNO 均属于酸,HO属于非金属氧化物,与众不同的是HO;
2 3 2 4 3 2 2
(2)
碱式碳酸铜可以看作是Cu(OH) 和CuCO 按照1∶1的比例组成的混合型化合物,则它与足
2 3
量盐酸反应生产氯化铜、水、二氧化碳,反应的化学方程式为
Cu (OH) CO+4HCl=2CuCl +3H O+CO↑。
2 2 3 2 2 2
21.(1) 丙同学
(2)用激光笔照射,有一条明亮的光路,则有 胶体生成
(3)能
(4) 正 有红褐色沉淀生成 电离出的 使 胶体发生聚
沉 半透膜 渗析
【分析】实验室制备氢氧化铁胶体的操作为:向25mL沸水中逐滴加入5~6滴 饱和溶
液,继续煮沸至溶液呈红褐色,停止加热,得到氢氧化铁胶体,其反应为
;
胶体具有的性质有:丁达尔效应;聚沉;吸附性;电泳;渗析;【详解】(1)甲同学向稀氯化铁溶液中加入少量的NaOH溶液,发生反应
,没有胶体生成,甲同学操作错误;
乙同学直接加热饱和FeCl 溶液,促进FeCl 溶液水解,得到氢氧化铁沉淀;
3 3
丙同学向25mL沸水中逐滴加入5~6滴FeCl 饱和溶液;继续煮沸至溶液呈红褐色,停止
3
加热,得到氢氧化铁胶体,其反应为 ,故填丙同学;
;
(2)根据胶体的丁达尔效应,证明有Fe(OH) 胶体生成的最简单实验是丁达尔效应,其操
3
作为用激光笔照射时,会有一道明亮的光路。故填用激光笔照射,有一条明亮的光路,则
有 胶体生成;
(3)滤纸孔径比半透膜大,溶液和胶体均能透过滤纸,胶体不能透过半透膜,故填能;
(4)①某些胶体微粒吸附阴离子或阳离子带电,可以发生电泳现象,将Fe(OH) 胶体装入
3
U形管内,用石墨作电极,接通直流电,因为阴离子向阳极移动,阳离子向阴极移动,通
电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH) 胶粒带正电荷,故填正;
3
②胶体具有聚沉的性质,向Fe(OH) 胶体中加入饱和NaSO 溶液,发生聚沉现象,有红褐
3 2 4
色沉淀生成,故填有红褐色沉淀生成;
③向氢氧化铁胶体中逐滴加入 溶液, 电离出的 使 胶体发生聚沉,
使 沉淀溶解,会观察到先出现红褐色沉淀,后沉淀消失,溶解为黄色溶液,反
应的化学方程式: ,故填 电离出的 使
胶体发生聚沉; ;
④ 、 均可以通过半透膜, 胶体不能透过,故可以采用渗析法来提纯胶体,
所用仪器物品是半透膜,提纯分离的方法为渗析,故填半透膜;渗析。
22.(1)丙
答案第8页,共2页(2) 用激光笔照射溶液,若出现明显的光路,证明有Fe(OH) 胶体生成 丁达尔
3
效应
(3) 正 D
(4)FeCl +3H O Fe(OH) (胶体)+3HCl
3 2 3
【详解】(1)实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,继续加
热至溶液变为红褐色时立即停止加热,因此操作正确的是丙同学,其它做法都不能生成胶
体,往往得到沉淀,故答案为:丙;
(2)胶体具有丁达尔效应,当用激光笔照射时,会有一道明亮的光路,因此证明有
Fe(OH) 胶体生成的实验操作是用激光笔照射溶液,若出现明显的光路,证明有Fe(OH) 胶
3 3
体生成,故答案为:用激光笔照射溶液,若出现明显的光路,证明有Fe(OH) 胶体生成;
3
丁达尔效应;
(3)①Fe(OH) 胶粒带正电,通电时带正电荷的粒子向阴极移动,阴极附近的颜色逐渐变
3
深,故答案为:正;D;
②电解质的凝聚能力主要取决于与胶粒带相反电荷的离子所带的电荷数,电荷数越大,凝
聚力越大。由于Fe(OH) 胶粒带正电,选项A~D中阴离子所带电荷数分别是1、1、2、
3
3,所以凝聚能力最强的为NaPO ,故答案选D;
3 4
(4)实验室制备 胶体的化学方程式为:FeCl +3H O Fe(OH) (胶体)+3HCl,故答
3 2 3
案为:FeCl +3H O Fe(OH) (胶体)+3HCl。
3 2 3答案第10页,共2页