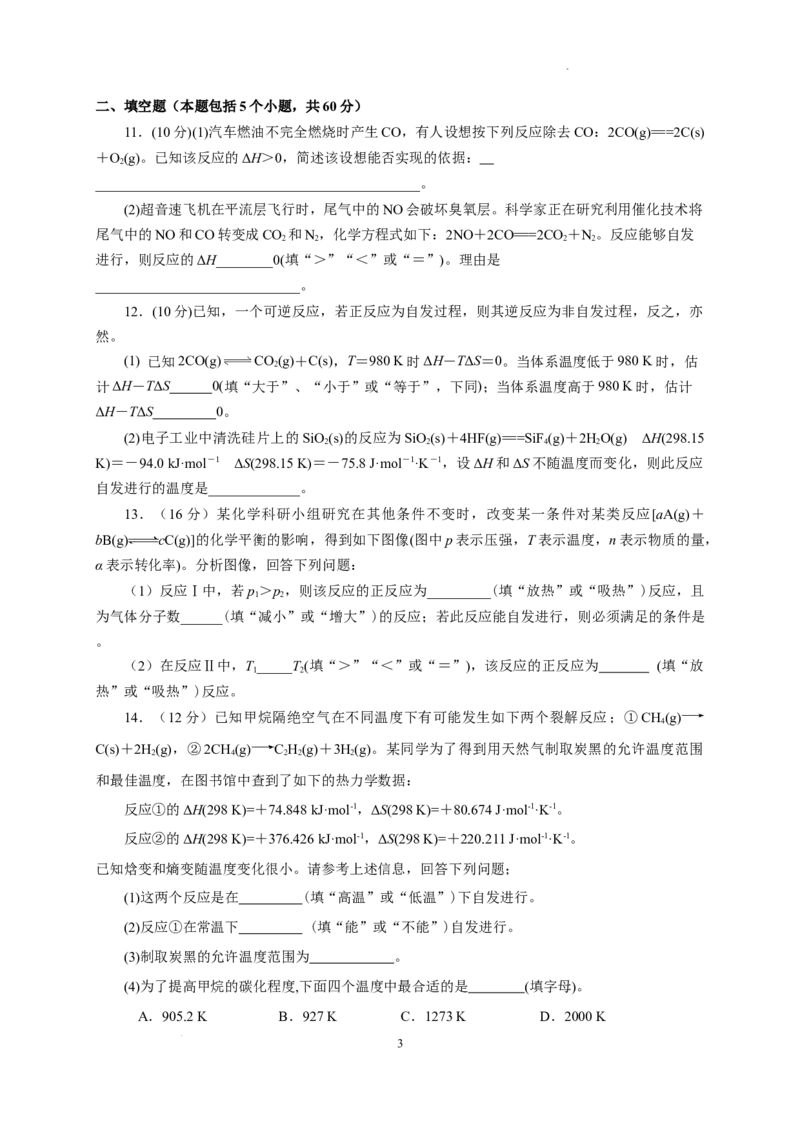文档内容
选择性必修1 第二章 第三节 化学反应的方向 测试题
榆次一中 李金虎
一、选择题(每小题只有一个正确选项,每小题4分,共40分)
1. 已知“凡气体分子总数增多的反应一定是熵增大的反应”。一定条件下,下列反应不能自发进
行的是( )
A.2O(g)===3O (g) ΔH<0
3 2
B.2CO(g)===2C(s)+O(g) ΔH>0
2
C.N(g)+3H(g) 2NH (g) ΔH<0
2 2 3
D.CaCO (s)===CaO(s)+CO(g) ΔH>0
3 2
2. 下列说法完全正确的是
A.自发进行的反应均是放热反应
B.ΔS为正值的反应均能自发进行
C.物质的量增加的反应,ΔS为正值
D.CaCO (s)受热分解为CaO(s)和CO(g):ΔS>0
3 2
3. 下列说法正确的是
A.凡是放热反应都是自发的,因为吸热反应都是非自发的
B.自发反应的现象一定非常明显,非自发反应的熵一定减小
C.常温下,C(s)+CO(g) 2CO(g)不能自发进行,则该反应的ΔH>0
2
D.反应2Mg(s)+CO(g)===C(s)+2MgO(s)能自发进行,则反应的ΔH>0
2
4. 碳酸铵[(NH )CO]在室温下就能自发地分解产生氨气,下列说法正确的是
4 2 3
A.碳酸铵分解是因为外界给予了能量
B.碳酸盐都不稳定,都能自发分解
C.碳酸铵分解是因为生成了易挥发的气体,使体系的熵增加
D.碳酸铵分解是吸热反应,根据焓判据不能自发分解
5. 研究化学反应的方向具有重要意义,下列说法正确的是
A.电解水的反应属于自发反应
B.能自发进行的反应一定能迅速发生
C.自发反应的熵一定增大,非自发反应的熵一定减小
D.2NO(g)+2CO(g) == N (g)+2CO(g) 在常温下能自发进行,则该反应的ΔH < 0
2 2
6. 在图Ⅰ中A、B两容器里,分别收集着两种互不作用的理想气体。若将中间活塞打开,如图Ⅱ,
两种气体分子立即都占有了两个容器。这是一个不伴随能量变化的自发过程。关于此过程的下
列说法不正确的是 ( )
1
学科网(北京)股份有限公司理想气体的自发混合
A.此过程是从混乱程度小的状态向混乱程度大的状态变化过程,即熵增大的过程
B.此过程为自发过程,而且没有热量的吸收或放出
C.此过程从有序到无序,混乱度增大
D.此过程是自发可逆的
7. 汽车尾气(含烃类、CO、NO与SO 等),是城市主要污染源之一,治理的办法之一是在汽车排
2
气管上装催化转化器,它使NO与CO反应生成可参与大气生态循环的无毒气体,反应原理:
2NO(g)+2CO(g)===N (g)+2CO(g),在298 K、100 kPa下,ΔH=-113 kJ·mol-1、 ΔS=-
2 2
145 J·mol-1·K-1。下列说法中错误的是( )
A.该反应中反应物的总能量高于生成物的总能量
B.该反应常温下不能自发进行,因此需要高温和催化剂
C.该反应常温下能自发进行,高温和催化剂只是加快反应的速率
D.汽车尾气中的这两种气体会与血红蛋白结合而使人中毒
8.下列关于自发过程的叙述中,正确的是
A.只有不需要任何条件就能够自动进行的过程才是自发过程
B.需要加热才能够进行的过程肯定不是自发过程
C.同一可逆反应的正、逆反应在不同条件下都有自发的可能
D.非自发过程在任何条件下都不可能变为自发过程
9. 汽车尾气(含烃类、CO、NO与SO 等)是城市主要污染源之一,治理的办法之一是在汽车排气
2
管上装催化转化器,它能使NO与CO反应生成可参与大气生态循环的无毒气体,其反应原理
是2NO(g)+2CO(g)===N (g)+2CO(g)。由此可知,下列说法中正确的是( )
2 2
A.该反应是熵增大的反应
B.该反应不能自发进行,因此需要合适的催化剂
C.该反应常温下能自发进行,催化剂条件只是加快反应的速率
D.该反应常温下能自发进行,因为正反应是吸热反应
10.在其他条件不变时,只改变某一条件,化学反应aA(g)+B(g) cC(g)的平衡变化图像如下
(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率),据此分析下列说法正确
的是( )
A.在图Ⅰ中,说明正反应为吸热反应
B.在图Ⅰ中,若p>p,则此反应的ΔS>0
1 2
C.在图Ⅱ中,说明该正反应为吸热反应
D.在图Ⅲ中,若T>T,则该反应能自发进行
1 2
2
学科网(北京)股份有限公司二、填空题(本题包括5个小题,共60分)
11.(10分)(1)汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)===2C(s)
+O(g)。已知该反应的ΔH>0,简述该设想能否实现的依据:
2
______________________________________________。
(2)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将
尾气中的NO和CO转变成CO 和N,化学方程式如下:2NO+2CO===2CO +N。反应能够自发
2 2 2 2
进行,则反应的ΔH________0(填“>”“<”或“=”)。理由是
_____________________________。
12.(10分)已知,一个可逆反应,若正反应为自发过程,则其逆反应为非自发过程,反之,亦
然。
(1) 已知2CO(g) CO(g)+C(s),T=980 K时ΔH-TΔS=0。当体系温度低于980 K时,估
2
计ΔH-TΔS 0(填“大于”、“小于”或“等于”,下同);当体系温度高于980 K时,估计
ΔH-TΔS 0。
(2)电子工业中清洗硅片上的SiO(s)的反应为SiO(s)+4HF(g)===SiF (g)+2HO(g) ΔH(298.15
2 2 4 2
K)=-94.0 kJ·mol-1 ΔS(298.15 K)=-75.8 J·mol-1·K-1,设ΔH和ΔS不随温度而变化,则此反应
自发进行的温度是_____________。
13.(16分)某化学科研小组研究在其他条件不变时,改变某一条件对某类反应[aA(g)+
bB(g) cC(g)]的化学平衡的影响,得到如下图像(图中p表示压强,T表示温度,n表示物质的量,
α表示转化率)。分析图像,回答下列问题:
(1)反应Ⅰ中,若p >p ,则该反应的正反应为_________(填“放热”或“吸热”)反应,且
1 2
为气体分子数______(填“减小”或“增大”)的反应;若此反应能自发进行,则必须满足的条件是
。
(2)在反应Ⅱ中,T_____T(填“>”“<”或“=”),该反应的正反应为 (填“放
1 2
热”或“吸热”)反应。
14.(12分)已知甲烷隔绝空气在不同温度下有可能发生如下两个裂解反应;①CH(g)
4
C(s)+2H(g),②2CH(g) C H(g)+3H(g)。某同学为了得到用天然气制取炭黑的允许温度范围
2 4 2 2 2
和最佳温度,在图书馆中查到了如下的热力学数据:
反应①的ΔH(298 K)=+74.848 kJ·mol-1,ΔS(298 K)=+80.674 J·mol-1·K-1。
反应②的ΔH(298 K)=+376.426 kJ·mol-1,ΔS(298 K)=+220.211 J·mol-1·K-1。
已知焓变和熵变随温度变化很小。请参考上述信息,回答下列问题;
(1)这两个反应是在 (填“高温”或“低温”)下自发进行。
(2)反应①在常温下 (填“能”或“不能”)自发进行。
(3)制取炭黑的允许温度范围为 。
(4)为了提高甲烷的碳化程度,下面四个温度中最合适的是 (填字母)。
A.905.2 K B.927 K C.1273 K D.2000 K
3
学科网(北京)股份有限公司15.(12分)已知在 100kPa、298.15K 时,石灰石分解反应:CaCO (s)═CaO(s)+CO (g) ΔH
3 2
=+178.3kJ·mol﹣1 ΔS=160.4J·mol﹣1·K﹣1,则:
(1)该反应________(填“能”或“不能”)自发进行;
(2)据本题反应数据分析,温度________(填“能”或“否”)成为反应方向的决定因素;
(3)若温度能决定反应方向,则该反应自发进行的最低温度为 。
(4)反应 CHOH(l)+NH(g)=CH NH (g)+H O(g) 在高温下自发向右进行,则下列判断正确的是
3 3 3 2 2
________。
A.ΔH>0 ΔH-TΔS<0 B.ΔH<0 ΔH-TΔS>0
C.ΔH>0 ΔH-TΔS>0 D.ΔH<0 ΔH-TΔS<0
1.答案B
解析: A项,是一个ΔH<0,ΔS>0的反应,一定能自发进行;B项,是一个ΔH>0,ΔS<0的反应,
一定不能自发进行;C项,是一个ΔH<0,ΔS<0的反应,低温条件下可自发进行;D项,是一个
ΔH>0,ΔS>0的反应,高温条件下可自发进行。
2.答案 D
解析:有些吸热反应也可以自发进行,如(NH )CO(s)===NHHCO (s)+NH (g),故A错;熵变与
4 2 3 4 3 3
反应的自发性有关,但不能独立地作为反应是否自发的判据,故B错;物质的量增加的反应,其混
乱度不一定增加,即ΔS不一定为正值,如2HS(g)+O(g)===2H O(l)+2S(s),故C错;CaCO (s)的
2 2 2 3
分解产生了气体,为熵增加反应,故D正确。
3.答案 C
解析:不能仅仅根据焓变判断反应的自发性,放热反应不一定都是自发进行的,吸热反应也可能是
自发进行的,A项错误;自发进行的反应,其现象不一定非常明显,非自发反应的熵不一定减小,
B项错误;根据反应C(s)+CO(g) 2CO(g)不能自发进行可知,该反应的 ΔH-TΔS>0,又知该
2
反应ΔS>0,则该反应的ΔH>0,C项正确;反应2Mg(s)+CO(g) ===C(s)+2MgO(s)能自发进行,
2
则ΔH-TΔS<0,因ΔS<0,则ΔH<0,D项错误。
4.答案 C
解析:碳酸铵分解是吸热反应,因此不能用焓判据来解释反应的自发性,其反应能够自发进行,是
因为体系中氨气的生成使熵增大。
5.答案 D
解析:电解水的反应属于非自发反应,A错误;能自发进行的反应不一定能迅速发生,B错误;自
发反应有熵减的,非自发反应有熵增的,C错误;2NO(g)+2CO(g)==N (g)+2CO(g)是一个熵减的
2 2
反应,常温下要自发一定是放热反应,ΔH < 0,D正确。
6.答案 D
4
学科网(北京)股份有限公司解析 根据题意ΔH=0,ΔS>0,由ΔH-TΔS推知该过程能自发进行,气体扩散为熵增过程,而其
逆过程不能自发进行。
7.答案 B
解析 该反应是放热反应,反应物总能量高于生成物的总能量,A项正确;常温下,ΔH-TΔS=-
113 kJ·mol-1-298 K×[-145 J·mol-1·K-1]×10-3 kJ/J<0,故常温下该反应可自发进行,高温和催化
剂只是加快反应速率,B项错误,C项正确;CO和NO均会与血红蛋白结合而使人中毒。
8.答案 C
解析:A项,自发过程可能需要在一定条件下自发进行,如木炭的燃烧,故A错;B项,木炭的燃
烧是需要加热的自发过程,故B错;D项,CaCO =====CaO+CO↑属于在高温下进行的非自发过
3 2
程,故D错。
9.答案 C
解析 只使用催化剂便可使尾气发生转化,故此反应能自发进行。因反应是气体物质的量减小的反
应,故为熵减小的反应。因熵减小不利于反应自发进行,故自发进行的原因是正反应为反应放热。
10.答案 D
解析 A项,由图Ⅰ可知,图中随着温度的升高反应物的平衡转化率减小,升高温度平衡向逆反应
方向移动,则正反应为放热反应,错误;B项,图Ⅰ可知,同一温度下,若p>p ,增大压强,反
1 2
应物的平衡转化率增大,平衡向正反应方向移动,则a+1>c,ΔS<0,错误;C项,由图Ⅱ可知,T
1
时反应速率快,T>T ,T 平衡时的n(C)小于T 平衡时的n(C),升高温度平衡向逆反应方向移动,
1 2 1 2
正反应为放热反应,错误;D项,由图Ⅲ可知,增大压强平衡不移动,则a+1=c,若T>T,升高
1 2
温度A的转化率减小,平衡向逆反应方向移动,则ΔH<0,该反应能自发进行,正确。
11.答案:(1)不能实现,因为该反应的ΔH>0,ΔS<0,反应不可能自发进行 (2)< 该反应的ΔS
<0,因该反应能自发进行,根据ΔG=ΔH-TΔS<0,可知ΔH<0
12.答案 (1)小于 大于 (2)小于1 240 K
解析 (1)C(s)+CO(g) 2CO(g)的反应为吸热反应,ΔH>0,则2CO(g) CO(g)+C(s)为放
2 2
热反应,ΔH<0,且该反应ΔS<0,则当T<980 K时,ΔH-TΔS<0,T>980 K时,ΔH-TΔS>0。
(2)由题给信息,要使反应能自发进行,须有 ΔH-TΔS<0,即-94.0 kJ·mol-1-T×[-75.8
J/(mol·K)]×10-3 kJ/J<0则T<=1.24×103 K。
13.答案 (1)放热 减小 低温 (2)< 放热
解析:(1)反应Ⅰ中,恒压下温度升高,α(A)减小,即升高温度平衡逆向移动,则该反应的正反
应为放热反应,ΔH<0;由p >p 知恒温时压强增大,α(A)增大,说明此反应为气体分子数减小的
1 2
反应,即为熵减反应,ΔS<0。放热、熵减反应只能在低温条件下自发进行。(2)反应Ⅱ中,T 条
2
件下反应先达到平衡状态,说明T >T ,温度越高,平衡时C的物质的量越小,即升高温度平衡逆
2 1
向移动,则该反应的正反应为放热反应。
14. 答案 (1)高温 (2)不能 (3)927.8~1790.4 K (4)C
解析 (1)该反应是吸热的熵增反应,在高温下自发。
5
学科网(北京)股份有限公司(2)ΔH-TΔS=74.848 kJ·mol-1-80.674×10-3 kJ·mol-1·K-1×298 K=50.807 kJ·mol-1>0,所以该反应在常温下
不能自发进行。
(3)甲烷裂解为炭黑和氢气时,ΔH-TΔS=74.848 kJ·mol-1-80.674×10-3 kJ·mol-1·K-1×T<0,解得T>927.8
K;裂解为乙炔时,ΔH-TΔS=376.426 kJ·mol-1-220.211×10-3 kJ·mol-1·K-1×T<0,解得T>1709.4 K,即
温度高于1709.4 K时自发裂解为乙炔和氢气,所以要制取炭黑,必须控制温度在927.8~1790.4 K的
范围内。
(4)要提高甲烷的碳化程度,应在927.8~1790.4 K的范围内尽可能提高温度。
15.答案(1)不能 (2)能 (3)1112K (4)A
解析(1)该反应的ΔG=ΔH-TΔS =178.3KJ•mol﹣1-298.15K×0.1604KJ•mol﹣=130.5KJ•mol﹣1 ,ΔG>
0,所以不能自发,故答案为:不能;(2)该反应的ΔG=ΔH-TΔS=178.3KJ•mol﹣1-
298.15K×0.1604KJ•mol﹣1=130.5KJ•mol﹣1 ,ΔG>0,所以在100Kpa、298.15K 时,石灰石分解反应
为非自发反应,但在高温的条件下能自发行进,故答案为:能;(3)要想反应能自发进行则需
ΔG=ΔH-TΔS<0,178.3KJ•mol﹣1﹣T×160.4KJ•mol﹣1=0,解得:T=1112K,故答案为:1112K;
(4)该反应在一定温度下能够自发的向右进行,这说明ΔH-TΔS一定是小于0,根据方程式可知该
反应的ΔS>0,所以如果ΔH<0,则该反应在任何温度下都是自发进行的,而该反应在一定温度下
能够自发的向右进行,因此该反应的反应热ΔH>0,故选A。
6
学科网(北京)股份有限公司7
学科网(北京)股份有限公司