文档内容
人教版(2019)必修第一册第二章第三节 物质的量
课时训练四
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共0分)
1.配制 溶液的操作如下所示。下列说法正确的是
A.操作1前需用称量纸称取质量为 的
B.操作1确认 完全溶解后,应立刻进行操作2
C.操作4如果俯视,则 溶液浓度偏大
D.操作5后液面下降,需补充少量水至刻度线
2.下列实验仪器或装置的选择正确的是
配制
50.00mL0.1000mol.L-1 除去Cl 中的HCl 蒸馏用冷凝管 盛装Na 2 SiO 3 溶液的
2 试剂瓶
NaCO 溶液
2 3
A B C D
A.A B.B C.C D.D
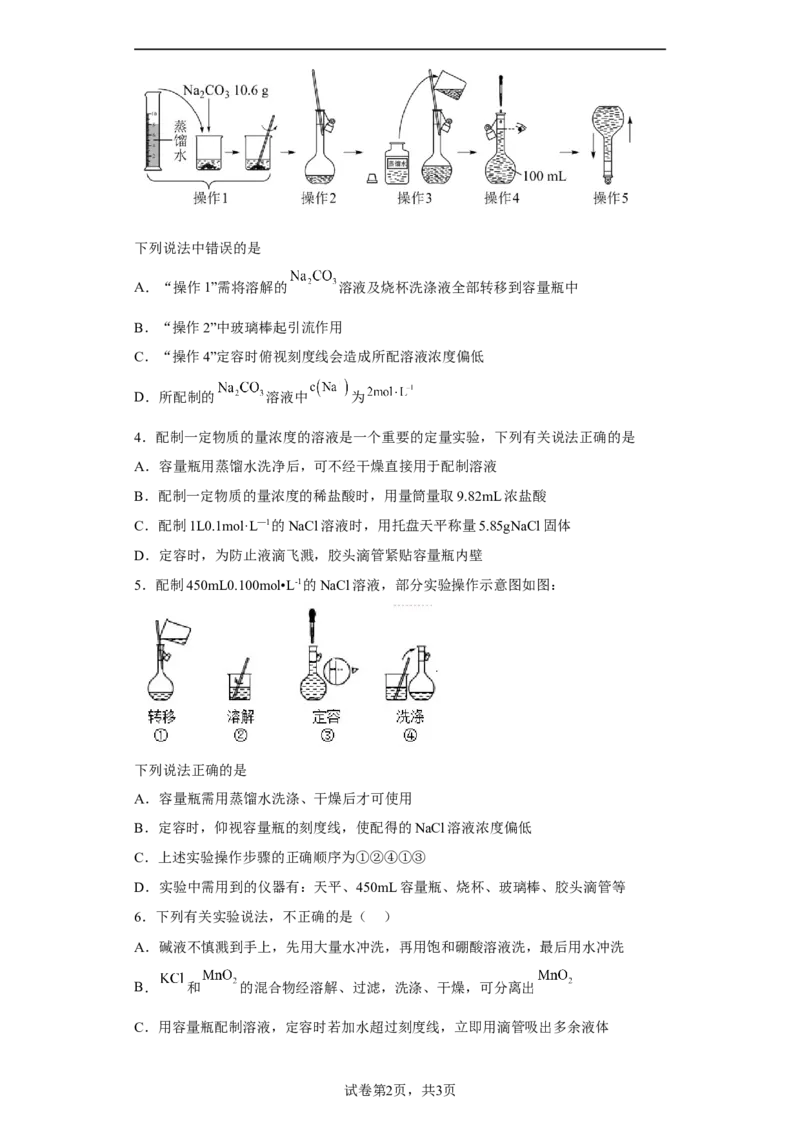
3.配制一定物质的量浓度的 溶液的操作过程示意图如下:下列说法中错误的是
A.“操作1”需将溶解的 溶液及烧杯洗涤液全部转移到容量瓶中
B.“操作2”中玻璃棒起引流作用
C.“操作4”定容时俯视刻度线会造成所配溶液浓度偏低
D.所配制的 溶液中 为
4.配制一定物质的量浓度的溶液是一个重要的定量实验,下列有关说法正确的是
A.容量瓶用蒸馏水洗净后,可不经干燥直接用于配制溶液
B.配制一定物质的量浓度的稀盐酸时,用量筒量取9.82mL浓盐酸
C.配制1L0.1mol·L—1的NaCl溶液时,用托盘天平称量5.85gNaCl固体
D.定容时,为防止液滴飞溅,胶头滴管紧贴容量瓶内壁
5.配制450mL0.100mol•L-1的NaCl溶液,部分实验操作示意图如图:
下列说法正确的是
A.容量瓶需用蒸馏水洗涤、干燥后才可使用
B.定容时,仰视容量瓶的刻度线,使配得的NaCl溶液浓度偏低
C.上述实验操作步骤的正确顺序为①②④①③
D.实验中需用到的仪器有:天平、450mL容量瓶、烧杯、玻璃棒、胶头滴管等
6.下列有关实验说法,不正确的是( )
A.碱液不慎溅到手上,先用大量水冲洗,再用饱和硼酸溶液洗,最后用水冲洗
B. 和 的混合物经溶解、过滤,洗涤、干燥,可分离出
C.用容量瓶配制溶液,定容时若加水超过刻度线,立即用滴管吸出多余液体
试卷第2页,共3页D.火柴头的浸泡液中滴加 溶液,稀 和 溶液,可检验火柴头是否
含有氯元素
7.某溶液中仅含有Na+、Mg2+、SO 2-、Cl-四种离子(不考虑水电离出的H+和OH
4
-),其物质的量浓度之比为c(Na+)∶c(Mg2+)∶c(Cl-)=5∶7∶7。若c(Na+)
为5 mol/L,则c(SO 2-)为( )。
4
A.5 mol/L B.6mol/L C.7mol/L D.8mol/L
8.将30mL 0.5mol/LHCl溶液加水稀释到500mL,稀释后溶液中HCl的物质的量浓度
为
A.0.03mol/L B.0.3mol/L C.0.05mol/L D.0.15mol/L
9.某同学购买了一瓶“84消毒液”,包装说明如下:
根据以上信息和相关知识判断,下列分析不正确的是
A.该“84消毒液”的物质的量浓度为4.0mol·L-1
B.一瓶该“84消毒液”能吸收空气中44.8L的CO(标准状况)而变质
2
C.取100mL该“84消毒液”稀释100倍后用以消毒,稀释后的溶液中c(Na+)约为
0.04mol·L-1
D.参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含25%NaClO的消毒液,
需要称量的NaClO固体质量为143g
10.用10mL0.1mol·L-1的BaCl 溶液恰好使相同体积的Fe (SO )、ZnSO 和FeSO 三种
2 2 4 3 4 4
溶液中的硫酸根离子完全转化为硫酸钡沉淀。则三种硫酸盐溶液的物质的量浓度之比
是
A.3:2:2 B.1:2:3 C.1:3:3 D.3:1:1
11.36.5g 气体溶解在1L水中(水的密度为 ),所得溶液的密度为 ,
质量分数为w,物质的量浓度为c, 表示阿伏加德罗常数的数值,下列叙述中正确
的是
A.所得溶液的物质的量浓度:
B.将该溶液加热蒸发浓缩至原来一半体积,则浓度变为原来两倍
C.36.5g 气体占有体积为22.4LD.所得溶液的溶质质量分数:
12.下列关于物质的量浓度表述正确的是
A.在标准状况下,VL氨气溶于1L水配成密度为ρg/cm3的氨水,该氨水的物质的量
浓度为 mol/L
B.0.3mol/L硫酸钠溶液中含有钠离子和硫酸根离子总物质的量为0.9mol
C.将40g氢氧化钠固体溶于1L水中,物质的量浓度为1mol/L
D.实验室使用的浓盐酸的溶质质量分数为36.5%,密度为1.19 g/cm3,则该浓盐酸物
质的量浓度是11.9 mol/L
13.a mol HSO 中含有b个氧原子,则阿伏加德罗常数可以表示为
2 4
A. mol-1 B. mol-1 C. mol-1 D. mol-1
14.设N 为阿伏加德罗常数的值,下列叙述正确的是
A
A.1mol/LHCl溶液中,HCl分子的数目为N
A
B.22.4L氢气中,H 分子的数目为N
2 A
C.180g葡萄糖中,C原子的数目为6N
A
D.1molN 中,σ键的数目为3N
2 A
15.N 代表阿伏加德罗常数的值。下列说法正确的是
A
A.1molHC≡CH分子中所含σ键数为5 N
A
B.1L0.1 mol·L-1的NaCO 溶液含 的数目为0.1 N
2 3 A
C.78 g NaO 与足量水完全反应,电子转移数为N
2 2 A
D.标准状况下,2.24 L C HOH所含氢原子数为0.6 N
2 5 A
二、填空题(共0分)
16.计算填空
(1)质量相同的SO 和SO 的物质的量之比是_______,摩尔质量之比是_______,含氧
2 3
原子个数比是_______,硫原子个数比是_______。
(2)标准状况下9.6 g 某气体体积与0.6 g 氢气体积相同,该气体的相对分子质量是
_______。
(3)标准状况下280 mL某气体质量为0.35 g,该气体的摩尔质量是_______。
试卷第4页,共3页(4)将5 mol•L-1 Mg(NO) 溶液 amL稀释至 bmL,求稀释后溶液中NO 的物质的量浓
3 2
度_______。
(5)ag H SO 中含有b个氧原子,则阿伏加德罗常数可以表示为_______。
2 4
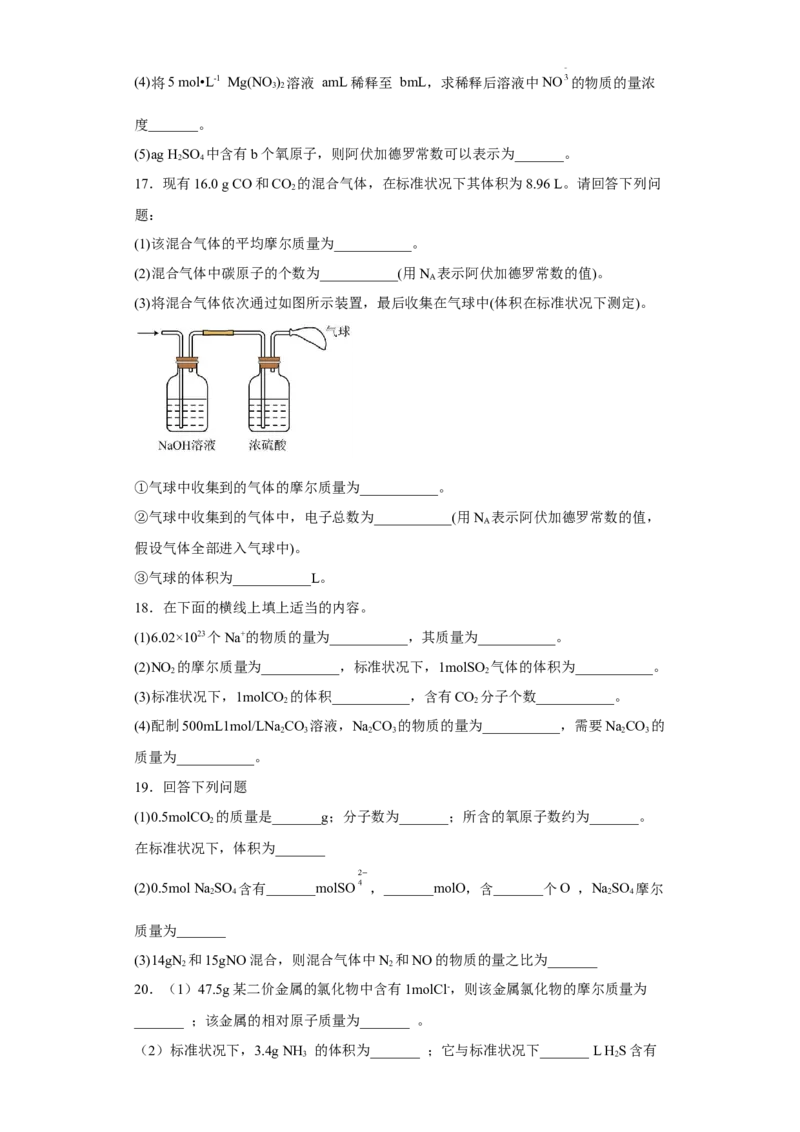
17.现有16.0 g CO和CO 的混合气体,在标准状况下其体积为8.96 L。请回答下列问
2
题:
(1)该混合气体的平均摩尔质量为___________。
(2)混合气体中碳原子的个数为___________(用N 表示阿伏加德罗常数的值)。
A
(3)将混合气体依次通过如图所示装置,最后收集在气球中(体积在标准状况下测定)。
①气球中收集到的气体的摩尔质量为___________。
②气球中收集到的气体中,电子总数为___________(用N 表示阿伏加德罗常数的值,
A
假设气体全部进入气球中)。
③气球的体积为___________L。
18.在下面的横线上填上适当的内容。
(1)6.02×1023个Na+的物质的量为___________,其质量为___________。
(2)NO 的摩尔质量为___________,标准状况下,1molSO 气体的体积为___________。
2 2
(3)标准状况下,1molCO 的体积___________,含有CO 分子个数___________。
2 2
(4)配制500mL1mol/LNa CO 溶液,NaCO 的物质的量为___________,需要NaCO 的
2 3 2 3 2 3
质量为___________。
19.回答下列问题
(1)0.5molCO 的质量是_______g;分子数为_______;所含的氧原子数约为_______。
2
在标准状况下,体积为_______
(2)0.5mol Na SO 含有_______molSO ,_______molO,含_______个O ,NaSO 摩尔
2 4 2 4
质量为_______
(3)14gN 和15gNO混合,则混合气体中N 和NO的物质的量之比为_______
2 2
20.(1)47.5g某二价金属的氯化物中含有1molCl-,则该金属氯化物的摩尔质量为
_______ ;该金属的相对原子质量为_______ 。
(2)标准状况下,3.4g NH 的体积为_______ ;它与标准状况下_______ L H S含有
3 2相同数目的氢原子。
(3)已知CO、CO 混合气体的质量共10.0g,在标准状况下的体积为6.72L,则混合
2
气体中CO的质量为_______ ;CO 在相同状况下的体积为_______ 。
2
(4)将4g NaOH 溶解在10mL水中,再稀释成1L,从中取出10mL,这10mL溶液的
物质 的量浓度为_______。
(5)已知ag氢气中含有b个氢原子,则阿伏加德罗常数的值可表示为 _______ 。
三、实验题
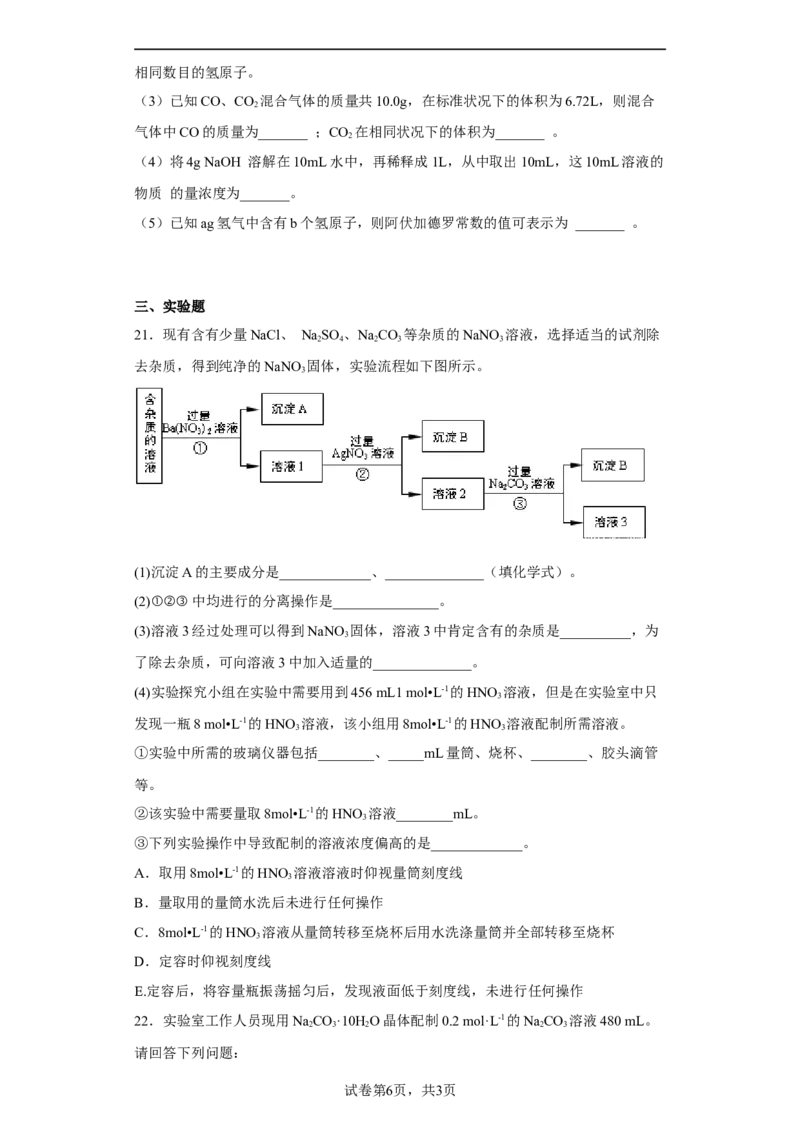
21.现有含有少量NaCl、 NaSO 、NaCO 等杂质的NaNO 溶液,选择适当的试剂除
2 4 2 3 3
去杂质,得到纯净的NaNO 固体,实验流程如下图所示。
3
(1)沉淀A的主要成分是_____________、______________(填化学式)。
(2)①②③中均进行的分离操作是_______________。
(3)溶液3经过处理可以得到NaNO 固体,溶液3中肯定含有的杂质是__________,为
3
了除去杂质,可向溶液3中加入适量的______________。
(4)实验探究小组在实验中需要用到456 mL1 mol•L-1的HNO 溶液,但是在实验室中只
3
发现一瓶8 mol•L-1的HNO 溶液,该小组用8mol•L-1的HNO 溶液配制所需溶液。
3 3
①实验中所需的玻璃仪器包括________、_____mL量筒、烧杯、________、胶头滴管
等。
②该实验中需要量取8mol•L-1的HNO 溶液________mL。
3
③下列实验操作中导致配制的溶液浓度偏高的是_____________。
A.取用8mol•L-1的HNO 溶液溶液时仰视量筒刻度线
3
B.量取用的量筒水洗后未进行任何操作
C.8mol•L-1的HNO 溶液从量筒转移至烧杯后用水洗涤量筒并全部转移至烧杯
3
D.定容时仰视刻度线
E.定容后,将容量瓶振荡摇匀后,发现液面低于刻度线,未进行任何操作
22.实验室工作人员现用NaCO·10H O晶体配制0.2 mol·L-1的NaCO 溶液480 mL。
2 3 2 2 3
请回答下列问题:
试卷第6页,共3页(1)应称取NaCO·10H O晶体的质量:_____________________。
2 3 2
(2)根据下列操作对所配溶液的浓度产生的影响,完成下列问题:
① Na CO·10H O晶体失去了部分结晶水
2 3 2
② 用“左码右物”的称量方法称量晶体(使用游码)
③ 碳酸钠晶体不纯,其中混有氯化钠
④ 称量碳酸钠晶体时所用砝码生锈
⑤ 容量瓶未经干燥使用
其中引起所配溶液浓度偏高的有____(填序号,下同),无影响的有_________。
(3)下列操作中,容量瓶所不具备的功能有_____(填序号)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.量取一定体积的液体
F.用来加热溶解固体溶质
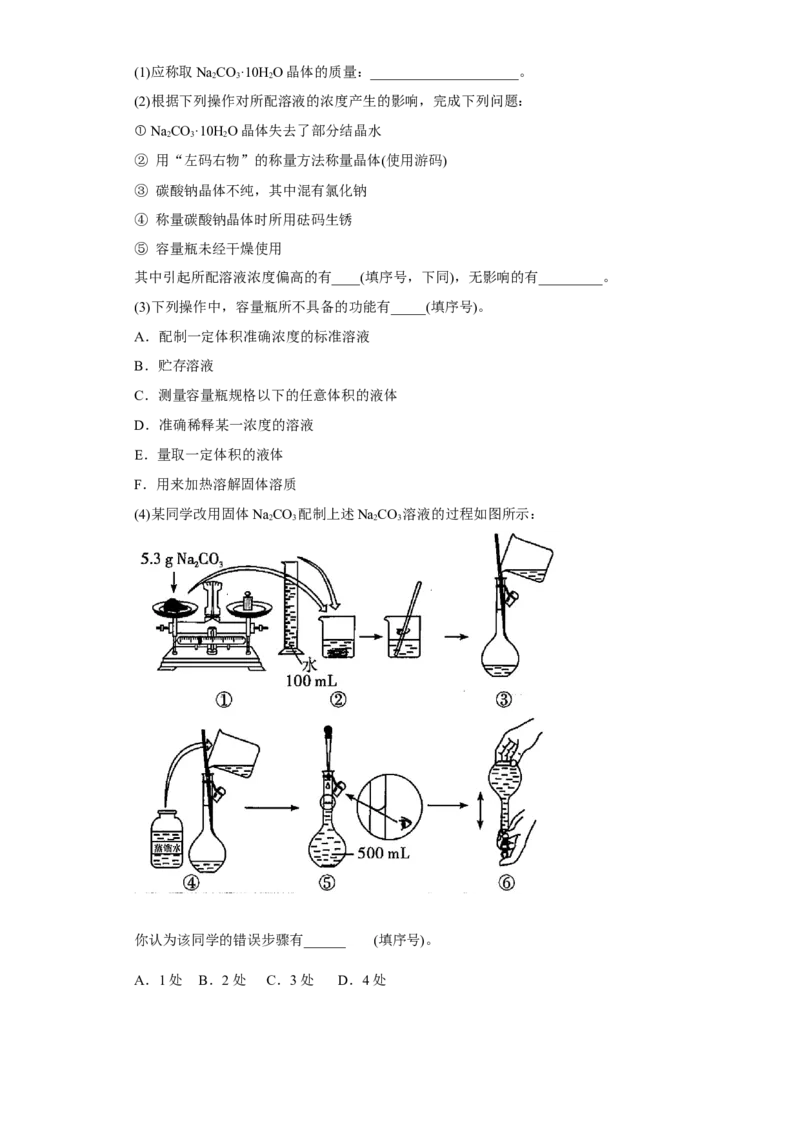
(4)某同学改用固体NaCO 配制上述NaCO 溶液的过程如图所示:
2 3 2 3
你认为该同学的错误步骤有______ (填序号)。
A.1处 B.2处 C.3处 D.4处参考答案:
1.C
【详解】A.氢氧化钠具有腐蚀性。不能用称量纸称量,A错误;
B. 操作1确认 完全溶解后,应冷却到室温、再进行操作2,B错误;
C. 操作4如果俯视,则导致体积偏小, 溶液浓度偏大,C正确;
D.若补充少量水至刻度线,则导致体积偏大, 溶液浓度偏小,D错误;
答案选C。
2.B
【详解】A.配制50.00mL0.1000mol.L-1NaCO 溶液需要用容量瓶,不能使用量筒配置溶液,
2 3
故A错误;
B.除去氯气中的氯化氢气体使用饱和氯化钠溶液,可以吸收氯化氢气体,根据氯气在水
中的反应:Cl
2
+H
2
O⇌H++Cl-+HClO,饱和氯化钠溶液中的氯离子使氯气溶于水的平衡逆向
移动,降低氯气在水中的溶解度,洗气瓶长进短出,利于除杂,故B正确;
C.蒸馏要使用直形冷凝管,接水口下口进上口出,球形冷凝管一般作反应装置,故C错
误;
D.硅酸钠溶液呈碱性,硅酸钠溶液是一种矿物胶,能将玻璃塞与试剂瓶的瓶口粘在一起,
盛装NaSiO 溶液的试剂瓶不能使用玻璃塞,应使用橡胶塞,故D错误。
2 3
答案选B。
3.C
【详解】A.溶解得到的溶液及洗涤烧杯2~3次的洗涤液均需转移到容量瓶中,保证溶质
完全转移,A项正确;
B.向容量瓶中转移溶液时用玻璃棒引流,B项正确;
C.定容时若俯视刻度线,水的量不足,溶液体积减小,造成所配溶液浓度偏大,C项错误;
D.碳酸钠的质量为10.6g, ,容量瓶规格为100mL, 溶液的物
质的量浓度为 , ,D项正确;
答案选C。
4.A
【详解】A.容量瓶用蒸馏水洗净后,不需要干燥,因定容时还需要加水,故A正确;
B.量筒的感量为0.1mL,可量取9.8mL浓盐酸,无法量取9.82mL浓盐酸,故B错误;
C.托盘天平的感量为0.1g,可称量5.8g固体,无法称量5.85gNaCl固体,故C错误;D.定容时,胶头滴管要悬空正放,不能紧贴容量瓶内壁,故D错误;
故选A。
5.B
【详解】A.容量瓶用蒸馏水洗净后,由于后面还需要加蒸馏水定容,无需干燥即可使用,
A错误;
B.仰视容量瓶的刻度线,使得液面高于刻度线,溶液体积偏大,浓度偏低,B正确;
C.溶液配制的基本步骤为计算、称量、溶解、转移、洗涤、定容、装瓶特标签。①为溶
液的转移;②为NaCl固体的溶解;③为定容;④为洗涤小烧杯和玻璃棒,所以顺序为
②①④①③,C错误;
D.实验室没有450mL容量瓶,应使用500mL容量瓶,D错误;
综上所述答案为B。
6.C
【详解】A. 若皮肤不慎沾上少量碱液,应先用大量水冲洗,再用2%醋酸溶液或饱和硼酸
溶液洗,避免皮肤受损,故A正确;
B.二氧化锰不溶于水,氯化钾可溶于水,所以混合物经溶解、过滤,洗涤、干燥,可分离
出 ,故B正确;
C.滴管吸出的液体中含有溶质,因此会导致所配溶液浓度偏小,正确操作应该是重新配制,
故C错误;
D. 火柴头中含有KClO,检验氯元素,应把ClO -还原为4Cl-,酸性条件下,NO -具有还原
3 3 2
性,向少量的火柴头浸泡液中滴加AgNO、稀HNO 和NaNO ,发生的离子反应为:ClO -
3 3 2 3
+3NO-+Ag+═AgCl↓+3NO -,出现白色沉淀,证明含有氯元素,故D正确;
2 3
故答案为C。
7.B
【详解】c(Na+)为5 mol/L,c(Na+)∶c(Mg2+)∶c(Cl-)=5∶7∶7,则c(Mg2+)=c(Cl-)=7mol/L;利
用电解质溶液中存在电荷守恒规律,可得出下列等量关系式:c(Na+)+2c(Mg2+)= c(Cl-)+
2c(SO 2-),代入数据,可得出c(SO 2-)=6 mol/L;
4 4
故选B。
8.A
【详解】由稀释定律可知,将30mL 0.5mol/L盐酸溶液加水稀释到500mL时,稀释后溶液
答案第2页,共2页中氯化氢的物质的量浓度为 =0.03mol/L,故选A。
9.D
【详解】A.根据c= 得,c(NaClO)= mol·L-1≈4.0mol·L-1,A正
确;
B.一瓶该“84消毒液”含有的n(NaClO)=1L×4.0mol·L-1=4.0mol,根据反应:CO+
2
NaClO+HO=NaHCO +HClO,吸收CO 的物质的量最多为4.0mol,即标准状况下V(CO)
2 3 2 2
=4.0mol×22.4L·mol-1=89.6L,则能吸收空气中44.8L的CO 而变质,B正确;
2
C.根据稀释前后溶质的物质的量不变,有100mL×4.0mol·L-1=100mL×100×c(NaClO),解
得稀释后c(NaClO)=0.04mol·L-1,c(Na+)=c(NaClO)=0.04mol·L-1,C正确;
D.应选取500mL的容量瓶进行配制,然后取出480mL,所以需要NaClO的质量为
0.5L×4.0mol·L-1×74.5g·mol-1=149g,D错误。
故选D。
10.C
【详解】用10mL0.1mol·L-1的BaCl 溶液恰好使相同体积的Fe (SO )、ZnSO 和FeSO 三种
2 2 4 3 4 4
溶液中的硫酸根离子完全转化为硫酸钡沉淀,n(BaCl )= 0.01L×0.1mol·L-1=0.001mol,则三
2
种溶液中n( )=0.001mol,n[Fe (SO )]= 、n(ZnSO)= 0.001mol、n(FeSO )=
2 4 3 4 4
0.001mol,溶液体积相等,所以三种硫酸盐溶液的物质的量浓度之比是 :0.001:
0.001=1:3:3,选C。
11.D
【详解】A.所得溶液的物质的量浓度: ,A错误;
B.将该溶液加热蒸发浓缩至原来一半体积,因 易挥发,会一起蒸发损失,故浓度不
是为原来两倍,B错误;
C.没确定温度和压强,不能确定36.5g 气体占有体积,C错误;
D.设溶液体积为1L,所得溶液的溶质质量分数: ,D正确;故选D。
12.D
【详解】A.VL氨气与1L水的体积不能相加,溶液的体积不是(V+1)L,A错误;
B.溶液的体积未知,无法算出物质的量,B错误;
C.1L水溶解氢氧化钠后,溶液体积不再是1L,C错误;
D.根据质量分数与物质的量浓度的换算c = mol·L-1可知该浓盐酸的物质的量浓
B
度= mol·L-1 =11.9 mol·L-1,D正确;
答案选D。
13.B
【详解】每个HSO 分子中含有4个氧原子,a mol H SO 中含有b个氧原子,则 ,
2 4 2 4
mol-1;
故选B。
14.C
【详解】A.体积未知,HCl分子的数目不能计算,故A错误;
B.没有标准状态,不能计算H 分子的数目,故B错误;
2
C.葡萄糖的分子式为C H O,故180g葡萄糖的分子的物质的量为1mol,C原子的数目
6 12 6
为6N ,故C正确;
A
D.1molN 中有1molσ键,故σ键的数目为N ,故D错误;
2 A
故选C。
15.C
【详解】A. HC≡CH中含有3个σ键和2个π键,所以1molHC≡CH分子中所含σ键数为3
N ,所以A错。
A
B.因为 会发生水解反应,所以1L0.1 mol·L-1的NaCO 溶液含 的数目小于0.1
2 3
N ,所以B错。
A
C. NaO 和水反应生成1molO ,转移电子数为2mol,78 g NaO 是1mol,只能产生
2 2 2 2 2
0.5molO,所以电子转移数为N ,所以C对。
2 A
答案第4页,共2页D. 标准状况下,C HOH是液体,不是气体,所以不能用 来计算,所以D错。
2 5
16.(1) 5∶4 4∶5 5∶6 5∶4
(2)32
(3)28 g·mol-1
(4)10a/b mol·L-1
(5)49b/2a
【解析】(1)
质量相同的SO 和SO 的物质的量之比是 ;摩尔质量之比为
2 3
64g/mol:80gmol=4:5;所含的氧原子个数之比是
;硫原子个数比为
。
(2)
0.6g氢气的物质的量为 =0.3mol,则气体的摩尔质量是 =32g/mol,以g/mol为
单位时相对分子质量在数值上等于摩尔质量,故为32。
(3)
标准状况下的物质的量为 =0.0125mol,该气体的摩尔质量为
=28g/mol。
(4)
稀释前后溶质的物质的量保持不变,a×10-3L×5mol/L×2=b×10-3L×c(NO ),解得c(NO
)=10a/b mol·L-1。
(5)每个HSO 分子中含有4个氧原子,a g HSO 中含有b个氧原子,则4 ×N =b,
2 4 2 4 A
N =49b/2a。
A
17.(1)40 g·mol-1
(2)0.4N
A
(3) 28 g·mol-1 1.4N 2.24
A
【分析】16.0 g CO和CO 的混合气体,在标准状况下其体积为8.96 L,则混合气体的总物
2
质的量是 ; 设混合气体中CO和CO 的物质的量分别为xmol、ymol;
2
,解得 。
(1)
该混合气体的平均摩尔质量为 g·mol-1;
(2)
CO和CO 分子中都只含1个碳原子,混合气体的总物质的量是0.4mol,所以混合气体中碳
2
原子的个数为0.4 N ;
A
(3)
①二氧化碳被氢氧化钠吸收,气球中收集到的气体是CO,CO的摩尔质量为28 g·mol-1;
②1个CO分子中有14个电子,气球中收集到的气体是0.1molCO,电子总数为1.4N ;
A
③气球中收集到的气体是0.1molCO,标准状况下,气球的体积为0.1mol×22.4L/
mol=2.24L。
18.(1) 1mol 23g
(2) 46g/mol 22.4L
(3) 22.4L 6.02×1023
(4) 0.5mol 53g
【解析】(1)
6.02×1023个Na+的物质的量为 ,其质量为 。
答案第6页,共2页(2)
NO 的相对分子质量为46,则其摩尔质量为46g/mol;标准状况下,1molSO 气体的体积为
2 2
。
(3)
标准状况下,1molCO 的体积为 ,含有CO 分子个数为
2 2
个。
(4)
500mL=0.5L,配制500mL1mol/LNa CO 溶液,NaCO 的物质的量为0.5L×1mol/
2 3 2 3
L=0.5mol,需要NaCO 的质量为 。
2 3
19.(1) 22 11.2L
(2) 0.5 2 142g/mol
(3)1:1
【分析】(1)
0.5molCO 的质量是 =22g,分子数为 ,所含的氧原子数
2
约为 ,在标准状况下,体积为 。
(2)
, 0.5mol Na SO 含有0.5molSO 、2molO、含 个O ;摩
2 4
尔质量以g/mol为单位数值上等于相对分子质量,则NaSO 摩尔质量为142g/mol。
2 4
(3)
14gN 的物质的量是 ,15gNO的物质的量是 ,则混合气
2
体中N 和NO的物质的量之比为0.5mol:0.5mol=1:1。
2
20. 95 g/mol 24 4.48L 6.72 5.6g 2.24L 0.1 mol/L b/a
【详解】(1)二价金属氯化物中含2个Cl-,含1molCl-的二价金属氯化物的物质的量为0.5mol,金属氯化物的摩尔质量为 =95g/mol。金属氯化物的相对分子质量为95,金
属的相对原子质量为95-2 35.5=24;
(2)n(NH )= =0.2mol,在标准状况下NH 的体积为0.2mol 22.4L/
3 3
mol=4.48L。其中含有H原子物质的量为0.6mol,含0.6molH的HS物质的量为0.3mol,
2
0.3molHS在标准状况下的体积为0.3mol 22.4L/mol=6.72L;
2
(3)28g/mol×n(CO)+44g/mol×n(CO)=10.0g,n(CO)+n(CO)= ,解
2 2
得n(CO)=0.2mol,n(CO)=0.1mol;混合气体中CO的质量为0.2mol 28g/mol=5.6g;
2
CO 在标准状况下的体积为0.1mol 22.4L/mol=2.24L;
2
(4)n(NaOH)= =0.1mol,配成1L溶液,所得溶液c(NaOH)=0.1mol
1L=0.1mol/L;从其中取出10mL,物质的量浓度不变,浓度仍为0.1mol/L;
(5)n(H)= = mol,n(H)=amol,阿伏加德罗常数为 = mol-1,阿伏加
2
德罗常数的值为 。
21. BaSO BaCO 过滤 NaCO HNO 500mL 容量
4 3 2 3 3
瓶 100 玻璃棒 62.5 AC
【分析】由实验流程可知,加入过量的Ba(NO ),生成BaSO、BaCO 沉淀,然后在滤液
3 2 4 3
中加入过量的AgNO,使Cl-全部转化为AgCl沉淀,在所得滤液中加入过量的NaCO,使
3 2 3
溶液中的Ag+、Ba2+完全沉淀,最后所得溶液为NaNO 和NaCO 的混合物,加入稀
3 2 3
HNO,最后进行蒸发操作可得固体NaNO 。
3 3
【详解】(1)加入过量的Ba(NO ),NaSO 、NaCO 和Ba(NO ) 反应生成BaSO、BaCO
3 2 2 4 2 3 3 2 4 3
沉淀,故答案为:BaSO; BaCO ;
4 3
(2)①②③中均进行的分离操作是分离固体和液体,为过滤操作,故答案为:过滤;
(3)溶液3为NaNO 和NaCO 的混合物,加入稀HNO,可除去NaCO,最后加热蒸发、
3 2 3 3 2 3
冷却结晶、过滤得到硝酸钠,故答案为:NaCO;HNO;
2 3 3
(4)①实验室只有500mL的容量瓶,则本实验需要配制的溶液体积为500mL,另外需要
答案第8页,共2页用量筒量8mol/L的HNO 溶液倒在烧杯中加水溶解,同时需要玻璃棒搅拌,转移到容量瓶
3
中时也需要玻璃棒引流,最后还需要用胶头滴管定容,整个实验需要的玻璃仪器包括
500mL容量瓶、100mL量筒、烧杯、玻璃棒、胶头滴管等,故答案为:500mL 容量瓶;
100; 玻璃棒;
②设需要量取8 mol•L-1的HNO 溶液VmL,则8 mol•L-1×V×10-3L=1 mol•L-1×500×10-3L,解
3
得:V=62.5mL,故答案为: 62.5 ;
③A.取8mol•L-1的HNO 溶液时仰视刻度线,液面在刻度线上方,即浓硝酸的体积偏大,
3
导致配制溶液浓度偏高,故A正确;
B.量取用的量筒水洗后未进行任何操作,会稀释浓硝酸,即浓硝酸的体积偏小,导致配
制溶液浓度偏低,故B错误;
C.量筒量取浓硝酸后,不应该水洗,否则浓硝酸的体积偏大,导致配制溶液浓度偏高,
故C正确;
D.定容时仰视刻度线,液面在刻度线上方,溶液体积偏大,导致浓度偏低,故D错误;
E.定容后,除容量瓶振荡摇匀,不能再加水定容,这样做对实验结果无影响,故E错误;
故答案为AC。
22. 28.6 g ① ④ ⑤ B、C、F B
【分析】配制0.2 mol·L-1的NaCO 溶液480 mL时,由于实验室没有480mL规格的容量瓶,
2 3
应选择500mL的容量瓶;分析误差时,用公式法进行分析。
【详解】(1)选择500mL的容量瓶,求所需溶质的质量时,使用500mL进行计算,所以应
称取NaCO·10H O晶体的质量:0.2 mol·L-1×0.5L×286g/mol=28.6 g。答案为:28.6 g;
2 3 2
(2)①Na CO·10H O晶体失去部分结晶水,则溶质的物质的量偏大,所配溶液的浓度偏高;
2 3 2
②用“左码右物”的称量方法称量晶体(使用游码),则所称取溶质的质量偏小,所配溶液
的浓度偏低;
③碳酸钠晶体不纯,其中混有氯化钠,则所称取溶质的质量偏小,所配溶液的浓度偏低;
④称量碳酸钠晶体时所用砝码生锈,则所称取溶质的质量偏大,所配溶液的浓度偏高;
⑤容量瓶未经干燥使用,对溶质的物质的量、溶液的体积都不产生影响,所配溶液的浓度
不变;
综合以上分析,引起所配溶液浓度偏高的有①④,无影响的有⑤。答案为:①④;⑤;
(3)A.使用容量瓶,可以将一定物质的量的溶质溶解在一定量的溶剂中,配成一定体积准
确浓度的标准溶液;
B.容量瓶不能用于贮存溶液,尤其是碱性溶液;C.容量瓶只有一个刻度线,所以只能配制确定体积的液体;
D.利用容量瓶,可以将一定物质的量的溶液,加水稀释配成准确浓度的溶液;
E.容量瓶只能量取与容量瓶规格相同的液体;
F.容量瓶是不耐热的仪器,不能用来加热溶解固体溶质;
综合以上分析,容量瓶所不具备的功能有B、C、F。答案为:B、C、F;
(4)改用固体NaCO 配制上述NaCO 溶液,所需NaCO 的质量为:0.2
2 3 2 3 2 3
mol·L-1×0.5L×106g/mol=10.6 g,①不正确;定容时,应平视刻度线,⑤不正确;
综合以上分析,该同学的错误步骤有2处,故选B。答案为:B。
【点睛】容量瓶是精确度高的仪器,不耐热,不能用于贮存溶液。
答案第10页,共2页