文档内容
高一化学试题卷
可能用到的相对原子质量 H:1 C:12 N;14 O:16 S:32
一、单选题(本大题共 20 小题,每小题 2 分,共 40 分)
1. 下列物质分类的正确组合是( )
选项 混合物 纯净物 单质 电解质
A 盐酸 NaOH 石墨 KSO 溶液
2 4
B 空气 Fe(OH) 胶体 铁 NaCO
3 2 3
C CuSO ·5H O CaCl 水银 铜
4 2 2
D 氯水 KNO 晶体 O NaCl
3 3
A. A B. B C. C D. D
【答案】D
【解析】
【分析】
【详解】A、硫酸钾溶液是混合物,不是电解质,也不是非电解质,A错误;
B、胶体是混合物,B错误;
C、CuSO ·5H O是纯净物,铜是单质,不是电解质,也不是非电解质,C错误;
4 2
D、物质分类均正确,D正确;
答案选D。
2. 下列电离方程式书写正确的是 ( )
A. MgSO =Mg+2+ B. Ba(OH)=Ba2++OH-
4 2
C. KCl=K++Cl- D. Ca(NO )=Ca2++2( )
3 2
【答案】C
【解析】
【分析】
【详解】A.硫酸镁是强电解质,电离成镁离子和硫酸根离子:MgSO =Mg2++ ,A错误;
4
B.氢氧化钡是强电解质,电离成钡离子和氢氧根离子: ,B错误;C.氯化钾是强电解质,电离成钾离子和氯离子:KCl=K++Cl-,C正确;
D.硝酸钙是强电解质,电离成钙离子和硝酸根离子: ,D错误;
答案选C。
3. 下列各反应中,氧化反应与还原反应在同种元素中进行的是( )
.
A Cl + 2NaOH=NaCl + NaClO + HO
2 2
B. 2KClO 2KCl + 3O↑
3 2
C. 2KMnO KMnO + MnO + O↑
4 2 4 2 2
D. 2HO 2H↑+ O↑
2 2 2
【答案】A
【解析】
【分析】
【详解】A. Cl + 2NaOH=NaCl + NaClO + HO中只有氯元素的化合价发生变化,氧化反应与还原反
2 2
应在同种元素中进行,A选;
B. 2KClO 2KCl + 3O↑中氯元素化合价降低,氧元素化合价升高,氧化反应与还原反应在不
3 2
同种元素中进行,B不选;
C. 2KMnO KMnO + MnO + O↑中锰元素化合价降低,氧元素化合价升高,氧化反应与还原反
4 2 4 2 2
应在不同种元素中进行,C不选;
D. 2HO 2H↑+ O↑中氢元素化合价降低,氧元素化合价升高,氧化反应与还原反应在不同种元
2 2 2
素中进行,D不选;答案选A。
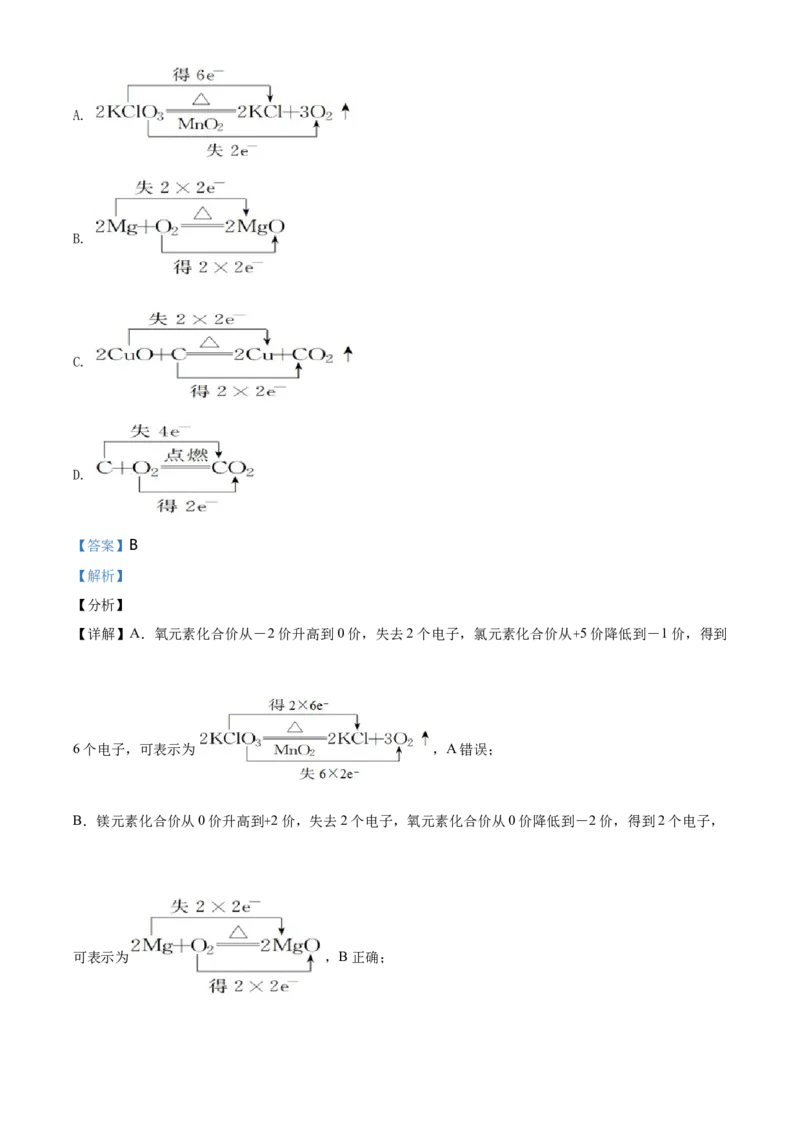
4. 下列氧化还原反应中,电子转移的方向和数目均正确的是( )A.
B.
C.
D.
【答案】B
【解析】
【分析】
【详解】A.氧元素化合价从-2价升高到0价,失去2个电子,氯元素化合价从+5价降低到-1价,得到
6个电子,可表示为 ,A错误;
B.镁元素化合价从0价升高到+2价,失去2个电子,氧元素化合价从0价降低到-2价,得到2个电子,
可表示为 ,B正确;C.碳元素化合价从0价升高到+4价,失去4个电子,铜元素化合价从+2价降低到0价,得到2个电子,
因此可表示为 ,C错误;
D.碳元素化合价从0价升高到+4价,失去4个电子,氧元素化合价从0价降低到-2价,得到2个电子,
因此可表示为 ,D错误;
。
答案选B
5. NaFeO 是一种新型水处理剂,既可杀菌消毒,又可净水。其中Fe元素的化合价为
2 4
A. +6 B. +3 C. +2 D. +2、+3
【答案】A
【解析】
【分析】
【详解】NaFeO 中钠元素的化合价为+1价,氧元素的化合价为-2价,设铁元素的化合价为x,根据化合
2 4
物元素的化合价之和等于0可知,(+1)×2+x+(-2)×4=0,铁元素的化合价为+6,答案选A。
6. 下列叙述正确的是
A. 分散质微粒直径的大小关系:溶液>胶体>浊液
B. 胶体分散质粒子较大,不能通过滤纸
C. 利用丁达尔效应可以区别溶液与胶体
D. 利用氯化铁溶液与氢氧化钠溶液反应可制得氢氧化铁胶体
【答案】C
【解析】
【分析】
【详解】A.胶体、溶液、浊液的微粒直径大小分别为:胶体为1-100 nm,小于1 nm的为溶液,大于100
nm的为浊液,分散质微粒直径大小为溶液<胶体<浊液,故A错误;
B.溶液、胶体的粒子都能透过滤纸,故B错误;C.丁达尔现象是胶体的性质,胶体有丁达尔现象,溶液没有,可以利用丁达尔效应区分溶液与胶体,故
C正确;
D.制备氢氧化铁胶体是向沸水中滴加饱和氯化铁溶液,继续加热至液体呈红褐色制备的,向氯化铁溶液
里滴入氢氧化钠溶液,得到氢氧化铁沉淀,故D错误;
故选C。
7. 关于O 和O,下列说法正确的是( )
2 3
A. O 和O 的性质完全相同
2 3
B. O 和O 都是由氧元素组成的,二者混合后仍属于纯净物
2 3
C. O 转化为O 属于同素异形体
2 3
D. O 和O 是同一种物质
2 3
【答案】C
【解析】
【分析】
【详解】A.O 和O 是由氧元素形成的不同单质,属于不同的物质,它们的性质不同,故A错误;
3 2
B.O 和O 是由氧元素组成的不同单质,二者混合后属于混合物,故B错误;
2 3
C.O 和O 是由氧元素形成的不同单质,互为同素异形体,故C正确;
2 3
D.O 和O 是由氧元素形成的不同单质,是不同的物质,故D错误;
2 3
故选C。
8. 下列物质的水溶液能导电,但该物质属于非电解质的是
A. HClO B. Cl C. NH D. NaHCO
2 3 3
【答案】C
【解析】
【分析】
【详解】非电解质的定义是在水溶液和熔融状态下不能导电的化合物。HClO、NaHCO 是电解质,Cl 是单
3 2
质既不是电解质也不是非电解质;答案选C。
9. 下列实验设计及其对应的离子方程式均正确的是( )
A. 将铜片插入硝酸银当中:Cu+2Ag+=Cu2++2Ag
B. NaO 与HO反应制备O:NaO+H O=2Na++2OH- +O ↑
2 2 2 2 2 2 2 2
C. 将氯气溶于水制备次氯酸:Cl+H O=2H++Cl-+ClO-
2 2
D. 将稀盐酸滴在石灰石上: +H+=CO ↑+H O
2 2
【答案】A
【解析】【分析】
【详解】A.将铜片插入硝酸银当中,铜的金属性强于银,可将银从溶液中置换出来,发生反应的离子方
程式为:Cu+2Ag+=Cu2++2Ag,故A符合题意;
B.NaO 与HO 反应生成NaOH和O,发生反应的离子方程式为:2NaO+2H O=4Na++4OH-+O ↑,题目
2 2 2 2 2 2 2 2 2
中离子方程式中氧原子个数不守恒,故B不符合题意;
C.将氯气溶于水生成盐酸和次氯酸,HClO为弱酸,写离子反应时不能拆分,发生反应的离子方程式为:
Cl+H O=H++Cl-+HClO,故C不符合题意;
2 2
D.稀盐酸和石灰石反应生成氯化钙、水和二氧化碳,碳酸钙难溶于水,离子方程式中应写成化学式,且
题中离子方程式中电荷不守恒,正确的离子方程式为CaCO +2H+=Ca2++CO ↑+H O,故D不符合题意;
3 2 2
答案选A。
10. 能在水中大量共存的一组离子是( )
A. 、Na+、Cl-、 B. H+、Na+、 、
C. K+、Ba2+、OH-、 - D. K+、Ag+、 、Cl-
【答案】A
【解析】
【分析】
【详解】A.微粒之间不会发生反应,在水溶液中能够大量共存,故A项符合题意;
B.H+与 之间会发生复分解反应,不能大量共存,故B项不符合题意;
C.Ba2+与 会发生反应生成难溶物BaSO,不能大量共存,故C项不符合题意;
4
D.Ag+与Cl-会发生反应生成难溶物AgCl,不能大量共存,故D项不符合题意;
综上所述,能在水中大量共存的一组离子是A项,故答案为A。
11. 化学与生产、生活密切相关。下列叙述正确的是( )
A. 二水氯化钙(CaCl ·2H O)属于混合物 B. 葡萄糖注射液不能产生丁达尔效应
2 2
C. 食盐水属于浊液 D. 氯化铵不属于盐类
【答案】B
【解析】
【分析】
【详解】A. 结晶水合物为纯净物,二水氯化钙(CaCl ·2H O)是结晶水合物为纯净物,故A错误;
2 2
B. 葡萄糖溶液是溶液不是胶体,丁达尔现象是胶体的特征性质,葡萄糖注射液不能产生丁达尔效应,故B
正确;C. 分散质微粒直径可知,食盐水是氯化钠的水溶液不是浊液,故C错误;
D. 氯化铵是铵根离子和氯离子形成的盐类化合物,属于铵盐,故D错误;
故答案选:B。
12. 已知反应:①2FeCl +2KI=2FeCl +2KCl+I ②2FeCl +Cl=2FeCl ③I+SO+2H O=HSO +2HI,下列粒子
3 2 2 2 2 3 2 2 2 2 4
的还原能力由强到弱顺序正确的是( )
A. I->Fe2+>Cl->SO B. Cl->Fe2+>SO >I-
2 2
C. Fe2+>I->Cl->SO D. SO >I->Fe2+>Cl-
2 2
【答案】D
【解析】
【分析】
所含元素化合价升高的反应物为还原剂,所含元素的化合价降低的为氧化剂,氧化剂得电子后被还原的产
物为还原产物;在氧化还原反应中,还原剂的还原性大于还原产物的还原性;根据还原剂和还原产物的概
念找出各个化学方程式中的还原剂和还原产物,然后比较它们的还原性强弱。
【详解】由反应①中,KI中碘元素的化合价从-1价升高到0价,KI是还原剂,FeCl 是FeCl 化合价降低后
2 3
得到的物质,FeCl 是还原产物,还原剂的还原性大于还原产物,故还原性:I->Fe2+;
2
反应②中:FeCl 中铁元素的化合价从+2价升高到+3价,FeCl 是还原剂,氧化剂是Cl,Cl 被还原为Cl-,
2 2 2 2
还原剂的还原性大于还原产物,所以还原性:Fe2+>Cl-;
反应③中:SO 中硫元素的化合价从+4价升高到+6价,SO 是还原剂,HI是碘单质化合价降低后得到的产
2 2
物,HI是还原产物,还原剂的还原性大于还原产物,所以还原性:SO >I-;综上分析,物质的还原能力:
2
SO >I->Fe2+>Cl-,答案选D。
2
13. 将下列物质分别投入水中,有气体放出的是
A. NaO B. NaO C. NaOH D. NaCO
2 2 2 2 3
【答案】A
【解析】
【分析】
【详解】A.Na O 与水反应生成氢氧化钠和氧气,故A正确;
2 2
B.Na O与水反应生成氢氧化钠,故B错误;
2
C.NaOH溶解于水得到NaOH溶液,故C错误;
D. Na CO 溶解于水得到Na CO 溶液,故D错误。
2 3 2 3
答案为A。
【点睛】
14. 下列关于钠及其氧化物的说法正确的是( )A. 钠的密度比水大
B. 钠着火可用湿布盖灭
C. NaO 露置于空气中最终变成NaOH
2 2
D. NaO 可用于呼吸面具中氧气的来源
2 2
【答案】D
【解析】
【分析】
【详解】A.钠的密度比水小,故A不符合题意;
B.湿布中含有水分,钠与水反应生成氢氧化钠和氢气,氢气易燃,容易使燃烧更剧烈,故钠着火不能用
湿布盖灭,可以用沙子隔绝空气盖灭,故B不符合题意;
C.过氧化钠露置于空气中,易与水反应生成氢氧化钠,氢氧化钠吸收空气中 的水和二氧化碳生成
NaCO∙xH O,NaCO∙xH O风化脱水生成碳酸钠,故C不符合题意;
2 3 2 2 3 2
D.过氧化钠能与人呼出的二氧化碳发生反应生成氧气,化学反应方程式为2NaO+2CO = 2Na CO+O ↑,
2 2 2 2 3 2
因此过氧化钠可用于呼吸面具中氧气的来源,故D符合题意;
答案选D。
15. NaCl是一种化工原料,可以制备一系列物质。下列说法正确的是
A. 25℃,NaHCO 在水中的溶解度比NaCO 的大
3 2 3
B. 石灰乳与Cl 的反应中,Cl 既是氧化剂,又是还原剂
2 2
C. 常温下干燥的Cl 能用钢瓶贮存,所以Cl 不与铁反应
2 2
D. 图中所示转化反应都是氧化还原反应
【答案】B
【解析】
【分析】
【详解】A、25 ℃,NaHCO 在水中的溶解度比NaCO 的小,A项错误;
3 2 3
B、石灰乳与Cl 的反应生成氯化钙、次氯酸钙和水,只有氯元素化合价发生变化,Cl 既是氧化剂,又是
2 2
还原剂,B项正确;C、常温下Cl 不与铁反应,加热条件下则可以反应,C项错误;
2
D、图中所示转化反应中生成NaHCO 、NaCO 的反应都是非氧化还原反应,D项错误。
3 2 3
答案选B。
16. 下列说法中正确的是 ( )
A. 摩尔是 7 个基本物理量之一 B. 物质的量是表示数量的单位
C. 1molH SO 的质量是 98g·mol−1 D. Na 的摩尔质量是 23 g·mol−1
2 4
【答案】D
【解析】
【分析】
【详解】A.物质的量为七个基本物理量之一,摩尔是物质的量的单位,故A错误;
B.物质的量是表示一定数目粒子的集合体,为七个基本物理量之一,数量的单位是个,故B错误;
C.1molH SO 的质量是98g,HSO 的摩尔质量是98g⋅mol-1,故C错误;
2 4 2 4
D.钠原子的相对原子质量为23,所以钠的摩尔质量为23gmol-1,故D正确;
故选D。 ⋅
17. 下列各物质所含原子数由多到少的顺序是( )
①0.2molHSO ②6gH ③1.204×1023个KNO ④5N 个O
2 4 2 3 A 3
A. ③②①④ B. ②③①④ C. ④①②③ D. ④②①③
【答案】D
【解析】
【分析】
先计算各物质的物质的量,根据各物质的的构成,得到所含原子的物质的量,根据N=nN 进行分析。
A
【详解】①一个HSO 分子含有7个原子,0.2molHSO 中所含原子的物质的量为0.2mol×7=1.4mol,根据
2 4 2 4
N=nN ,所含原子的数目为1.4N ;
A A
②6gH 的物质的量n= = =3mol,一个氢分子含有两个氢原子,原子的物质的量为
2
3mol×2=6mol,根据N=nN ,所含原子的数目为6N ;
A A
③1.204×1023个KNO 中有1.204×1023×5个=6.02×1023个原子,所含原子 的数目为N ;
3 A
④一个O 分子含有三个氧原子,5N 个O 含有氧原子数为5N ×3=15N ;
3 A 3 A A
所含原子数由多到少的顺序④②①③,答案选D。
18. 下列关于氯气的叙述中,不正确的是
A. 氯气能溶于水
B. 氯气、液氯和氯水是同一种物质C. 氯气是一种黄绿色、有刺激性气味的气体
D. 氯气是一种有毒的气体
【答案】B
【解析】
【分析】
【详解】A.氯气能溶于水,1体积的水能溶解2体积的氯气,故A正确;
B.液氯是氯气的液态,所以氯气和液氯是同一种物质;氯水是氯气的水溶液,是一种混合物,液氯和氯
气与氯水不是同一种物质,故B错误;
C.氯气呈黄绿色、有刺激性气味,故C正确;
D.氯气是一种有刺激性气味的有毒气体,故D正确;
故选B。
19. 已知1.505 ×1023个X气体分子的质量为8g,则X气体的摩尔质量是
A. 16g B. 32g C. 32g/mol D. 64g /mol
【答案】C
【解析】
【分析】
【详解】根据n= ,1.505 ×1023个X气体的物质的量= =0.25mol,气体的摩尔质量M= =
=32g/mol,答案选C。
20. 下列粒子不具有氧化性的是( )
A. Cl B. H+ C. Mg D. CO
2 2
【答案】C
【解析】
【分析】
处于元素的最高价或中间价态的微粒具有氧化性,处于元素最低价的微粒不具有氧化性,由此分析。
【详解】A.氯元素的化合价有-1价、0价、+1价、+3价、+5价、+7价等,Cl 中氯元素的化合价为0价,
2
处于中间价态,具有氧化性,故A不符合题意;
B.氢元素的化合价有-1价、0价、+1价等,H+中氢元素的化合价为+1价,处于最高价,具有氧化性,故
B不符合题意;
C.Mg元素的化合价有+2价、0价,Mg元素的化合价为0价,为最低价,不具有氧化性,具有还原性,故C符合题意;
D.C元素的化合价有-4价、-2价、0价、+2价、+4价等,CO 中碳元素的化合价为+4价,为最高价,具
2
有氧化性,故D不符合题意;
答案选C。
二、填空题(共 60 分)
21. 按要求填空
(1)氢氧化铁胶体制备涉及的化学方程式_____;
(2)氯气自来水消毒涉及的化学方程式_____;
(3)过氧化钠与二氧化碳反应的化学方程式_____,其中过氧化钠什么颜色_____,还原剂是_____,氧化产
物是_____,还原产物是_____,n(氧化剂)∶n(还原剂)=_____,每生成 1molO ,转移_____mole-;
2
(4)漂白粉的制备涉及的化学方程式_____;
(5)把(4)中反应改写成离子方程式_____;
(6)氢气在氯气中燃烧实验现象有哪 4 个_____,_____,_____,_____。
【 答 案 】 (1). FeCl +3H O Fe(OH) ( 胶 体 )+3HCl (2). Cl+H O=HCl+HClO (3).
3 2 3 2 2
2NaO+2CO =2Na CO+O (4). 淡黄色 (5). NaO (6). O (7). NaCO (8). 1∶1 (9). 2 (10).
2 2 2 2 3 2 2 2 2 2 3
2Cl+2Ca(OH) =CaCl +Ca(ClO) +2H O (11). Ca(OH) +Cl═Ca2++ClO-+Cl-+H O (12). 安静燃烧 (13).
2 2 2 2 2 2 2 2
苍白色火焰 (14). 有白雾 (15). 瓶壁内有小水珠
【解析】
【分析】
(1)氯化铁水解生成氢氧化铁胶体和氯化氢;
(2)氯气溶于水,溶于水的氯气与水反应生成盐酸和次氯酸;
(3)过氧化钠与二氧化碳反应生成碳酸钠和氧气,反应中过氧化钠自身发生氧化还原反应,O元素化合价
由-1价分别变化为0、-2价,据此分析解答;
(4)将氯气通入石灰乳[Ca(OH) ]制取漂白粉,据此分析解答(4)和(5);
2
(6)氢气在氯气中安静地燃烧,Cl + H 2HCl,据此分析解答。
2 2
【详解】(1)氯化铁水解生成氢氧化铁胶体和氯化氢,反应的化学方程式为FeCl +3H O Fe(OH) (胶体)
3 2 3+3HCl,故答案为:FeCl +3H O Fe(OH) (胶体)+3HCl;
3 2 3
(2)氯气溶于水,溶于水的氯气与水反应生成盐酸和次氯酸,反应的化学方程式为Cl+H O=HCl+HClO,故
2 2
答案为:Cl+H O=HCl+HClO;
2 2
(3)过氧化钠与二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为2NaO+2CO =2Na CO+O ,过氧化
2 2 2 2 3 2
钠是淡黄色的固体粉末,反应中过氧化钠自身发生氧化还原反应,O元素化合价由-1价分别变化为0、-2
价,该反应中氧化剂、还原剂都是过氧化钠,水既不是氧化剂也不是还原剂,氧化产物是O,还原产物是
2
NaCO,n(氧化剂)∶n(还原剂)= 1∶1,每生成 1molO ,转移2mole-,故答案为:
2 3 2
2NaO+2CO =2Na CO+O ;淡黄色;NaO;O;NaCO;1∶1;2;
2 2 2 2 3 2 2 2 2 2 3
(4)漂白粉的主要成分是次氯酸钙[Ca(ClO) ]和氯化钙,将氯气通入石灰乳[Ca(OH) ]制取漂白粉,同时有水
2 2
生成,反应的化学方程式为2Cl+2Ca(OH) =Ca(ClO) +CaCl +2H O,故答案为:2Cl+2
2 2 2 2 2 2
Ca(OH) =CaCl +Ca(ClO) +2H O;
2 2 2 2
(5) 石灰乳[Ca(OH) ]中氢氧化钙几乎没有溶解,2Cl+2Ca(OH) =CaCl +Ca(ClO) +2H O改成离子方程式为
2 2 2 2 2 2
Ca(OH) +Cl═Ca2++ClO-+Cl-+H O,故答案为:Ca(OH) +Cl═Ca2++ClO-+Cl-+H O;
2 2 2 2 2 2
(6)氢气在氯气中安静地燃烧,发出苍白色的火焰,瓶口有白雾,瓶壁内有小水珠生成,故答案为:安静燃
烧;苍白色火焰;有白雾;瓶壁内有小水珠。
【点睛】本题的易错点为(5),要注意工业制漂白粉用的是石灰乳,不是澄清石灰水;难点是(3),要注意过
氧化钠与二氧化碳的反应中只有过氧化钠中的O元素的化合价发生变化。
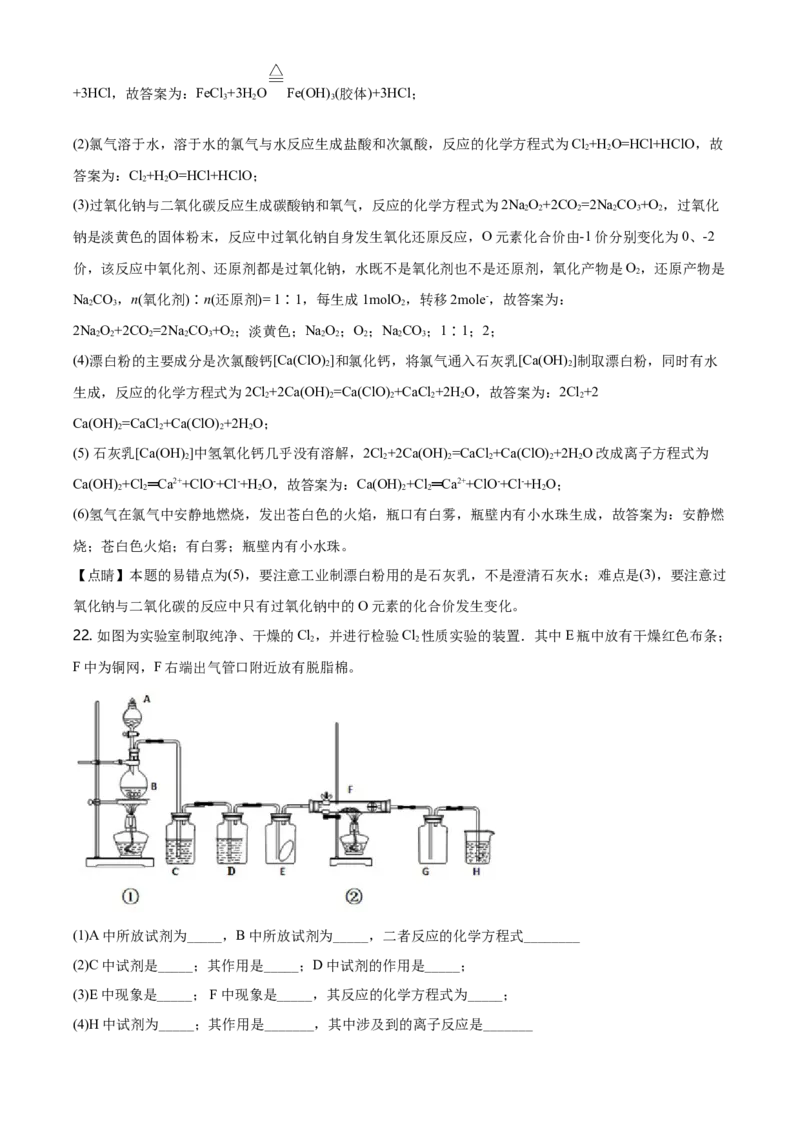
22. 如图为实验室制取纯净、干燥的Cl,并进行检验Cl 性质实验的装置.其中E瓶中放有干燥红色布条;
2 2
F中为铜网,F右端出气管口附近放有脱脂棉。
(1)A中所放试剂为_____,B中所放试剂为_____,二者反应的化学方程式________
(2)C中试剂是_____;其作用是_____;D中试剂的作用是_____;
(3)E中现象是_____; F中现象是_____,其反应的化学方程式为_____;
(4)H中试剂为_____;其作用是_______,其中涉及到的离子反应是_______(5)整套装置中有两处用酒精灯加热,两处酒精灯点燃的先后顺序是_____(用①或②填写)。
(6)实验室制备Cl 还可以用以下方法制备,请配平_______
2
HCl浓+ KMnO = MnCl + KCl+ Cl ↑ + HO
4 2 2 2
【答案】 (1). 浓HCl (2). MnO (3). MnO +4HCl(浓) MnCl +Cl↑+2H O (4). 饱和食盐水
2 2 2 2 2
(5). 吸收Cl 中的HCl (6). 干燥Cl 吸收HO (7). 红色布条不褪色 (8). 产生棕黄色的烟 (9).
2 2 2
Cu+Cl CuCl (10). NaOH溶液 (11). 处理尾气,防止污染环境 (12). Cl+2OH-=Cl-+ClO-+H O
2 2 2 2
(13). 先①后② (14). 16HCl(浓)+2KMnO =2MnCl +2KCl+5Cl ↑+8H O
4 2 2 2
【解析】
【分析】
装置A中为浓盐酸,B中为二氧化锰,将浓盐酸滴入二氧化锰中加热发生反应生成氯气、二氯化锰和水,
氯气中含有水蒸气和氯化氢,通过装置C中的饱和食盐水吸收氯化氢,通过装置D中的浓硫酸吸收水蒸气,
得到干燥的氯气,进入装置E干燥的氯气不能使干燥的有色布条褪色,进入装置F中加热反应生成无水氯
化铜,进入G中冷却得到氯化铜固体,最后剩余气体为氯气等,污染空气需要用装置 H中氢氧化钠溶液吸
收,由此分析。
【详解】(1)实验室是利用二氧化锰和浓盐酸加热反应生成氯气,A中是浓盐酸,B中是二氧化锰固体,二
者在加热的条件下反应生成二氯化锰、氯气和水,反应的化学方程式为 MnO +4HCl(浓)
2
MnCl +Cl↑+2H O;
2 2 2
(2)氯气中含有水蒸气和氯化氢,通过装置C中的饱和食盐水吸收氯化氢,C中试剂是饱和食盐水;其作用
是吸收Cl 中的HCl;通过装置D中的浓硫酸吸收水蒸气,得到干燥的氯气,作用是干燥Cl,吸收HO;
2 2 2
(3)进入装置E的是干燥的氯气,干燥的氯气不能使干燥的有色布条褪色;故E中现象是红色布条不褪色;
装置F中是氯气和铜在加热的条件下反应生成氯化铜,F中现象是产生棕黄色的烟,其反应的化学方程式
为Cu+Cl CuCl ;
2 2
(4)该实验的尾气是氯气,氯气有毒,会污染空气,需要用装置H吸收,H中盛装的是氢氧化钠溶液,氯气
和氢氧化钠反应生成氯化钠、次氯酸钠和水,反应的离子方程式为Cl+2OH-=Cl-+ClO-+H O;
2 2(5)两处用酒精灯加热,先点燃的是①,使氯气将整个装置中的空气排尽,再点燃②,可以观察到铜和氯气
的反应;若先点燃②,会使铜和空气中的氧气反应生成氧化铜,不能发生氯气和铜的反应,故点燃酒精灯
的先后顺序为先①后②;
(6)实验室制备Cl 还可以用浓盐酸和高锰酸钾常温下发生氧化还原反应生成二氯化锰、氯气、氯化钾和水,
2
将反应物和生成物写入化学方程式,浓盐酸中的氯原子化合价从-1价升高到0价,两个氯原子化合价共升
高了2价,高锰酸钾中锰元素的化合价从+7价降低到+2价,共降低了5价,化合价的最小公倍数为10,
KMnO 的系数为2,浓盐酸的系数为5,根据元素守恒、电荷守恒确定其他物质的系数,配平后的化学方
4
程式为:16HCl(浓)+2KMnO =2MnCl +2KCl+5Cl ↑+8H O。
4 2 2 2
23. 某同学做了有关氯水成分 的探究实验,按要求填空
实验序号 实验方法 实验现象 结论 离子反应
将氯水滴加到 (2)氯水中含
1 (1)生成___ (3)_____
AgNO 溶液中 _____
3
将氯水滴到淀粉KI (4)淀粉KI试纸 (5)氯水中含有
2 (6)_____
试纸上 _____ _____
将足量的氯水滴加 (7)溶液中有 (8)氯水中含有
3 (9)_____
到NaCO 溶液中 _____ _____
2 3
(11)氯水中含
将氯水滴到石蕊溶
4 (10)_____ _____(12)和 无
液中
_____
【答案】 (1). 白色沉淀 (2). Cl- (3). Ag++Cl-=AgCl↓ (4). 变蓝 (5). Cl (6). Cl+2I-=I +2Cl-
2 2 2
(7). 有气泡产生 (8). H+ (9). 2H++ =CO ↑+H O (10). 先变红后褪色 (11). H+ (12). HClO
2 2
【解析】
【分析】
由于氯水中含有Cl、HO、HClO、H+、Cl-、ClO-、少量OH-微粒,根据氯水的成分可以确定氯水的性质,
2 2
由此分析。
【详解】实验1中,氯水中含有Cl-,将氯水滴加到AgNO 溶液中,Cl-和Ag+会发生反应生成氯化银白色沉
3
淀,离子反应方程式为:Ag++Cl-=AgCl↓;实验2中,氯水中含有Cl,将氯水滴到淀粉KI试纸上,氯水中的Cl 具有氧化性,会将I-氧化成碘单质,
2 2
发生氧化还原反应,离子反应方程式为:Cl+2I-=I +2Cl-;碘单质遇淀粉变蓝,故实验现象为淀粉KI试纸
2 2
会变蓝;
实验3中,氯水中含有H+,将足量的氯水滴加到NaCO 溶液中, 和H+会发生反应生成水和二氧化碳,
2 3
离子方程式为:2H++ =CO ↑+H O;实验现象为有气泡产生;
2 2
实验4中,氯水中含有H+、HClO,将氯水滴到石蕊溶液中,石蕊溶液遇酸变红,由于还含有HClO,
HClO具有漂白性,可以使红色石蕊溶液褪色。
24. (1)CO 的摩尔质量为_________;88gCO 的物质的量为_____,所含二氧化碳分子数为_____。
2 2
(2)1.7gNH 共有_____mol 质子;0.1molCH 共有_____个电子。
3 4
(3)已知 1.2gRSO 中含 0.01molR2+,则 RSO 的摩尔质量是_____;R 的相对原子质量是_____。
4 4
【答案】 (1). 44g/mol (2). 2mol (3). 1.204×1024(或2 N ) (4). 1 (5). N (或6.02×1023) (6).
A A
120g/mol (7). 24
【解析】
【分析】
【详解】(1)CO 的相对分子质量为 44,CO 的摩尔质量为 44g/mol,88g CO 的物质的量为
2 2 2
=2mol,所含二氧化碳分子数为 2mol×6.02×1023 mol-1=1.204×1024,故答案为:44g/mol;2mol;
1.204×1024(或2 N );
A
(2) 一个氨气分子含有10个质子,1.7g NH 共有 ×10=1mol 质子;一个甲烷分子含有10个电子,
3
0.1mol CH 共有0.1mol×10×6.02×1023 mol-1=6.02×1023 个电子,故答案为:1;N (或6.02×1023);
4 A
(3)已知1.2gRSO 中含0.01molR2+,则RSO 的摩尔质量是 =120g/mol,R的相对原子质量是120-
4 4
96=24,故答案为:120g/mol;24。