文档内容
2023−2024 学年上学期期末模拟考试 02
高一化学
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号填
写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:人教版2019必修第一册全册。
5.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Fe 56
第Ⅰ卷(选择题 共 54 分)
一、选择题:本题共18个小题,每小题3分,共54分。在每小题给出的四个选项中,只有一项是符合题目要
求的。
1.化学与生产、生活、科技等密切相关。下列说法不正确的是
A.Na着火可用泡沫灭火器灭火
B.氯气可用于自来水的杀菌、消毒
C.氯化铁溶液可用作覆铜板蚀刻的腐蚀液
D.氧化铝可用于制造耐高温的容器
2.化学物质种类繁多,通过分类思想来学习可以化繁为简。下列关于物质分类正确是
选
混合物 碱 碱性氧化物
项
A 冰水混合物 苛性钾
B 、石墨混合物 氨水
C
D 漂白粉
3.用N 代表阿伏加德罗常数的数值,下列说法正确的是
A
A.浓盐酸与足量MnO 反应生成11.2 L Cl ,转移电子数为N
2 2 A
学学科科网网((北北京京))股股份份有有限限公公司司B.将1 mol Cl 通入足量水中,HClO、Cl-、ClO-微粒数之和为2N
2 A
C.有铁粉参加的反应,若生成2 mol Fe2+,则转移电子数一定为4N
A
D.0.1 mol FeCl 加入沸水中完全反应生成Fe(OH) 胶体粒子数小于0.1N
3 3 A
4.下列有关物质性质的比较正确的是
A.碱性:
B.离子半径:
C.还原性:
D.热稳定性:
5.下列有关化学用语的表示正确的是
A.N 的电子式:
2
B.HO的结构式:H−O−H
2
C.钠离子的结构示意图:
D.质量数为44、中子数为24的钙原子: Ca
6.下列叙述不正确的是
A.钠在氧气中燃烧比在空气中更为剧烈
B.钠燃烧发出黄色火焰,生成淡黄色固体NaO
2 2
C.金属钠很活泼,金属性很强
D.将Na投入FeSO 溶液中可置换出Fe
4
7.下列离子组能大量共存且溶液为无色的是
A.Mg2+、K+、SO 、NO B.Fe3+、Ba2+、Cl-、NO
C.Ca2+、K+、CO 、OH- D.Na+、Al3+、OH-、Cl-
8.为了检验某FeCl 溶液是否变质,可以向溶液中加入
2
A.盐酸 B.铁片 C.KSCN溶液 D.石蕊溶液
9.下列有关物质性质与用途具有对应关系的是
A.明矾易溶于水,可用作净水剂
B. 受热易分解,可用于治疗胃酸过多
C. 具有两性,可用作耐高温材料
D.次氯酸具有强氧化性,可用于杀菌消毒
10.下列制取氯气的实验装置或者操作正确的是
学学科科网网((北北京京))股股份份有有限限公公司司A.制备氯气 B.除去 中的 气体 C.干燥氯气 D.吸收多余的氯气
11.“类比”是研究物质变化规律的重要方法。下列有关“类比”对物质性质的推测正确的是
A. 溶液显酸性, 溶液也显酸性
B. 是酸性氧化物, 也是酸性氧化物
C.Na在空气中加热生成 ,Li在空气中加热也生成
D. 溶解度大于 , 的溶解度也大于
12.为除去括号内的杂质,下列各选项中所选用的试剂或方法错误的是
A. 固体 :加热
B. 气体 :通过饱和 溶液,洗气
C. ( ):将混合物在氧气中加热
D. 固体 :加入足量的 溶液,过滤
13.下列关于铝及其化合物的说法不正确的是
A.铝的化学性质不活泼
B.Al(OH) 是一种医用胃酸中和剂
3
C.向AlCl 溶液中滴加氨水可产生白色沉淀
3
D.铝制餐具不可以用来长时间存放碱性食物
14.实验室欲用氯化钠固体配制500mL 0.10mol·L-1的NaCl溶液,下列叙述正确的是
A.实验可用的玻璃仪器:烧杯、500mL容量瓶、玻璃棒、胶头滴管
B.用托盘天平称取29.25gNaCl固体配制溶液
C.定容时若俯视刻度线,则所得溶液浓度偏低
D.加水时不慎超过了刻度线,用胶头滴管直接吸出多余液体
15.下列关于氯气和氯水的叙述正确的是
A.可以用 pH 试纸测定新制氯水的 pH
B.氯水放置数天后,溶液的酸性逐渐减弱
C.新制的氯水一定含有 H、HO 和 HClO 三种分子
2 2
D.加入硝酸酸化的 AgNO 溶液产生白色沉淀说明有 Cl-的存在
3
16.下列各组物质中,满足图示关系并在一定条件下能一步转化的组合是
学学科科网网((北北京京))股股份份有有限限公公司司序号 X Y Z W
① NaCl Na
②
③ HCl HClO
④ Al
A.①② B.①③ C.②③ D.③④
17.短周期主族元素X、Y、Z、W的原子序数依次增大,Y在短周期中原子半径最大,Z是地壳中含量最高
的金属元素,X和W同主族,W的最高正化合价与最低负化合价的代数和为4。下列说法正确的是
A.简单气态氢化物的稳定性:
B.原子半径由小到大的顺序:
C.最高价氧化物对应水化物的碱性:
D.X与Y形成的化合物中只能形成离子键,不能形成共价键
18.双碱法脱硫过程如图所示。下列说法不正确的是
A.过程Ⅰ中, 表现出酸性氧化物的性质
B.过程Ⅱ中,1mol 可氧化2mol
C.总反应为
D.双碱法脱硫过程中, 可以循环利用
第 II 卷(非选择题 共 46 分)
二、非选择题:本题共5个小题,共46分。
19.(8分)分类是研究物质组成及其变化的一种常用的科学方法。
I.现有以下物质:①液氯;②氢氧化铁胶体;③NaO 粉末;④熔融NaHSO;⑤饱和食盐水。
2 2 4
(1)在上述物质中,属于化合物的是 (填标号,下同),属于电解质的是 ,能导电的
是 。
(2)写出④的电离方程式 。
(3)写出①在水中发生反应的离子方程式 。
学学科科网网((北北京京))股股份份有有限限公公司司II.四种基本反应类型与氧化还原反应的关系如图所示,其中甲、乙、丙、丁分别表示一种基本反应类型。
(4)下列反应中,与图中丙所表示反应类型一致的是 ,属于氧化还原反应且水只用作还原剂的是
。
A.2NaCl+2H O 2NaOH+Cl ↑+H ↑
2 2 2
B.3Fe+4H O(g) Fe O+4H
2 3 4 2
C.2F+2H O=4HF+O
2 2 2
D.3NO +H O=2HNO +NO
2 2 3
20.(8分)下表是部分元素周期表的结构图,表中每一个序号代表一种元素。请根据要求回答下列问题。
①
② ③ ④
⑤ ⑥ ⑦ ⑧
(1)以上元素中金属性最强的元素符号是 。
(2)元素④、⑤所形成的简单离子半径较大的是 (用化学符号表示)。
(3)以上元素的最高价氧化物对应的水化物中,酸性最强的酸是 (填化学式)。
(4)A、B均为以上某两种元素组成的含四个原子核的分子,A中有10个电子,B中有18个电子,则A的电
子式 ,B的分子式 。
(5)由①、③、⑧三种元素以原子个数比 形成的化合物中含有的化学键类型是 。
(6)元素⑤、⑥的最高价氧化物对应水化物之间反应的离子方程式为 。
21.(10分)现有 七种物质,它们之间能发生如下反应(图中部分反应物、产物及反应条件末标出)。请
根据以上信息回答下列问题:
(1)写出下列物质的化学式:B 、C 、乙 。
(2)A物质在空气中燃烧的产物是 色的粉末,该物质与 反应放出的气体是 。
(3)写出反应③和⑤的离子反应方程式: 。
(4)在物质 中加入 溶液,现象为 ,发生反应的化学方程式为 。
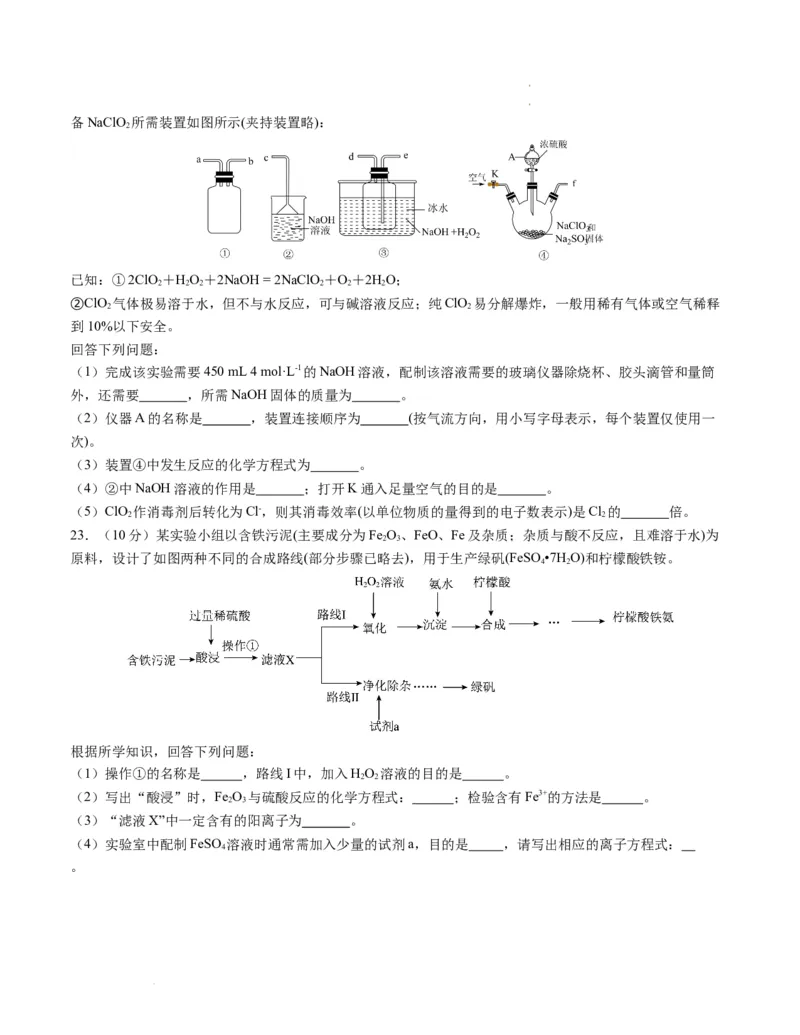
22.(10分)NaClO 是一种高效的氧化剂和优质漂白剂,在水中溶解度较大,遇酸放出ClO ,某探究小组制
2 2
学学科科网网((北北京京))股股份份有有限限公公司司备NaClO 所需装置如图所示(夹持装置略):
2
已知:①2ClO +HO+2NaOH = 2NaClO +O+2HO;
2 2 2 2 2 2
②ClO 气体极易溶于水,但不与水反应,可与碱溶液反应;纯ClO 易分解爆炸,一般用稀有气体或空气稀释
2 2
到10%以下安全。
回答下列问题:
(1)完成该实验需要450 mL 4 mol·L-1的NaOH溶液,配制该溶液需要的玻璃仪器除烧杯、胶头滴管和量筒
外,还需要 ,所需NaOH固体的质量为 。
(2)仪器A的名称是 ,装置连接顺序为 (按气流方向,用小写字母表示,每个装置仅使用一
次)。
(3)装置④中发生反应的化学方程式为 。
(4)②中NaOH溶液的作用是 ;打开K通入足量空气的目的是 。
(5)ClO 作消毒剂后转化为Cl-,则其消毒效率(以单位物质的量得到的电子数表示)是Cl 的 倍。
2 2
23.(10分)某实验小组以含铁污泥(主要成分为Fe O、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为
2 3
原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾(FeSO •7H O)和柠檬酸铁铵。
4 2
根据所学知识,回答下列问题:
(1)操作①的名称是 ,路线I中,加入HO 溶液的目的是 。
2 2
(2)写出“酸浸”时,Fe O 与硫酸反应的化学方程式: ;检验含有Fe3+的方法是 。
2 3
(3)“滤液X”中一定含有的阳离子为 。
(4)实验室中配制FeSO 溶液时通常需加入少量的试剂a,目的是 ,请写出相应的离子方程式:
4
。
学学科科网网((北北京京))股股份份有有限限公公司司