文档内容
2024—2025 学年第一学期半期考
高一化学试卷
本试卷满分 100分,考试用时 75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在
本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.本试卷主要考试内容:鲁科版必修第一册第 1章、第 2章第 1节。
5.可能用到的相对原子质量:
学科网(北京)股份有限公司
H 1 C 1 2 N 1 4 O 1 6 N a 2 3 C l 3 5 . 5 C u 6 4
一、选择题:本题共 10小题,每小题 4分,共40分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.化学与生活密切相关。下列生活中常用物质的主要成分为无机化合物的是( )
A.白糖 B.菜刀(钢制)
C.食盐 D.塑料杯
2.某同学利用所学知识去探究 F e
2
O
3
的性质,设计了如下研究程序,合理的是( )
A.观察(得出 F e
2
O
3
的物理性质)→实验→分类(预测 F e
2
O
3
的化学性质)→比较并得出结论
B.实验→分类(预测 F e
2
O
3
的化学性质)→观察(得出 F e
2
O
3
的物理性质)→比较并得出结论
C.分类(预测 F e
2
O
3
的化学性质)→观察(得出 F e
2
O
3
的物理性质)→实验→比较并得出结论
D.观察(得出 F e
2
O
3
的物理性质)→分类(预测 F e
2
O
3
的化学性质)→实验(观察实验现象、验证预测)
→比较得出结论,对于异常现象再预测,再实验,再验证
3.铜器久置于空气中会和空气中的 H
2
O 、 C O
2
、 O
2
作用产生“绿锈”,该“绿锈”俗称“铜绿”[化学式
为Cu OH CO ],又称“孔雀石”。某同学利用如图所示的一系列反应实现了“铜→铜绿→……→铜”
2 2 3
的转化。下列说法错误的是( )
铜铜绿盐酸CuCl NaOH溶液CuOH △CuOH2 /△Cu
① ② 2 ③ 2 ④ ⑤
A.上述转化中铜元素的存在形态有两种
B.上述转化中涉及四种基本反应类型
C.氧化铜的摩尔质量是NaOH的摩尔质量的2倍
D.将135gCuCl 溶于1L水,所得溶液的浓度为1molL1
24.下列对有关概念的理解正确的是( )
A.摩尔是基本物理量之一
B.一定温度下,溶液中溶质的浓度不随所取溶液体积的变化而变化
C.22.4L任何气体所含的分子数均相等
D.1mol任何物质所含的原子数均为N
A
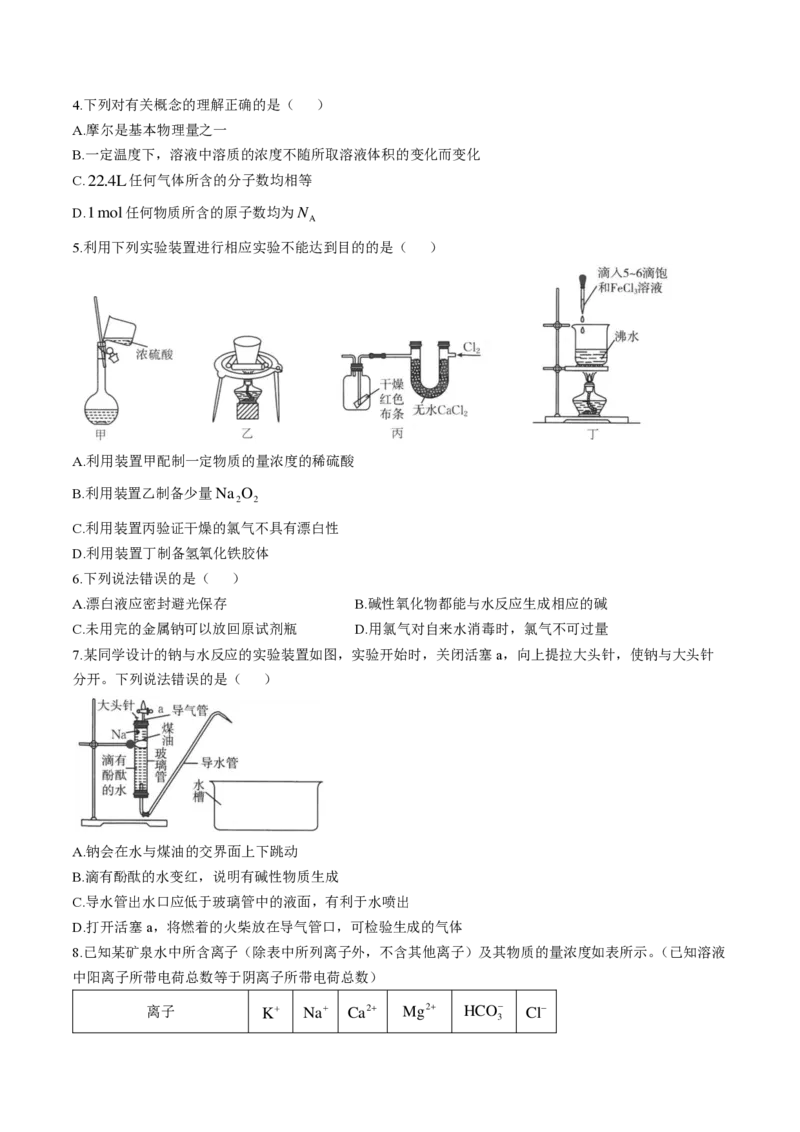
5.利用下列实验装置进行相应实验不能达到目的的是( )
A.利用装置甲配制一定物质的量浓度的稀硫酸
B.利用装置乙制备少量Na O
2 2
C.利用装置丙验证干燥的氯气不具有漂白性
D.利用装置丁制备氢氧化铁胶体
6.下列说法错误的是( )
A.漂白液应密封避光保存 B.碱性氧化物都能与水反应生成相应的碱
C.未用完的金属钠可以放回原试剂瓶 D.用氯气对自来水消毒时,氯气不可过量
7.某同学设计的钠与水反应的实验装置如图,实验开始时,关闭活塞a,向上提拉大头针,使钠与大头针
分开。下列说法错误的是( )
A.钠会在水与煤油的交界面上下跳动
B.滴有酚酞的水变红,说明有碱性物质生成
C.导水管出水口应低于玻璃管中的液面,有利于水喷出
D.打开活塞a,将燃着的火柴放在导气管口,可检验生成的气体
8.已知某矿泉水中所含离子(除表中所列离子外,不含其他离子)及其物质的量浓度如表所示。(已知溶液
中阳离子所带电荷总数等于阴离子所带电荷总数)
离子 K Na Ca2 Mg2 HCO Cl
3
学科网(北京)股份有限公司物质的量浓度/
molL1
104 103 103 2103 3103 x
则x的值为( )
A.104 B.1.1103 C.3.0103 D.4.1103
9.下列钠及其化合物的有关叙述中错误的是( )
A.常温下,NaHCO 和Na CO 在水中的溶解度不同
3 2 3
B.等质量的Na CO 和NaHCO 跟足量盐酸充分反应产生的CO 质量不同
2 3 3 2
C.钠及其化合物灼烧时,焰色相同
D.Na O、Na O 溶于水时的现象相同
2 2 2
10.标准状况下,含有b个原子的气态化合物XY 的质量为ag。则cgXY 气体在标准状况下的体积为
2 2
(N 为阿伏加德罗常数的值)( )
A
22.4bc 22.4bc
A. L B. L
aN 3aN
A A
22.4bc 22.4bc
C. L D. L
a 3a
二、非选择题:共 4小题,共 60分。
11.(15分)A、B、C、D、E、F、G为七种常见物质。常温下,A为淡黄色固体,A、B、D、E、F均为
纯净物且含有相同的金属元素,F、G为单质,它们满足如图所示转化关系(“ ”表示两种物质间可以相
互转化,部分反应物和生成物未列出)。
请回答:
(1)从组成元素角度分析,A物质所属的类别为________,写出其常见的一种用途:________。
(2)写出一个A水BC的化学方程式:________。
(3)E在熔融状态下能导电的原因为________。
(4)F与G反应的现象为________。
(5)CFA的条件为________;若无此条件,造成的结果为________。
12.(15分)实验室需配制240mL0.8molL1的NaCl溶液,根据所学知识,回答下列问题:
(1)若选用氯化钠固体进行配制,则需要称取________g的氯化钠。
(2)配制该溶液时,提供的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管:
学科网(北京)股份有限公司①要完成该实验,还需使用到的玻璃仪器为________。
②该实验中,玻璃棒的作用为________。
③________(填“能”或“不能”)用5mL医用注射器代替胶头滴管进行上述实验。
(3)分析下列操作将导致所配溶液的物质的量浓度如何变化(其余操作均正确):
①容量瓶洗净后未经干燥处理________(填“偏高”“偏低”或“无影响”,下同)
②加水定容时,仰视刻度线________
③所使用的烧杯和玻璃棒只洗涤了1次________
④移液时不慎将液体洒在容量瓶外面________
13.(15分)过量的CO 通入NaOH溶液中发生的反应分两步进行,第一步反应为
2
CO 2NaOH Na CO 2H O,第二步反应为CO Na CO H O2NaHCO 。现向
2 2 3 2 2 2 3 2 3
学科网(北京)股份有限公司
2 0 0 m L
质量分数为20%的NaOH溶液(密度为1.2gcm3)中通入一定量的CO ,同学们对反应后溶液的溶质
2
进行了探究。已知CaCl 稀溶液呈中性,且与NaHCO 溶液混合无白色沉淀产生;CaCl 浓溶液与
2 3 2
NaHCO 溶液反应有白色沉淀生成。
3
I.(1)该NaOH溶液的物质的量浓度为________molL1。
II.预测反应后溶液溶质成分
(2)①NaOH和Na CO ;②全部为Na CO ;③________;④全部为NaHCO 。
2 3 2 3 3
Ⅲ.实验探究溶液溶质成分
(3)第二步反应的离子方程式为________。
(4)取少许反应后的溶液于试管中,滴入过量的CaCl 稀溶液,有白色沉淀产生,静置后取上层清液,
2
分装于甲、乙两支试管中,向甲中加入几滴酚酞试液,溶液变红。
a.生成白色沉淀的离子方程式为________。
b.该溶液的溶质一定含有________,可能含有________。
(5)若预测③是正确的,则向乙试管中滴入________,有________产生,通入的CO 的体积(标准状况
2
下)范围为________LV ________L。
高温、高压
14.(15分)含氮物质发生如下反应:①N 3H 2NH ,②
2 2 3
催化剂
△
8NH 3Cl N 6NH Cl,③NH ClNaOH NaClH ONH ,④
3 2 2 4 4 2 3△
NH Cl NH HCl。请回答下列问题:
4 3
(1)上述反应中,反应①④分别属于四大基本反应类型的________、________。
(2)标准状况下,11.2LCl 的摩尔质量为________,物质的量为________mol,质量为________g。
2
(3)3.65gHCl中含有的H原子个数与gH O中含有的H原子个数相同。
2
(4)标准状况下,8.96L由N 和NH 组成的混合气体质量为8.8g,则此混合气体的平均摩尔质量为
2 3
________gmol1,nN :nNH ________,氮原子总数为________N (保留两位有效数字)。
2 3 A
学科网(北京)股份有限公司2024—2025 学年第一学期半期考
高一化学试卷参考答案
1.C 2.D 3.D 4.B 5.A 6.B 7.C 8.D 9.D 10.B
11.(1)氧化物(或化合物,2分);作供氧剂(2分)
(2)2Na O 2H O4NaOHO (2分)
2 2 2 2
(3)有自由移动的离子(或存在自由移动的带电微粒,2分)
(4)剧烈燃烧,火焰呈黄色,生成大量白烟(每点1分,共3分)
(5)加热或点燃(2分);反应产物发生变化(2分)
12.(1)11.7(2分)
(2)①250mL容量瓶(2分)
②引流和搅拌(2分)
③能(1分)
(3)①无影响(2分)
②偏低(2分)
③偏低(2分)
④偏低(2分)
13.(1)6.0(2分)
(2)Na CO 和NaHCO (2分)
2 3 3
(3)CO2 H OCO 2HCO(2分)
3 2 2 3
(4)a.Ca2 CO2 CaCO (2分)
3 3
b.Na CO (1分);NaOH或NaHCO (2分)
2 3 3
(5)CaCl 浓溶液(或其他合理答案,1分);白色沉淀(1分);13.44(1分);26.88(1分)
2
14.(1)化合反应(1分);分解反应(1分)
(2)71gmol1(2分);0.5(1分);35.5(2分)
(3)0.9(2分)
(4)22(2分);5:6(2分);0.58(2分)
学科网(北京)股份有限公司