文档内容
龙东十校联盟高二学年4月化学学科试题
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,考试结束后,将答题卡交回。
注意事项:
1. 答题前,考生先将自己的姓名、准考证号码填写清楚,将条形码准确粘贴在考生信息条形码粘贴
区。
2. 选择题必须使用2B铅笔填涂;非选择题必须使用0.5毫米黑色字迹笔书写,字体工整、笔迹清楚。
3. 请按照题号顺序在各题目的答题区域作答,超出答题区域书写的答案无效;在草稿纸、试题卷上
答题无效。
4.保持卡面清洁,不得折叠,不要弄破、弄皱,不准使用涂改液、修正带、刮纸刀。
可能用到的相对原子质量:H-1 O-16 S-32 Fe-56 Cu-64
第Ⅰ卷(选择题,共45分)
一、选择题(每小题只有一个正确选项,每小题3分,共45分)
1. 三四月间,松花江佳木斯段开江,下列有关“冰与水”的说法正确的是
A. 冰刚刚融化为液态水时(温度低于4℃),水分子的空隙减小,密度增大
B. 冰是由水分子通过分子间作用力形成的分子晶体,故冰中不含共价键
C. 接近水沸点的水蒸气相对分子质量的测定值为18
D. 向冰雪路面上撒盐,可提高冰雪的熔点
2. 下列有关物质聚集状态的说法正确的是
A. 在极光和雷电里,存在离子液体
B. 液晶是常温下呈液态的晶体
C. 某些纳米晶体的熔点会随着颗粒大小发生变化
D. 非晶体的X射线衍射图谱中只有分立的斑点,没有明锐的衍射峰
3. 杭州某民营企业的主导产品是人形机器人,它由关节模组、躯体结构、灵巧手和计算平台等构成。有
关各部分的说法正确的是
A. 关节模组:空心杯电机的转子材料铜含有阴阳离子,具有较好的导电性
B. 躯体结构:外壳所用的聚醚醚酮( O O C n)的链节中有手性碳原子
O
C. 计算平台:中央处理器材料中的单晶硅,可以通过“拉单晶”的方法由熔融态硅制备
D. 灵巧手: 腱绳材料 中的超高分子量聚乙烯纤维与普通聚乙烯纤维属于同系物
4. 下列晶体熔化时,破坏的作用力的类型完全相同的是
A. LiPF 和NaAlCl
6 4B. 干冰和NaCl
C. MgCl 和AlCl
2 3
D. 石墨和晶体硫
5. 下列制备晶体的操作,不正确的是
A. 用于制造激光器的KH PO 大晶体是由其水溶液结晶出来的
2 4
B. 用装有冷水的表面皿或小烧瓶盖在碘蒸气上,可得到碘晶体
C. 向饱和氯化钠溶液中,滴入浓盐酸,有氯化钠晶体析出
D. 将氯化铁溶液蒸干灼烧得到无水氯化铁晶体
6. 某同学认真阅读教科书后,提出下列有关元素周期表的说法,其中错误的是
A. 按照核外电子排布分区,d区、f区的元素种类相同
B. 由于Be、Al在元素周期表中处于对角线位置,它们化合物的许多性质相似,但不完全相同
C. 元素周期表中p区元素均为非金属元素
D. 俄国化学家门捷列夫成功预测了几种当时未知元素的性质
7. 下列关于元素周期律的说法正确的是
A. 稀有气体元素的第一电离能在同周期中最小
B. 第三周期内,比左右相邻元素的第一电离能都大的元素有两种
C. 每个短周期中,除稀有气体外,随着原子序数递增,原子半径递增
D. 电负性最大的元素与电负性最小的元素不容易形成二元化合物
8. 下列每组物质中,前者的数据大于后者的是
A. 沸点:邻羟基苯甲醛和对羟基苯甲醛
B. 水中溶解度: 1-戊醇和乙醇
C. 基态原子未成对电子数:铬(Cr)和锰(Mn)
D. 阳离子的配位数: NaCl晶体和CsCl晶体
9. 臭氧是氧气的同素异形体,因有一种特殊的腥臭味而得名,关于臭氧的说法正确的是
A. 氧气在静电作用下会被氧化为臭氧,所以在复印机工作时会闻到特殊腥味
B. 中心氧原子形成的sp2杂化轨道,两个轨道与两旁的氧原子形成σ键,另一个轨道容纳孤对电子
C. 已知臭氧中O-O键的键长比氧气中的略长,可知其键能也较大
D. 臭氧是含非极性键的极性分子,可微溶于水
10. 白磷与红磷是磷元素的两种常见的同素异形体,白磷转化为红磷时,有热量放出。下图为某种红磷分
子结构,它是由P 分子断开一个键转变成等边三角形而连成的链状巨分子。有关说法错误的是
4A. 白磷分子中的键角为60º,比p轨道间的夹角90º小,p-p键的张力较大
B. 红磷较白磷稳定
C. 1个该红磷分子的基本单元中4个磷原子处于同一平面
D. 1个白磷分子可结合10个氧原子形成PO
4 10
11. Al O 具有12种晶体结构,其中α- AlO(刚玉)不溶于水和酸,用作切削工具等;β- Al O 有离子传
2 3 2 3 2 3
导能力(允许Na+通过);γ- Al O 不溶于水,但能溶于酸和碱。有关说法正确的是
2 3
A. γ- Al O 是两性氧化物,其物理性质与其他晶型相同
2 3
B. 以β- Al O 为固体电解质的钠-硫蓄电池,放电时Na+向正极移动
2 3
C. α- Al O 的晶体中Al3+与O2-个数比为3:2
2 3
D. α- Al O 的晶体虽属于共价晶体,但其中也有一定离子键的成分,最好看成混合型晶体
2 3
12. 某储氢材料由La、H两种原子构成,立方晶胞结构如下。在储氢时,每个氢原子结合4个H形成类似
甲烷的结构,有关说法错误的是
A. LaH 中,H原子位于由La原子围成的四面体空隙中
2
B. LaH 中,La与H原子数之比为1:10
x
C. LaH 中,H原子的配位数为8
2
D. 储氢后晶胞参数发生了变化
13. 镍能形成多种配合物,如正四面体形的Ni(CO) 、平面正方形的[Ni(CN) ]2-和八面体形的[Ni(NH )]2+等,
4 4 3 6
下列说法正确的是
A. Ni(CO) 中的配位原子是氧原子
4
B. [Ni(CN) ]2-中Ni、C、N不可能处在同一直线上
4
C. [Ni(NH )]2+中H-N-H键角比NH 中的小
3 6 3
D. 根据微粒空间结构与杂化轨道的关系,[Ni(CN) ]2-和 [Ni(NH )]2+中可能有d轨道参与杂化
4 3 6
14. 干冰的晶胞结构如图,晶胞参数为a,下列有关干冰的说法错误的是
A. 1个CO 分子周围有12个紧邻分子
2B. 晶胞中含有4个CO 分子
2
√2
C. 紧邻CO 分子的碳原子距离为 a
2
2
D. CO 分子的空间取向(有四种)影响其热稳定性
2
15. 分子间通过分子间相互作用(如氢键、范德华力和疏水相互作用等)自发地形成有序分子聚集体的过
程称为超分子的自组装。下列过程不能表现这种特性的是
A. 表面活性剂分子在水溶液中通过疏水作用自发形成胶束
B. DNA 中两条链通过碱基之间的氢键(A-T和C-G配对)形成稳定的双螺旋结构
C. 淀粉与丙烯酸钠在一定条件下反应生成以淀粉为主链的接枝共聚物
D. 两亲水性分子(如磷脂)在水溶液中自发排列形成双层膜结构
第Ⅱ卷(非选择题,共55分)
二、非选择题(共55分)
16. (14分)1886年法国科学家莫瓦桑制备氟气之后,氟元素日益受到关注。由于氟原子有半径很小,
电负性很大且d轨道一般不参与成键等特性,使得含氟化合物具有独特的性质及应用。
(1)NF 是微电子工业中一种优良的等离子蚀刻气体,可由NH 和F 在Cu催化剂存在下反应直接
3 3 2
得到:
4NH +3F NF +3NHF
3 2 3 4
上述化学方程式中的5种物质所属的晶体类型有______(填序号)。
a. 离子晶体 b. 分子晶体 c. 共价晶体 d. 金属晶体
(2)BF 与一定量的水形成 (H O) ·BF 晶体(记作Q),Q在一定条件下可转化为R:
3 2 2 3
Q转化为R的过程中,破坏的微粒间的作用力不涉及______(填序号)。
a. 离子键 b. 极性共价键 c. 非极性共价键 d. 金属键 e. 氢键 f. 范德华力
(3)GaF 的熔点高于1 000 ℃,GaCl 的熔点为77.9 ℃,原因是______________________。
3 3
(4)NH BF(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 mol NH BF 含有____mol配位键。
4 4 4 4
(5)CaF 难溶于水,但可溶于含Al3+的溶液中,原因是________________ 。(结合离子方程式进行
2
解释)。已知AlF3-在溶液中可稳定存在。
6
(6)静电作用是影响超分子识别的重要因素之一,15-冠-5-醚(空腔直径170-220pm)依靠氧原子上
的孤对电子与Na+(直径204pm)的静电作用,实现对Na+的识别,而二十氟-15-冠-5-醚(如下图)可识别Li+(直径152pm),已知这两种冠醚的空腔直径接近,从静电作用的角度分析,二十氟-15-冠-5-醚可
以识别Li+的原因可能是_______________________________。
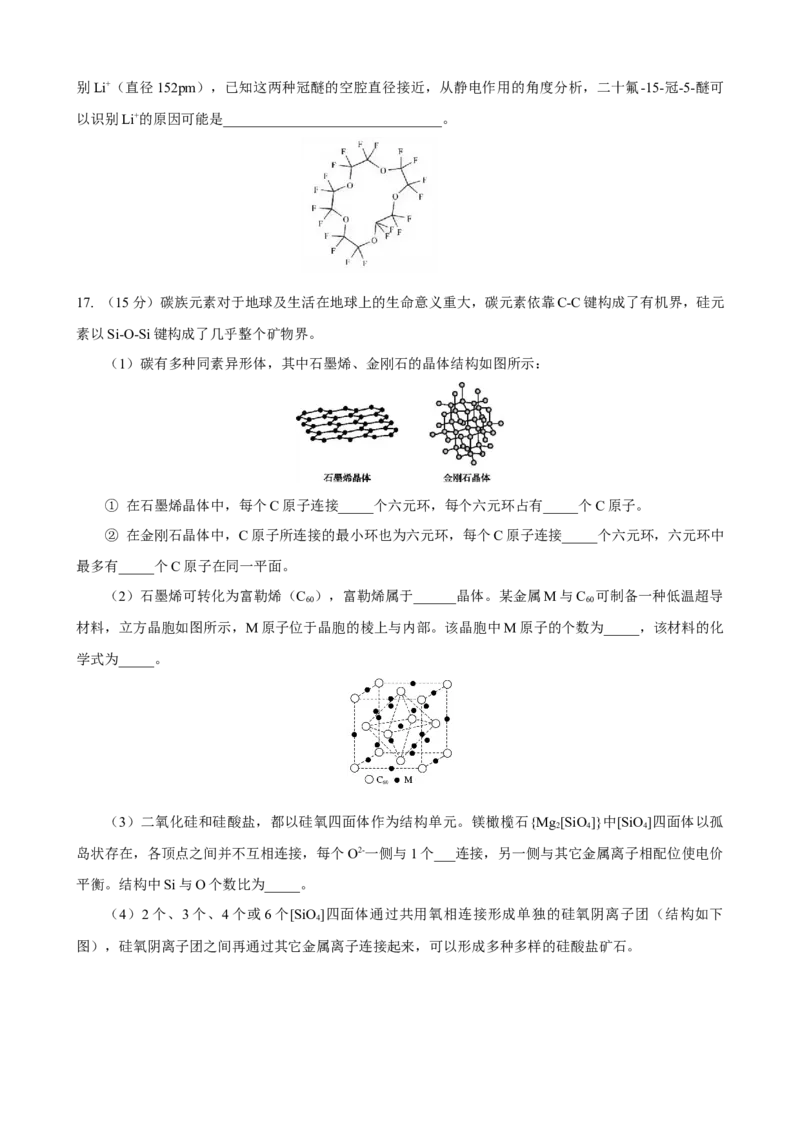
17. (15分)碳族元素对于地球及生活在地球上的生命意义重大,碳元素依靠C-C键构成了有机界,硅元
素以Si-O-Si键构成了几乎整个矿物界。
(1)碳有多种同素异形体,其中石墨烯、金刚石的晶体结构如图所示:
① 在石墨烯晶体中,每个C原子连接_____个六元环,每个六元环占有_____个C原子。
② 在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接_____个六元环,六元环中
最多有_____个C原子在同一平面。
(2)石墨烯可转化为富勒烯(C ),富勒烯属于______晶体。某金属M与C 可制备一种低温超导
60 60
材料,立方晶胞如图所示,M原子位于晶胞的棱上与内部。该晶胞中M原子的个数为_____,该材料的化
学式为_____。
(3)二氧化硅和硅酸盐,都以硅氧四面体作为结构单元。镁橄榄石{Mg[SiO]}中[SiO]四面体以孤
2 4 4
岛状存在,各顶点之间并不互相连接,每个O2-一侧与1个___连接,另一侧与其它金属离子相配位使电价
平衡。结构中Si与O个数比为_____。
(4)2个、3个、4个或6个[SiO]四面体通过共用氧相连接形成单独的硅氧阴离子团(结构如下
4
图),硅氧阴离子团之间再通过其它金属离子连接起来,可以形成多种多样的硅酸盐矿石。① 其中A的化学式为_________,B结构的Si与O个数比为_________。
② 若镁方柱石化学式写作Ca Mg[Si O],绿宝石(Be和Al的硅酸盐)的硅氧阴离子结构如D,则其
2 2 7
化学式为___________。
(5)钒酸根VO 3-与PO 3-结构相似,钒酸盐也有类似硅酸盐的聚合,则二聚钒酸钠的化学式为
4 4
________,偏钒酸根是由[VO ]四面体通过共享氧原子连接而成的无限链状结构(如下图),则偏钒酸铵
4
的化学式为________。
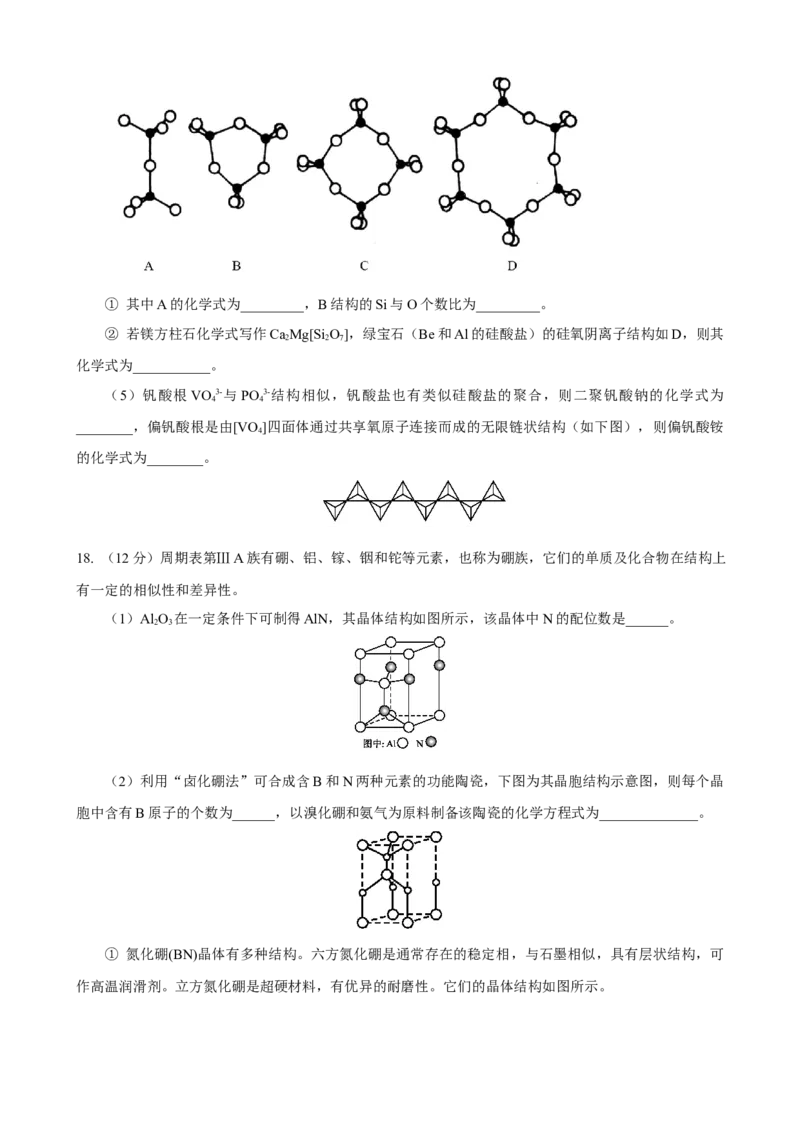
18. (12分)周期表第ⅢA族有硼、铝、镓、铟和铊等元素,也称为硼族,它们的单质及化合物在结构上
有一定的相似性和差异性。
(1)Al O 在一定条件下可制得AlN,其晶体结构如图所示,该晶体中N的配位数是______。
2 3
(2)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,下图为其晶胞结构示意图,则每个晶
胞中含有B原子的个数为______,以溴化硼和氨气为原料制备该陶瓷的化学方程式为______________。
① 氮化硼(BN)晶体有多种结构。六方氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可
作高温润滑剂。立方氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所示。关于这两种晶体的说法,正确的是______(填序号)。
a. 立方氮化硼含有σ键和π键,所以硬度大
b. 六方相氮化硼层间作用力小,所以质地软
c. 两种晶体中的B-N键主要为共价键
d. 两种晶体均难溶于水,易溶于有机溶剂
② 六方氮化硼晶体层内一个硼原子的相邻氮原子围成______形,六方氮化硼的结构与石墨相似却不
导电,原因是___________________。
③ 立方氮化硼与金刚石的晶体结构相似,硼原子位于面心立方晶胞的顶点和面心位置,氮原子位于
晶胞内部的四个四面体空隙。某同学在阅读教科书时发现,氮化硼熔点高于碳化硅,一时感到困惑,查
某人工智能技术得到如下信息(网络截图):
该同学结合以上信息,得到如下推断,其中错误的是
a. 立方氮化硼中氮的配位数为4,硼的配位数为3
b. 需结合原子半径数据分析共价键B-N和Si-C的键长大小
c. 键的极性的大小可用于比较结构相似的晶体的熔点
d. 信息中的“离子性较强”一句,说明氮化硼和碳化硅晶体中存在离子键
④ 立方氮化硼晶体的天然矿物在青藏高原地下约300 km的古地壳中被发现。根据这一矿物形成事
实,可推断实验室由六方氮化硼合成立方氮化硼需要的条件应是______。
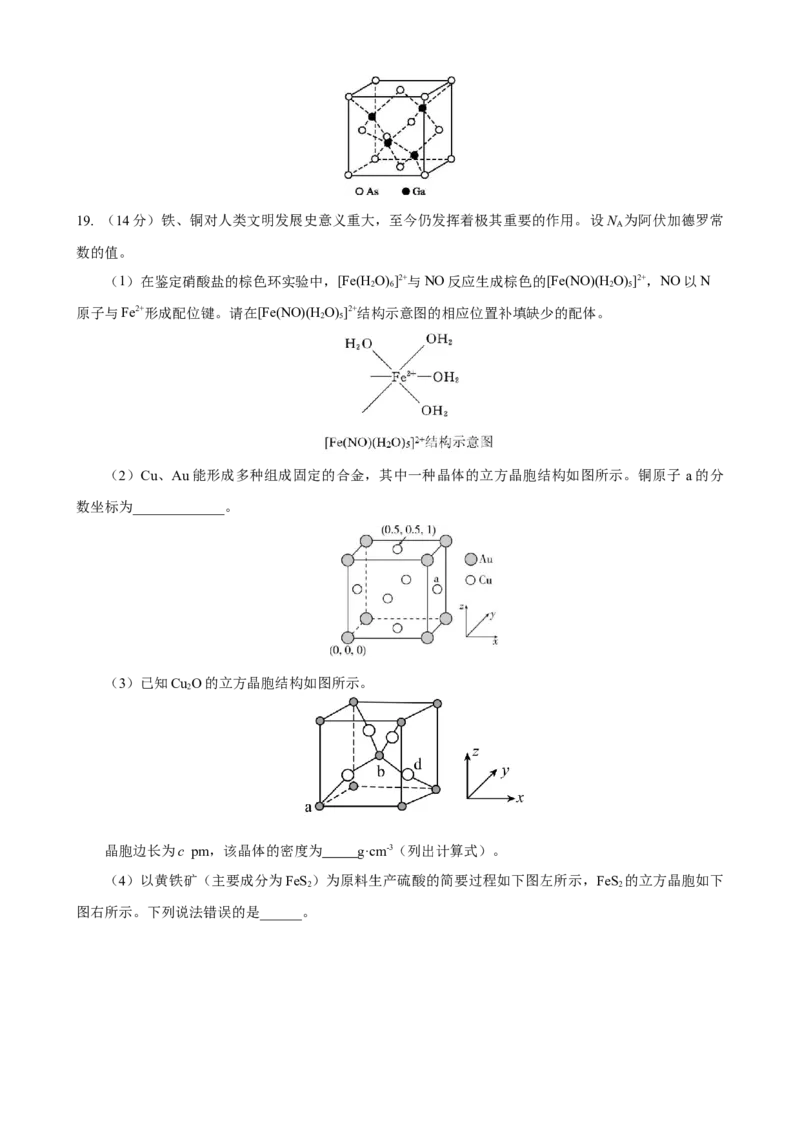
(3)GaAs的熔点为1 238 ℃,密度为ρ g·cm-3,其立方晶胞结构如图所示。Ga与As以______键键
合。Ga和As的摩尔质量分别为M g·mol-1和M g·mol-1,原子半径分别为r pm和r pm,阿伏加
Ga As Ga As
德罗常数值为N ,则GaAs晶胞中原子的体积占晶胞体积的百分率为______。
A19. (14分)铁、铜对人类文明发展史意义重大,至今仍发挥着极其重要的作用。设N 为阿伏加德罗常
A
数的值。
(1)在鉴定硝酸盐的棕色环实验中,[Fe(H O) ]2+与NO反应生成棕色的[Fe(NO)(H O) ]2+,NO以N
2 6 2 5
原子与Fe2+形成配位键。请在[Fe(NO)(H O) ]2+结构示意图的相应位置补填缺少的配体。
2 5
(2)Cu、Au能形成多种组成固定的合金,其中一种晶体的立方晶胞结构如图所示。铜原子 a的分
数坐标为_____________。
(3)已知Cu O的立方晶胞结构如图所示。
2
晶胞边长为c pm,该晶体的密度为 g·cm-3(列出计算式)。
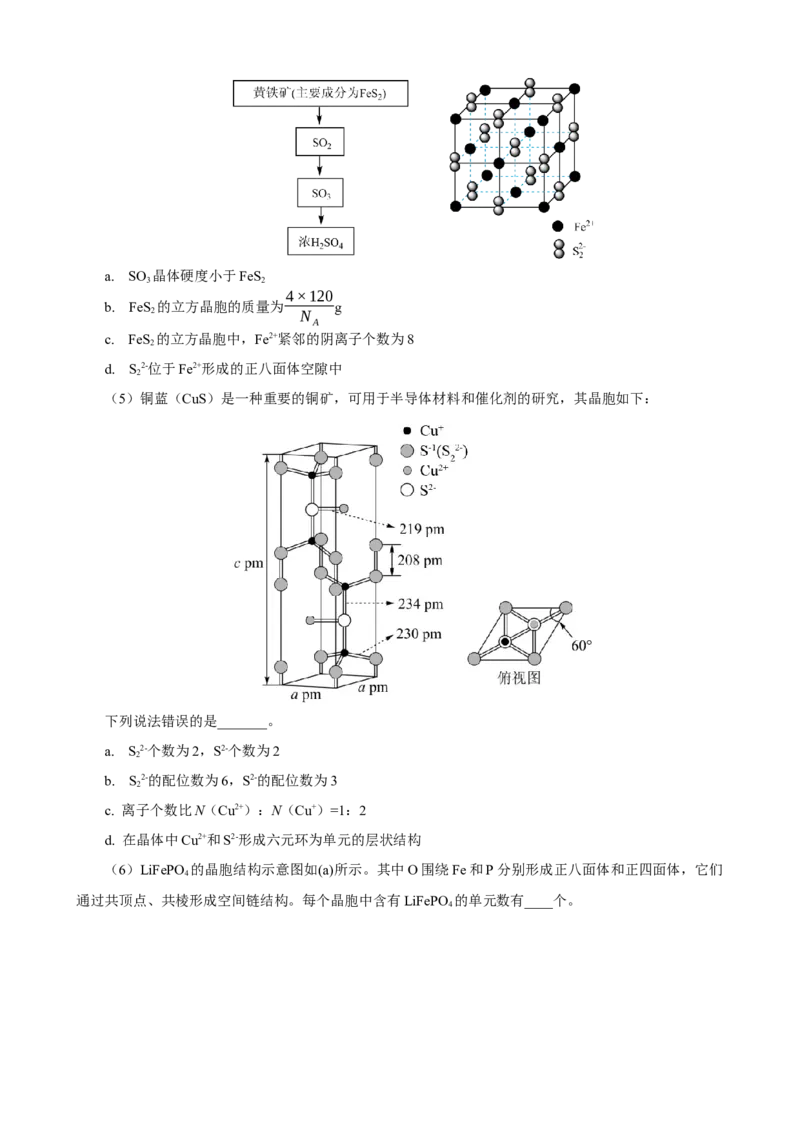
(4)以黄铁矿(主要成分为FeS )为原料生产硫酸的简要过程如下图左所示,FeS 的立方晶胞如下
2 2
图右所示。下列说法错误的是______。a. SO 晶体硬度小于FeS
3 2
4×120
b. FeS 的立方晶胞的质量为 g
2 N
A
c. FeS 的立方晶胞中,Fe2+紧邻的阴离子个数为8
2
d. S2-位于Fe2+形成的正八面体空隙中
2
(5)铜蓝(CuS)是一种重要的铜矿,可用于半导体材料和催化剂的研究,其晶胞如下:
下列说法错误的是_______。
a. S2-个数为2,S2-个数为2
2
b. S2-的配位数为6,S2-的配位数为3
2
c. 离子个数比N(Cu2+):N(Cu+)=1:2
d. 在晶体中Cu2+和S2-形成六元环为单元的层状结构
(6)LiFePO 的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们
4
通过共顶点、共棱形成空间链结构。每个晶胞中含有LiFePO 的单元数有____个。
4电池放电时,FePO 嵌入部分Li+,形成Li FePO ,结构示意图如(b)所示,则x=_____。充电过程中
4 1−x 4
n(Fe2+):n(Fe3+) _______(填“逐步增大”、“逐步减小”或“不变”)。参考答案及详解
1. 选A
详解:A项,冰分子间有氢键的作用,且氢键有方向性,所以比液态水密度小,冰开始融化时,冰
(水)分子间间距变小,密度增大,至4℃时,密度最大,随后,因热运动加剧,分子间距增大,而导致
密度变小,故A项正确;B项,冰中的水分子内部含有H-O共价键,B项错误;C项,接近水沸点的水蒸
气,由于氢键的作用,部分水分子形成缔合分子(H O) ,故“水分子”的相对分子质量变大,C项错误;
2 n
D项,向冰雪上撒盐,形成冰盐混合物,破坏了冰晶结构,熔点降低(一般说法为‘降低了冰点’,其
实这里的冰已经是混合物了),冰雪在温度较低时融化,D项错误。
2. 选C
详解:A项,在极光和雷电里,存在等离子体,它是物质的一种聚集状态,A项错误;B项,液晶是介于
液态和晶态之间的物质状态,不是晶体,B项错误;C项,纳米晶体是晶体颗粒尺寸在纳米量级的晶体,
由于晶体的表面积增大,在一定范围内,可能随晶粒变大熔点增大,故 C项正确;D项,非晶体的X射
线衍射图既没有分立的斑点,也没有明锐的衍射峰,D项错误。
3. 选C
详解:A项,铜为金属晶体,只含阳离子和自由电子,没有阴离子,A项错误;B项,聚醚醚酮链节中没
有手性碳原子,B项错误;C项,这个选项来自教科书,是熔融态结晶的一个具体且很有意义的例子,有
点像“拔丝地瓜”!故C项正确;D项,同系物必须是纯净物,而聚合物都为混合物,D项错误。
4. 选A
详解:A项,由于这两种晶体的阴离子半径较大,熔点比较低,熔化时破坏离子键,故 A项正确;B项,
干冰熔化破坏分子间作用力,氯化钠晶体熔化破坏离子键,B项错误;C项,氯化镁晶体熔化破坏离子键,
而氯化铝属于分子晶体,熔化时破坏分子间作用力,C项错误;D项,石墨属于混合型晶体,熔化时需要
破坏分子间作用力和共价键等,而晶体硫属于分子晶体,熔化时只破坏分子间作用力,D项错误。
5. 选D
详解:A项,同样来自教科书,是从溶液中结晶获取晶体的一个比较“高科技”的例子,要特别注意一
下这里面的“大”字,引导学生学习教科书93页关于“明矾晶体的制备”这一栏目,这其实是一个得到
较大而规整明矾晶粒的实验,A项正确;B项,碘蒸气的凝华可以得到晶体,B项正确;C项,饱和氯化
钠溶液(氯离子浓度小于浓盐酸)加入浓盐酸后,溶液氯离子浓度增大,抑制氯化钠溶解,C项正确;D
项,由于铁离子水解程度较大且加热后更大,极容易生成氢氧化铁,蒸干灼烧后得到氧化铁,故 D项错
误。
6. 选C
详解:A项,按现行人教版教科书,d区有30种元素,注意:不包括镧和锕,f区包括镧系元素和锕系元素各15种,A项正确;B项,对角线相似的几对元素,其主要性质还是符合本族元素的特征,只是有些
呈现对角线相似,B项正确;C项,p区元素种的惰性气体不属于非金属元素,故C项错误;门捷列夫除
了绘制出第一张现代周期表,他的贡献还包括根据周期性预测了预测了镓(Ga)、锗(Ge)和钪(Sc)
等的存在及性质,D项正确。
7. 选B
详解:A项,稀有气体元素难以失去电子,其第一电离能在同周期中最大,A项错误;B项,第二、三周
期内,比左右相邻元素的第一电离能都大的元素各有两种分别为 Be、N,Mg、P,故B项正确;C项,
每个短周期中,除稀有气体外,从左至右,原子半径减小,C项错误; D项,电负性最大的元素与电负
性最小的元素容易形成离子化合物,D项错误。
8. 选C
详解:A项,对羟基苯甲醛容易形成分子间氢键,故沸点高于易形成分子内氢键的邻羟基苯甲醛,A项错
误;B项,1-戊醇和乙醇虽然都能与水形成氢键,但后者的-OH与水中的-OH相似度更高,因而乙醇更易
溶于水,而戊醇的溶解度却不大,而且可以降低某些离子化合物在水中的溶解度,B项错误;C项,铬的
未成对电子数为6,锰的为5,故C项正确;D项,NaCl晶体和CsCl晶体的阳离子的配位数分别为6和
8,D项错误。
9. 选B
详解:A项,氧气转变为臭氧的过程没有发生氧化还原反应,A项错误;B项,中心氧原子形成3个sp2
杂化轨道,1个轨道容纳孤对电子,2个轨道与两旁的氧原子形成σ键,故B项正确;C项,键长越长,
一般键能越小,C项错误;D项,臭氧的中心氧原子受到两旁氧原子作用,带部分正电,两旁氧原子带部
分负电,故O-O键为极性键,整个分子也因为正负电中心不重合,而成为极性分子,D项错误。
10. 选C
详解:A项,张力(角张力)的概念学生可能比较陌生,如四面体理想键角为109º28′,小于这个角度
的键角会有比较大的张力,导致稳定性下降,同理,键角60º较p轨道间夹角小,也会比较“紧张”,稳
定性下降,A项正确;B项,由白磷转化为红磷放热,可判断出后者较稳定,B项正确;C项,基本单元
中的4个磷原子(采取sp3杂化)分别处于异面内的两个正三角形中,故 C项错误;D项,PO 是所谓五
4 10
氧化二磷的分子式,D项正确。
11. 选B
详解:A项,不同晶型的Al O 的物理性质不同,化学性质也有一定差异,A项错误;B项,固体电解质
2 3
中阳离子向正极(电势高)移动,故B项正确;C项,Al3+与O2-个数比应为2:3,C项错误;D项, 根
据人教版教科书,结合题意,α- Al O 应为过渡晶体,可看作共价晶体,D项错误。
2 3
12. 选C
详解:A项,面心立方晶胞的8个四面体空隙被氢原子占据,A项正确;B项,8个氢原子,每一个均结合4个氢原子,氢原子总数为40,而镧原子总数为4,B项正确; C项,氢原子处于镧原子形成的四面体
空隙中,所以氢原子配位数为4,故C项错误;D项,根据图示可知D项正确,晶胞参数的这种变化,也
证明了晶体中的微粒的振动性,神奇的是,LaH 吸氢后晶胞参数变小了!
2
13. 选D
详解:A项,配体CO中电负性较小的C提供孤对电子,C是配原子,A项错误;B项,根据[Ni(CN) ]2-
4
是平面正方形结构可知Ni位于4个配原子C形成的四方形的中心,由于CN-中碳原子采取sp杂化,离子
呈直线形,所以Ni、C、N处在同一直线上,B项错误;C项,NH 中氮原子的孤对电子对数为1 ,而六
3
氨合镍离子中氮原子与具有空轨道的镍离子形成配位键,孤对电子对数为 0,而孤电子对与成键电子对之
间的斥力较大,所以NH 的H−N−H键角较小,C项错误;D项,看似超纲,实则可以根据已知推得,4
3
个杂化轨道的sp3杂化既然是四面体结构,那么同样是形成4个杂化轨道的dsp2杂化就应该是四方形,正
八面体形的[Ni(NH )]2+由于中心离子需形成6个杂化轨道故必须有d轨道参与杂化,D项正确。
3 6
14. 选D
详解:A项,CO 晶胞属于密堆积,配位数为12,A项正确;B项正确;C项,CO 晶胞是面心立方,
2 2
CO 分子间最近距离为面对角线的一半,C项正确;D项,CO 分子有四种空间取向,会影响其部分物理
2 2
性质,而其热稳定性主要与键能有关,故D项错误。
15. 选C
详解: A项, 疏水作用指表面活性剂在水中会形成亲水基团向外、疏水基团(或称憎水基团)向内的
胶束,胶束是一种比较典型的超分子,胶束的形成也表现了超分子的自组装能力,A项,能表现;B项,
DNA的双螺旋结构的形成也是分子间通过氢键形成超分子的典型例子,B项,能表现;C项,淀粉与丙
烯酸钠在一定条件下反应生成以淀粉为主链的接枝共聚物,这是通过旧键断裂和新键形成而发生的化学
变化,化学变化不属于超分子的自组装范畴,故C项不能表现;D项,与A、B项类似,D项能表现。
16. (14分)
(1)a(1分)、b(1分)、d(1分)。
评分标准:1个1分,选C扣1分,扣完为止。
讲解说明:NF、NH、F 属于分子晶体,NHF属于离子晶体,Cu属于金属晶体。
3 3 2 4
(2)a(1分)、c(1分)、d(1分)。
评分标准:1个1分,选b、e、f中的任何一个,每选一个扣一分,扣完为止。
讲解说明:Q转化为R的过程中,破坏的微粒间的作用力有H-O极性共价键,O…H-O氢键以及
与HO之间的范德华力。
2
(3)GaF 为离子晶体,GaCl 为分子晶体,一般地说,离子晶体熔点较高(2分)。
3 3评分标准:答出GaF 为离子晶体为1分,答出GaCl 为分子晶体为1分,离子晶体熔点较高不采分。
3 3
讲解说明:GaF、GaCl 组成相似,离子晶体熔点较高,一般在接近1000 ℃或更高,分子晶体的熔点多在
3 3
几百度及以下。
(4)2(2分)。
讲解说明: NHBF 中NH+有1个配位键,BF-有1个配位键。
4 4 4 4
(5)CaF 中存在沉淀溶解平衡:CaF (s) Ca2+(aq)+2F-(aq),溶液中的F-与Al3+形成配离子AlF3-,使沉
2 2 6
淀溶解平衡向右移动,导致氟化钙溶解(2分)。
评分标准:方程式1分,答出形成AlF3-或溶解平衡右移均可得1分。
6
讲解说明:由题给信息可知:AlF3-较CaF 稳定,也可从稳定常数和溶度积常数分析。
6 2
(6)氟原子是电负性最强的元素,它的引入改变了冠醚分子的电子分布,增强了氧原子的孤对电子与
Li⁺之间的静电相互作用。Li⁺具有很高的电荷密度(半径小,电荷高),使其更容易与冠醚形成强静电相
互作用(2分)。
评分标准:答出(氟原子的引入)增强了氧原子对锂离子的静电作用得1分,答出锂离子半径小给1分。
讲解说明:氟原子电负性很大,增强了氧原子与锂离子的作用力,可以参考FCHCOOH酸性强于CHCOOH的
2 3
分析。
17. (15分)
(1)①3(1分)、2(1分);②12(1分)、4(1分)。
评分标准:按参考答案。
讲解说明:略
(2)分子(1分);12(1分);MC (1分)。
3 60
评分标准:按参考答案。
1
讲解说明:M原子12个位于棱心,1个位于体心,8个四面体空隙各1个,M原子数:12× +1+8=12;C
4 60
位于顶点和面心,共4个,所以化学式为MC 。
3 60
(3)Si4+(1分);1:4(1分)。
评分标准:按参考答案,第一问,写成Si不给分。
讲解说明:独立的硅氧四面体中Si:O=1:4。
(4)①[Si O]6-(1分)、1:3(1分);②Be Al [Si O ]或Al Be [Si O ](2分)。
2 7 3 2 6 18 2 3 6 18
评分标准:第一问不写[]也给分。②问如果将金属元素写在后面也可酌情给分
讲解说明:①根据Si的化合价为+4、O的化合价为-2,可求得离子的电荷数。②参考镁方柱石的化学式,
书写化学式时,可知活泼金属在前,较不活泼的金属写在后面,再根据D中硅氧原子个数可知硅原子数
为6,氧原子数为18,阴离子的电荷数为-12,据此书写化学式。
(5)NaV₂O₇(1分);NH VO (1分)。
4 4 3评分标准:按参考答案。阴离子用[]扩上,给分。
讲解说明:偏钒酸根离子可结合图示,每个单元中,有2个氧原子是钒原子独占(其中1个被遮盖)的,
另外还有2个氧原子需与另一单元分享,所以每个钒原子平均与3个氧原子结合,且偏钒酸根离子的电荷
数为-1,据此书写化学式。
18. (12分)
(1)4(1分)。
评分标准:按参考答案。
讲解说明:据图示信息可知。
(2)2(1分);BBr +NH =BN+3HBr(1分)。
3 3
评分标准:按参考答案。
讲解说明:略。
①bc(2分);
评分标准:按参考答案。
讲解说明:a项,立方氮化硼中无π键,硼原子2s上的1个电子激发后,采取sp3杂化与4个氮原子形
成4个σ键,氮原子则通过孤对电子和3个p电子与硼原子成键,二者的配位数均为4。a项错误。b项,
六方氮化硼类似石墨,层间靠分子间作用力连接,质地软。b项正确。c项,考虑到过渡晶体的概念,题
干中加了“主要”二字,保证了科学性,c项正确。d项,两种晶体均难溶于水,也不易溶于一般有机溶
剂。d项错误。
②平面正三角(1分)、层状结构的层内没有自由移动的电子(1分);
评分标准:平面正三角写成正三角或三角均给分;后一空答出“没有自由电子”即可给分。
讲解说明:虽然结构与石墨相似,但由于硼原子采取sp2杂化与氮原子成键后,没有价电子了,而氮原子
虽有孤对电子,但是由于氮元素电负性很大,很难与硼原子形成离域Π键,没有自由移动的p电子,导
致其导电性很差。
③a(1分);
评分标准:按参考答案。
讲解说明:a项,可参考(2)问的讲解知a项错误。b项,非金属原子半径属于共价半径,为单质双原子
分子共价键键长的一半,b项正确。c项,晶胞结构相似的共价晶体,共价键极性越大,一般熔点越高
(当然,这仅是初步判断),c项正确。d项,这里考查的是过渡晶体的概念,d项正确。
④高温高压(1分)。
评分标准:按参考答案。
讲解说明:结合信息可知。可结合教科书84页讲解。4π×10-30N ρ(r3 +r3 )
(3)共价(1分); A Ga As ×100%(2分)。
3(M +M )
Ga As
评分标准:第一问按参考答案,第二问酌情给分。
讲解说明:根据晶胞图示可知一个晶胞中含有4个As、4个Ga,晶胞中的原子的总体积为:
4
4× π(r3+r3)×10-30;晶胞的质量为:4×(M g·mol-1+M g·mol-1)÷Nmol-1、晶胞的体积为:
3 Ga As Ga As A
4×(M g·mol-1和M g·mol-1)÷(ρg·cm-3×Nmol-1)。
Ga As A
19. (14分)
(1) (2分)。
评分标准:必须将N、O朝向Fe2+;NO与HO的位置可互换。
2
讲解说明:配体为分子或复杂离子时,一般电负性小的原子作配原子,且配原子需与中心离子相连。
(2)(1,0.5,0.5)(2分)。
评分标准:写成分数给分。酌情给分。
讲解说明:略。
(3) (2分)。
评分标准:酌情给分。
讲解说明:晶胞中4个铜原子、2个氧原子,晶胞质量为:(4×64g·mol-1+2×16g·mol-1)÷Nmol-1,
A
晶胞的体积为c3×10-30cm3。
(4)c(2分)。
评分标准:按参考答案。
讲解说明:a项,SO 晶体为分子晶体,硬度小于离子晶体FeS,a项正确。b项,晶胞中含4个Fe2+、4个
3 2
4×120
S2-,FeS 的摩尔质量为120 g•mol-1,一个晶胞的质量为 g b项正确。c项,FeS 晶胞与氯化钠晶
2 2 N 2
A
胞相似,与Fe2+紧邻的阴离子个数为6,c项错误。d项,S2-位于Fe2+形成的正八面体空隙中,d项正确。
2
(5)b(2分)。
评分标准:按参考答案。
讲解说明:a项,晶胞中每个立棱上有一个S2-,每个顶点有半个S2-,一共有4个棱边,每个棱边分摊
2 2
1/4,所以S2-个数为(1+1/2+1/2×4×1/4=2,晶胞的体心含有两个S2-,所以S2-个数为2,a项正确。b项,
2
S2-中每个S被3个Cu+所共用,所以S2-的配位数为6。S2-与3个Cu2+(此4个原子形成的平面内,见c项
2 2分析)和2个Cu+(上下)紧邻,配位数为5。b项错误。c项,由图可知,晶胞中有2个Cu2+、4个Cu+,
故N(Cu2+):N(Cu+)=1:2,c项正确。d项,每个Cu2+处于3个S2-所形成的正三角形中心,每个S2-也
处于3个Cu2+所形成的正三角形中心,Cu2+与S2-形成类似石墨的以六元环为单元的片层结构,d项正确。
(6)4(2分) 3/16 (1分)逐步减小(1分)。
评分标准:按参考答案。
讲解说明:第一个空:由图(a)知,晶胞中由4个八面体和4个四面体,4个锂离子,故有4个LiFePO
4
单元。第二个空:由图(b)知,Li的个数为8×1/8+3×1/4+3×1/2=13/4,Fe个数为4,Li与Fe的个
数比为13:16,则1-x=13/16,x=3/16。第三个空:充电过程中锂原子逐步减少,而阳离子总电荷数保
持不变,所以Fe3+比例逐步增大,n(Fe2+):n(Fe3+)应逐步减小。