文档内容
1.轴烯是一类独特的星形环烃。三元轴烯( )与苯
A.均为芳香烃 B.互为同素异形体
C.互为同系物 D.互为同分异构体
2.下列化工生产过程中,未涉及氧化还原反应的是
A.海带提碘 B.氯碱工业
C.氨碱法制碱 D.海水提溴
3.硼的最高价含氧酸的化学式不可能是
A.HBO B.H BO C.H BO D.H B O
2 2 3 3 3 2 4 7
4.下列各组物质的熔点均与所含化学键的键能有关的是
A.CaO与CO B.NaCl与HCl C.SiC与SiO D.Cl 与I
2 2 2 2
5.烷烃 的命名正确的是
A.4-甲基-3-丙基戊烷 B.3-异丙基己烷
C.2-甲基-3-丙基戊烷 D.2-甲基-3-乙基己烷
二、选择题(本题共36分,每小题3分,每题只有一个正确选项)
6.能证明乙酸是弱酸的实验事实是
A.CH COOH溶液与Zn反应放出H
3 2
B.0.1 mol/L CH COONa溶液的pH大于7
3
C.CH COOH溶液与NaCO 反应生成CO
3 3 2
D.0.1 mol/L CH COOH溶液可使紫色石蕊变红
3
7.已知W、X、Y、Z为短周期元素,原子序数依次增大。W、Z同主族,X、Y、Z同周期,其中只有X
为金属元素。下列说法一定正确的是
A.原子半径:X>Y>Z>W
B.W的含氧酸的酸性比Z的含氧酸的酸性强
C.W的气态氢化物的稳定性小于Y的气态氢化物的稳定性
第1页 | 共9页D.若W与X原子序数差为5,则形成化合物的化学式为X W
3 2
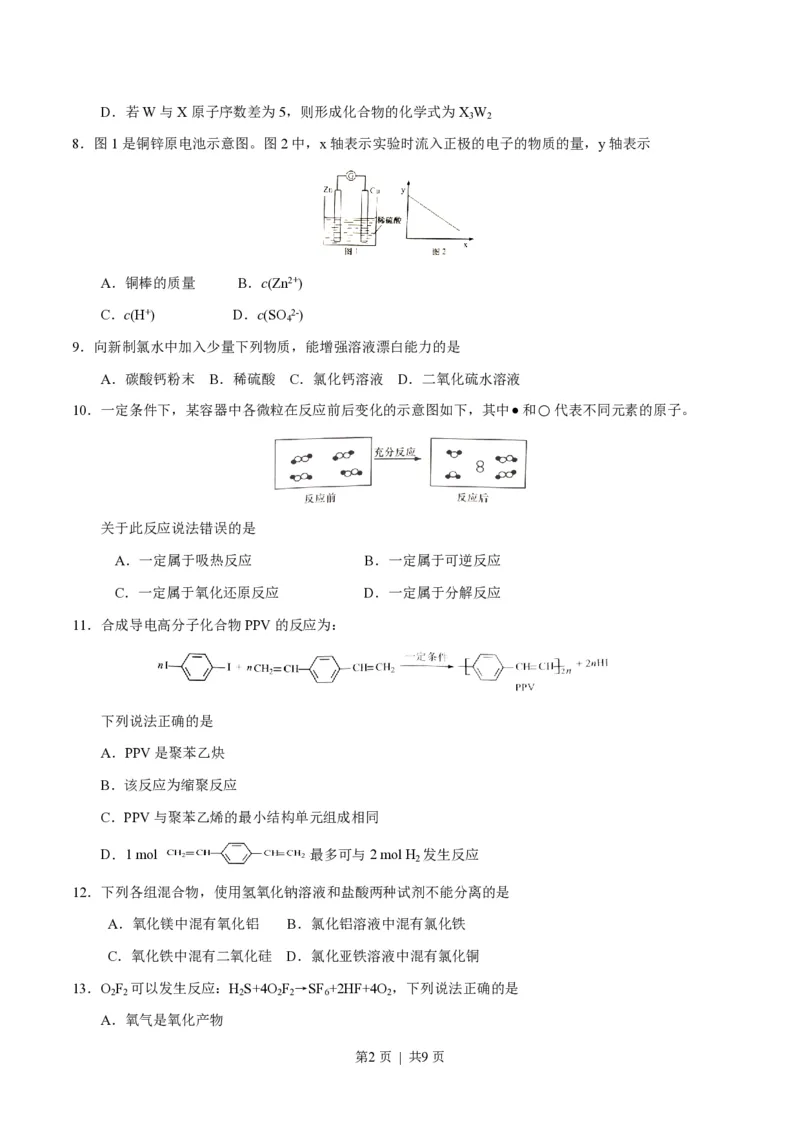
8.图1是铜锌原电池示意图。图2中,x轴表示实验时流入正极的电子的物质的量,y轴表示
A.铜棒的质量 B.c(Zn2+)
C.c(H+) D.c(SO 2-)
4
9.向新制氯水中加入少量下列物质,能增强溶液漂白能力的是
A.碳酸钙粉末 B.稀硫酸 C.氯化钙溶液 D.二氧化硫水溶液
10.一定条件下,某容器中各微粒在反应前后变化的示意图如下,其中·和 代表不同元素的原子。
d
关于此反应说法错误的是
A.一定属于吸热反应 B.一定属于可逆反应
C.一定属于氧化还原反应 D.一定属于分解反应
11.合成导电高分子化合物PPV的反应为:
下列说法正确的是
A.PPV是聚苯乙炔
B.该反应为缩聚反应
C.PPV与聚苯乙烯的最小结构单元组成相同
D.1 mol 最多可与2 mol H 发生反应
2
12.下列各组混合物,使用氢氧化钠溶液和盐酸两种试剂不能分离的是
A.氧化镁中混有氧化铝 B.氯化铝溶液中混有氯化铁
C.氧化铁中混有二氧化硅 D.氯化亚铁溶液中混有氯化铜
13.O F 可以发生反应:H S+4O F →SF +2HF+4O ,下列说法正确的是
2 2 2 2 2 6 2
A.氧气是氧化产物
第2页 | 共9页B.O F 既是氧化剂又是还原剂
2 2
C.若生成4.48 L HF,则转移0.8 mol电子
D.还原剂与氧化剂的物质的量之比为1:4
14.在硫酸工业生产中,为了有利于SO 的转化,且能充分利用热能,采用了中间有热交换器的接触室(见
2
下图)。下列说法错误的是
A.a、b两处的混合气体成分含量相同,温度不同
B.c、d两处的混合气体成分含量相同,温度不同
C.热交换器的作用是预热待反应的气体,冷却反应后的气体
D.c处气体经热交换后再次催化氧化的目的是提高SO 的转化率
2
15.下列气体的制备和性质实验中,由现象得出的结论错误的是
选项 试剂 试纸或试液 现象 结论
A 浓氨水、生石灰 红色石蕊试纸 变蓝 NH 为碱性气体
3
HCl为酸性气体
[来
B 浓盐酸、浓硫酸 pH试纸 变红
源:学|科|网]
C 浓盐酸、二氧化锰 淀粉碘化钾试液 变蓝 Cl 具有氧化性
2
D 亚硫酸钠、硫酸 品红试液 褪色 SO 具有还原性
2
16.实验室提纯含少量氯化钠杂质的硝酸钾的过程如右图所示。
下列分析正确的是
A.操作Ⅰ是过滤,将固体分离除去
B.操作Ⅱ是加热浓缩,趁热过滤,除去杂质氯化钠
C.操作Ⅲ是过滤、洗涤,将硝酸钾晶体从溶液中分离出来
D.操作Ⅰ~Ⅲ总共需两次过滤
17.某铁的氧化物(Fe O)1.52 g溶于足量盐酸中,向所得溶液中通入标准状况下112 ml Cl ,恰好将Fe2+
x 2
完全氧化。x值为
第3页 | 共9页A.0.80 B.0.85 C.0.90 D.0.93
三、选择题(本题共20分,每小题4分,每小题有一个或两个正确选项。只有一个正确选项的,多选不给
分;有两个正确选项的,选对一个给2分,选错一个,该小题不给分)
18.一定条件下,一种反应物过量,另一种反应物仍不能完全反应的是
A.过量的氢气与氮气 B.过量的浓盐酸与二氧化锰
C.过量的铜与浓硫酸 D.过量的锌与18 mol/L硫酸
19.已知:SO 2-+I +H O→SO 2-+2I-+2H+。某溶液中可能含有Na+、NH +、Fe2+、K+、I−、SO 2- 、SO 2−,
3 2 2 4 4 3 4
且所有离子物质的量浓度相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判
断正确的是
A.肯定不含I− B.肯定不含SO 2−
4
C.肯定含有SO 2− D.肯定含有NH +
3 4
20.已知NaOH+Al(OH) →Na[Al(OH) ]。向集满CO 的铝制易拉罐中加入过量NaOH浓溶液,立即封闭罐
3 4 2
口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。上述实验过程中没有发生的离子反应是
A.CO +2OH−→CO 2−+H O B.Al O +2OH−+3H O→2[Al(OH) ] −
2 3 2 2 3 2 4
C.2 Al+2OH−+6H O→2 [Al(OH) ] −+3H ↑ D.Al3++4 OH−→[Al(OH) ]−
2 4 2 4
21.类比推理是化学中常用的思维方法。下列推理正确的是
[来源:Zxxk.Com]
A.CO 是直线型分子,推测CS 也是直线型分子
2 2
B.SiH 的沸点高于CH ,推测H Se的沸点高于H S
4 4 2 2
C.Fe与Cl 反应生成FeCl ,推测Fe与I 反应生成FeI
2 3 2 3
D.NaCl与浓H SO 加热可制HCl,推测NaBr与浓H SO 加热可制HBr
2 4 2 4
22.称取(NH ) SO 和NH HSO 混合物样品7.24 g,加入含0.1 mol NaOH的溶液,完全反应,生成NH 1792
4 2 4 4 4 3
mL(标准状况),则(NH ) SO 和NH HSO 的物质的量比为
4 2 4 4 4
A.1:1 B.1:2 C.1.87:1 D.3.65:1
四、(本题共12分)
NaCN超标的电镀废水可用两段氧化法处理:
(1)NaCN与NaClO反应,生成NaOCN和NaCl
(2)NaOCN与NaClO反应,生成Na CO 、CO 、NaCl和N
2 3 2 2
已知HCN(K=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。
i
完成下列填空:
第4页 | 共9页23.第一次氧化时,溶液的pH应调节为____________(选填“酸性”、“碱性”或“中性”);原因是
______________________。
24.写出第二次氧化时发生反应的离子方程式。
_______________________________________
25.处理100 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO___g(实际用量应为理论值的4倍),
才能使NaCN含量低于0.5 mg/L,达到排放标准。
26.(CN) 与Cl 的化学性质相似。(CN) 与NaOH溶液反应生成_________、__________和H O。
2 2 2 2
27.上述反应涉及到的元素中,氯原子核外电子能量最高的电子亚层是___________;H、C、N、O、
Na的原子半径从小到大的顺序为_______。
五、(本题共12分)
随着科学技术的发展和环保要求的不断提高,CO 的捕集利用技术成为研究的重点。
2
完成下列填空:
29.目前国际空间站处理CO 的一个重要方法是将CO 还原,所涉及的反应方程式为:
2 2
CO (g)+4H (g) CH (g)+2H O(g)
2 2 4 2
已知H 的体积分数随温度升高而增加。
2
若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化。(选填“增大”、“减小”或“不
变”)
v v 平衡常数K 转化率α
正 逆
30.相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
[来源:学科网]
[CO ]/mol·L-1 [H ]/mol·L-1 [CH ]/mol·L-1 [H O]/mol·L-1
2 2 4 2
平衡Ⅰ a b c d
平衡Ⅱ m n x y
a、b、c、d与m、n、x、y之间的关系式为_________。
31.碳酸:H CO ,K =4.3×10-7,K =5.6×10-11
2 3 i1 i2
草酸:H C O ,K =5.9×10-2,K =6.4×10-5
2 2 4 i1 i2
0.1 mol/L Na CO 溶液的pH____________0.1 mol/L Na C O 溶液的pH。(选填“大于”、“小于”或“等于”)
2 3 2 2 4
等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是___________。
若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是_____。(选填
第5页 | 共9页编号)
a.[H+]>[HC O -]>[HCO -]>[CO 2-] b.[HCO -]>[HC O -]>[C O 2-]>[CO 2-]
2 4 3 3 3 2 4 2 4 3
c.[H+]>[HC O -]>[C O 2-]>[CO 2-] d.[H CO ] >[HCO -]>[HC O -]>[CO 2-]
2 4 2 4 3 2 3 3 2 4 3
32.人体血液中的碳酸和碳酸氢盐存在平衡:H++ HCO - H CO ,当有少量酸性或碱性物质进入血液
3 2 3
中时,血液的pH变化不大,用平衡移动原理解释上述现象。
____________________________________________________________________________________
六、(本题共12分)
乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用a装置来制备。
完成下列填空:
33.实验时,通常加入过量的乙醇,原因是______________。加入数滴浓硫酸即能起催化作用,但实际用
量多于此量,原因是_______________;浓硫酸用量又不能过多,原因是____________。
34.饱和Na CO 溶液的作用是___________、_____________、_____________。
2 3
35.反应结束后,将试管中收集到的产品倒入分液漏斗中,_________、________,然后分液。
36.若用b装置制备乙酸乙酯,其缺点有__________、__________。由b装置制得的乙酸乙酯粗产品经饱
和碳酸钠溶液和饱和食盐水洗涤后,还可能含有的有机杂质是________,分离乙酸乙酯与该杂质的方
法是_______________。
七、(本题共12分)
半水煤气是工业合成氨的原料气,其主要成分是H 、CO、CO 、N 和H O(g)。半水煤气经过下列步
2 2 2 2
骤转化为合成氨的原料。
完成下列填空:
第6页 | 共9页37.半水煤气含有少量硫化氢。将半水煤气样品通入____溶液中(填写试剂名称),出现_______,可以证
明有硫化氢存在。
38.半水煤气在铜催化下实现CO变换:CO+H O CO +H
2 2 2
若半水煤气中V(H ):V(CO):V(N )=38:28:22,经CO变换后的气体中:V(H ):V(N )=____________。
2 2 2 2
39.碱液吸收法是脱除二氧化碳的方法之一。已知:
Na CO K CO
2 3 2 3
20℃碱液最高浓度(mol/L) 2.0 8.0
碱的价格(元/kg) 1.25 9.80
若选择Na CO 碱液作吸收液,其优点是__________;缺点是____________。如果选择K CO 碱液作吸收液,
2 3 2 3
用什么方法可以降低成本?
___________________________________________
[来源:Z,xx,k.Com]
写出这种方法涉及的化学反应方程式。_______________________
[来源:Z。xx。k.Com]
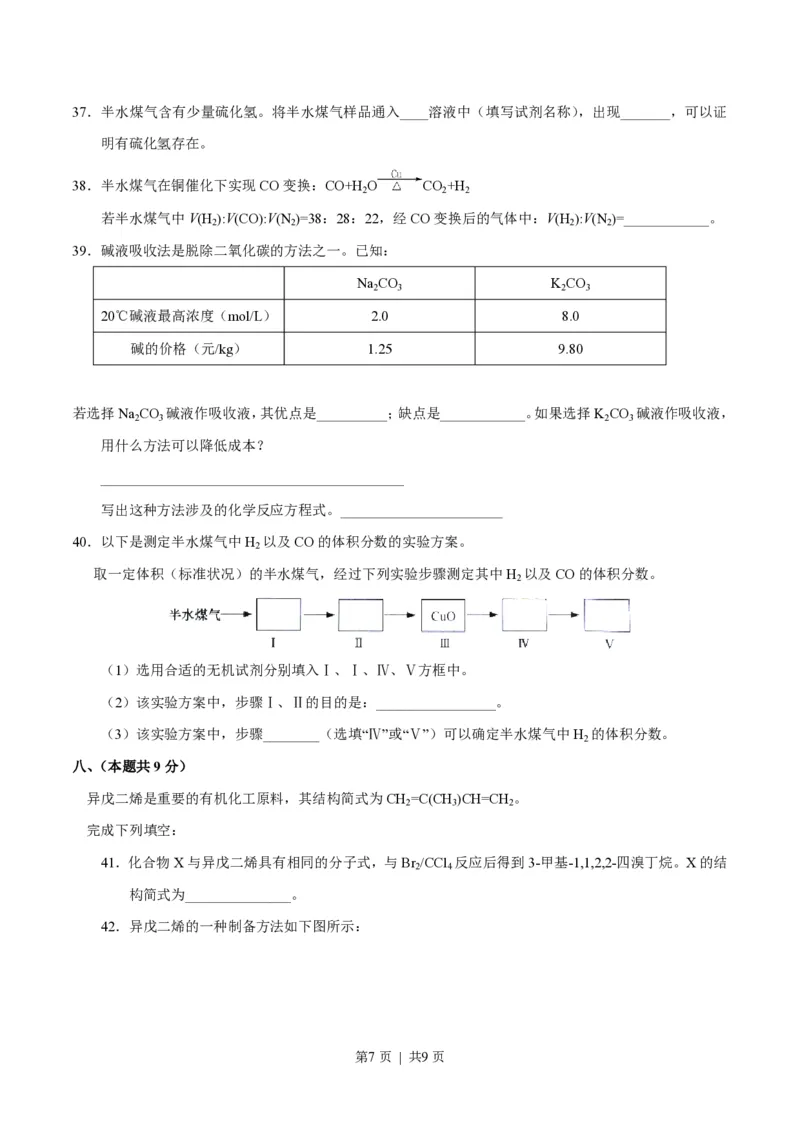
40.以下是测定半水煤气中H 以及CO的体积分数的实验方案。
2
取一定体积(标准状况)的半水煤气,经过下列实验步骤测定其中H 以及CO的体积分数。
2
(1)选用合适的无机试剂分别填入Ⅰ、Ⅰ、Ⅳ、Ⅴ方框中。
(2)该实验方案中,步骤Ⅰ、Ⅱ的目的是:_________________。
(3)该实验方案中,步骤________(选填“Ⅳ”或“Ⅴ”)可以确定半水煤气中H 的体积分数。
2
八、(本题共9分)
异戊二烯是重要的有机化工原料,其结构简式为CH =C(CH )CH=CH 。
2 3 2
完成下列填空:
41.化合物X与异戊二烯具有相同的分子式,与Br /CCl 反应后得到3-甲基-1,1,2,2-四溴丁烷。X的结
2 4
构简式为_______________。
42.异戊二烯的一种制备方法如下图所示:
第7页 | 共9页A能发生的反应有___________。(填反应类型)
B的结构简式为______________。
43.设计一条由异戊二烯制得有机合成中间体 的合成路线。
(合成路线常用的表示方式为: )
九、(本题共13分)
M是聚合物胶黏剂、涂料等的单体,其一条合成路线如下(部分试剂及反应条件省略):
完成下列填空:
44.反应①的反应类型是____________。反应④的反应条件是_____________。
45.除催化氧化法外,由A得到 所需试剂为___________。
46.已知B能发生银镜反应。由反应②、反应③说明:在该条件下,_______________。
47.写出结构简式。C________________ M________________
48.D与1-丁醇反应的产物与氯乙烯共聚可提高聚合物性能,写出该共聚物的结构简式。_____________
49.写出一种满足下列条件的丁醛的同分异构体的结构简式。____________
①不含羰基 ②含有3种不同化学环境的氢原子
已知:双键碳上连有羟基的结构不稳定。
十、(本题共14分)
CO 是重要的化工原料,也是应用广泛的化工产品。CO 与过氧化钠或超氧化钾反应可产生氧气。
2 2
完成下列计算:
50.CO 通入氨水生成NH HCO ,NH HCO 很容易分解。2.00 mol NH HCO 完全分解,分解产物经干燥
2 4 3 4 3 4 3
后的体积为_________L(标准状况)。
第8页 | 共9页51. 某H 中含有2.40 mol CO ,该混合气体通入2.00 L NaOH溶液中,CO 被完全吸收。如果NaOH完全
2 2 2
反应,该NaOH溶液的浓度为_______。
52.CO 和KO 有下列反应:
2 2
4KO +2CO →2K CO +3O
2 2 2 3 2
4KO +4CO +2H O→4KHCO +3O
2 2 2 3 2
若9 mol CO 在密封舱内和KO 反应后生成9 mol O ,则反应前密封舱内H O的量应该是多少?列式计
2 2 2 2
算。
53.甲烷和水蒸气反应的产物是合成甲醇的原料:CH +H O CO+3H
4 2 2
已知:CO+2H CH OH CO +3H CH OH+H O
2 3 2 2 3 2
300 mol CH 完全反应后的产物中,加入100 mol CO 后合成甲醇。若获得甲醇350 mol,残留氢气120
4 2
mol,计算CO 的转化率。
2
第9页 | 共9页