文档内容
第三篇 化学反应与能量
专项 21 燃料电池
燃料电池是一种把燃料所具有的化学能直接转换成电能的化学装置,又称电化学发电器。它是继水力
发电、热能发电和原子能发电之后的第四种发电技术。由于燃料电池是通过电化学反应把燃料的化学能直
接转换成电能,能量转化效率高,燃料和空气分别送进燃料电池,它直接将燃料的化学能转化为电能,中
间不经过燃烧过程,同时没有机械传动部件,故排放出的有害气体极少,使用寿命长。从节约能源和保护
生态环境的角度来看,燃料电池是最有发展前途的发电技术。常见的燃料电池有氢氧燃料电池、甲烷燃料
电池、甲醇燃料电池等。燃料电池的正极反应物一般为氧气。电解质不同,电极反应就不同。
1.氢氧燃料电池是目前最成熟的燃料电池,可分为酸性和碱性两种。
种类 酸性 碱性
负极反应式 2H-4e-===4H+ 2H+4OH--4e-===4H O
2 2 2
正极反应式 O+4e-+4H+===2H O O+2HO+4e-===4OH-
2 2 2 2
电池总反应式 2H+O===2H O
2 2 2
备注 燃料电池的电极不参与反应,有很强的催化活性,起导电作用
2.燃料电池常用的燃料
H、CO、烃(如CH、C H)、醇(如CHOH)、肼(N H)等。
2 4 2 6 3 2 4
3.燃料电池常用的电解质
①酸性电解质溶液,如HSO 溶液;②碱性电解质溶液,如NaOH溶液;③熔融氧化物;④熔融碳酸
2 4
盐,如KCO;⑤质子交换膜等。
2 3
1.(2022•海南省选择性考试)一种采用HO(g)和N(g)为原料制备NH (g)的装置示意图如下。
2 2 3下列有关说法正确的是( )
A.在b电极上,N 被还原
2
B.金属Ag可作为a电极的材料
C.改变工作电源电压,反应速率不变
D.电解过程中,固体氧化物电解质中O2-不断减少
【答案】A
【解析】由装置可知,b电极的N 转化为NH ,N元素的化合价降低,得到电子发生还原反应,因此
2 3
b为阴极,电极反应式为N+3H O+6e-=2NH+3O2-,a为阳极,电极反应式为2O2-+4e-=O 。A项,由分析可
2 2 3 2
得,b电极上N 转化为NH ,N元素的化合价降低,得到电子发生还原反应,即N 被还原,A正确;B项,
2 3 2
a为阳极,若金属Ag作a的电极材料,则金属Ag优先失去电子,B错误;C项,改变工作电源的电压,
反应速率会加快,C错误;D项,电解过程中,阴极电极反应式为N+3H O+6e-=2NH+3O2-,阳极电极反
2 2 3
应式为2O2-+4e-=O ,因此固体氧化物电解质中O2-不会改变,D错误;故选A。
2
2.(2021•山东卷)以KOH溶液为离子导体,分别组成CHOH—O、NH—O、(CH)NNH—O 清洁
3 2 2 4 2 3 2 2 2
燃料电池,下列说法正确的是( )
A.放电过程中,K+均向负极移动
B.放电过程中,KOH物质的量均减小
C.消耗等质量燃料,(CH)NNH—O 燃料电池的理论放电量最大
3 2 2 2
D.消耗1molO 时,理论上NH—O 燃料电池气体产物的体积在标准状况下为11.2L
2 2 4 2
【答案】C
【解析】碱性环境下,甲醇燃料电池总反应为:2CHOH+3O +4KOH=2K CO+6H O;NH-O 清洁燃
3 2 2 3 2 2 4 2
料电池总反应为:NH+O =N +2H O;偏二甲肼[(CH )NNH]中C和N的化合价均为-2价,H元素化合价
2 4 2 2 2 3 2 2
为+1价,所以根据氧化还原反应原理可推知其燃料电池的总反应为:
(CH)NNH+4O +4KOH=2K CO+N +6H O。A项,放电过程为原电池工作原理,所以钾离子均向正极移动,
3 2 2 2 2 3 2 2
A错误;B项,根据上述分析可知,NH-O 清洁燃料电池的产物为氮气和水,其总反应中未消耗KOH,
2 4 2所以KOH的物质的量不变,其他两种燃料电池根据总反应可知,KOH的物质的量减小,B错误;C项,
理论放电量与燃料的物质的量和转移电子数有关,设消耗燃料的质量均为mg,则甲醇、NH 和
2 4
(CH)NNH 放电量(物质的量表达式)分别是: 、 、 ,通过比较可
3 2 2
知(CH)NNH 理论放电量最大,C正确;D项,根据转移电子数守恒和总反应式可知,消耗1molO 生成的
3 2 2 2
氮气的物质的量为1mol,在标准状况下为22.4L,D错误;故选C。
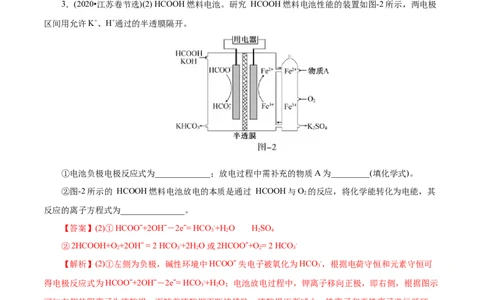
3.(2020•江苏卷节选)(2) HCOOH燃料电池。研究 HCOOH燃料电池性能的装置如图-2所示,两电极
区间用允许K+、H+通过的半透膜隔开。
①电池负极电极反应式为_____________;放电过程中需补充的物质A为_________(填化学式)。
②图-2所示的 HCOOH燃料电池放电的本质是通过 HCOOH与O 的反应,将化学能转化为电能,其
2
反应的离子方程式为_______________。
【答案】(2)①HCOOˉ+2OHˉ-2eˉ= HCO -+H O H SO
3 2 2 4
②2HCOOH+O +2OHˉ = 2 HCO -+2H O或2HCOOˉ+O = 2 HCO-
2 3 2 2 3
【解析】(2)①左侧为负极,碱性环境中HCOOˉ失电子被氧化为HCO -,根据电荷守恒和元素守恒可
3
得电极反应式为HCOOˉ+2OHˉ-2eˉ= HCO -+H O;电池放电过程中,钾离子移向正极,即右侧,根据图示
3 2
可知右侧的阴离子为硫酸根,而随着硫酸钾不断被排除,硫酸根逐渐减少,铁离子和亚铁离子进行循环,
所以需要补充硫酸根,为增强氧气的氧化性,溶液最好显酸性,则物质A为HSO ;②根据装置图可知电
2 4
池放电的本质是HCOOH在碱性环境中被氧气氧化为HCO -,根据电子守恒和电荷守恒可得离子方程式为
3
2HCOOH+O +2OHˉ = 2 HCO -+2H O或2HCOOˉ+O = 2 HCO-。
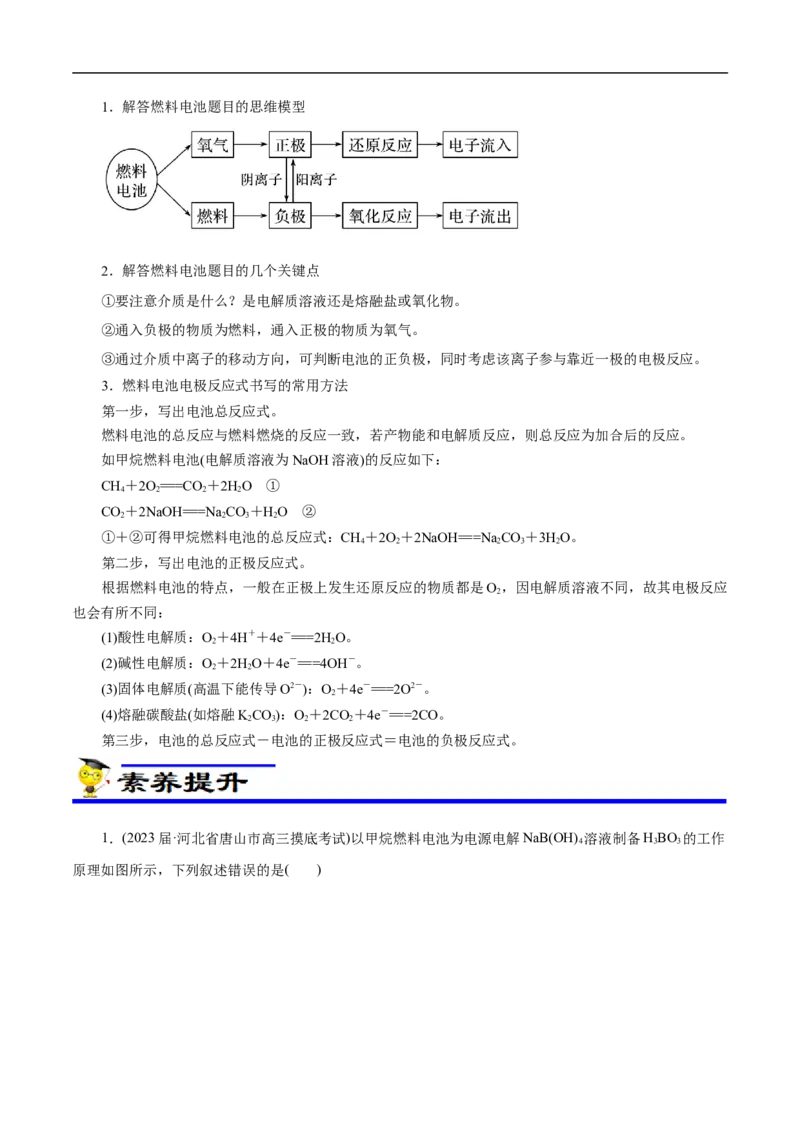
2 3 2 2 31.解答燃料电池题目的思维模型
2.解答燃料电池题目的几个关键点
①要注意介质是什么?是电解质溶液还是熔融盐或氧化物。
②通入负极的物质为燃料,通入正极的物质为氧气。
③通过介质中离子的移动方向,可判断电池的正负极,同时考虑该离子参与靠近一极的电极反应。
3.燃料电池电极反应式书写的常用方法
第一步,写出电池总反应式。
燃料电池的总反应与燃料燃烧的反应一致,若产物能和电解质反应,则总反应为加合后的反应。
如甲烷燃料电池(电解质溶液为NaOH溶液)的反应如下:
CH+2O===CO +2HO ①
4 2 2 2
CO+2NaOH===Na CO+HO ②
2 2 3 2
①+②可得甲烷燃料电池的总反应式:CH+2O+2NaOH===Na CO+3HO。
4 2 2 3 2
第二步,写出电池的正极反应式。
根据燃料电池的特点,一般在正极上发生还原反应的物质都是O ,因电解质溶液不同,故其电极反应
2
也会有所不同:
(1)酸性电解质:O+4H++4e-===2H O。
2 2
(2)碱性电解质:O+2HO+4e-===4OH-。
2 2
(3)固体电解质(高温下能传导O2-):O+4e-===2O2-。
2
(4)熔融碳酸盐(如熔融KCO):O+2CO+4e-===2CO。
2 3 2 2
第三步,电池的总反应式-电池的正极反应式=电池的负极反应式。
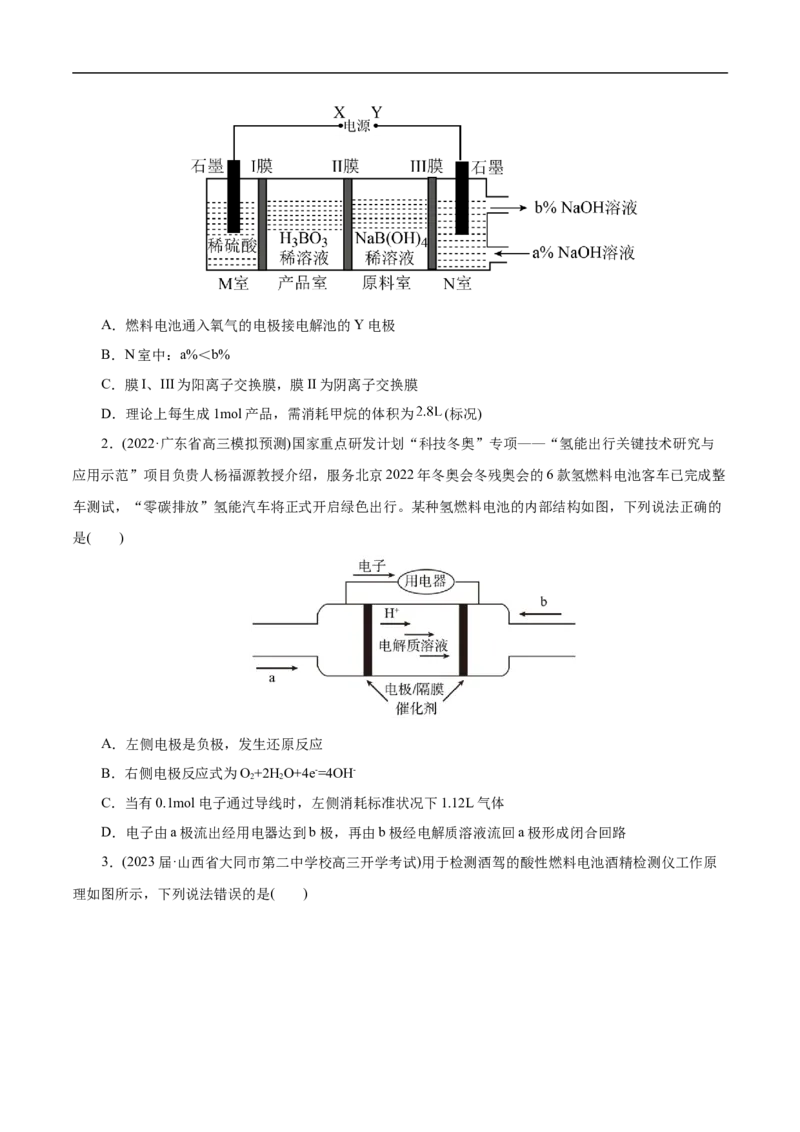
1.(2023届·河北省唐山市高三摸底考试)以甲烷燃料电池为电源电解NaB(OH) 溶液制备HBO 的工作
4 3 3
原理如图所示,下列叙述错误的是( )A.燃料电池通入氧气的电极接电解池的Y电极
B.N室中:a%<b%
C.膜I、III为阳离子交换膜,膜II为阴离子交换膜
D.理论上每生成1mol产品,需消耗甲烷的体积为 (标况)
2.(2022·广东省高三模拟预测)国家重点研发计划“科技冬奥”专项——“氢能出行关键技术研究与
应用示范”项目负贵人杨福源教授介绍,服务北京2022年冬奥会冬残奥会的6款氢燃料电池客车已完成整
车测试,“零碳排放”氢能汽车将正式开启绿色出行。某种氢燃料电池的内部结构如图,下列说法正确的
是( )
A.左侧电极是负极,发生还原反应
B.右侧电极反应式为O+2H O+4e-=4OH-
2 2
C.当有0.1mol电子通过导线时,左侧消耗标准状况下1.12L气体
D.电子由a极流出经用电器达到b极,再由b极经电解质溶液流回a极形成闭合回路
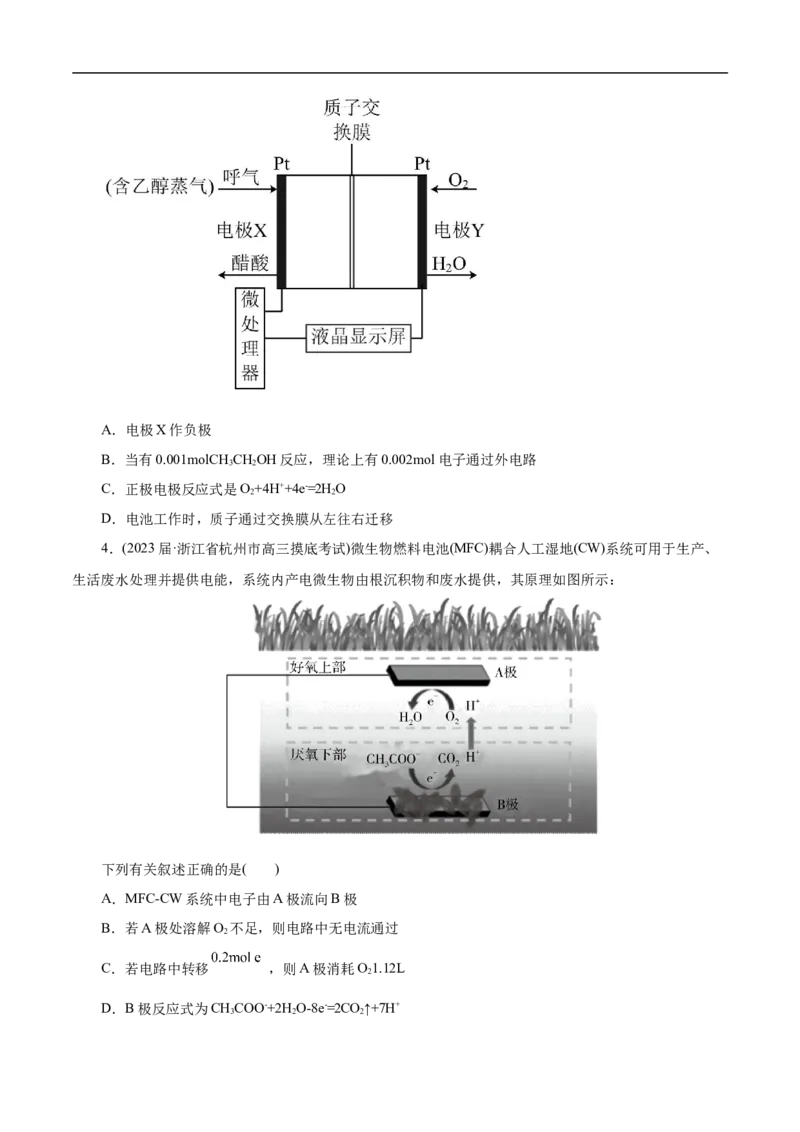
3.(2023届·山西省大同市第二中学校高三开学考试)用于检测酒驾的酸性燃料电池酒精检测仪工作原
理如图所示,下列说法错误的是( )A.电极X作负极
B.当有0.001molCHCHOH反应,理论上有0.002mol电子通过外电路
3 2
C.正极电极反应式是O+4H++4e-=2H O
2 2
D.电池工作时,质子通过交换膜从左往右迁移
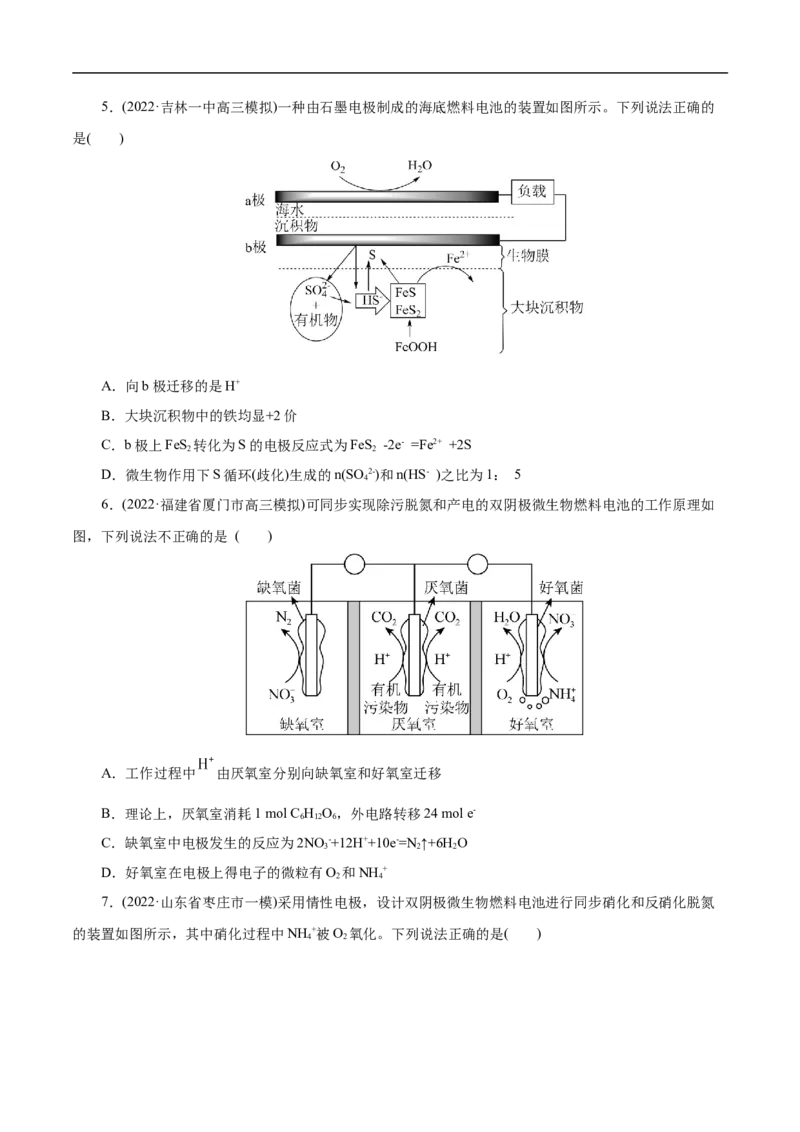
4.(2023届·浙江省杭州市高三摸底考试)微生物燃料电池(MFC)耦合人工湿地(CW)系统可用于生产、
生活废水处理并提供电能,系统内产电微生物由根沉积物和废水提供,其原理如图所示:
下列有关叙述正确的是( )
A.MFC-CW系统中电子由A极流向B极
B.若A极处溶解O 不足,则电路中无电流通过
2
C.若电路中转移 ,则A极消耗O1.12L
2
D.B极反应式为CHCOO-+2H O-8e-=2CO ↑+7H+
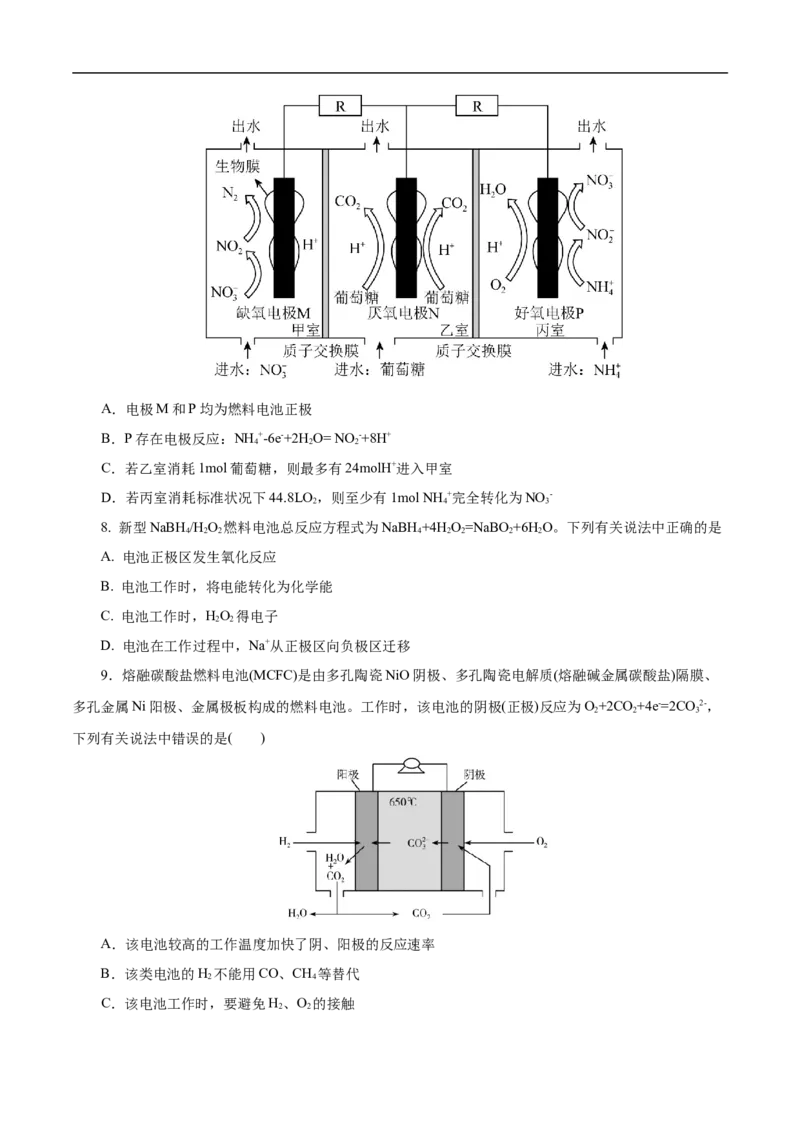
3 2 25.(2022·吉林一中高三模拟)一种由石墨电极制成的海底燃料电池的装置如图所示。下列说法正确的
是( )
A.向b极迁移的是H+
B.大块沉积物中的铁均显+2价
C.b极上FeS 转化为S的电极反应式为FeS -2e- =Fe2+ +2S
2 2
D.微生物作用下S循环(歧化)生成的n(SO 2-)和n(HS- )之比为1: 5
4
6.(2022·福建省厦门市高三模拟)可同步实现除污脱氮和产电的双阴极微生物燃料电池的工作原理如
图,下列说法不正确的是 ( )
A.工作过程中 由厌氧室分别向缺氧室和好氧室迁移
B.理论上,厌氧室消耗1 mol C H O,外电路转移24 mol e-
6 12 6
C.缺氧室中电极发生的反应为2NO -+12H++10e-=N ↑+6H O
3 2 2
D.好氧室在电极上得电子的微粒有O 和NH +
2 4
7.(2022·山东省枣庄市一模)采用情性电极,设计双阴极微生物燃料电池进行同步硝化和反硝化脱氮
的装置如图所示,其中硝化过程中NH +被O 氧化。下列说法正确的是( )
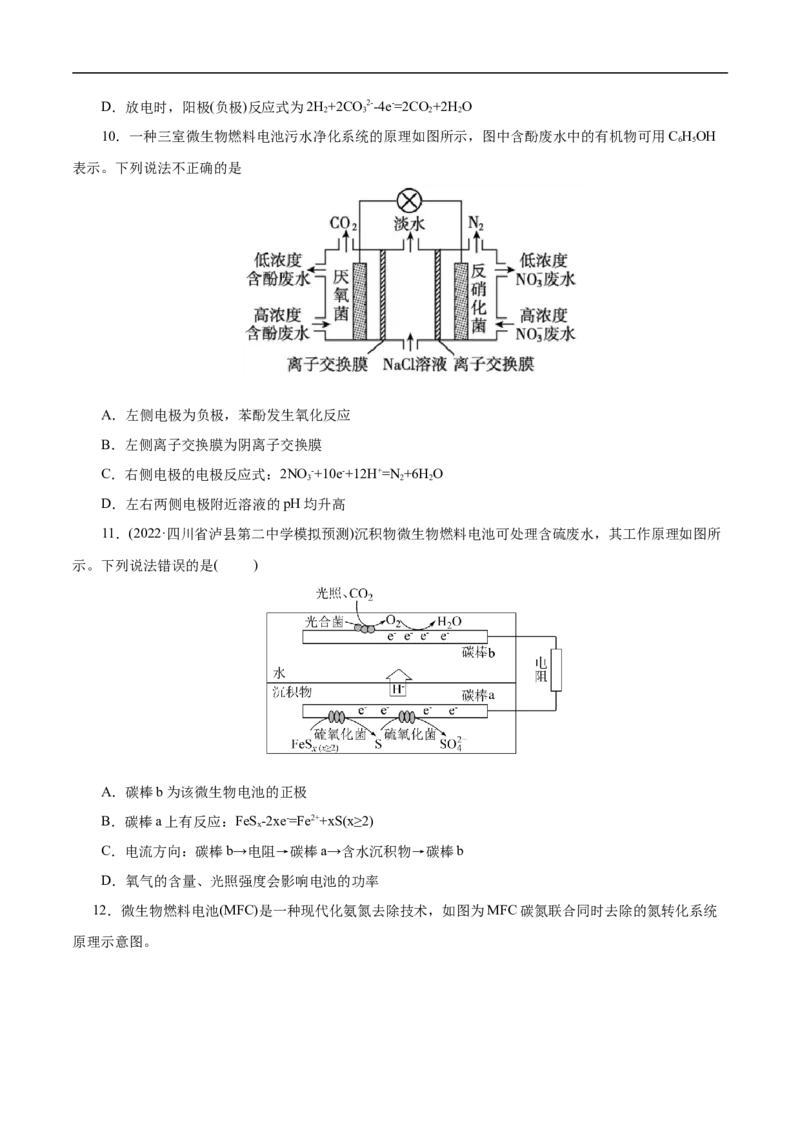
4 2A.电极M和P均为燃料电池正极
B.P存在电极反应:NH +-6e-+2H O= NO-+8H+
4 2 2
C.若乙室消耗1mol葡萄糖,则最多有24molH+进入甲室
D.若丙室消耗标准状况下44.8LO ,则至少有1mol NH +完全转化为NO -
2 4 3
8. 新型NaBH /H O 燃料电池总反应方程式为NaBH +4H O=NaBO +6H O。下列有关说法中正确的是
4 2 2 4 2 2 2 2
A. 电池正极区发生氧化反应
B. 电池工作时,将电能转化为化学能
C. 电池工作时,HO 得电子
2 2
D. 电池在工作过程中,Na+从正极区向负极区迁移
9.熔融碳酸盐燃料电池(MCFC)是由多孔陶瓷NiO阴极、多孔陶瓷电解质(熔融碱金属碳酸盐)隔膜、
多孔金属Ni阳极、金属极板构成的燃料电池。工作时,该电池的阴极(正极)反应为O+2CO +4e-=2CO 2-,
2 2 3
下列有关说法中错误的是( )
A.该电池较高的工作温度加快了阴、阳极的反应速率
B.该类电池的H 不能用CO、CH 等替代
2 4
C.该电池工作时,要避免H、O 的接触
2 2D.放电时,阳极(负极)反应式为2H+2CO 2--4e-=2CO +2H O
2 3 2 2
10.一种三室微生物燃料电池污水净化系统的原理如图所示,图中含酚废水中的有机物可用C HOH
6 5
表示。下列说法不正确的是
A.左侧电极为负极,苯酚发生氧化反应
B.左侧离子交换膜为阴离子交换膜
C.右侧电极的电极反应式:2NO -+10e-+12H+=N +6H O
3 2 2
D.左右两侧电极附近溶液的pH均升高
11.(2022·四川省泸县第二中学模拟预测)沉积物微生物燃料电池可处理含硫废水,其工作原理如图所
示。下列说法错误的是( )
A.碳棒b为该微生物电池的正极
B.碳棒a上有反应:FeS-2xe-=Fe2++xS(x≥2)
x
C.电流方向:碳棒b→电阻→碳棒a→含水沉积物→碳棒b
D.氧气的含量、光照强度会影响电池的功率
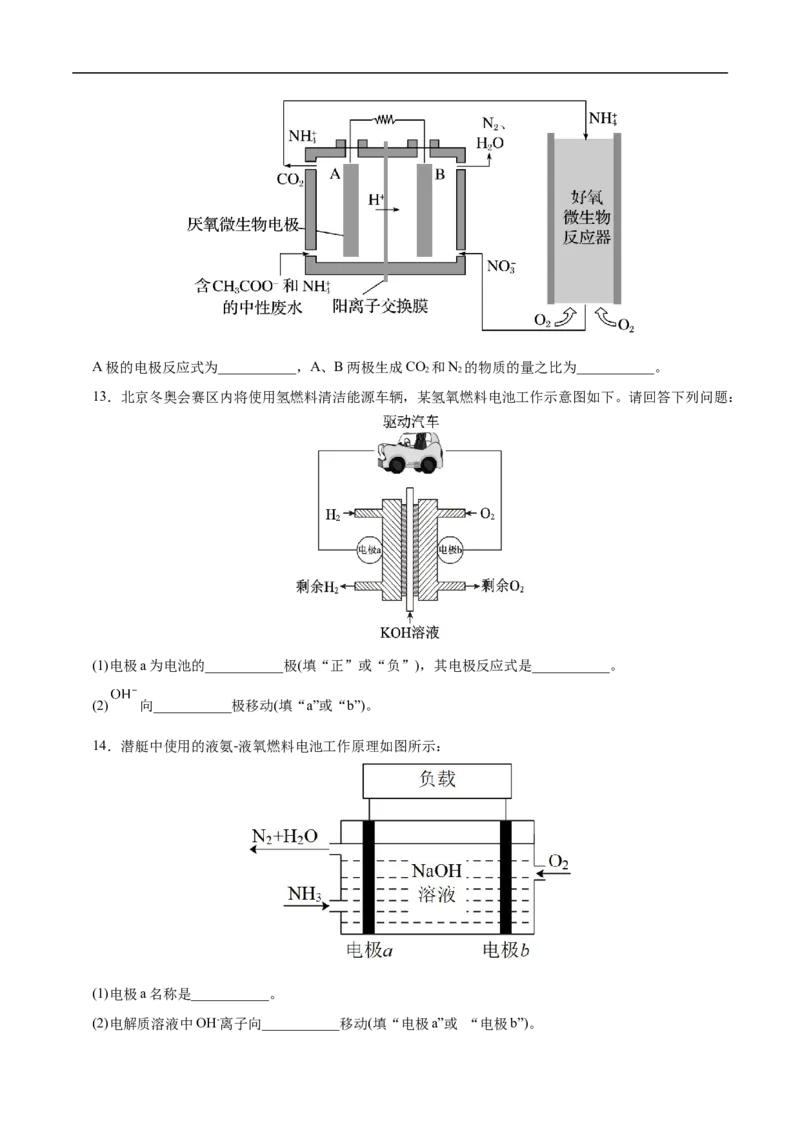
12.微生物燃料电池(MFC)是一种现代化氨氮去除技术,如图为MFC碳氮联合同时去除的氮转化系统
原理示意图。A极的电极反应式为___________,A、B两极生成CO 和N 的物质的量之比为___________。
2 2
13.北京冬奥会赛区内将使用氢燃料清洁能源车辆,某氢氧燃料电池工作示意图如下。请回答下列问题:
(1)电极a为电池的___________极(填“正”或“负”),其电极反应式是___________。
(2) 向___________极移动(填“a”或“b”)。
14.潜艇中使用的液氨-液氧燃料电池工作原理如图所示:
(1)电极a名称是___________。
(2)电解质溶液中OH-离子向___________移动(填“电极a”或 “电极b”)。(3)电极b的电极反应式为___________。
15.甲醇燃料电池可使甲醇作燃料时的能量转化更高效,某种甲醇燃料电池的工作原理如图所示,其电
极反应如下:2CHOH+2H O-12e- =12H++2CO , 3O+12H++12e-=6H O。
3 2 2 2 2
(3)电极A的名称是_______(填“正极”或“负极”);甲醇从_______(填“b”或“c”)处通入。
(4)甲醇燃料电池供电时的总反应方程式为_______
(5)当该装置消耗64g甲醇时,转移电子的数目为_______;若这部分电子全部用于电解水,理论上可产
生标准状况下氢气_______L。
16. 目前,我们日常生活中使用的电能主要还是来自火力发电,火力发电是利用化石燃料燃烧,通过
蒸汽机将产生的能量转化为电能,能量利用率低;燃料电池可以将燃料的化学能直接转化为电能,能量利
用率高。
(1)火力发电厂利用燃煤发电,其能量转化形式为化学能→_______→_______→电能。
(2)磷酸盐燃料电池(PAFC)是当前商业化发展最快的一种燃料电池,以浓磷酸为电解质,以贵金属催化
的气体扩散电极为正、负电极。其优点为构造简单,稳定,电解质挥发度低。磷酸盐燃料电池正极的电极
反应式为_______。
(3)碱性燃料电池(AFC)是最早进入实用阶段的燃料电池之一,也是最早用于车辆的燃料电池,以
KOH、NaOH溶液之类的强碱性溶液为电解质溶液。其优点为性能可靠,具有较高的效率。甲烷碱性燃料
电池正极的电极反应式为_______。
(4)固体氧化物型燃料电池(SOFC),其效率更高,可用于航空航天。如图1所示的装置中,以稀土金属
材料作惰性电极,在电极上分别通入甲烷和空气,其中固体电解质是掺杂了YO 和ZrO 的固体,它在高
2 3 2
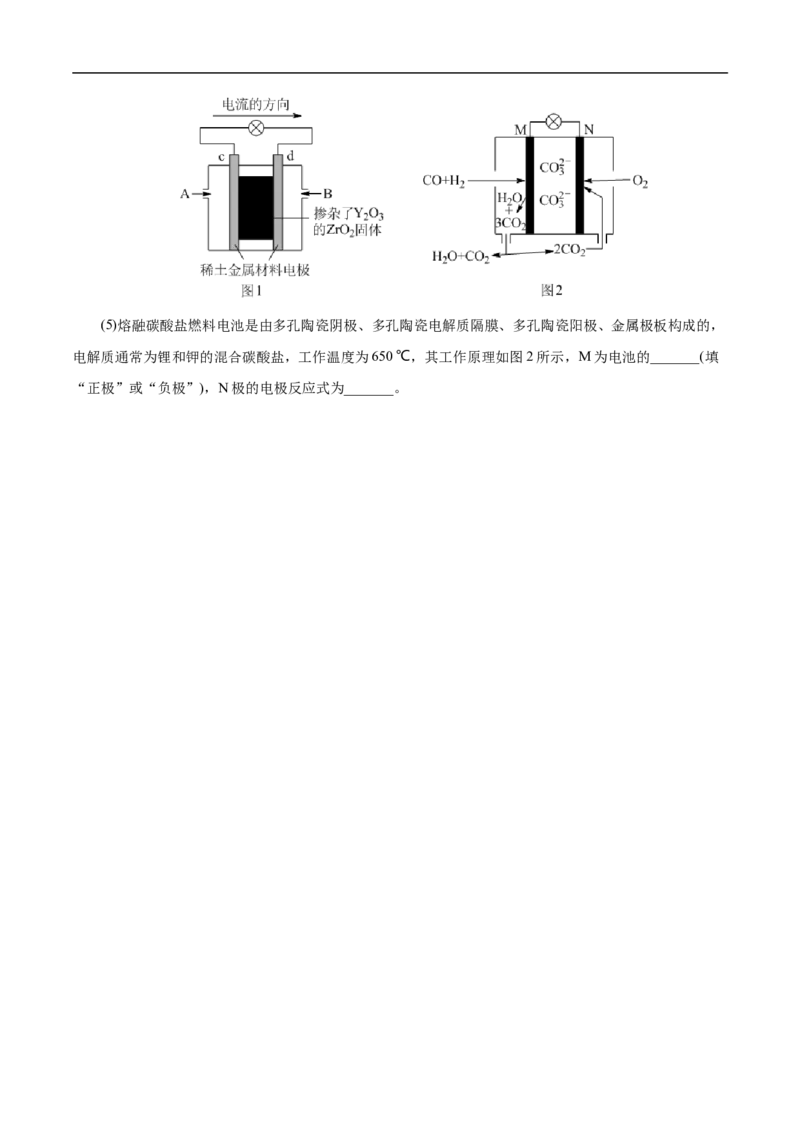
温下能传导O2-;A通入的气体为_______,d电极上的电极反应式为_______。(5)熔融碳酸盐燃料电池是由多孔陶瓷阴极、多孔陶瓷电解质隔膜、多孔陶瓷阳极、金属极板构成的,
电解质通常为锂和钾的混合碳酸盐,工作温度为650 ℃,其工作原理如图2所示,M为电池的_______(填
“正极”或“负极”),N极的电极反应式为_______。