文档内容
专题 25 电解池 金属的腐蚀与防护
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 电解原理及其应用
考点二 金属的腐蚀与防护
考点一 电解原理及其应用
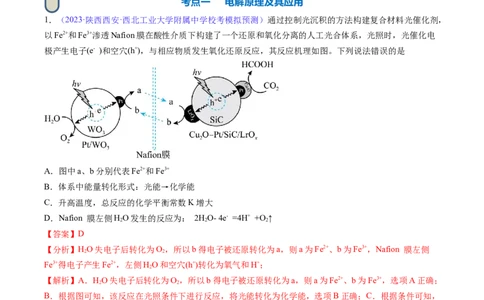
1.(2023·陕西西安·西北工业大学附属中学校考模拟预测)通过控制光沉积的方法构建复合材料光催化剂,
以Fe2+和Fe3+渗透Nafion膜在酸性介质下构建了一个还原和氧化分离的人工光合体系,光照时,光催化电
极产生电子(e- )和空穴(h+),与相应物质发生氧化还原反应,其反应机理如图。下列说法错误的是
A.图中a、b分别代表Fe2+和Fe3+
B.体系中能量转化形式:光能→化学能
C.升高温度,总反应的化学平衡常数K增大
D.Nafion 膜左侧HO发生的反应为: 2HO- 4e- =4H+ +O ↑
2 2 2
【答案】D
【分析】HO失电子后转化为O,所以b得电子被还原转化为a,则a为Fe2+、b为Fe3+,Nafion 膜左侧
2 2
Fe3+得电子产生Fe2+,左侧HO和空穴(h+)转化为氧气和H+;
2
【解析】A.HO失电子后转化为O,所以b得电子被还原转化为a,则a为Fe2+、b为Fe3+,选项A正确;
2 2
B.根据图可知,该反应在光照条件下进行反应,将光能转化为化学能,选项B正确;C.根据条件可知,
该反应为吸热反应,升高温度平衡正向移动,总反应的化学平衡常数K增大,选项C正确;D.Nafion 膜
左侧Fe3+得电子产生Fe2+,则HO失电子产生氧气,发生的反应为: 2HO+ 4(h+)=4H+ +O ↑,选项D不正
2 2 2
确;答案选D。
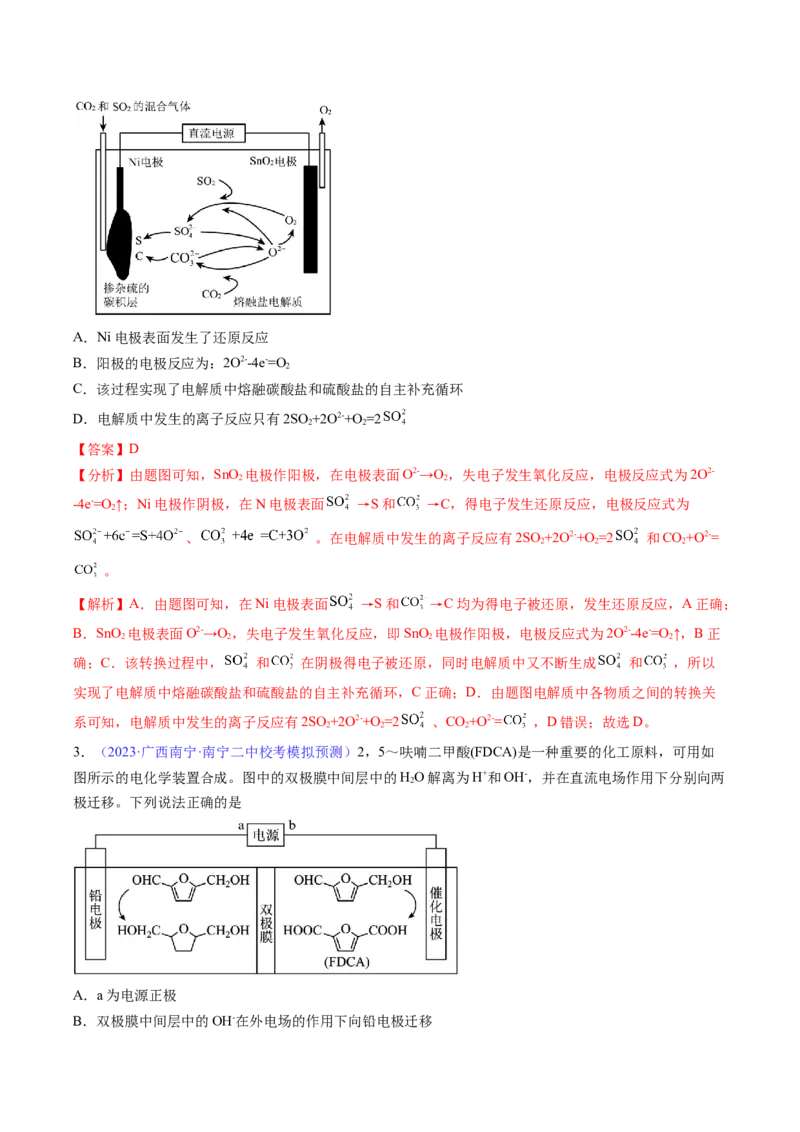
2.(2023·河南郑州·郑州外国语学校校考模拟预测)电解法处理CO 和SO 的混合气体的原理如图所示,
2 2
电解质为熔融碳酸盐和硫酸盐,通电一段时间后,Ni表面电极表面掺杂硫的碳积层。下列有关说法错误的
是
1
原创精品资源学科网独家享有版权,侵权必究!A.Ni电极表面发生了还原反应
B.阳极的电极反应为:2O2--4e-=O
2
C.该过程实现了电解质中熔融碳酸盐和硫酸盐的自主补充循环
D.电解质中发生的离子反应只有2SO +2O2-+O =2
2 2
【答案】D
【分析】由题图可知,SnO 电极作阳极,在电极表面O2-→O,失电子发生氧化反应,电极反应式为2O2-
2 2
-4e-=O ↑;Ni电极作阴极,在N电极表面 →S和 →C,得电子发生还原反应,电极反应式为
2
、 。在电解质中发生的离子反应有2SO +2O2-+O =2 和CO+O2-=
2 2 2
。
【解析】A.由题图可知,在Ni电极表面 →S和 →C均为得电子被还原,发生还原反应,A正确;
B.SnO 电极表面O2-→O,失电子发生氧化反应,即SnO 电极作阳极,电极反应式为2O2--4e-=O ↑,B正
2 2 2 2
确;C.该转换过程中, 和 在阴极得电子被还原,同时电解质中又不断生成 和 ,所以
实现了电解质中熔融碳酸盐和硫酸盐的自主补充循环,C正确;D.由题图电解质中各物质之间的转换关
系可知,电解质中发生的离子反应有2SO +2O2-+O =2 、CO+O2-= ,D错误;故选D。
2 2 2
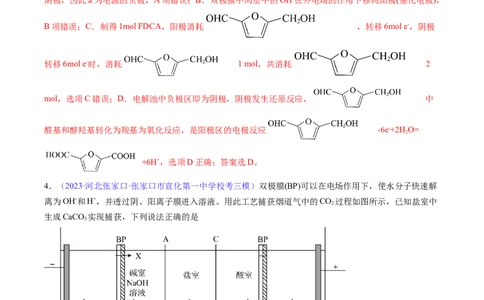
3.(2023·广西南宁·南宁二中校考模拟预测)2,5~呋喃二甲酸(FDCA)是一种重要的化工原料,可用如
图所示的电化学装置合成。图中的双极膜中间层中的HO解离为H+和OH-,并在直流电场作用下分别向两
2
极迁移。下列说法正确的是
A.a为电源正极
B.双极膜中间层中的OH-在外电场的作用下向铅电极迁移C.制得1mol FDCA,理论上共消耗1 mol
D.阳极区的电极反应:
【答案】D
【分析】铅电极附近醛基转化为羟基、五元环内2个碳碳双键转化为单键,发生还原反应,铅电极为阴极,
催化电极为阳极;
【解析】A.铅电极附近醛基转化为羟基、五元环内2个碳碳双键转化为单键,发生还原反应,铅电极为
阴极,因此a为电源的负极,A项错误;B.双极膜中间层中的OH-在外电场的作用下移向阳极(催化电极),
B项错误;C.制得1mol FDCA,阳极消耗 ,转移6mol e-,阴极
转移6mol e-时,消耗 1 mol,共消耗 2
mol,选项C错误;D.电解池中负极区即为阴极,阴极发生还原反应, 中
醛基和醇羟基转化为羧基为氧化反应,是阳极区的电极反应 -6e-+2H O=
2
+6H+,选项D正确;答案选D。
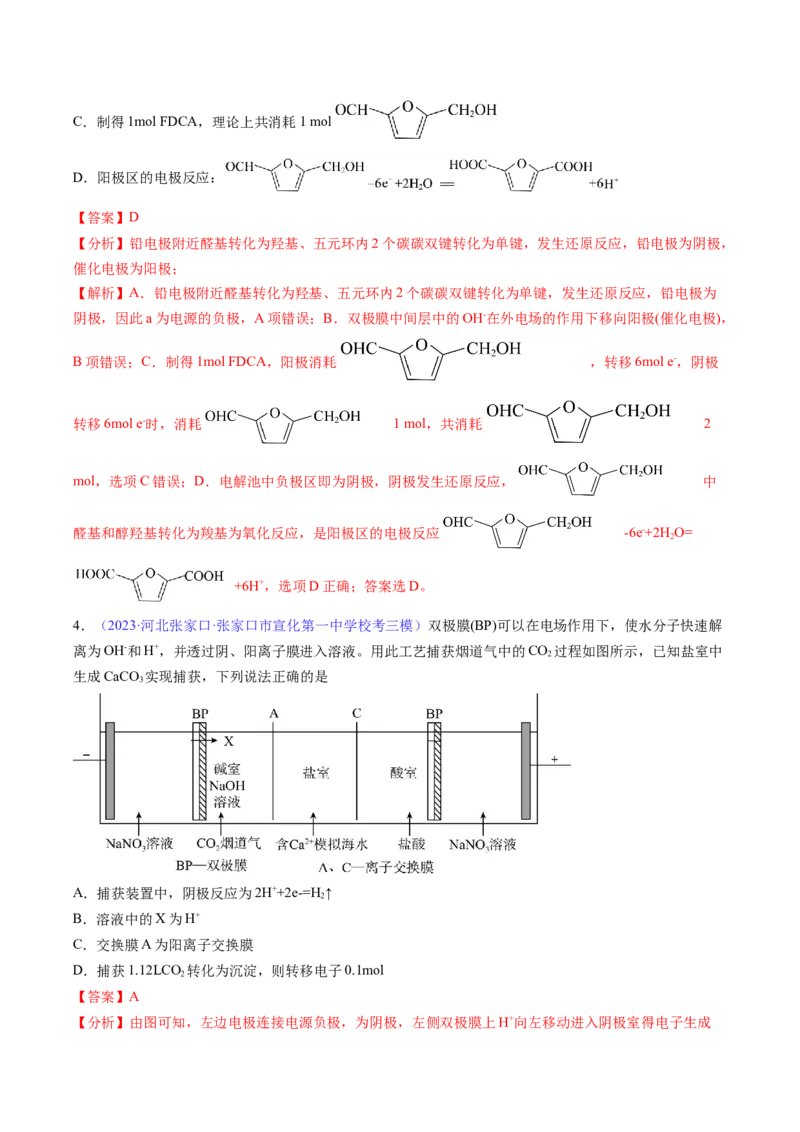
4.(2023·河北张家口·张家口市宣化第一中学校考三模)双极膜(BP)可以在电场作用下,使水分子快速解
离为OH-和H+,并透过阴、阳离子膜进入溶液。用此工艺捕获烟道气中的CO 过程如图所示,已知盐室中
2
生成CaCO 实现捕获,下列说法正确的是
3
A.捕获装置中,阴极反应为2H++2e-=H↑
2
B.溶液中的X为H+
C.交换膜A为阳离子交换膜
D.捕获1.12LCO 转化为沉淀,则转移电子0.1mol
2
【答案】A
【分析】由图可知,左边电极连接电源负极,为阴极,左侧双极膜上H+向左移动进入阴极室得电子生成H,OH-进入碱室与CO 反应生成 , 透过离子交换膜A进入盐室生成CaCO ;右侧电极为阳极,
2 2 3
右侧双极膜上OH-进入阳极室,H+进入酸室,Cl-透过离子交换膜C进入酸室形成盐酸。
【解析】A.阴极发生还原反应,溶液中 放电,为 ,A正确;B.碱室是 转化为
,应由双极膜产生 不断补充,保持碱的浓度,X应为 ,B错误;C.盐室生成 ,就需
要 穿过交换膜A,所以交换膜A为阴离子交换膜,C错误;D.捕获1.12L ,未指明标准状况,
无法计算转移电子数,D错误;故选A。
5.(2023·河北保定·定州一中校考模拟预测)双极膜是由阳离子交换膜和阴离子交换膜复合而成的,其内
层为水层,装置工作时水层中的HO解离成H+和OH-,分别向两侧发生迁移。CO 电化学还原法制备甲醇
2 2
的电解原理如图所示。该装置工作时,下列说法正确的是
A.催化电极上发生氧化反应
B.石墨电极区溶液pH不变
C.H+穿过b膜进入右室溶液
D.电解一段时间后,右室HCO的物质的量减少
【答案】C
【解析】A.催化电极上CO 转化为甲醇,碳元素化合价降低,发生还原反应,A错误;B.石墨电极上电
2
极反应式为 ,水层中的HO解离成H+和OH-,OH-通过a膜向阳极(石墨电极)移动,石
2
墨电极消耗的OH-与迁移过来的OH-数目相等,石墨电极区溶液中OH-物质的量不变,但电解过程中石墨
电极区生成了水,溶液的pH减小,B错误;C.水电离的H+通过b膜向阴极移动,进入右室溶液,C正确;
D.催化电极上的电极反应式为 ,通过b膜迁移过来的H+与 反
应生成 ,故 的物质的量不变,D错误;故选C。
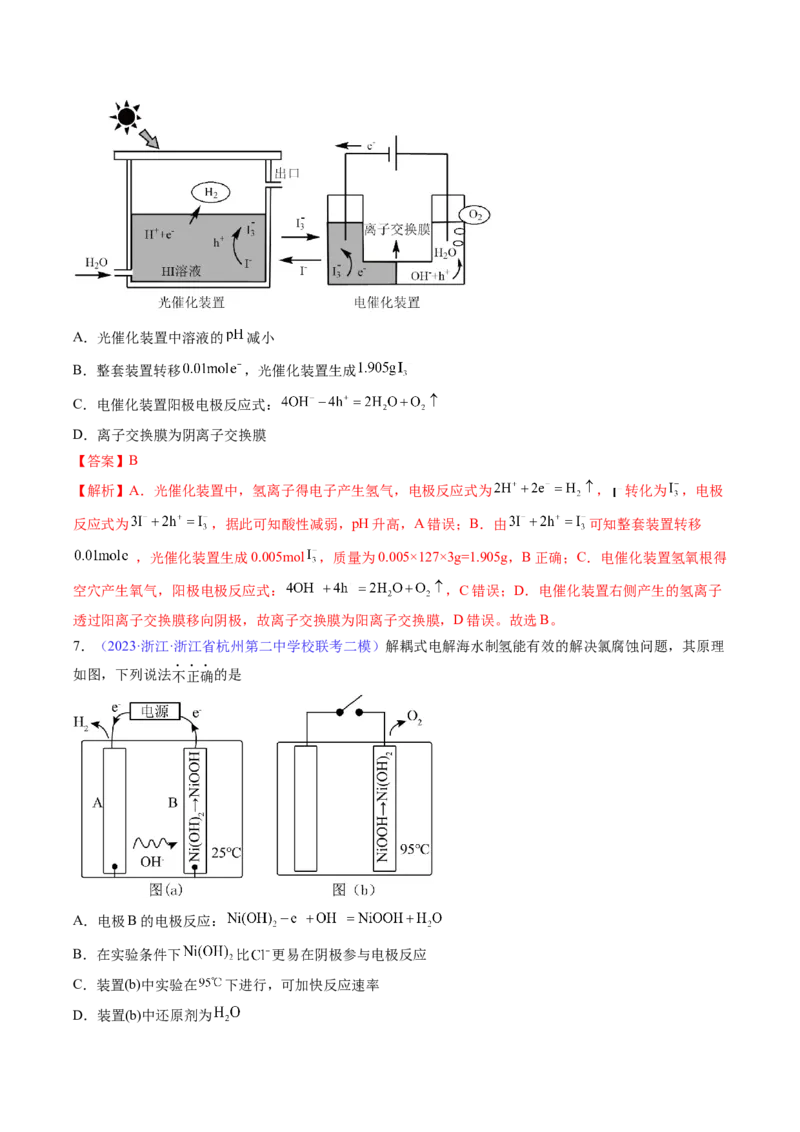
6.(2023·辽宁大连·大连八中校考模拟预测)Adv.Mater报道我国科学家耦合光催化/电催化分解水的装置
如图,光照时,光催化电极产生电子( )和空穴( )。下列有关说法正确的是A.光催化装置中溶液的 减小
B.整套装置转移 ,光催化装置生成
C.电催化装置阳极电极反应式:
D.离子交换膜为阴离子交换膜
【答案】B
【解析】A.光催化装置中,氢离子得电子产生氢气,电极反应式为 , 转化为 ,电极
反应式为 ,据此可知酸性减弱,pH升高,A错误;B.由 可知整套装置转移
,光催化装置生成0.005mol ,质量为0.005×127×3g=1.905g,B正确;C.电催化装置氢氧根得
空穴产生氧气,阳极电极反应式: ,C错误;D.电催化装置右侧产生的氢离子
透过阳离子交换膜移向阴极,故离子交换膜为阳离子交换膜,D错误。故选B。
7.(2023·浙江·浙江省杭州第二中学校联考二模)解耦式电解海水制氢能有效的解决氯腐蚀问题,其原理
如图,下列说法不正确的是
A.电极B的电极反应:
B.在实验条件下 比 更易在阴极参与电极反应
C.装置(b)中实验在 下进行,可加快反应速率
D.装置(b)中还原剂为【答案】B
【解析】A. 电极B上电子流出、电极A上电子流入,则A为阴极,B为阳极,阳极上发生氧化反应,则
B电极反应为: ,A正确;B. 图a为电解池,电极B为阳极,结合
已知:解耦式电解海水制氢能有效的解决氯腐蚀问题,则在实验条件下 比 更易在阳极参与电
极反应,B错误;C. 装置(b)中实验在 下进行,温度升高能加快离子运动速率、增强导电性、可加快
反应速率,C正确;D. 装置(b)为原电池,氧气由水失去电子发生氧化反应得到,则还原剂为 ,D正
确;答案选B。
8.(2023·山东济南·济南市历城第二中学校考模拟预测)羟基自由基 是自然界中氧化性仅次于氟的
氧化剂。我国科学家设计了一种能将苯酚氧化为CO 和HO的原电池-电解池组合装置,实现了发电、环
2 2
保两位一体。下列说法错误的是
A.a极1 mol Cr O 参与反应,理论上NaCl溶液中减少的离子为12N
2 A
B.电池工作时,b极附近pH减小
C.右侧装置中,c、d两极产生气体的体积比(相同条件下)为7:3
D.d极区苯酚被氧化的化学方程式为
【答案】A
【分析】由图示结合题意分析可知左侧为原电池装置,右侧为电解池装置,且a极反应为
,b极反应为 。
【解析】A.a极 得电子生成 ,所以a是正极、b是负极;又a极反应
,则 a极 参与反应转移6mol电子,OH-通过阴离子交换
膜进入NaCl溶液中;b是负极,转移6mol电子时有6molH+通过阳离子交换膜进入NaCl溶液中,HO-、
H+反应生成水,理论上NaCl溶液中离子数不变,A错误;B.电池工作时,b极反应为
,b极附近pH减小,B正确;C.右侧为电解装置,c是阴极,c极反
应式为 ,d为阳极,d极反应式为 , ,转
移28mol电子,c极生成14mol氢气,d极生成6mol二氧化碳气体,所以两极产生气体的体积比(相同条件
下)为7∶3,C正确;D.d极区苯酚被·OH氧化为二氧化碳,反应的化学方程式为,D正确;故选A。
9.(2023·北京海淀·北京市十一学校校考三模)库仑滴定法是常用的快捷检测煤中全硫含量的方法。其方
法为将煤中的硫元素在催化剂作用下转化为 ,再将 通入库仑测硫仪中,库仑测硫仪中电解原理示
意图如图所示,检测前,电解质溶液中 保持定值时,电解池不工作。待测气体进入电解池后, 溶
解并将 还原,测硫仪便立即自动进行电解到 又回到原定值,测定结束,通过测定电解消耗的电量
可以求得煤中含硫量,下列说法不正确的是
A. 在电解池中发生反应的离子方程式为
B.测硫仪工作时电解池的阳极反应式为
C.煤样为 ,电解消耗的电量为 库仑,煤样中硫的质量分数为 (已知:电解中转移 电子所
消耗的电量为96500库仑)
D.煤中硫元素在催化剂作用下会有少量 产生,使测得的全硫含量偏小
【答案】C
【分析】由图可知,测硫仪工作时,左侧铂电极为电解池的阳极,碘离子在阳极失去电子发生氧化反应生
成碘三离子,电极反应式为 ,反应生成的碘三离子与二氧化硫反应生成碘离子、硫酸根离子和
氢离子,反应的离子方程式为 ,右侧铂电极为阴极,溶液中的氢离子在阴极
得到电子发生还原反应生成氢气。
【解析】A.由分析可知,二氧化硫在电解池中发生的反应为反应生成的碘三离子与二氧化硫反应生成碘
离子、硫酸根离子和氢离子,反应的离子方程式为 ,故A正确;B.由分析
可知,测硫仪工作时,左侧铂电极为电解池的阳极,碘离子在阳极失去电子发生氧化反应生成碘三离子,
电极反应式为 ,故B正确;C.由硫原子守恒和得失电子数目守恒可得如下关系:S—SO —
2
—2e—,电解消耗的电量为x库仑,则煤样中硫的质量分数为 ×100%= ,故C错误;
D.三氧化硫没有还原性,不能与溶液中的碘三离子反应,则煤中硫元素在催化剂作用下若生成少量三氧化硫,会使电解消耗的电量减小,导致测得的全硫含量偏小,故D正确;故选C。
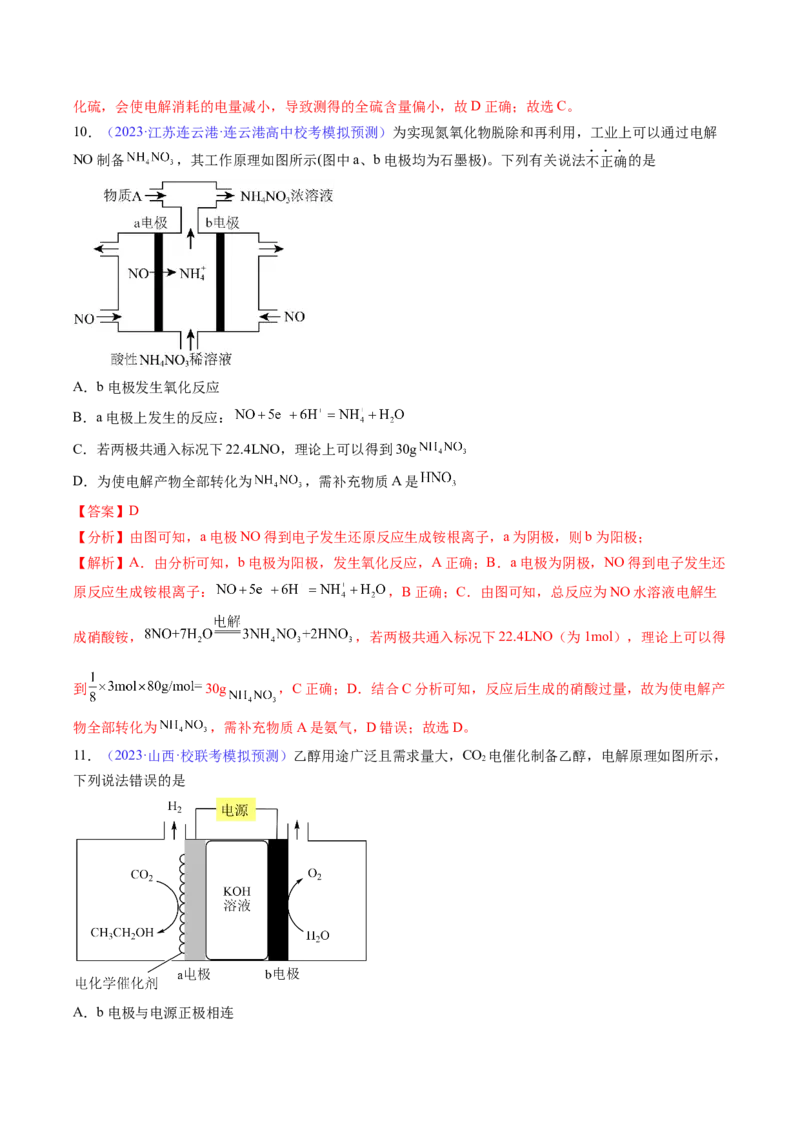
10.(2023·江苏连云港·连云港高中校考模拟预测)为实现氮氧化物脱除和再利用,工业上可以通过电解
NO制备 ,其工作原理如图所示(图中a、b电极均为石墨极)。下列有关说法不正确的是
A.b电极发生氧化反应
B.a电极上发生的反应:
C.若两极共通入标况下22.4LNO,理论上可以得到30g
D.为使电解产物全部转化为 ,需补充物质A是
【答案】D
【分析】由图可知,a电极NO得到电子发生还原反应生成铵根离子,a为阴极,则b为阳极;
【解析】A.由分析可知,b电极为阳极,发生氧化反应,A正确;B.a电极为阴极,NO得到电子发生还
原反应生成铵根离子: ,B正确;C.由图可知,总反应为NO水溶液电解生
成硝酸铵, ,若两极共通入标况下22.4LNO(为1mol),理论上可以得
到 30g ,C正确;D.结合C分析可知,反应后生成的硝酸过量,故为使电解产
物全部转化为 ,需补充物质A是氨气,D错误;故选D。
11.(2023·山西·校联考模拟预测)乙醇用途广泛且需求量大,CO 电催化制备乙醇,电解原理如图所示,
2
下列说法错误的是
A.b电极与电源正极相连B.阳极区溶液的pH在增大
C.a电极的电极反应为2CO+9H O+12e-=C HOH+12OH-
2 2 2 5
D.更换高选择性的电化学催化剂可以抑制a电极发生析氢腐蚀
【答案】B
【分析】二氧化碳催化加氢制备乙醇,则a电极为电解池的阴极,二氧化碳碱性条件下在阴极得到电子生
成乙醇,电极反应式为2CO+12e-+9H O=CHCHOH+12OH-;b电极为电解池的阳极,电极反应式为
2 2 3 2
2HO-4e-=O ↑+4H+。
2 2
【解析】A.根据分析,b电极是阳极,与电源正极相连,A正确;B.阳极电极反应式为2HO-4e-
2
=O ↑+4H+,H+浓度增大,pH下降,B错误;C.a电极是阴极,电极反应式为2CO+12e-
2 2
+9H O=CHCHOH+12OH-,C正确;D.选择高选择性和高活性的电化学催化剂可以有效抑制a电极发生
2 3 2
析氢反应,D正确;故选B。
12.(2023·河南·校联考模拟预测)南开大学教授罗景山课题组基于中性水分解反应体系对CaCO 进行处
3
理转化,此过程利用中性水分解反应中析氧反应过程产生的H+与CaCO 反应生成Ca2+及CO,Ca2+与体系
3
中生成的OH -结合形成Ca( OH),可直接用于水泥生产,工作原理如图所示。
2
下列叙述正确的是
A.电极电势:c>d
B.气体1为O,气体2为H
2 2
C.通过交换膜M和交换膜N的OH-、H+总数一定相等
D.制备C H 的电极反应为2CO +8H O + 12e-= C H + 12OH-
2 4 2 2 2 4
【答案】D
【分析】由图中离子移动的方向可知b、d是电源的正极,a、c是电源的负极,与a相连是电解池的阴极区,
发生反应为: ,与d相连是电解池的阳极区,发生反应为: ,
b、c连接极区生成烃类、一氧化碳等。
【解析】A.由分析可知电极电势:d>c,A错误;B.由分析可知气体1为H,气体2为O,B错误;
2 2
C.通过交换膜M和交换膜N的是OH-和Ca2+,两者总数不相等,C错误;D.制备C H 时CO 得到电子
2 4 2
同时还生成OH-,电极反应为 ,D正确;故选D。
13.(2023·河南南阳·南阳中学校考三模)近日,科学家利用溴辅助氧化C H 电催化CO 合成三乙醇胺、
2 4 2
利用金属酞菁电催化剂上*Br相对于*OH的优先吸附,C H 进一步氧化并与亚硝酸盐还原偶联形成三乙醇
2 4
胺,串联使用两个电解槽,工作原理如图所示。下列说法错误的是
A.X极为阳极,N极为阴极
B.膜1为阳离子交换膜
C.Y极的电极反应式为2CO+ 8H O+12e -= C H+ 12OH-
2 2 2 4
D.右侧电池中,理论上转移6mol电子时生成1molN(CH CHOH)
2 2 3
【答案】B
【分析】Y极由CO 生成C H 发生还原反应是阴极,X为阳极,M极Br-被氧化为Br 发生氧化反应,是阳
2 2 4 2
极,N是阴极。
【解析】A.X极为阳极,N极为阴极,故A正确;B.X极是阳极,发生4OH--4e-=O ↑+2H O, Y极的电
2 2
极反应式为2CO+ 8H O+12e -= C H+ 12OH-,Y极产生的氢氧根离子通过膜1进入X极一边失去电子,因
2 2 2 4
此膜1是阴离子交换膜,可以通过氢氧根离子,故B错误;C.Y极的电极反应式为2CO+ 8H O+12e -=
2 2
C H+ 12OH-,方程式正确,故C正确;D.生成1molN(CH CHOH) ,有1mol亚硝酸根离子得6mol电子
2 4 2 2 3
生成1molNH ,理论上转移6mol电子生成1mol N(CH CHOH) ,故D正确;答案选B。
3 2 2 3
14.(2023·陕西西安·陕西师大附中校考模拟预测)利用光伏电池与膜电解法制备Ce(SO) 溶液的装置如
4 2
下图所示,下列说法不正确的是
A.电解池中阴极的电极反应式为
B.该离子交换膜为阴离子交换膜, 由左池向右池迁移
C.该光伏电池的N电极为负极
D.电路中有0.1mol电子通过时,阳极室生成33.2g Ce(SO )
4 2
【答案】B
【分析】光伏电池内负电荷向N极移动,则N极为负极,P电极为正极,电解池中纯铜为阴极,石墨为阳
极。【解析】A.由分析可知,纯铜为阴极,阴极发生还原反应,电极反应式为 ,故A正确;
B.Ce3+在石墨极发生反应后变为Ce4+,发生了氧化反应,Ce4+与 结合变为Ce(SO) 而流出,消耗了硫
4 2
酸根离子,因此右池中的 向左池迁移,不断进行补充,故B错误;C.光伏电池内负电荷向N极移动,
则N极为负极,故C正确;D.由电路中有0.1mol电子通过时,根据电极反应: 可知,阳
极室生成 即 ,故D正确;故答案选B。
15.(2023·黑龙江哈尔滨·哈师大附中校考模拟预测)下图装置可将CO 转化为CaCO 而矿化封存,进而
2 3
减少碳排放,下列说法错误的是
A.两个双极膜中的OH—均向右侧迁移
B.b极的电极反应式:2H+ +2e- = H ↑
2
C.中间室中发生反应: +Ca2+ = CaCO↓
3
D.向碱室中加入NaHCO 固体,不利于CO 的矿化封存
3 2
【答案】B
【分析】由图可知,与直流电源负极相连的电极a为电解池的阴极,水在阴极得到电子发生还原反应生成
氢气和氢氧根离子,双极膜中氢离子进入阴极室中与放电生成的氢氧根离子反应生成水,氢氧根离子进入
碱室,与通入的二氧化碳反应生成碳酸根离子;电极b为阳极,水在阳极失去电子发生氧化反应生成氧气
和氢离子,双极膜中氢氧根离子进入阳极室中中和放电生成的氢离子,氢离子进入酸室,导致阳离子的电
荷数大于阴离子,使得中间室中的氯离子进入酸室,碱室中的碳酸根离子进入中间室与溶液中钙离子反应
生成碳酸钙沉淀。
【解析】A.由分析可知,两个双极膜中的氢氧根离子均向右侧迁移,故A正确;B.由分析可知,电极b
为阳极,水在阳极失去电子发生氧化反应生成氧气和氢离子,电极反应式为2HO—4e—=O ↑+4H+,故B错
2 2
误;C.由分析可知,中间室中发生反应为碱室中的碳酸根离子进入中间室与溶液中钙离子反应生成碳酸
钙沉淀,离子方程式为 +Ca2+ = CaCO↓,故C正确;D.向碱室中加入碳酸氢钠固体,碳酸氢钠与
3
迁移至碱室的氢氧根离子反应,不利于二氧化碳与碱的反应,导致二氧化碳难以矿化封存,故D正确;故
选B。
16.(2023·辽宁鞍山·统考一模)海水中有丰富的锂资源,我国科学家研发出利用太阳能从海水中提取金属锂的技术,提取原理如图所示,下列说法错误的是
A.该装置将光能间接转变为化学能
B.a极为阴极,电极上发生还原反应
C.电解过程中可监测到b极附近溶液pH减小
D.固体陶瓷膜允许Li+、HO等较小微粒通过
2
【答案】D
【分析】本装置利用太阳能从海水中提取金属锂,由于锂能与水发生反应,所以Li应在电极a生成,从而
得出电极a为阴极,电极b为阳极。
【解析】A.该装置是将太阳能转化为电能,然后电解海水制取锂,则将光能间接转变为化学能,A正确;
B.由分析可知,a极为阴极,电极上Li+得电子生成Li,发生还原反应,B正确;C.电解过程中,b极Cl-
失电子生成Cl,Cl 溶于水后有一部分与水反应生成HCl和HClO,所以电极附近溶液pH减小,C正确;
2 2
D.海水中的Li+通过固体陶瓷膜进入电极a,得电子生成Li,若HO也进入电极a附近,则生成的Li与
2
HO发生反应,所以固体陶瓷膜允许Li+通过,但不允许HO等较小微粒通过,D错误;故选D。
2 2
考点二 金属的腐蚀与防护
1.(2023·全国·模拟预测)白铁皮和镀锡铁皮的腐蚀情况如图所示。下列有关说法不正确的是
A.白铁皮和镀锡铁皮破损后,后者铁更易被腐蚀
B.白铁皮发生电化学腐蚀时,Zn做负极,Fe做正极
C.镀锡铁皮发生电化学腐蚀时,Fe的腐蚀电势比Sn的腐蚀电势高
D.两种材料发生电化学腐蚀时,正极的电极反应式均为
【答案】C
【分析】如图,相同条件下,Zn比铁活泼,所以白铁皮即使破损,Zn依然作负极,被氧化,铁作正极,
被保护起来;镀锡铁皮中,因为铁比锡活泼,所以由铁锡形成的原电池中,铁作负极,发生氧化反应,被
腐蚀;
【解析】A.Zn的金属活动性强于Fe的,白铁皮破损后,Zn做负极被腐蚀,Fe做正极被保护;Fe的金属
活动性强于Sn,镀锡铁皮破损后,Fe做负极被腐蚀,因此,镀锡铁皮更易被腐蚀,A说法正确;B.Zn的
金属活动性强于Fe,白铁皮发生电化学腐蚀时,Zn做负极,Fe做正极,B说法正确;C.Fe的金属活动
性强于Sn,镀锡铁皮发生电化学腐蚀时,Fe做负极,Sn做正极,因此Fe的腐蚀电势比Sn的腐蚀电势低,C说法错误;D.两种材料发生电化学腐蚀时,正极均是 参与反应,电极反应式均为
,D说法正确;故选C。
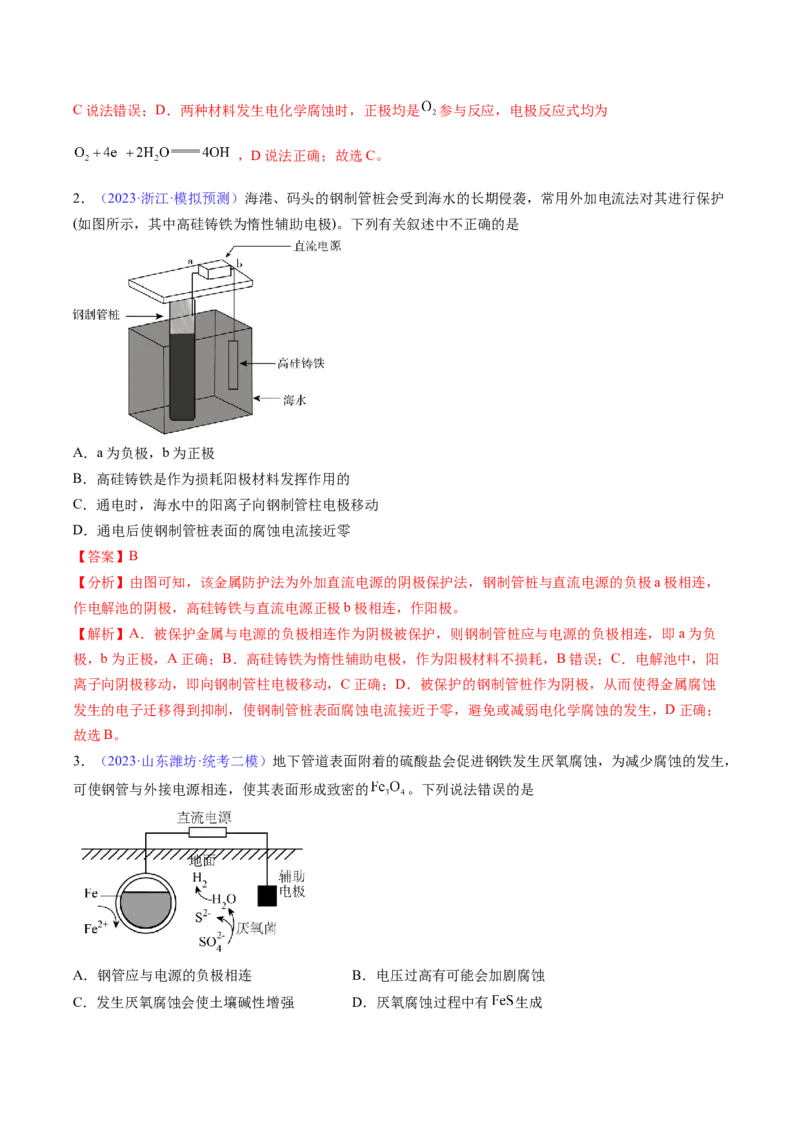
2.(2023·浙江·模拟预测)海港、码头的钢制管桩会受到海水的长期侵袭,常用外加电流法对其进行保护
(如图所示,其中高硅铸铁为惰性辅助电极)。下列有关叙述中不正确的是
A.a为负极,b为正极
B.高硅铸铁是作为损耗阳极材料发挥作用的
C.通电时,海水中的阳离子向钢制管柱电极移动
D.通电后使钢制管桩表面的腐蚀电流接近零
【答案】B
【分析】由图可知,该金属防护法为外加直流电源的阴极保护法,钢制管桩与直流电源的负极a极相连,
作电解池的阴极,高硅铸铁与直流电源正极b极相连,作阳极。
【解析】A.被保护金属与电源的负极相连作为阴极被保护,则钢制管桩应与电源的负极相连,即a为负
极,b为正极,A正确;B.高硅铸铁为惰性辅助电极,作为阳极材料不损耗,B错误;C.电解池中,阳
离子向阴极移动,即向钢制管柱电极移动,C正确;D.被保护的钢制管桩作为阴极,从而使得金属腐蚀
发生的电子迁移得到抑制,使钢制管桩表面腐蚀电流接近于零,避免或减弱电化学腐蚀的发生,D正确;
故选B。
3.(2023·山东潍坊·统考二模)地下管道表面附着的硫酸盐会促进钢铁发生厌氧腐蚀,为减少腐蚀的发生,
可使钢管与外接电源相连,使其表面形成致密的 。下列说法错误的是
A.钢管应与电源的负极相连 B.电压过高有可能会加剧腐蚀
C.发生厌氧腐蚀会使土壤碱性增强 D.厌氧腐蚀过程中有 生成【答案】A
【解析】A.钢管表面形成 ,失去电子,作为阳极,应与正极相连,故A错误;B.电压过高,内层
金属可能会继续失电子被氧化,加剧腐蚀,故B正确;C.厌氧腐蚀中氢离子浓度减小,氢氧根离子增大,
碱性增强,故C正确;D.铁失电子生成Fe2+,与S2-生成 ,故D正确;故答案选A。
4.(2023·广东·广州市第二中学校联考三模)利用原电池原理可以避免金属腐蚀,某小组同学设计了如下
图所示的实验方案来探究铁片的腐蚀情况。下列说法中正确的是
A.甲中的铁片附近会出现蓝色
B.甲中形成了原电池,锌片作正极
C.乙中铜片附近会出现红色
D.乙中的铜片上发生氧化反应
【答案】C
【解析】A.甲中锌为负极,其失去电子变为锌离子,而铁片是正极,其被保护而不会被腐蚀,没有亚铁
离子生成,而铁氰化钾与亚铁离子反应会生成蓝色物质,实验室常用此法来检验亚铁离子,因此铁片附近
不会出现蓝色,故A错误;B.甲中形成了原电池,锌为负极,锌失去电子变为锌离子,铁为正极,铁不
反应,故B错误;C.乙中铁作负极,铜作正极,铜附近氧气得到电子变为氢氧根而使溶液呈碱性,因此,
酚酞变为红色,故铜片附近出现红色,故C正确;D.乙中铁作为负极,其失去电子变为亚铁离子发生氧
化反应;铜片作为正极,其表面上有氧气发生还原反应,故D错误;故答案选C。
5.(2023·河北沧州·沧州市第二中学校联考三模)出土于陕西的两千多年前的越王剑(主要成分为铁),现
藏于广州博物馆,该剑剑格左右侧皆以鸟虫书体铸刻“王戊”二字,剑色为水银古,时至如今,依然锋利。
剑脊含铜量较多,韧性好,不易折断;刃部含锡高,硬度强,可见其性能优异,锻造技术优良。下列叙述
错误的是
已知:剑在地下因构成原电池发生了腐蚀,导致生锈(Fe O)。
2 3
A.铁与铜、锡构成原电池时,铁为负极
B.铁发生的电极反应为Fe-3e-=Fe3+
C.酸性环境下剑腐蚀的过程中会产生氢气D.生成80gFe O 时理论上转移3mol电子
2 3
【答案】B
【解析】A.铁与铜、锡构成原电池时,铁的活泼性强于铜和锡,铁作负极,A正确;B.铁电极反应为
Fe-2e-=Fe2+,B错误;C.酸性环境下剑腐蚀的过程为析氢腐蚀,正极会产生氢气:2H++2e-=H ,C正确;
2
D.生成 Fe O 时理论上转移电子 3mol,D正确;故选B。
2 3
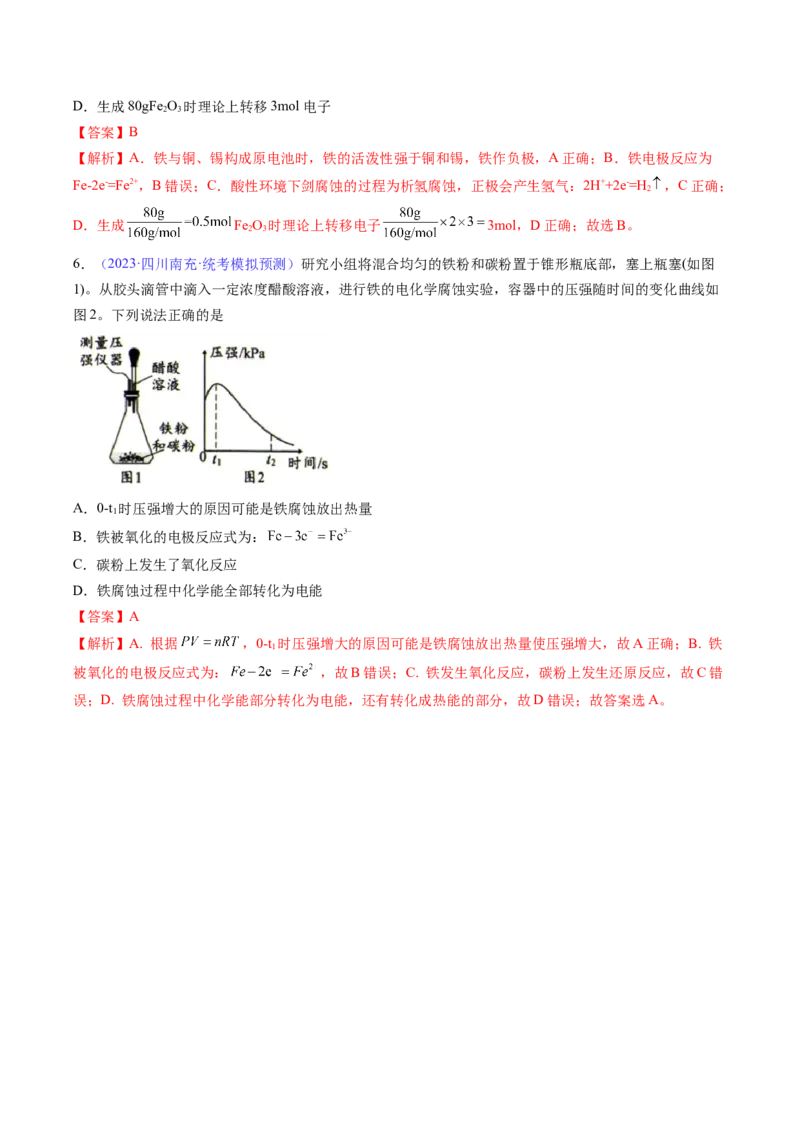
6.(2023·四川南充·统考模拟预测)研究小组将混合均匀的铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图
1)。从胶头滴管中滴入一定浓度醋酸溶液,进行铁的电化学腐蚀实验,容器中的压强随时间的变化曲线如
图2。下列说法正确的是
A.0-t 时压强增大的原因可能是铁腐蚀放出热量
1
B.铁被氧化的电极反应式为:
C.碳粉上发生了氧化反应
D.铁腐蚀过程中化学能全部转化为电能
【答案】A
【解析】A. 根据 ,0-t 时压强增大的原因可能是铁腐蚀放出热量使压强增大,故A正确;B. 铁
1
被氧化的电极反应式为: ,故B错误;C. 铁发生氧化反应,碳粉上发生还原反应,故C错
误;D. 铁腐蚀过程中化学能部分转化为电能,还有转化成热能的部分,故D错误;故答案选A。