文档内容
微专题 19 海水资源的综合利用(提取溴和
碘)
1.(2023·全国·高三专题练习)下列物质用途的描述正确的是
A.明矾溶液用作铜绿去除剂,利用了其水解显酸性
B.淀粉溶液用作碘量法滴定的指示剂,利用了其不饱和性
C.FeS用作除去含Cu2+废水的沉淀剂,利用了其还原性
D.SO 用作海水提溴的吸收剂,利用了其漂白性
2
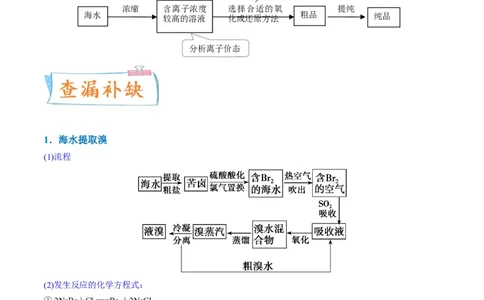
2.(2023·全国·高三专题练习)工业上用活性炭吸附海带提碘后废水中的 制取 ,其流程如图:
下列说法错误的是
A. 氧化 时使溶液 变大
B.活性炭吸附是为了净化水溶液
C. 与 (浓、热)反应的化学方程式:
D.热空气能吹出 ,是因为 在水中溶解度小、易升华
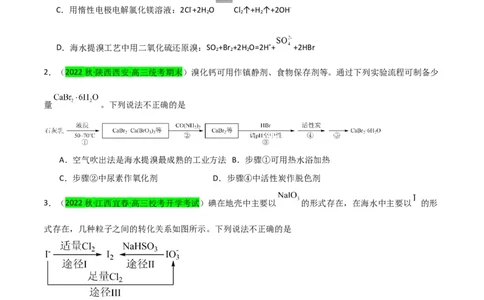
1从海水中提取物质的思路
海水中提取溴和碘的反应都是将其-1价离子氧化成单质。涉及工业实际,最主要的问题是如何将大量海
水中分布的元素富集起来。溴的制取一般是氧化→吹出→吸收→再氧化的路线,碘一般是由海带提取,主
要过程是灼烧→溶解→过滤→氧化→萃取的路线。工艺模式如图所示:
关键点
浓缩 含离子浓度 选择合适的氧 提纯
海水 较高的溶液 化或还原方法 粗品 纯品
分析离子价态
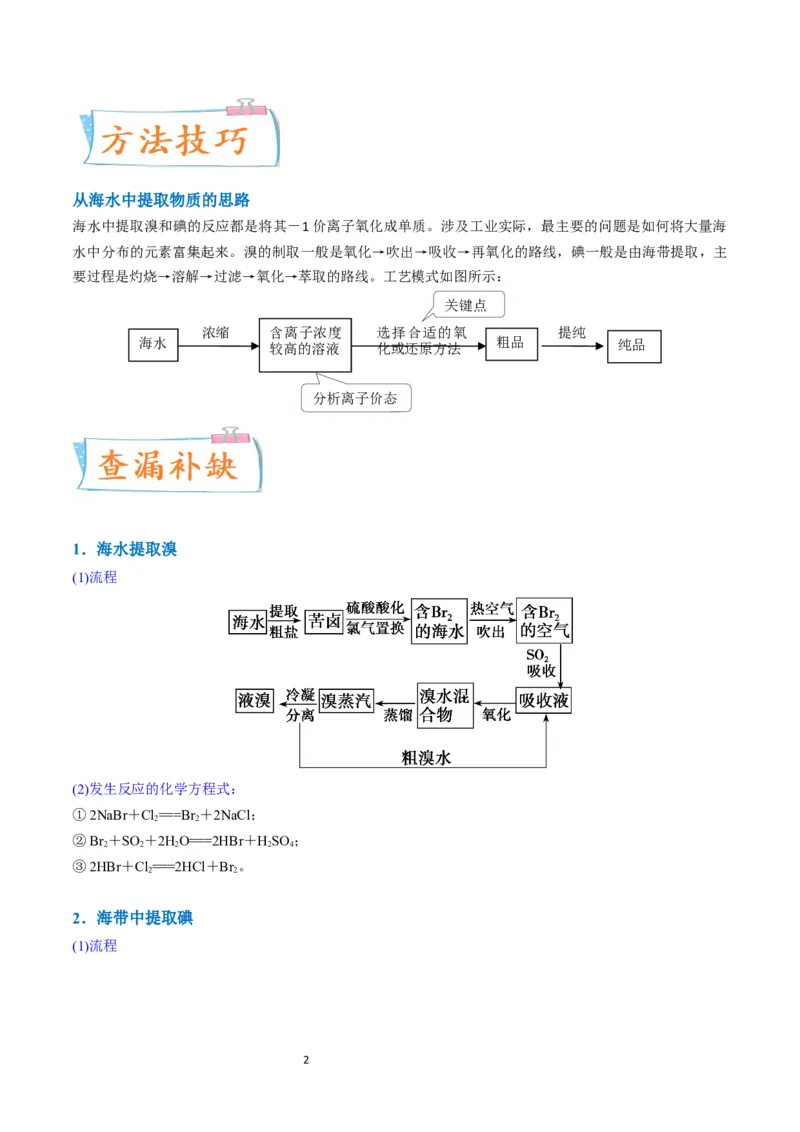
1.海水提取溴
(1)流程
(2)发生反应的化学方程式:
①2NaBr+Cl===Br +2NaCl;
2 2
②Br +SO +2HO===2HBr+HSO ;
2 2 2 2 4
③2HBr+Cl===2HCl+Br 。
2 2
2.海带中提取碘
(1)流程
2(2)发生反应的离子方程式:
Cl+2I-===I +2Cl-。
2 2
(3)主要的物理原理:单质碘用CCl 或苯萃取,分液后用蒸馏法将碘与有机溶剂分开。
4
1.(2023秋·江苏泰州·高三姜堰中学校联考阶段练习)以卤水(富含I—)为原料用高分子树脂提取碘的工艺
流程如图所示,下列说法不正确的是
A.“氧化1”过程既可以用Cl ,也可以用H O
2 2 2
B.“解脱”用Na SO 将I 还原为I—,离子方程式为I +SO +2OH—=2I—+2SO +H O
2 3 2 2 2
C.用高分子树脂“吸附”,再“解脱”是为了便于分离富集碘元素
D.“提纯”过程先萃取分液、蒸馏得到粗产品,再升华纯化
2.(2022秋·福建龙岩·高三上杭一中校联考期中)海水中的碘富集在海藻中,我国海带产量居世界第一,
除供食用外,大量用于制碘。实验室提取碘的途径如下所示:
干海带 海带灰 水溶液 碘单质
下列有关叙述错误的是
A.实验室在坩埚中焙烧干海带
B.“氧化”时,试剂可选用O 、H O
2 2 2
C.“系列操作”中涉及的操作是萃取、分液
D.在含I-的水溶液中加入氧化剂后滴加几滴淀粉溶液,溶液变蓝,说明I-被氧化
31.(2023·安徽芜湖·统考二模)能正确表示下列反应的离子方程式的是
A.用K [Fe(CN) ]溶液检验Fe2+:Fe2++K++[Fe(CN) ]3-=KFe[Fe(CN) ]↓
3 6 6 6
B.向二元弱酸亚磷酸(H PO )溶液中滴加足量的烧碱溶液:H PO +3OH-= +3H O
3 3 3 3 2
C.用惰性电极电解氯化镁溶液:2Cl-+2H O Cl ↑+H ↑+2OH-
2 2 2
D.海水提溴工艺中用二氧化硫还原溴:SO +Br +2H O=2H++ +2HBr
2 2 2
2.(2022秋·陕西西安·高三统考期末)溴化钙可用作镇静剂、食物保存剂等。通过下列实验流程可制备少
量 。下列说法不正确的是
A.空气吹出法是海水提溴最成熟的工业方法 B.步骤①可用热水浴加热
C.步骤②中尿素作氧化剂 D.步骤④中活性炭作脱色剂
3.(2022秋·江西宜春·高三校考开学考试)碘在地壳中主要以 的形式存在,在海水中主要以 的形
式存在,几种粒子之间的转化关系如图所示。下列说法不正确的是
A.用淀粉-KI试纸和食醋检验加碘盐时淀粉-KI试纸会变蓝
B.足量Cl 能使湿润的、已变蓝的淀粉-KI试纸褪色的原因可能
2
C.途径Ⅱ中若生成1mol ,则反应中转移10mol电子
D.由题图可知氧化性的强弱顺序为
4.(2022秋·重庆北碚)溴及其化合物在医药、农药、染料等生产中有广泛应用。工业上常用的一种海水
4提取溴技术叫做“吹出法”,其生产流程如图所示。下列说法错误的是
A.溶液X的主要成分是HBr和H SO
2 4
B.通过吹出塔、吸收塔实现了对溴的富集
C.用热空气将Br 吹出利用了Br 易挥发的性质
2 2
D.在工业生产中,也可以用足量的Na CO 溶液代替SO 和水,发生的反应为:
2 3 2
6Na CO +3Br =5NaBr+NaBrO +6CO ↑
2 3 2 3 2
5.(2022春·全国·高三专题练习)下列说法正确的是
A.FeSO 、Fe(OH) 都可以通过化合反应制得
4 3
B.往海带灰的浸泡液中加入过量的氯水,保证I-完全氧化为I
2
C.氨气、溴中毒时,要立即到室外呼吸新鲜空气,必要时进行人工呼吸
D.AgBr见光易分解,故可用于人工降雨
6.(2022·陕西安康·统考一模)溴、碘主要存在于海水中,有“海洋元素”的美称.海水中的碘富集在海藻
中,我国海带产量居世界第一,除供食用外,大量用于制碘。实验室提取碘的途径如下所示:
下列有关叙述错误的是
A.实验室在坩埚中焙烧干海带,并且用玻璃棒搅拌
B.在含 的水溶液中加入稀硫酸和双氧水后,碘元素发生氧化反应
C.操作a是萃取,操作b是分液,操作a和b均在分液漏斗中进行
D.在含 的水溶液加入氧化剂后滴加几滴淀粉溶液,溶液变蓝色,说明 完全被氧化
7.(2022秋·黑龙江哈尔滨·高三尚志市尚志中学校考期中)“空气吹出法”是目前海水提溴最成熟的工业
方法,部分工艺流程如下:
5下列说法错误的是
A.步骤③发生时溶液的酸性增强 B.溶液中Br 的浓度:Ⅰ Ⅱ
2
C.步骤②利用了溴易挥发的性质 D.使用乙醇萃取溶液Ⅱ中Br 后再蒸馏
2
8.(2022·山东·高三专题练习)海藻中含有丰富的碘元素。下图是实验室模拟从海藻里提取碘的流程的一
部分,下列判断正确的是
A.步骤④的操作是过滤
B.可用淀粉溶液检验步骤②的反应是否进行完全
C.步骤①、③的操作分别是过滤、分液
D.步骤③中加入的有机溶剂可以是四氯化碳
1.(2023秋·黑龙江大庆)目前海水提溴的最主要方法之一是空气吹出法,其部分流程图如下:
以下推断不合理的是
A.热空气能吹出溴是利用溴易挥发的性质
B.SO 吸收溴的反应方程式:SO +2H O+Br =H SO +2HBr
2 2 2 2 2 4
C.因为氧化性Fe3+<Br ,所以氧化过程可选用FeCl 溶液
2 3
D.没有采用直接蒸馏含Br 的海水得到单质溴主要是为了节能
2
2.(2023·全国·高三专题练习)从海带中提取粗碘的某种工艺流程如图所示(部分操作名称已省略)。
6下列有关说法错误的是( )
A.步骤②的操作是萃取
B.步骤③的NaOH是还原剂
C.步骤④的试剂X是稀硫酸
D.步骤⑤的操作Y是过滤
3.(2023·全国·高三专题练习)用高分子吸附树脂提取卤水中的碘(主要以I -形式存在)的工艺流程如下:
下列说法不正确的是
A.经①和④所得溶液中,c(I-)后者大于前者
B.④的作用是将吸附的碘氧化而脱离高分子树脂
C.若②和⑤中分别得到等量I ,则消耗的n(Cl ):n(KClO ) =3:1
2 2 3
D.由⑥得到碘产品的过程,主要发生的是物理变化
4.(2023·全国·高三专题练习)某海水浓缩液中含有大量的Clˉ、Brˉ、Iˉ,取1L该浓缩液,向其中通入一
定量的Cl ,溶液中三种离子的物质的量与通入Cl 的体积(标准状况)的关系如下表。下列有关说法中不
2 2
正确的是
Cl 的体积(标准状况) 2.8L 5.6L 11.2L
2
n(Clˉ) 1.25mol 1.5mol 2mol
n(Brˉ) 1.5mol 1.4mol 0.9mol
n(Iˉ) amol 0 0
A.当通入Cl 的体积为2.8L时,只有Iˉ与Cl 发生反应
2 2
B.当通入Cl 的体积为2.8L~5.6L时,只有Brˉ与Cl 发生反应
2 2
C.a=0.15
D.原溶液中c(Clˉ)∶c(Brˉ)∶c(Iˉ)=10∶15∶4
75.(2023·全国·高三专题练习)有关海洋中部分资源的利用的说法不正确的是( )
A.用MgCl •6H O晶体制无水MgCl ,需在HCl气流中加热脱水
2 2 2
B.SO 水溶液吸收Br 的化学方程式为Br +SO +2H O=H SO +2HBr
2 2 2 2 2 2 4
C.粗碘中混有少量ICl和IBr可加入KI进行升华提纯工业上利用
D.Cl 与澄清石灰水反应制取漂白粉
2
6.(2023·全国·高三专题练习)历史上海藻提碘中得到一种红棕色液体,由于性质相似, 误认为是
,从而错过了一种新元素的发现。该元素是 。
7.(2022·全国·高三专题练习)碘单质对动植物的生命极其重要,还可用于医药、照相、染料和系统监测
等。某学习小组在实验室中从海藻和油井盐水生产母液中提取碘单质的主要步骤如图所示:
已知:本实验条件下,氧化性:Cl >IO >MnO >I
2 2 2
检验海藻和油井盐水生产母液中含有I-的操作和现象为 。
8.(2021秋·天津·高三校联考期中)海水中含有大量的卤族元素,具有十分巨大的开发利用潜力。
I.氯气是非常重要的化工产品
(1)用浓盐酸和二氧化锰制氯气是实验室常用的方法,写出该反应的化学方程式: 。
(2)也可用浓盐酸和高锰酸钾制氯气,反应方程式如下:2KMnO +16HCl(浓)=KCl+2MnCl +5Cl ↑+8H O,实验
4 2 2 2
室用该方法制氯气时,可选用的发生装置是 (写编号)。
编号 A B C
发生装置
(3)为证明氯气与水反应产物具有漂白性,将Cl 缓缓通过下列装置:
2
8试剂a应选择 ;试剂b的作用是 ; 。
(4)通常使用84消毒液时需要把消毒对象在其中浸泡一段时间,以提高消毒效果。请结合反应方程式分析
原因
II.地球上99%的溴元素以Br-形式存在于海水中。海水中Br-含量约为65mg/L,而苦卤(海水晒盐后得到的母
液)中Br-含量高很多,苦卤常作海水提溴的主要原料。目前最成熟的“空气吹出法”海水提溴工艺流程如
图(已知:溴的沸点为59℃):
(5)为实现Br-转化为Br 的目的,所加试剂X应必有的化学性质是 。
2
(6)利用“空气吹出法”将“氧化室”产生的低浓度Br 分离出来的方法利用了溴的 这一物理性
2
质。
(7)将低浓度Br 富集为高浓度Br 历经步骤iii反应的离子方程式为: 。
2 2
9.(2022·全国·高三专题练习)碘是人体必需的微量元素,也可用于工业、医药等领域。大量的碘富集于
海藻灰(主要成分是NaI)中,因此从海藻灰中提取碘,可有效利用海洋资源。
(1)某兴趣小组以海藻灰为原料进行I 的制备实验。具体步骤如下:将海藻灰加热浸泡后,得到了NaI溶液,
2
将适量Na SO 固体溶于NaI溶液中,再将CuSO 饱和溶液滴入上述溶液中,生成白色CuI沉淀,该反应的离
2 3 4
子方程式为 。
(2)待I-沉淀完全后,过滤,将沉淀物置于小烧杯中,在搅拌下逐滴加入适量浓HNO ,观察到
3
(颜色)气体放出, (颜色)晶体析出。出于安全和环保考虑,该实验操作需在 (条件)
下进行。该反应的化学方程式为 。
(3)用倾析法弃去上清液,固体物质用少量水洗涤后得到粗I ,进一步精制时,选择必需的仪器搭建装置,
2
并按次序排列: (夹持装置略)。
9A.
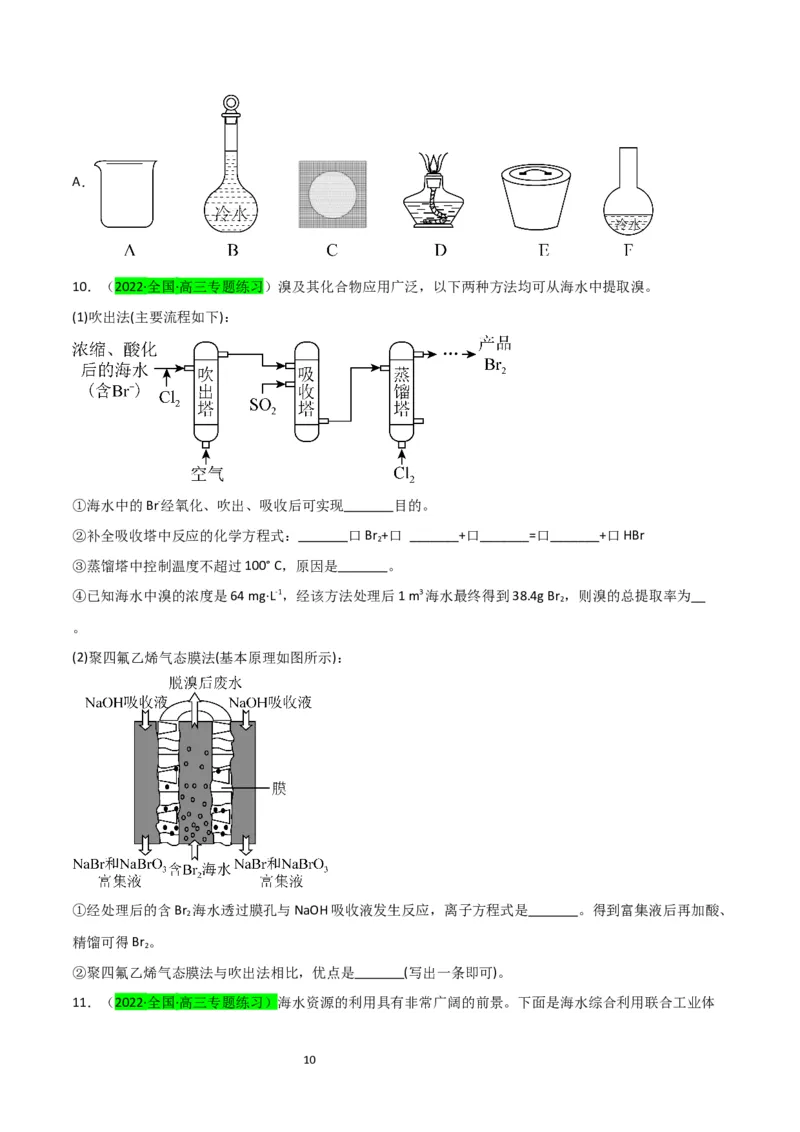
10.(2022·全国·高三专题练习)溴及其化合物应用广泛,以下两种方法均可从海水中提取溴。
(1)吹出法(主要流程如下):
①海水中的Br-经氧化、吹出、吸收后可实现 目的。
②补全吸收塔中反应的化学方程式: 口Br +口 _______+口_______=口_______+口HBr
2
③蒸馏塔中控制温度不超过100° C,原因是 。
④已知海水中溴的浓度是64 mg·L-1,经该方法处理后1 m3海水最终得到38.4g Br ,则溴的总提取率为
2
。
(2)聚四氟乙烯气态膜法(基本原理如图所示):
①经处理后的含Br 海水透过膜孔与NaOH吸收液发生反应,离子方程式是 。得到富集液后再加酸、
2
精馏可得Br 。
2
②聚四氟乙烯气态膜法与吹出法相比,优点是 (写出一条即可)。
11.(2022·全国·高三专题练习)海水资源的利用具有非常广阔的前景。下面是海水综合利用联合工业体
10系的简图:
回答下列问题:
I.海水淡化
(1)人类可以从海水中获得淡水,以解决水资源危机。海水淡化的方法主要有 、 等。
Ⅱ.海水制盐
(2)过程Ⅰ采用的操作是 。
(3)粗盐中可溶性的杂质离子主要有SO 、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入
了试剂NaOH溶液、BaCl 溶液、Na CO 溶液、盐酸,其中Na CO 溶液的作用是 。
2 2 3 2 3
Ⅲ.海水提溴
(4)工业上从海水中提取溴单质的流程图中,步骤④的离子方程式为 ;从理论上考虑下列也能吸收Br 的
2
是 。
A.NaCl B.FeCl C.Na SO D.H O E.K S
2 2 3 2 2
(5)经过步骤①②已获得Br ,不直接用含Br 的海水进行蒸馏得到液溴,而要经过“空气吹出、SO 吸收、
2 2 2
通入氯气”后再蒸馏,其目的是 。
Ⅳ.海水提镁
(6)该工业生产过程中,为了使MgCl 转化为Mg(OH) ,应加入的试剂为 。
2 2
11