文档内容
微专题24 Cl 、NH 、SO 的实验室制备与应用
2 3 2
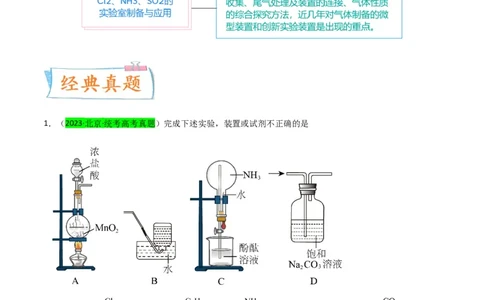
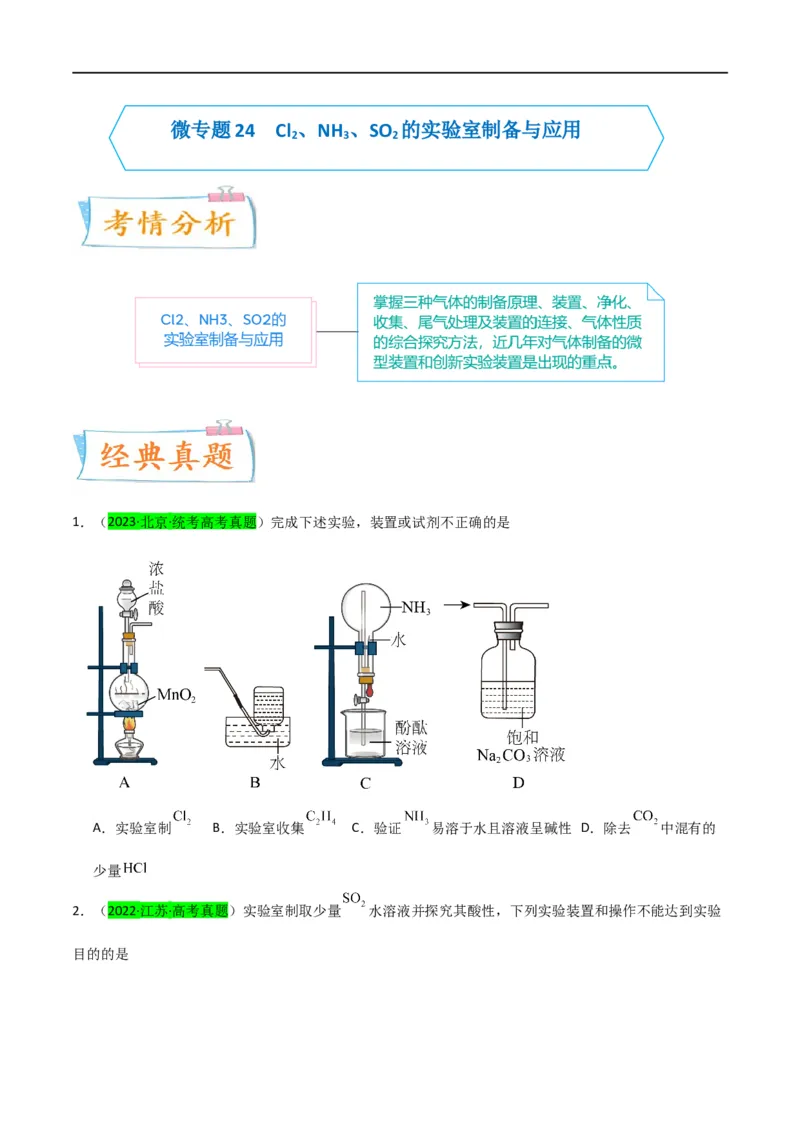
1.(2023·北京·统考高考真题)完成下述实验,装置或试剂不正确的是
A.实验室制 B.实验室收集 C.验证 易溶于水且溶液呈碱性 D.除去 中混有的
少量
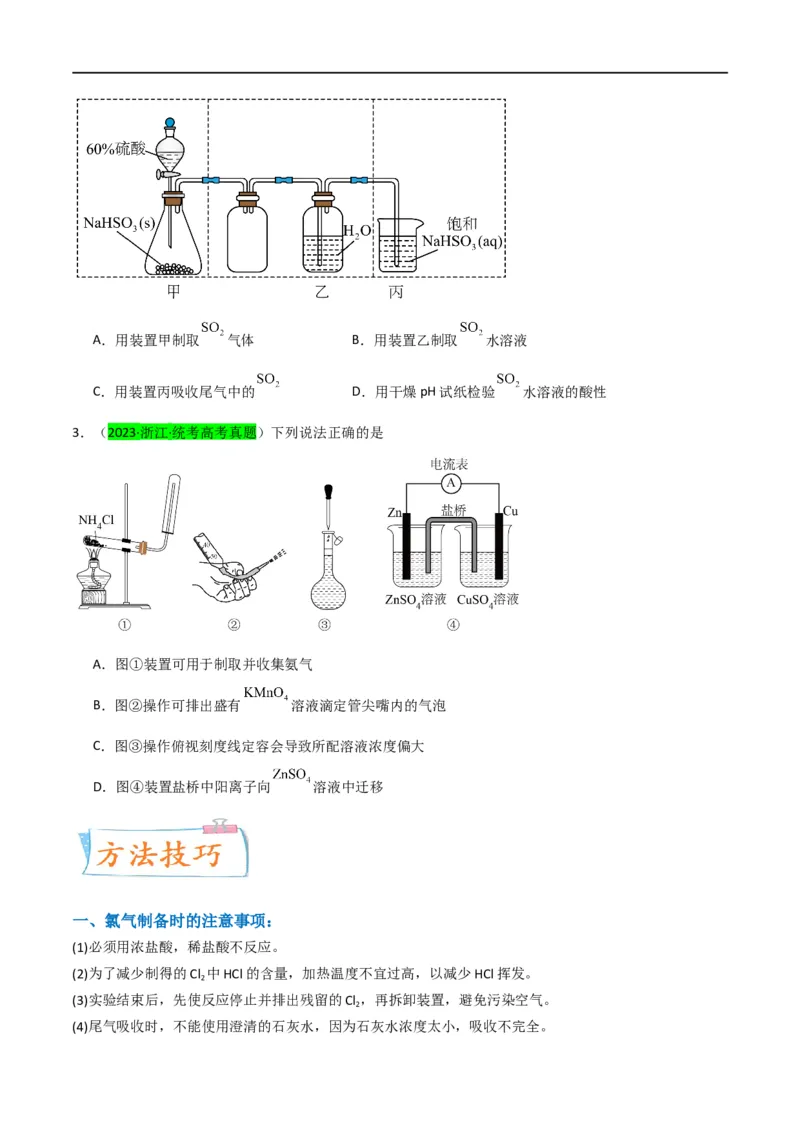
2.(2022·江苏·高考真题)实验室制取少量 水溶液并探究其酸性,下列实验装置和操作不能达到实验
目的的是A.用装置甲制取 气体 B.用装置乙制取 水溶液
C.用装置丙吸收尾气中的 D.用干燥pH试纸检验 水溶液的酸性
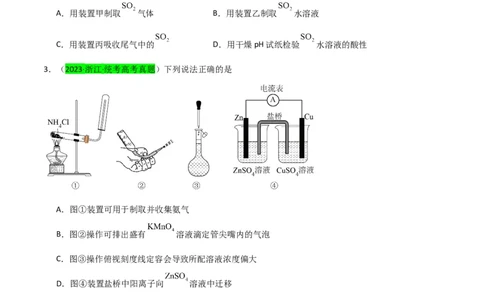
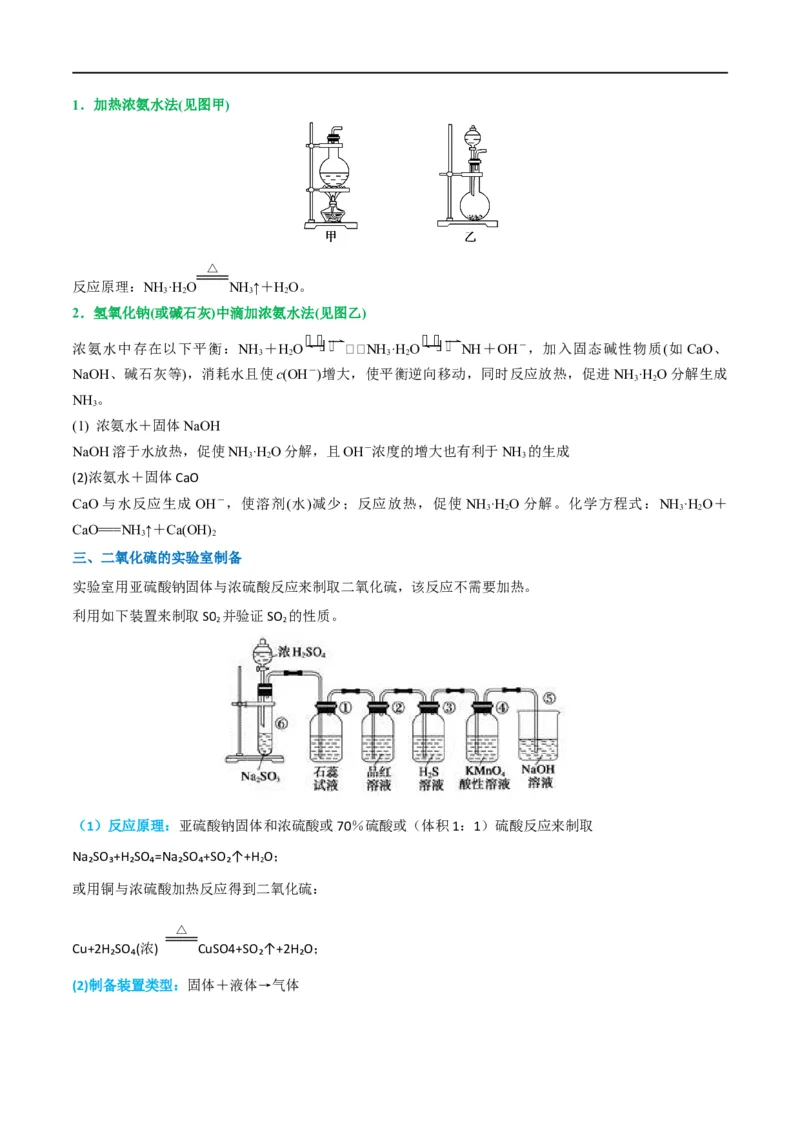
3.(2023·浙江·统考高考真题)下列说法正确的是
A.图①装置可用于制取并收集氨气
B.图②操作可排出盛有 溶液滴定管尖嘴内的气泡
C.图③操作俯视刻度线定容会导致所配溶液浓度偏大
D.图④装置盐桥中阳离子向 溶液中迁移
一、氯气制备时的注意事项:
(1)必须用浓盐酸,稀盐酸不反应。
(2)为了减少制得的Cl 中HCl的含量,加热温度不宜过高,以减少HCl挥发。
2
(3)实验结束后,先使反应停止并排出残留的Cl ,再拆卸装置,避免污染空气。
2
(4)尾气吸收时,不能使用澄清的石灰水,因为石灰水浓度太小,吸收不完全。二、氨气制备时的注意事项:
(1)制氨时,选用的铵盐及碱都有一定的要求。选铵盐时,不选(NH ) CO 、NH HCO 、NH NO 等,因它们受
4 2 3 4 3 4 3
热易分解,使产生的NH 中混有较多的杂质气体,另外NH NO 易爆炸;选碱时,用Ca(OH) 而不用NaOH
3 4 3 2
或KOH,因NaOH、KOH具有吸湿性,易结块,不利于产生氨气,且在高温下均能腐蚀玻璃。
(2)干燥氨气不能用浓硫酸,也不能用无水CaCl (8NH +CaCl ===CaCl ·8NH ),通常用碱石灰干燥氨气。
2 3 2 2 3
三、二氧化硫制备时的注意事项:
由于SO₂易溶于水,所以应选用浓H₂SO₄和Na₂SO₃(s)反应,反应是在固体和液体之间, Na₂SO₃(s)为
粉末状,为控制反应速率,浓H₂SO₄应从分液漏斗中逐滴滴下。
浓盐酸是不能采用的,因为其中含有大量的水(常温常压下,质量分数最大的浓盐酸为 45%的浓盐酸),
否则会有大量的SO₂(溶解在水中.
18.0mol·L-1的浓H₂SO₄(即质量分数为98%的浓H₂SO₄)也不能采用,因为其中缺少水分,硫酸并未电离,
仍以分子形式存在,而Na₂SO₃(s)与H₂SO₄的反应是在H₂SO₄电离成离子的状态下才能顺利进行的.故通
常采用体积比为1∶1的浓H₂SO₄或70%硫酸。
Cl 、NH 、SO 的实验室制备与应用
2 3 2
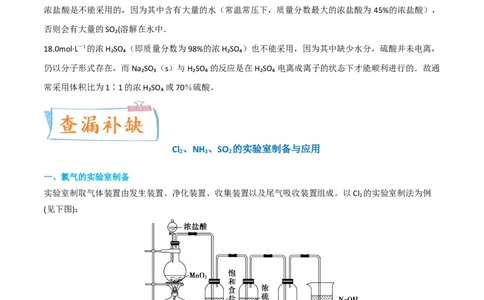
一、氯气的实验室制备
实验室制取气体装置由发生装置、净化装置、收集装置以及尾气吸收装置组成。以Cl 的实验室制法为例
2
(见下图):
(1)反应原理:用MnO (或其他强氧化剂,如KMnO 、K Cr O 、KClO 等)氧化浓盐酸。
2 4 2 2 7 3
其他制取Cl 的原理:
2
△
MnO +4HCl(浓) MnCl +Cl ↑+2H O
2 2 2 2
①14HCl+K Cr O ===2KCl+2CrCl +7H O+3Cl ↑
2 2 7 3 2 2
②16HCl+2KMnO ===2KCl+2MnCl +8H O+5Cl ↑
4 2 2 2③6HCl(浓)+KClO ===KCl+3H O+3Cl ↑
3 2 2
④4HCl+Ca(ClO) ===CaCl +2H O+2Cl ↑
2 2 2 2
2NaCl+3H₂SO₄(浓)+MnO₂==2NaHSO₄+MnSO₄+2H₂O+Cl₂↑
其中,①②④使用稀盐酸就可发生反应产生氯气。
(2)制备装置类型:固体+液体 气体
(3)净化方法:用 _ 饱和食盐水 除去HCl,再用浓硫酸除去水蒸气。
(4)收集气体:向上排空气法或排饱和食盐水法。
(5)尾气吸收:用强碱溶液(如NaOH溶液)吸收,不用Ca(OH) 溶液吸收的原因是Ca(OH) 溶解度小,溶液浓
2 2
度低,吸收不完全。
(6)验满方法:
①将湿润的淀粉碘化钾试纸靠近盛Cl 的集气瓶口,观察到试纸立即变蓝,则证明已集满。
2
②将湿润的蓝色石蕊试纸靠近盛Cl 的集气瓶口,观察到试纸先变红后褪色,则证明已集满。
2
③实验室制取Cl 时,常常根据集气瓶中气体的颜色判断是否集满。
2
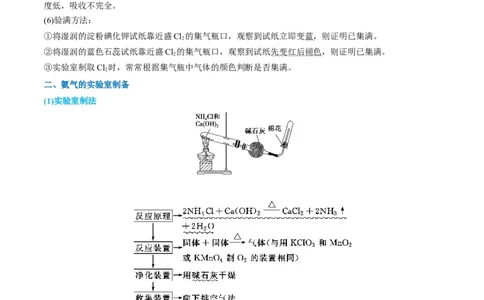
二、氨气的实验室制备
(1)实验室制法
(2)实验室制取少量氨气的两种简易方法1.加热浓氨水法(见图甲)
△
反应原理:NH ·H O NH ↑+HO。
3 2 3 2
2.氢氧化钠(或碱石灰)中滴加浓氨水法(见图乙)
浓氨水中存在以下平衡:NH +HO NH ·H O NH+OH-,加入固态碱性物质(如CaO、
3 2 3 2
NaOH、碱石灰等),消耗水且使c(OH-)增大,使平衡逆向移动,同时反应放热,促进NH ·H O分解生成
3 2
NH 。
3
(1) 浓氨水+固体NaOH
NaOH溶于水放热,促使NH ·H O分解,且OH-浓度的增大也有利于NH 的生成
3 2 3
(2)浓氨水+固体CaO
CaO与水反应生成OH-,使溶剂(水)减少;反应放热,促使 NH ·H O分解。化学方程式:NH ·H O+
3 2 3 2
CaO===NH↑+Ca(OH)
3 2
三、二氧化硫的实验室制备
实验室用亚硫酸钠固体与浓硫酸反应来制取二氧化硫,该反应不需要加热。
利用如下装置来制取S0 并验证SO 的性质。
2 2
(1)反应原理:亚硫酸钠固体和浓硫酸或70%硫酸或(体积1:1)硫酸反应来制取
Na₂SO₃+H₂SO₄=Na₂SO₄+SO₂↑+H O;
2
或用铜与浓硫酸加热反应得到二氧化硫:
△
Cu+2H₂SO₄(浓) CuSO4+SO₂↑+2H₂O;
(2)制备装置类型:固体+液体→气体(3)净化方法:若制取的SO₂气体中含有HCl或HNO 气体,则需通过饱和NaHSO₃溶液除HCl或HNO,
3 3
再用浓硫酸除去水蒸气。
(4)收集气体:向上排空气法。
(5)尾气吸收:用强碱溶液(如NaOH溶液)吸收,不用Ca(OH) 溶液吸收的原因是Ca(OH) 溶解度小,溶液浓
2 2
度低,吸收不完全。
(6)验满方法:将湿润的品红试纸靠近盛SO₂的集气瓶口,观察到试纸立即褪色,则证明已集满。
(7)尾气处理:通入氢氧化钠溶液 2NaOH+SO₂=Na₂SO₃+H₂O。
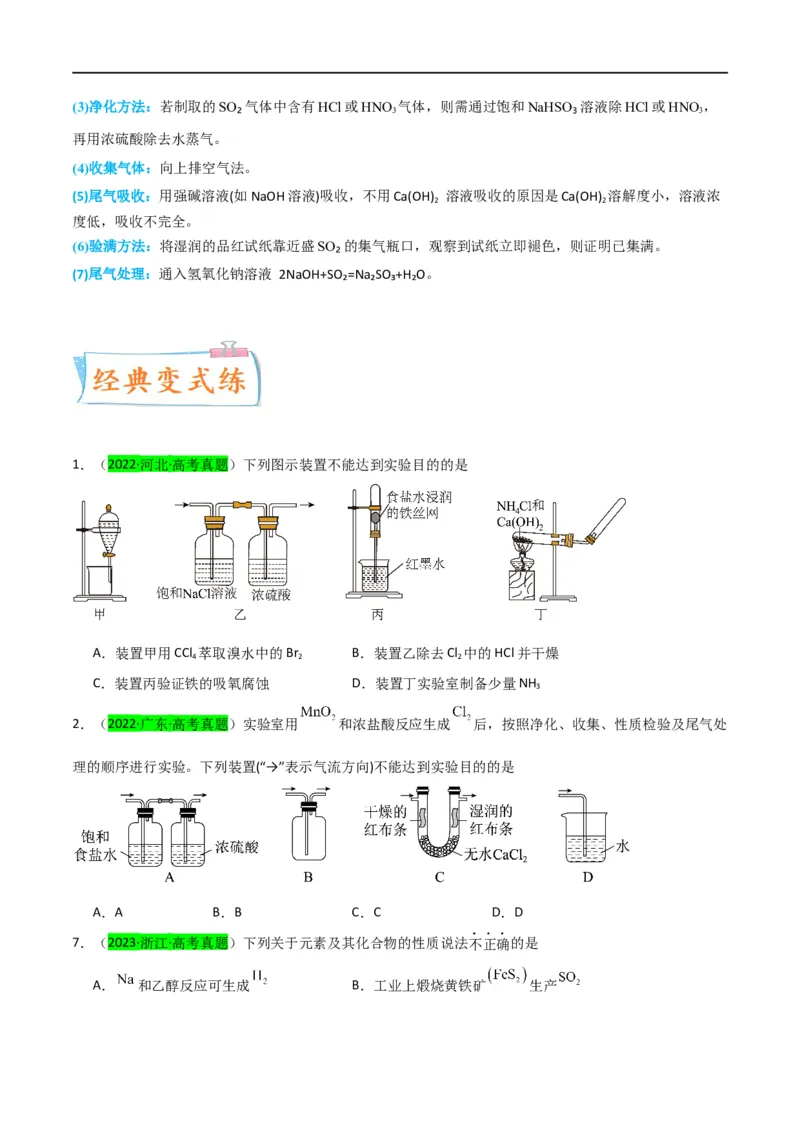
1.(2022·河北·高考真题)下列图示装置不能达到实验目的的是
A.装置甲用CCl 萃取溴水中的Br B.装置乙除去Cl 中的HCl并干燥
4 2 2
C.装置丙验证铁的吸氧腐蚀 D.装置丁实验室制备少量NH
3
2.(2022·广东·高考真题)实验室用 和浓盐酸反应生成 后,按照净化、收集、性质检验及尾气处
理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是
A.A B.B C.C D.D
7.(2023·浙江·高考真题)下列关于元素及其化合物的性质说法不正确的是
A. 和乙醇反应可生成 B.工业上煅烧黄铁矿 生产C.工业上用氨的催化氧化制备 D.常温下铁与浓硝酸反应可制备
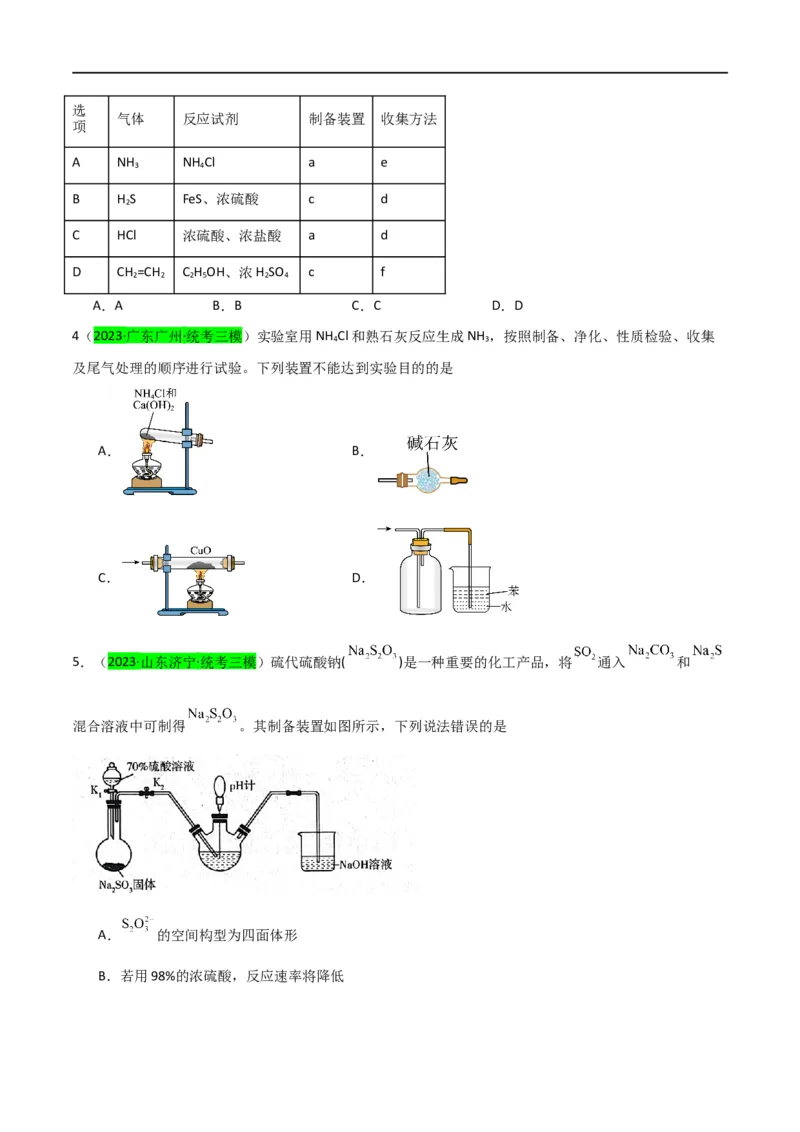
1.(2023·江苏·统考二模)实验小组利用如图所示装置制备氯酸钠。下列实验装置和操作不能达到实验目
的的是
A.用装置甲制备氯气 B.用装置乙处理余氯
C.用装置丙除去氯化氢 D.用装置戊检验氯气
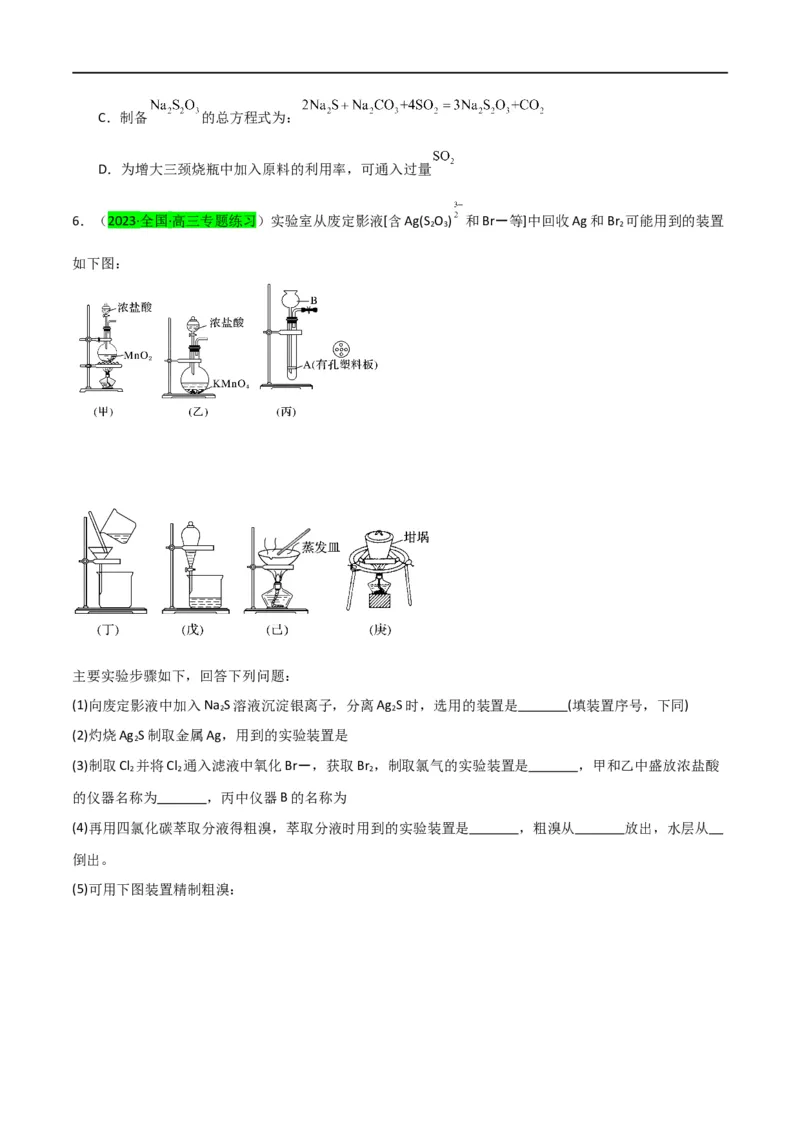
2.(2023秋·广东梅州·高三丰顺县丰顺中学校考期末)下列图示实验正确的是
A.制备氯气 B.实验室快速制备NH
3
C.收集NO 并防止其污染环境 D.制备并观察Fe(OH) 的颜色
2 2
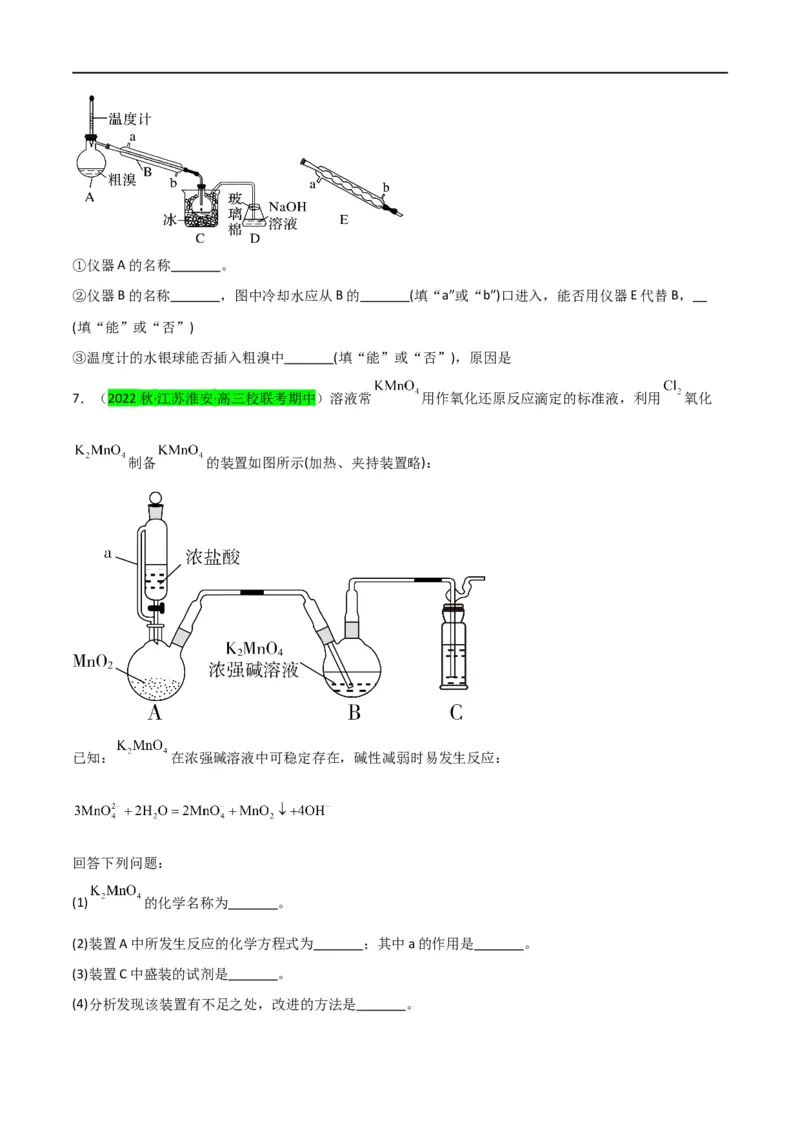
3.(2022秋·广东惠州·高三统考阶段练习)实验室制取下列气体,所选反应试剂、制备装置与收集方法合
理的是选
气体 反应试剂 制备装置 收集方法
项
A NH NH Cl a e
3 4
B H S FeS、浓硫酸 c d
2
C HCl 浓硫酸、浓盐酸 a d
D CH =CH C H OH、浓H SO c f
2 2 2 5 2 4
A.A B.B C.C D.D
4(2023·广东广州·统考三模)实验室用NH Cl和熟石灰反应生成NH ,按照制备、净化、性质检验、收集
4 3
及尾气处理的顺序进行试验。下列装置不能达到实验目的的是
A. B.
C. D.
5.(2023·山东济宁·统考三模)硫代硫酸钠( )是一种重要的化工产品,将 通入 和
混合溶液中可制得 。其制备装置如图所示,下列说法错误的是
A. 的空间构型为四面体形
B.若用98%的浓硫酸,反应速率将降低C.制备 的总方程式为:
D.为增大三颈烧瓶中加入原料的利用率,可通入过量
6.(2023·全国·高三专题练习)实验室从废定影液[含Ag(S O ) 和Br-等]中回收Ag和Br 可能用到的装置
2 3 2
如下图:
主要实验步骤如下,回答下列问题:
(1)向废定影液中加入Na S溶液沉淀银离子,分离Ag S时,选用的装置是 (填装置序号,下同)
2 2
(2)灼烧Ag S制取金属Ag,用到的实验装置是
2
(3)制取Cl 并将Cl 通入滤液中氧化Br-,获取Br ,制取氯气的实验装置是 ,甲和乙中盛放浓盐酸
2 2 2
的仪器名称为 ,丙中仪器B的名称为
(4)再用四氯化碳萃取分液得粗溴,萃取分液时用到的实验装置是 ,粗溴从 放出,水层从
倒出。
(5)可用下图装置精制粗溴:①仪器A的名称 。
②仪器B的名称 ,图中冷却水应从B的 (填“a”或“b”)口进入,能否用仪器E代替B,
(填“能”或“否”)
③温度计的水银球能否插入粗溴中 (填“能”或“否”),原因是
7.(2022秋·江苏淮安·高三校联考期中)溶液常 用作氧化还原反应滴定的标准液,利用 氧化
制备 的装置如图所示(加热、夹持装置略):
已知: 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
回答下列问题:
(1) 的化学名称为 。
(2)装置A中所发生反应的化学方程式为 ;其中a的作用是 。
(3)装置C中盛装的试剂是 。
(4)分析发现该装置有不足之处,改进的方法是 。(5)为测定某 固体的纯度,现用 的酸性 溶液进行滴定。(已知:
)称取 固体溶于水配成500mL溶液,取
溶液置于锥形瓶中,用 溶液滴定至终点,消耗 溶液V mL。滴定终点的现
象为 , 固体的纯度为 。
1.(2023·江苏扬州·扬州中学校考模拟预测)氯及其化合物应用广泛。氯的单质Cl 可由MnO 与浓盐酸共
2 2
热得到,Cl 能氧化Br-,可从海水中提取Br ;氯的氧化物ClO 可用于自来水消毒,ClO 是一种黄绿色气体,
2 2 2 2
易溶于水,与碱反应会生成ClO 与ClO ;亚氯酸钠(NaClO )是一种高效漂白剂和氧化剂。实验室欲由下列
2
装置制取高浓度的HClO溶液,有关实验装置和原理能达到各自实验目的的是
A. 制取氯气 B. 制取氯水
C. 提高HClO浓度 D. 分离HClO
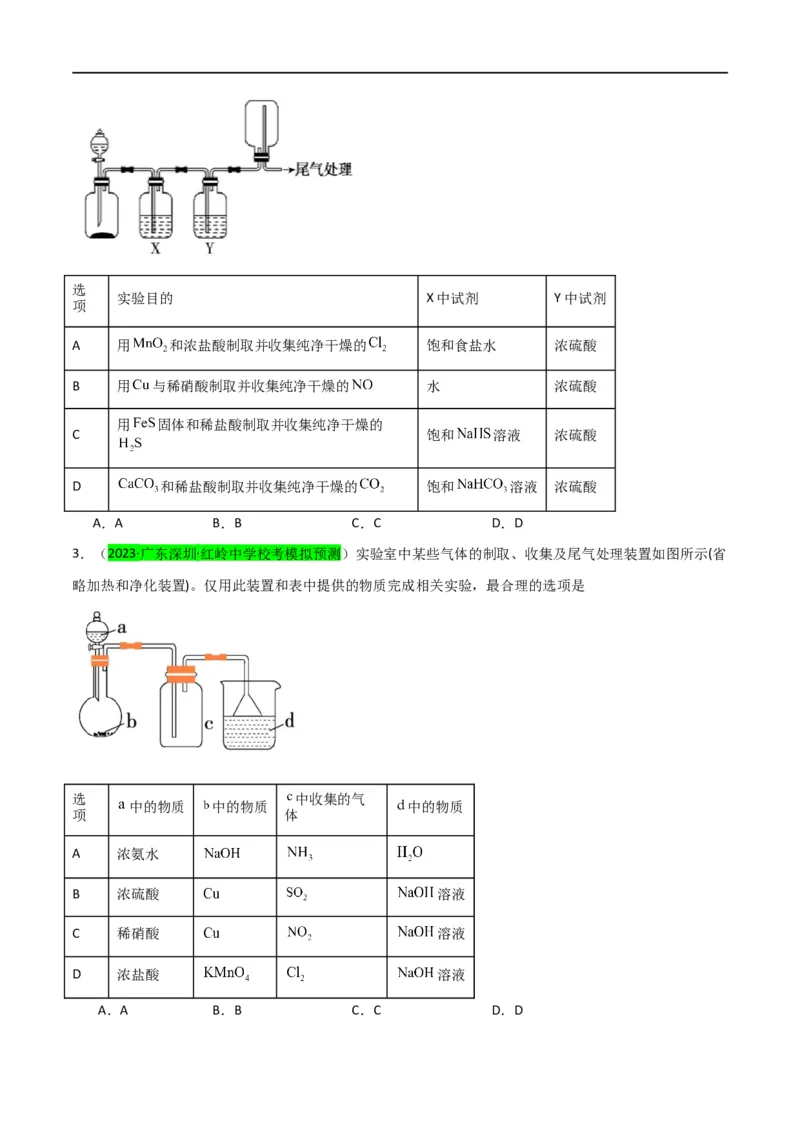
2.(2023春·北京海淀·高三首都师范大学附属中学校考阶段练习)利用如图装置可以进行实验并能达到实
验目的的是选
实验目的 X中试剂 Y中试剂
项
A 用 和浓盐酸制取并收集纯净干燥的 饱和食盐水 浓硫酸
B 用 与稀硝酸制取并收集纯净干燥的 水 浓硫酸
用 固体和稀盐酸制取并收集纯净干燥的
C 饱和 溶液 浓硫酸
D 和稀盐酸制取并收集纯净干燥的 饱和 溶液 浓硫酸
A.A B.B C.C D.D
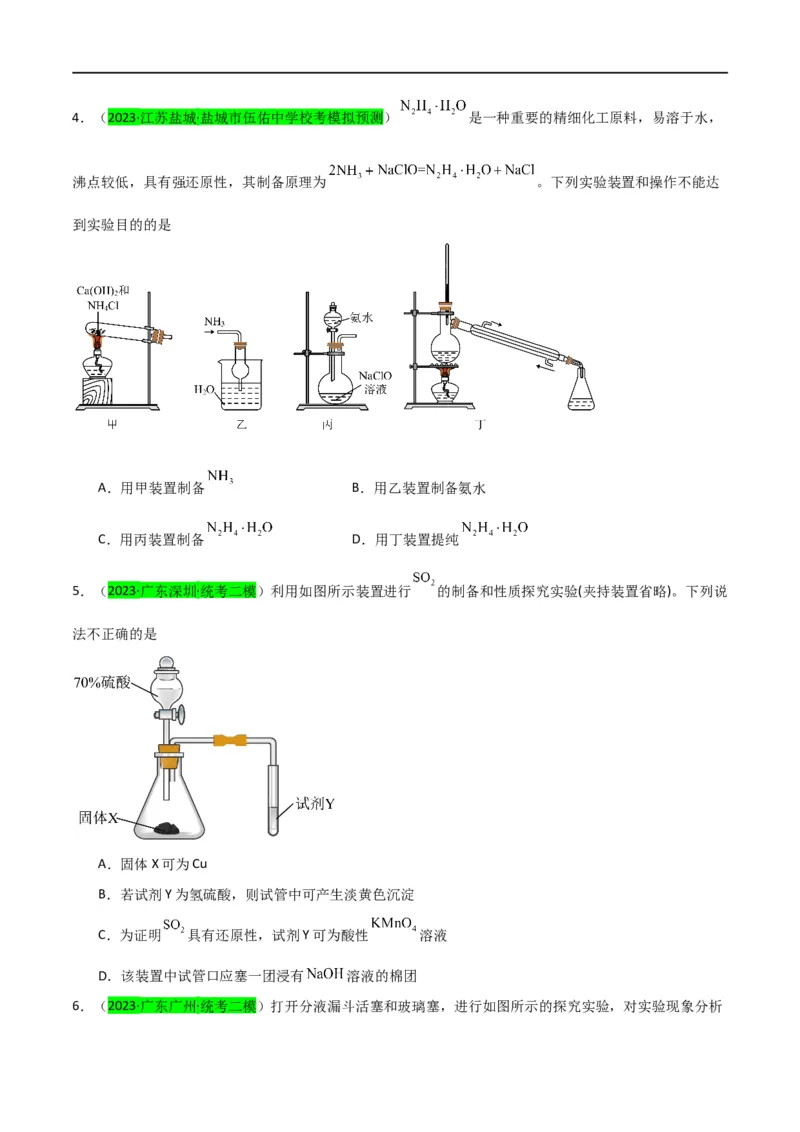
3.(2023·广东深圳·红岭中学校考模拟预测)实验室中某些气体的制取、收集及尾气处理装置如图所示(省
略加热和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是
选 中收集的气
中的物质 中的物质 中的物质
项 体
A 浓氨水
B 浓硫酸 溶液
C 稀硝酸 溶液
D 浓盐酸 溶液
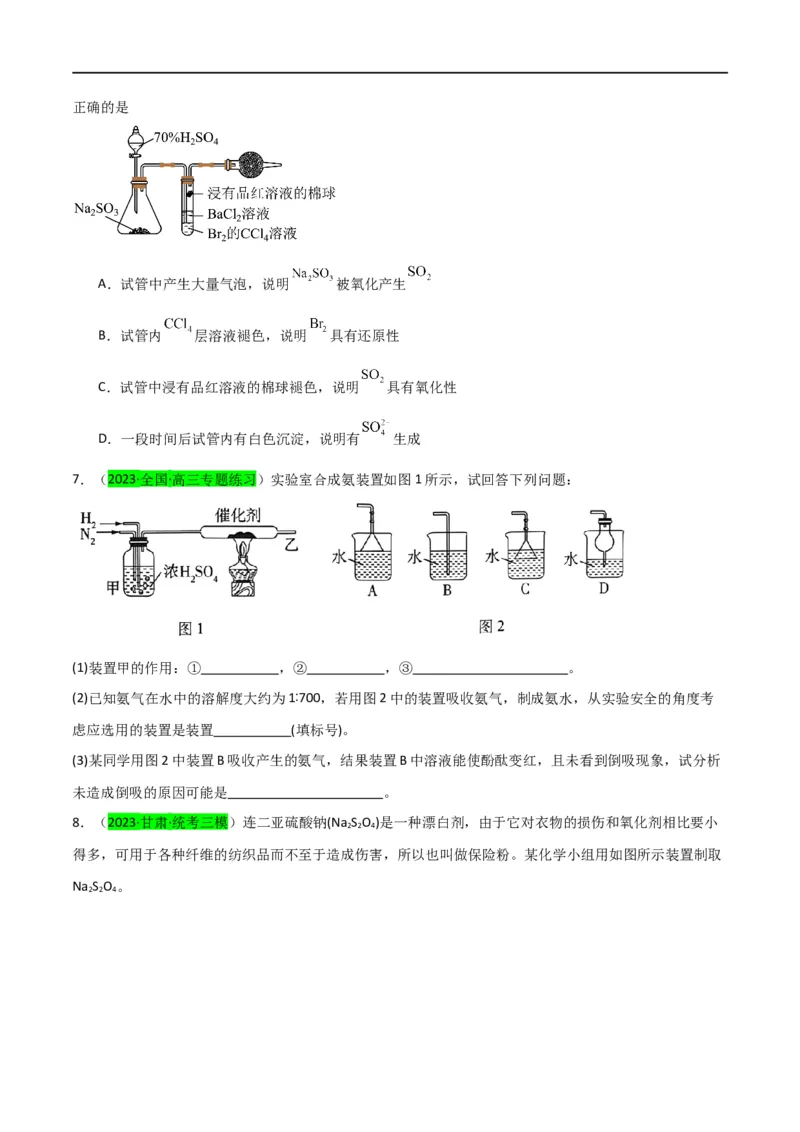
A.A B.B C.C D.D4.(2023·江苏盐城·盐城市伍佑中学校考模拟预测) 是一种重要的精细化工原料,易溶于水,
沸点较低,具有强还原性,其制备原理为 。下列实验装置和操作不能达
到实验目的的是
A.用甲装置制备 B.用乙装置制备氨水
C.用丙装置制备 D.用丁装置提纯
5.(2023·广东深圳·统考二模)利用如图所示装置进行 的制备和性质探究实验(夹持装置省略)。下列说
法不正确的是
A.固体X可为Cu
B.若试剂Y为氢硫酸,则试管中可产生淡黄色沉淀
C.为证明 具有还原性,试剂Y可为酸性 溶液
D.该装置中试管口应塞一团浸有 溶液的棉团
6.(2023·广东广州·统考二模)打开分液漏斗活塞和玻璃塞,进行如图所示的探究实验,对实验现象分析正确的是
A.试管中产生大量气泡,说明 被氧化产生
B.试管内 层溶液褪色,说明 具有还原性
C.试管中浸有品红溶液的棉球褪色,说明 具有氧化性
D.一段时间后试管内有白色沉淀,说明有 生成
7.(2023·全国·高三专题练习)实验室合成氨装置如图1所示,试回答下列问题:
(1)装置甲的作用:① ,② ,③ 。
(2)已知氨气在水中的溶解度大约为1∶700,若用图2中的装置吸收氨气,制成氨水,从实验安全的角度考
虑应选用的装置是装置 (填标号)。
(3)某同学用图2中装置B吸收产生的氨气,结果装置B中溶液能使酚酞变红,且未看到倒吸现象,试分析
未造成倒吸的原因可能是 。
8.(2023·甘肃·统考三模)连二亚硫酸钠(Na S O )是一种漂白剂,由于它对衣物的损伤和氧化剂相比要小
2 2 4
得多,可用于各种纤维的纺织品而不至于造成伤害,所以也叫做保险粉。某化学小组用如图所示装置制取
Na S O 。
2 2 4已知:连二亚硫酸钠不溶于醇,遇水会分解,在碱性介质中较稳定。
(1)装置a、c中能保持恒压,原因是 。
(2)单向阀的作用是防止倒吸,下列装置不能代替单向阀的是 (填字母)。
(3)制备前应先打开恒压滴液漏斗 (填“a”或“c”)的活塞;在A、B和C、D之间都应添加一个装置,
该装置的作用是 。
(4)已知亚硫酸的结构式为 ,则S O 的结构式为 ,其中S元素的化合价为 价。
2
(5)制备时打开B装置的活塞,向三颈烧瓶中滴加 (填“少量”或“过量”)的NaOH溶液;写出生成
Na S O 的化学方程式[甲酸被氧化为CO ]: 。
2 2 4 2
(6)制备结束后,过滤,用 洗涤,干燥,制得Na S O 。
2 2 4