文档内容
第 36 讲 物质的聚集状态 常见晶体类型
[复习目标] 1.了解晶体和非晶体的区别。2.了解常见晶体的类型,了解不同类型晶体中结
构微粒、微粒间作用力的区别。3.了解分子晶体、 共价晶体、 离子晶体、金属晶体结构与
性质的关系。4.了解四种晶体类型熔点、沸点、溶解性等性质的不同。
考点一 物质的聚集状态 晶体与非晶体
1.物质的聚集状态
(1)物质的聚集状态除了固态、液态、气态,还有________、________以及介乎________和
____________之间的塑晶态、液晶态等。
(2)等离子体和液晶
①等离子体:由________、________和电中性粒子组成的整体上呈电中性的物质聚集体。具
有良好的导电性和流动性。
②液晶:介于液态和晶态之间的物质状态。既具有液体的流动性、黏度、形变性等,又具有
晶体的导热性、光学性质等。
2.晶体与非晶体
(1)晶体与非晶体的比较
晶体 非晶体
结构特征 原子在三维空间里呈___________排列 原子排列____________
自范性
性质
熔点
特征
异同表现
(2)得到晶体的途径
①熔融态物质凝固;②气态物质冷却不经液态直接凝固(凝华);
③溶质从溶液中析出。
(3)晶体与非晶体的测定方法
①测熔点:晶体有固定的熔点,非晶体没有固定的熔点。
②最可靠方法:对固体进行____________实验。
1.在物质的三态相互转化过程中只是分子间距离发生了变化( )
2.晶体和非晶体的本质区别是晶体中粒子在微观空间里呈现周期性的有序排列( )
3.晶体的熔点一定比非晶体的熔点高( )
4.具有规则几何外形的固体一定是晶体( )
5.缺角的NaCl晶体在饱和NaCl溶液中会慢慢变为完美的立方体块( )
一、物质聚集状态的多样性
1.下列有关物质特殊聚集状态与结构的说法不正确的是( )
A.液晶中分子的长轴取向一致,表现出类似晶体的各向异性
B.等离子体是一种特殊的气体,由阳离子和电子两部分构成
C.纯物质有固定的熔点,但其晶体颗粒尺寸在纳米量级时也可能发生变化
D.超分子内部的分子间一般通过非共价键或分子间作用力结合成聚集体
2.水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到 165 K时形成的。
玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,下列有关玻璃
态水的叙述正确的是( )
A.水由液态变为玻璃态,体积缩小
B.水由液态变为玻璃态,体积膨胀
C.玻璃态是水的一种特殊状态
D.在玻璃态水的X射线图谱上有分立的斑点或明锐的衍射峰
二、晶体与非晶体的区别
3.下列关于晶体和非晶体的说法正确的是( )
A.晶体在三维空间里呈周期性有序排列,因此在各个不同的方向上具有相同的物理性质
B.晶体在熔化过程中需要不断地吸热,温度不断地升高
C.普通玻璃在各个不同的方向上力学、热学、电学、光学性质相同
D.晶体和非晶体之间不可以相互转化
4.玻璃是常见的非晶体,在生产生活中有着广泛的用途,如图是玻璃的结构示意图,下列
有关玻璃的说法错误的是( )A.玻璃内部微粒排列是无序的
B.玻璃熔化时吸热,温度不断上升
C.光导纤维和玻璃的主要成分都可看成是SiO,二者都是非晶体
2
D.利用X射线衍射实验可以鉴别石英玻璃和水晶
考点二 常见晶体类型
1.四种常见晶体类型的比较
类型
分子晶体 共价晶体 金属晶体 离子晶体
比较
金属阳离子、自
构成微粒
由电子
微粒间的相互 ______________
作用力 (某些含氢键)
有的很大,有的
硬度 较小
很小
有的很高,有的
熔、沸点 较低 较高
很低
一般不溶于水, 大多易溶于水等
溶解性 相似相溶 难溶于一般溶剂
少数与水反应 极性溶剂
一般不具有导电 晶体不导电,水
一般不导电,溶
导电、导热性 性,个别为半导 电和热的良导体 溶液或熔融态导
于水后有的导电
体 电
2.常见晶体的结构模型
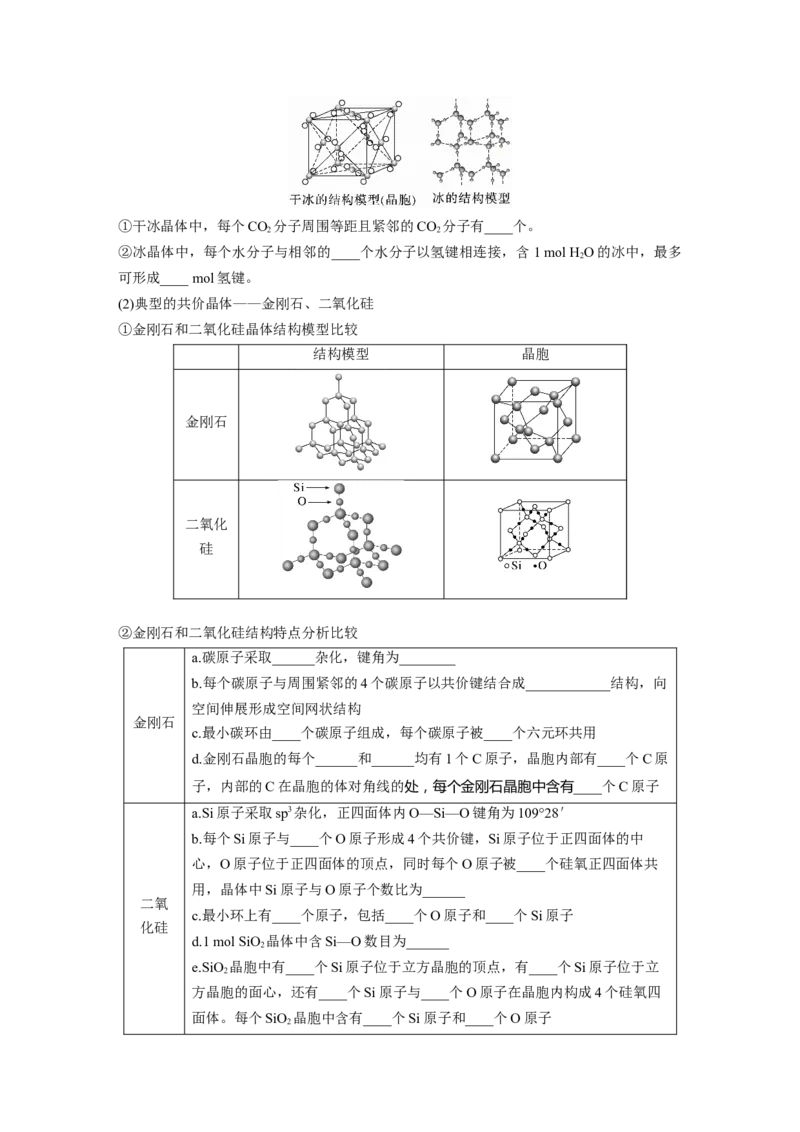
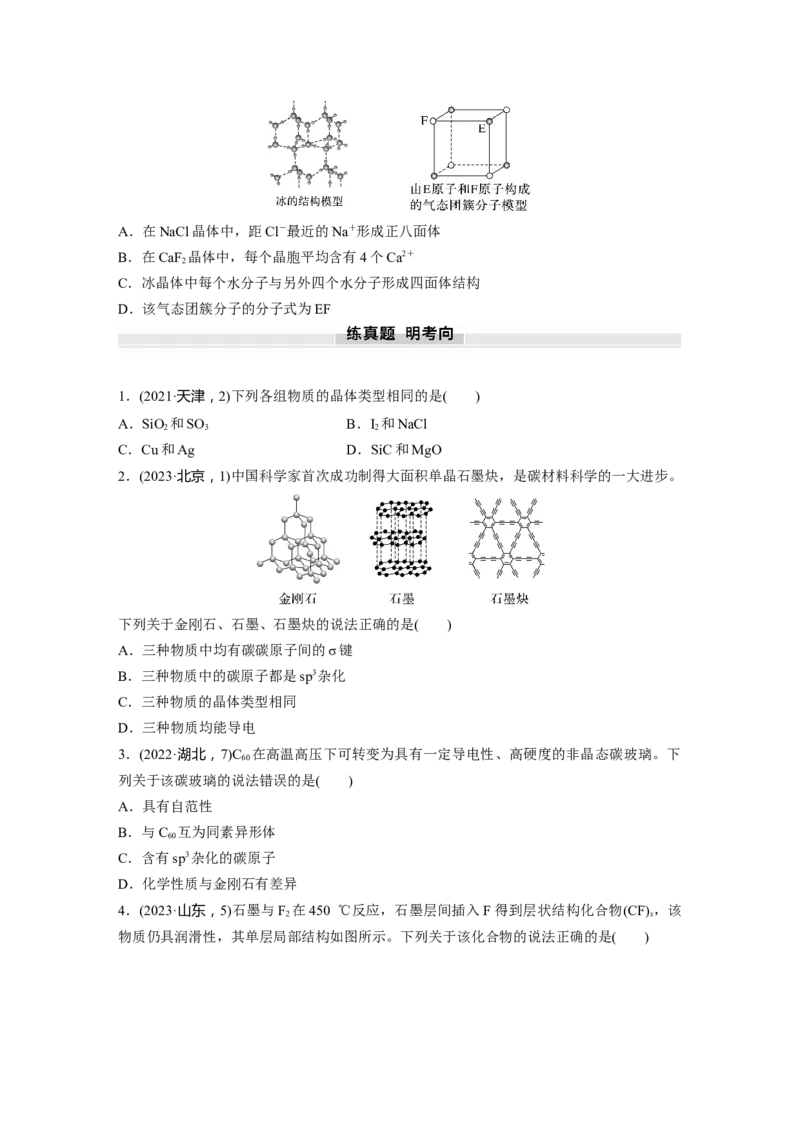
(1)典型的分子晶体——干冰和冰①干冰晶体中,每个CO 分子周围等距且紧邻的CO 分子有____个。
2 2
②冰晶体中,每个水分子与相邻的____个水分子以氢键相连接,含1 mol H O的冰中,最多
2
可形成____ mol氢键。
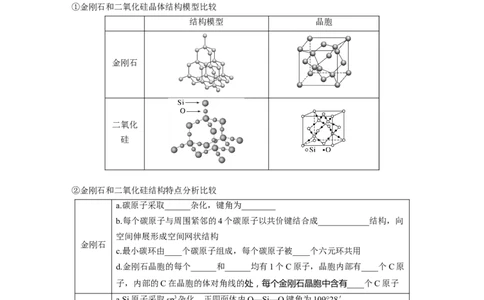
(2)典型的共价晶体——金刚石、二氧化硅
①金刚石和二氧化硅晶体结构模型比较
结构模型 晶胞
金刚石
二氧化
硅
②金刚石和二氧化硅结构特点分析比较
a.碳原子采取______杂化,键角为________
b.每个碳原子与周围紧邻的4个碳原子以共价键结合成____________结构,向
空间伸展形成空间网状结构
金刚石
c.最小碳环由____个碳原子组成,每个碳原子被____个六元环共用
d.金刚石晶胞的每个______和______均有1个C原子,晶胞内部有____个C原
子,内部的C在晶胞的体对角线的处,每个金刚石晶胞中含有____个C原子
a.Si原子采取sp3杂化,正四面体内O—Si—O键角为109°28′
b.每个Si原子与____个O原子形成4个共价键,Si原子位于正四面体的中
心,O原子位于正四面体的顶点,同时每个O原子被____个硅氧正四面体共
用,晶体中Si原子与O原子个数比为______
二氧
c.最小环上有____个原子,包括____个O原子和____个Si原子
化硅
d.1 mol SiO 晶体中含Si—O数目为______
2
e.SiO 晶胞中有____个Si原子位于立方晶胞的顶点,有____个Si原子位于立
2
方晶胞的面心,还有____个Si原子与____个O原子在晶胞内构成4个硅氧四
面体。每个SiO 晶胞中含有____个Si原子和____个O原子
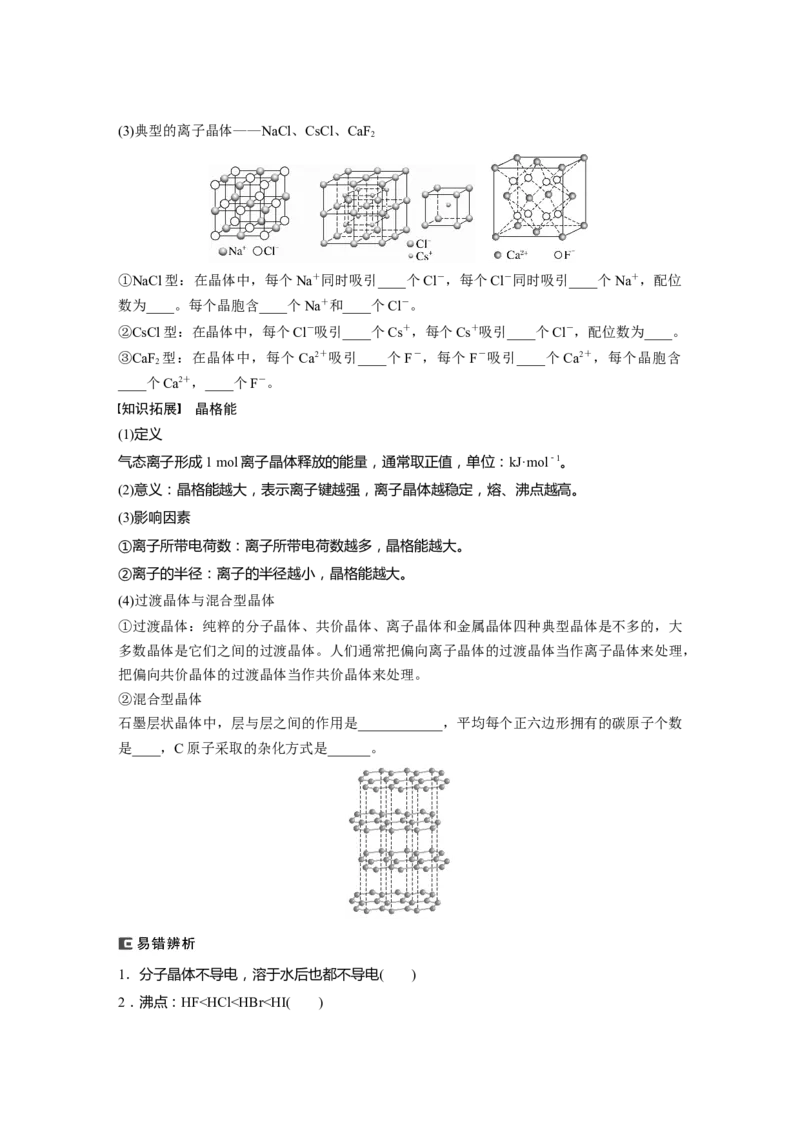
2(3)典型的离子晶体——NaCl、CsCl、CaF
2
①NaCl型:在晶体中,每个Na+同时吸引____个Cl-,每个Cl-同时吸引____个Na+,配位
数为____。每个晶胞含____个Na+和____个Cl-。
②CsCl型:在晶体中,每个Cl-吸引____个Cs+,每个Cs+吸引____个Cl-,配位数为____。
③CaF 型:在晶体中,每个 Ca2+吸引____个F-,每个F-吸引____个Ca2+,每个晶胞含
2
____个Ca2+,____个F-。
知识拓展 晶格能
(1)定义
气态离子形成1 mol离子晶体释放的能量,通常取正值,单位:kJ·mol-1。
(2)意义:晶格能越大,表示离子键越强,离子晶体越稳定,熔、沸点越高。
(3)影响因素
①离子所带电荷数:离子所带电荷数越多,晶格能越大。
②离子的半径:离子的半径越小,晶格能越大。
(4)过渡晶体与混合型晶体
①过渡晶体:纯粹的分子晶体、共价晶体、离子晶体和金属晶体四种典型晶体是不多的,大
多数晶体是它们之间的过渡晶体。人们通常把偏向离子晶体的过渡晶体当作离子晶体来处理,
把偏向共价晶体的过渡晶体当作共价晶体来处理。
②混合型晶体
石墨层状晶体中,层与层之间的作用是____________,平均每个正六边形拥有的碳原子个数
是____,C原子采取的杂化方式是______。
1.分子晶体不导电,溶于水后也都不导电( )
2.沸点:HF3 550 2 600 1 415
金刚石熔点比晶体硅熔点高的原因是______________________________________________
______________________________________________________________________________。
答题规范(6) 晶体熔、沸点高低原因解释
1.不同类型晶体熔、沸点比较
答题模板:×××为×××晶体,而×××为×××晶体。
例1 (1)金刚石的熔点比NaCl高,原因是_________________________________________
______________________________________________________________________________。
(2)SiO 的熔点比CO 高,原因是_________________________________________________
2 2
______________________________________________________________________________。
2.同类型晶体熔、沸点比较
(1)分子晶体
答题模板:
①同为分子晶体,×××存在氢键,而×××仅存在较弱的范德华力。
②同为分子晶体,×××的相对分子质量大,范德华力强,熔、沸点高。
③同为分子晶体,两者的相对分子质量相同(或相近),×××的极性大,熔、沸点高。
④同为分子晶体,×××形成分子间氢键,而×××形成的则是分子内氢键,分子间氢键会
使熔、沸点升高。
例2 (1)NH 的沸点比PH 高,原因是____________________________________________
3 3
______________________________________________________________________________。
(2)CO 比CS 的熔、沸点低,原因是______________________________________________
2 2
______________________________________________________________________________。(3)CO比N 的熔、沸点高,原因是_______________________________________________
2
______________________________________________________________________________。
(4) 的沸点比 高,原因是___________________________
_______________________________________________________________________________
_______________________________________________________________________________
。
(2)共价晶体
答题模板:同为共价晶体,×××晶体的键长短,键能大,熔、沸点高。
例3 Si单质比化合物SiC的熔点低,理由是_______________________________________
_______________________________________________________________________________
。
(3)离子晶体
答题模板:
①阴、阳离子电荷数相等,则看阴、阳离子半径:
同为离子晶体,Rn-(或Mn+)半径小于Xn-(或Nn+),故×××晶体离子键强(或晶格能大),
熔、沸点高。
②阴离子(或阳离子)电荷数不相等,阴离子(或阳离子)半径不相同:
同为离子晶体,Rn-(或Mn+)半径小于Xm-(或Nm+),Rn-(或Mn+)电荷数大于Xm-(或Nm+),
故×××晶体离子键强(或晶格能大),熔、沸点高。
例4 (1)ZnO和ZnS的晶体结构相似,熔点较高的是ZnO,理由是_____________________
_______________________________________________________________________________
。
(2)FeO的熔点小于Fe O 的熔点,原因是___________________________________________
2 3
_______________________________________________________________________________
_______________________________________________________________________________
。
1.FeF 具有较高的熔点(高于1 000 ℃),其化学键类型是________,FeBr 的相对分子质量
3 3
大 于 FeF , 但 其 熔 点 只 有 200 ℃ , 原 因 是
3
_____________________________________________
_______________________________________________________________________________
。
2.已知:KO 的熔点为 770 ℃,NaO 的熔点为 1 275 ℃,二者的晶体类型均为
2 2
____________ , KO 的 熔 点 低 于 NaO 的 原 因 是
2 2
__________________________________________________________________________________________________________________________________
。
3.已知氨(NH ,熔点:-77.8 ℃、沸点:-33.5 ℃),联氨(N H ,熔点:2 ℃、沸点:
3 2 4
113.5 ℃) , 解 释 其 熔 、 沸 点 高 低 的 主 要 原 因 :
_________________________________________________
_______________________________________________________________________________
。
4.已知氮化硼与砷化镓属于同种晶体类型。则两种晶体熔点较高的是__________(填化学
式 ) , 其 理 由 是
________________________________________________________________________
_______________________________________________________________________________
。
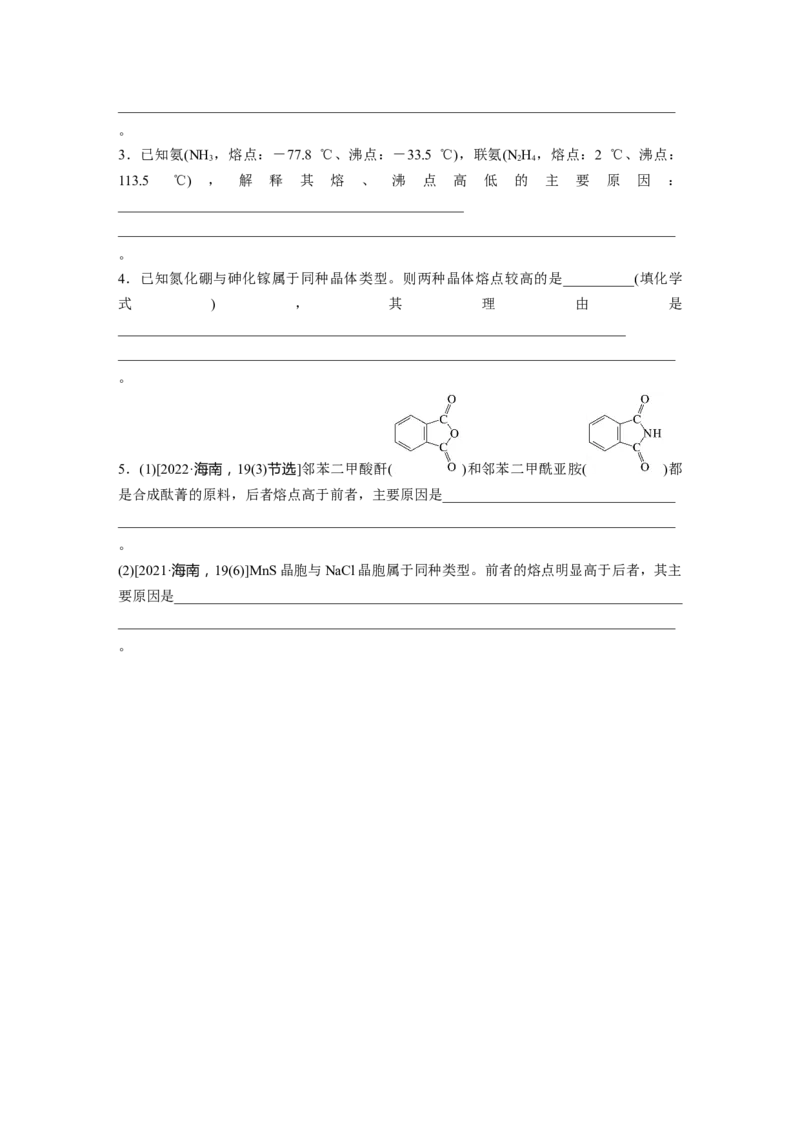
5.(1)[2022·海南,19(3)节选]邻苯二甲酸酐( )和邻苯二甲酰亚胺( )都
是合成酞菁的原料,后者熔点高于前者,主要原因是_________________________________
_______________________________________________________________________________
。
(2)[2021·海南,19(6)]MnS晶胞与NaCl晶胞属于同种类型。前者的熔点明显高于后者,其主
要原因是________________________________________________________________________
_______________________________________________________________________________
。