文档内容
专题 02 海水中的重要元素——钠和氯
第 04 练 钠及其化合物
1.保存少量金属钠的方法是( )
A.放在棕色瓶中 B.放在CCl 中 C.放在水中 D.放在煤油中
4
2.可用于治疗胃酸过多的物质是( )
A.碳酸氢钠 B.氯化钠 C.氯化钾 D.氢氧化钠
3.常用作调味品且具有防腐作用的物质是( )
A.碳酸氢钠 B.碳酸钠 C.氯化钠 D.谷氨酸钠
4.钠着火不能用二氧化碳灭火。钠在二氧化碳中燃烧生成炭黑和一种白色固体,它可能是( )
A. 碳酸钠 B. 硫酸钠 C. 碳酸氢钠 D. 氢氧化钠
5.NaO和NaO 具有的相似的性质是 ( )
2 2 2
A.颜色 B.水溶液的酸碱性 C.氧化性 D.漂白性
6.下列物质与NaCO 溶液不发生化学反应的是( )
2 3
A.CO B.NaOH C.BaCl D.稀HSO
2 2 2 4
7.下列各组物质与其用途的关系不正确的是( )
A.过氧化钠:供氧剂 B.烧碱:治疗胃酸过多的一种药剂
C.小苏打:发酵粉主要成分 D.纯碱:除物品上的油污
8.下列有关金属钠与水反应的现象描述不正确的是( )
A.钠熔成小球 B.钠沉入水底 C.钠四处游动 D.发出嘶嘶声
9.钠是人体必需的常量元素,下列说法正确的是( )
A. 钠的相对原子质量为11 g B. 钠原子在化学反应中易失电子
C. 钠由液态变为气态,微粒间间隔变小 D. 人体缺钠会导致甲状腺疾病
10.有关实验安全的叙述不正确的是( )
A.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗
B. 标准符号 示意“腐蚀性物质”
C.观察活泼金属与HO反应时,需要戴护目镜
2
D.金属钠着火时应立即用沙土盖灭
11.下列有关钠及其化合物说法不正确的是( )
A.实验室将Na保存在煤油中B.相同质量的NaCO 和NaHCO 分别与足量盐酸反应,NaHCO 放出CO 多
2 3 3 3 2
C.金属钠和氧气反应,条件不同,产物不同
D.过氧化钠是一种淡黄色的固体,是碱性氧化物
12.某物质在灼烧时透过蓝色钴玻璃看到火焰呈紫色,下列说法正确的是( )
A.该物质是钾单质 B.该物质是钾盐
C.该物质含有钾元素 D.该物质含有钾元素,不含钠元素
13.下列有关说法正确的是( )
A.为了除去NaCO 溶液中混有的少量NaHCO ,可以采用直接加热的方法
2 3 3
B.NaO 中阴阳离子个数比为1:1
2 2
C.常温时,NaCO 在水中的溶解度大于NaHCO
2 3 3
D.热稳定性:NaHCO 大于NaCO
3 2 3
14.下列关于碳酸钠和碳酸氢钠的比较中,正确的是( )
A.两者在水中的溶解度不同,碳酸氢钠的溶解度大于碳酸钠
B.两者热稳定性不同,碳酸钠的热稳定性小于碳酸氢钠
C.两者都能与盐酸反应放出二氧化碳气体,等质量时生成CO 的量一样多
2
D.两者都能和澄清石灰水反应,且现象一样
15.化学创造美好生活,下列相关说法错误的是( )
A.过氧化钠可用作呼吸面具的供氧剂
B.节日燃放的烟花的焰火,实质上是金属元素的焰色反应所呈现的色彩
C.为防止中秋月饼等富脂食品被氧化,常在包装袋中放入生石灰
D.红酒中的花青素在碱性环境下显蓝色,可用苏打粉检验假红酒
1.将绿豆粒大小的方形金属钠投入足量且含酚酞的水中,根据相应现象不能得出的结论是( )
选项 实验现象 结论
A 方形金属钠变成小球 钠反应速率快
B 钠浮于水面 水的密度大于钠
C 酚酞溶液变成红色 有NaOH生成
钠球游动,有“嘶嘶”的响
D 有气体生成
声
2.下列关于碳酸钠和碳酸氢钠的叙述,正确的是( )
A.常温时,在水中的溶解性:碳酸钠>碳酸氢钠B.热稳定性:碳酸钠<碳酸氢钠
C.质量相同时,分别与同体积同浓度盐酸反应的快慢:碳酸钠>碳酸氢钠
D.物质的量相同时,分别与足量的盐酸反应,生成CO 的质量:碳酸钠<碳酸氢钠
2
3.下列实验方案中,不能准确测定NaCO 和NaHCO 混合物中NaCO 质量分数的是( )
2 3 3 2 3
A.取a g混合物充分加热,减重b g
B.取a g混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b g固体
C.取a g混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b g
D.取a g混合物与足量Ba(OH) 溶液充分反应,过滤、洗涤、烘干,得b g固体
2
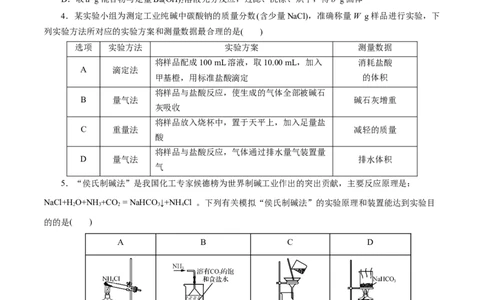
4.某实验小组为测定工业纯碱中碳酸钠的质量分数(含少量NaCl),准确称量W g样品进行实验,下
列实验方法所对应的实验方案和测量数据最合理的是( )
选项 实验方法 实验方案 测量数据
将样品配成100 mL溶液,取10.00 mL,加入 消耗盐酸
A 滴定法
甲基橙,用标准盐酸滴定 的体积
将样品与盐酸反应,使生成的气体全部被碱石
B 量气法 碱石灰增重
灰吸收
将样品放入烧杯中,置于天平上,加入足量盐
C 重量法 减轻的质量
酸
将样品与盐酸反应,气体通过排水量气装置量
D 量气法 排水体积
气
5.“侯氏制碱法”是我国化工专家候德榜为世界制碱工业作出的突出贡献,主要反应原理是:
NaCl+H O+NH +CO = NaHCO ↓+NHCl 。下列有关模拟“侯氏制碱法”的实验原理和装置能达到实验目
2 3 2 3 4
的的是( )
A B C D
制取氨气 制取NaHCO 分离NaHCO 制取NaCO
3 3 2 3
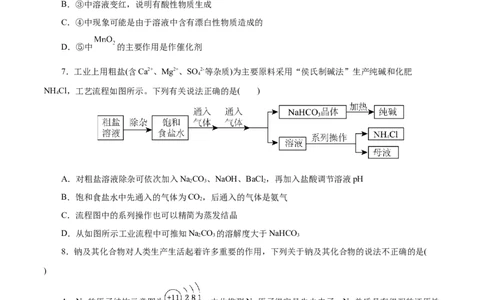
6.某实验小组通过下图所示实验,探究 与水的反应:下列说法错误的是( )
A.②中的大量气泡的主要成分是氧气
B.③中溶液变红,说明有酸性物质生成
C.④中现象可能是由于溶液中含有漂白性物质造成的
D.⑤中 的主要作用是作催化剂
7.工业上用粗盐(含Ca2+、Mg2+、SO 2-等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥
4
NH Cl,工艺流程如图所示。下列有关说法正确的是( )
4
A.对粗盐溶液除杂可依次加入NaCO、NaOH、BaCl ,再加入盐酸调节溶液pH
2 3 2
B.饱和食盐水中先通入的气体为CO,后通入的气体是氨气
2
C.流程图中的系列操作也可以精简为蒸发结晶
D.从如图所示工业流程中可推知NaCO 的溶解度大于NaHCO
2 3 3
8.钠及其化合物对人类生产生活起着许多重要的作用,下列关于钠及其化合物的说法不正确的是(
)
A.Na的原子结构示意图为 ,由此推测Na原子很容易失去电子,Na单质具有很强的还原性
B.NaO 做供氧剂时发生了反应:2CO+2Na O=2Na CO+O ,在该反应中NaO 只起还原剂的作用
2 2 2 2 2 2 3 2 2 2
C.NaCO 俗称苏打或纯碱,可由NaHCO 受热分解制得
2 3 3
D.NaHCO 溶解度小于NaCO,向饱和NaCO 溶液中通入CO 气体后,试管中会出现白色结晶
3 2 3 2 3 2
9.密闭容器中装1mol NaHCO 和0.8mol Na O 加热充分反应后,容器内残留的固体是( )
3 2 2
A.0.8mol Na CO 和1mol NaOH B.1mol Na CO 和0.6mol NaOH
2 3 2 3
C.1.3mol Na CO D.0.5mol Na CO 和1.6mol NaOH
2 3 2 310.我国化学家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如图。下列说法中错误的是(
)
A.沉淀池中发生反应的离子方程式为:
B.上述物质中X物质是CO
2
C.侯氏制碱使原料NaCl的利用率从70%提高到90%以上,主要是设计了循环1的循环
D.母液中物质的量:
1.(2021•浙江1月选考)下列“类比”合理的是( )
A.Na与HO反应生成NaOH和H,则Fe与HO反应生成Fe(OH) 和H
2 2 2 3 2
B.NaClO溶液与CO 反应生成NaHCO 和HClO,则NaClO溶液与SO 反应生成NaHSO 和HClO
2 3 2 3
C.NaN与盐酸反应生成NaCl和NH Cl,则MgN 与盐酸反应生成MgCl 和NH Cl
3 4 3 2 2 4
D.NaOH溶液与少量AgNO 溶液反应生成Ag O和NaNO ,则氨水与少量AgNO 溶液反应生成Ag O
3 2 3 3 2
和NH NO
4 3
2.有NaO、NaO、NaCO、NaHCO 、NaCl中的某几种组成的混合物,向混合物中加入足量的盐酸
2 2 2 2 3 3
有气体放出,将放出的气体通过过量的NaOH溶液后,气体体积有所减少,若将上述混合物在空气中充分
加热,也有气体放出,且加热后残留固体物质的质量比加热前有所增加,下列推断正确的是( )
A.混合物中一定不含有NaO
2
B.混合物中一定不含有NaCO 和NaCl
2 3
C.混合物中是否含有NaCO 和NaCl无法确定
2 3
D.混合物中一定不含有NaO 和NaCl
2 23.下列实验对应的结论正确的是( )
A.装置甲组成Zn—Cu原电池
B.装置乙证明非金属性:Cl>C>Si
C.装置丙可以除去SO 中混有的HCl气体
2
D.装置丁证明NaHCO 的热稳定性弱于NaCO
3 2 3
4.为了使宇航员在飞船中得到一个稳定的,良好的生存环境,一、般在飞船内安装盛有NaO 或
2 2
KO 颗粒的装置,它的用途是产生氧气。下列关于NaO 的叙述不正确的是( )
2 2 2 2
A.NaO 中正负离子的个数比为2:1
2 2
B.NaO 与SO 反应时NaO 作氧化剂
2 2 2 2 2
C.NaO 与CO 反应产生2.24L O (标准状况)时,转移电子的物质的量为0.4mol
2 2 2 2
D.NaO 分别与水及CO 反应产生相同量的O 时,需要水和CO 的物质的量相等
2 2 2 2 2
5.钠在液氨中溶剂化速度极快,生成蓝色的溶剂合电子,该过程表示为:Na+(x+y)NH Na+
3
(NH )x+e-(NH ),下列说法不正确的是( )
3 3 y
A.钠加入液氨中溶液的导电性增强
B.e-(NH ) 的可能结构为
3 y
C.e-(NH ) 具有强还原性,钠/液氨体系可以还原炔烃、苯等有机物
3 y
D.e-(NH ) 在液氨体系中会产生H
3 y 2
6.海水资源开发利用的部分过程如图所示:下列说法正确的是( )
A.粗盐(含Mg2+、Ca2+、SO 等)提纯所加试剂顺序为NaOH→Na CO→BaCl →过滤→HCl
2 3 2
B.过程①为了提高产率一般先通CO 再通NH
2 3
C.用澄清石灰水可以鉴别NaHCO 和NaCO 溶液
3 2 3
D.过程②③④可以达到富集溴的目的
7.实验室可通过沉淀重量法测量样品纯度,按如下装置测定纯碱(含少量NaCl)的纯度,下列说法正
确的是( )
A.装置A中药品应为浓硫酸,C中试剂应该为BaCl 溶液
2
B.在B~C之间应增添盛有饱和NaHCO 溶液的洗气装置,以除去氯化氢气体
3
C.只要测定装置C在吸收CO 前后的质量差,就可以确定碳酸钠的质量分数
2
D.反应结束后,需经过过滤、洗涤、干燥、称量等操作测定C中沉淀质量
8.H 与碱金属等单质在较高温度下可以化合形成离子型金属氢化物,如NaH、LiH等,它们具有极
2
强的还原性,也是良好的野外生氢剂(NaH+HO=NaOH+H↑),下列说法不正确的是( )
2 2
A.金属氢化物具有强还原性的原因是其中的氢元素为-l价
的
B.NaH 电子式可表示为Na+[:H]-
C.NaAlH 与水反应:NaAlH +HO=NaOH+Al(OH) +H↑
4 4 2 3 2
D.工业上用有效氢含量衡量含氢还原剂的供氢能力,有效氢指单位质量(克)的含氢还原剂的还原能力
相当于多少克氢气的还原能力。则LiAlH 的有效氢含量约为0.21
4
9.如表所示,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
选项 陈述Ⅰ 陈述Ⅱ 判断
A 碳酸钠溶液可用于治疗胃病 NaCO 可与盐酸反应 Ⅰ对,Ⅱ对,有
2 3
向滴有酚酞的水溶液中加入
B NaO 与水反应生成氢氧化钠 Ⅰ对,Ⅱ错,无
NaO 变红色 2 2
2 2
C 金属钠具有强还原性 高压钠灯发出透雾性强的黄光 Ⅰ对,Ⅱ对,有NaO 能与CO 和HO反应生
D 过氧化钠可为航天员供氧 2 2 2 2 Ⅰ对,Ⅱ对,有
成O
2
10.已知氢化钠(NaH)可由氢气和钠在高温下化合形成,其使用需要惰性环境,遇水放出易燃气体,
下列说法不正确的是( )
A.氢化钠与水反应产生的气体,通过盛有碱石灰的干燥管,用向下排空气法可以收集得到一定量的
H
2
B.氢化钠与水反应产生的气体通过灼热的氧化铜,若出现黑色变红色现象,则说明产生的气体中一
定含有H
2
C.氢化钠在无水条件下除去钢铁表面铁锈的反应方程式为3 NaH+Fe O═2Fe+3NaOH
2 3
D.锌和盐酸反应后的气体经浓硫酸干燥后,与钠在高温下反应得到纯净的NaH
11.过碳酸钠2NaCO·3H O ,外观为白色结晶,主要用作漂白剂和氧化剂,以及作去污剂、清洗剂、
2 3 2 2
杀菌剂。生产过程的主反应方程式:2NaCO+3H O=2Na CO·3H O,下列说法不正确的是
2 3 2 2 2 3 2 2
A.过碳酸钠具有强氧化性
B.生产过程中采用较低温度,目的是防止产品及反应物的分解
C.在生产过程中酸、铁盐、铜盐等都可能导致产率下降
D.将过碳酸钠溶液和亚硫酸氢钠溶液混合,发生的反应为 2NaCO·3H O + 3NaHSO =2Na CO +
2 3 2 2 3 2 3
3NaHSO +3H O
4 2
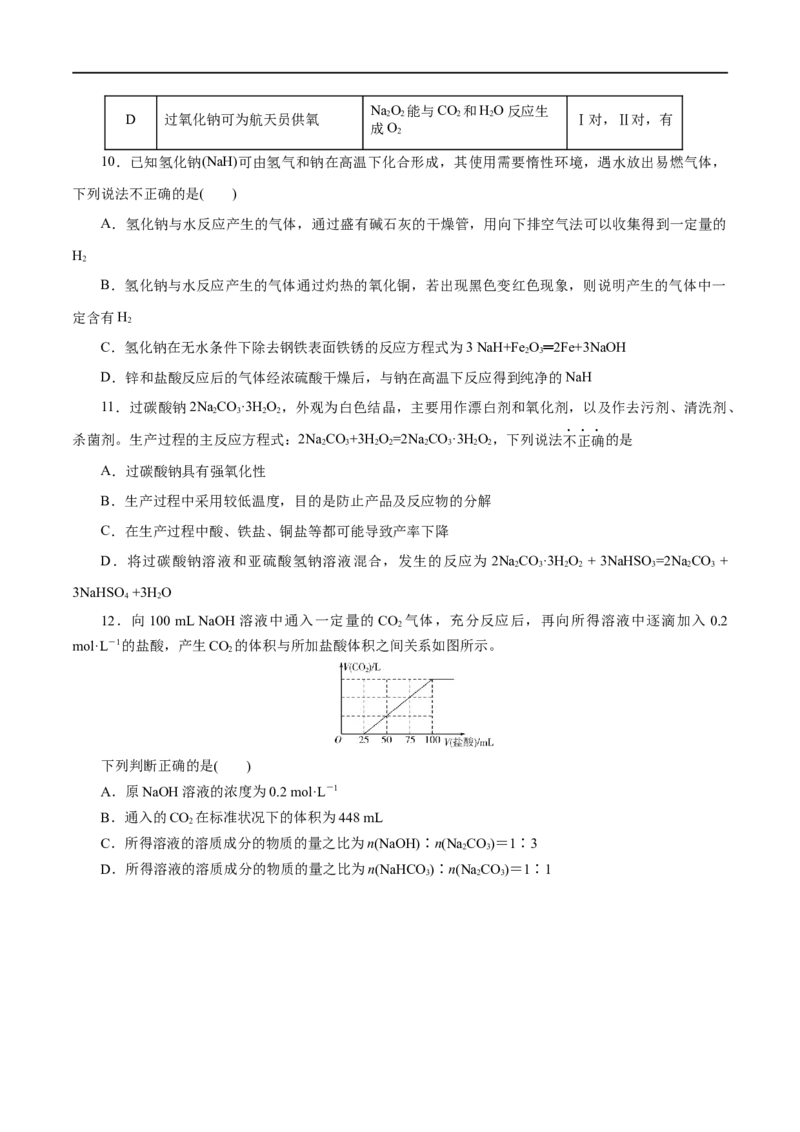
12.向100 mL NaOH溶液中通入一定量的 CO 气体,充分反应后,再向所得溶液中逐滴加入 0.2
2
mol·L-1的盐酸,产生CO 的体积与所加盐酸体积之间关系如图所示。
2
下列判断正确的是( )
A.原NaOH溶液的浓度为0.2 mol·L-1
B.通入的CO 在标准状况下的体积为448 mL
2
C.所得溶液的溶质成分的物质的量之比为n(NaOH)∶n(Na CO)=1∶3
2 3
D.所得溶液的溶质成分的物质的量之比为n(NaHCO )∶n(Na CO)=1∶1
3 2 3