文档内容
专题 15 晶体结构与性质
第 44 练 金属晶体与离子晶体
1.构成金属晶体的基本微粒是( )
A.分子 B.原子
C.阳离子与阴离子 D.阳离子与自由电
子
【答案】D
【解析】构成金属晶体的基本微粒为阳离子和自由移动的电子,D符合题意;故选D。
2.从严格意义上讲石墨属于( )
A.分子晶体 B.原子晶体 C.金属晶体 D.混合型晶体
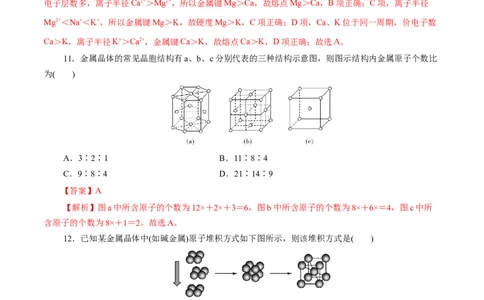
【答案】D
【解析】石墨晶体中层与层之间通过分子间作用力相连,同一层内通过共价键相连,所以从严格意义
上讲石墨属于混合型晶体,故选D。
3.下列各类物质中,固态时只能形成离子晶体的是( )
A.非金属氧化物 B.非金属单质 C.强酸 D.强碱
【答案】D
【解析】非金属氧化物属于共价化合物,A错误;非金属单质可能是分子晶体,也可能是原子晶体,
B错误;强酸属于共价化合物,C错误;强碱属于离子化合物,固态时只能形成离子晶体,D正确。
4.下列性质中,可以较充分说明某晶体是离子晶体的是( )
A.具有较高的熔点 B.固态不导电,水溶液能导电
C.可溶于水 D.固态不导电,熔融状态能导电
【答案】D
【解析】A选项,SiO 晶体熔点也较高,但不是离子晶体;B选项,HCl晶体的水溶液也能导电,也
2
不是离子晶体;C选项,有些晶体如固体氨溶于水,不属于离子晶体;D选项,离子晶体固态时不能导电,
在熔融时可导电。
5.离子晶体不可能具有的性质是( )
A.较高的熔、沸点 B.良好的导电性
C.溶于极性溶剂 D.坚硬而易粉碎
【答案】B【解析】离子晶体是阴、阳离子通过离子键结合而成的,在固态时,阴、阳离子受到彼此的束缚不能
自由移动,因而不导电。离子晶体溶于水或在熔融状态下,解离成自由移动的离子,可以导电。
6.下列说法正确的是( )
A.晶体中若存在阴离子,就一定存在阳离子
B.离子晶体不一定是化合物
C.离子晶体都易溶于水
D.离子晶体一定是由活泼金属和活泼非金属形成的
【答案】A
【解析】离子晶体的构成微粒是阴离子与阳离子,A项正确。离子晶体中存在离子键,存在电子得失,
一定是化合物,B项错。CaCO 、BaSO 等离子晶体难溶于水,C项错。NH Cl晶体全部由非金属元素组成,
3 4 4
D项错。
7.Al O 的下列性质能用晶格能解释的是( )
2 3
A.Al O 可用作耐火材料 B.固态时不导电,熔融时能导电
2 3
C.Al O 是两性氧化物 D.晶体Al O 可以作宝石
2 3 2 3
【答案】A
【解析】Al O 中Al3+和O2-所带电荷都比较多,半径又都很小,因此Al O 的晶格能很大,熔点很高,
2 3 2 3
故Al O 可作耐火材料。
2 3
8.下列有关离子晶体的数据大小比较,不正确的是( )
A.熔点:NaF>MgF >AlF B.晶格能:NaF>NaCl>NaBr
2 3
C.阴离子的配位数:CsCl>NaCl>CaF D.硬度:MgO>CaO>BaO
2
【答案】A
【解析】由于r(Na+)>r(Mg2+)>r(Al3+),且Na+、Mg2+、Al3+所带电荷数依次增大,所以NaF、
MgF 、AlF 的晶格能依次增大,离子键依次增强,故熔点依次升高,A不正确。r(F-)