文档内容
第 30 讲 配合物 分子间作用力 超分子
复习目标 1.了解配位键的形成和配合物的组成。2.了解分子间作用力的类型、特征、实质
及其对物质性质的影响。3.能列举存在氢键的物质,并能解释氢键对物质性质的影响。
考点一 配位键 配合物
1.配位键
(1)配位键的形成:成键原子一方提供孤电子对,另一方提供空轨道形成共价键。
(2)配位键的表示:常用“→”来表示配位键,箭头指向接受孤电子对的原子,如 NH可表
示为 ,在NH中,虽然有一个N—H形成过程与其他3个N—H形成过程
不同,但是一旦形成之后,4个共价键就完全相同。
2.配位化合物
(1)概念:金属离子或原子(称为中心离子或原子)与某些分子或离子(称为配体或配位体)以配
位键结合形成的化合物。
(2)形成条件
中心离子或原子:有空轨道,一般是带正电的金属离子,特别是过渡金属离子,如Fe3+、
Cu2+、Zn2+、Ag+等,但也有电中性的原子等。
配位体:其中的配位原子(配位体中直接同中心离子或原子配合的原子)有孤电子对。配位体
可以是分子,如CO、NH 、HO等,也可以是离子,如F-、Cl-、Br-、I-、CN-、SCN
3 2
-、OH-等。
(3)组成:如[Cu(NH )]SO
3 4 4
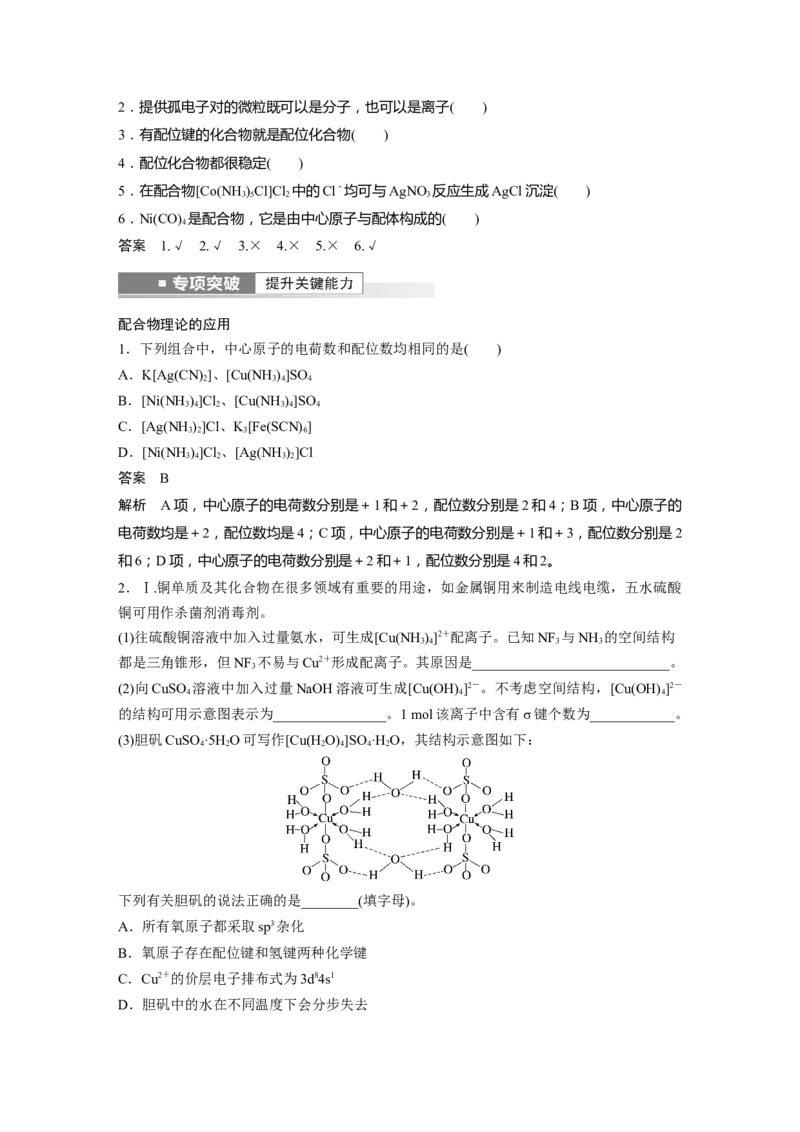
1.配位键实质上是一种特殊的共价键( )2.提供孤电子对的微粒既可以是分子,也可以是离子( )
3.有配位键的化合物就是配位化合物( )
4.配位化合物都很稳定( )
5.在配合物[Co(NH )Cl]Cl 中的Cl-均可与AgNO 反应生成AgCl沉淀( )
3 5 2 3
6.Ni(CO) 是配合物,它是由中心原子与配体构成的( )
4
答案 1.√ 2.√ 3.× 4.× 5.× 6.√
配合物理论的应用
1.下列组合中,中心原子的电荷数和配位数均相同的是( )
A.K[Ag(CN) ]、[Cu(NH )]SO
2 3 4 4
B.[Ni(NH )]Cl 、[Cu(NH )]SO
3 4 2 3 4 4
C.[Ag(NH)]Cl、K[Fe(SCN) ]
3 2 3 6
D.[Ni(NH )]Cl 、[Ag(NH)]Cl
3 4 2 3 2
答案 B
解析 A项,中心原子的电荷数分别是+1和+2,配位数分别是2和4;B项,中心原子的
电荷数均是+2,配位数均是4;C项,中心原子的电荷数分别是+1和+3,配位数分别是2
和6;D项,中心原子的电荷数分别是+2和+1,配位数分别是4和2。
2.Ⅰ.铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸
铜可用作杀菌剂消毒剂。
(1)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH )]2+配离子。已知NF 与NH 的空间结构
3 4 3 3
都是三角锥形,但NF 不易与Cu2+形成配离子。其原因是____________________________。
3
(2)向CuSO 溶液中加入过量NaOH溶液可生成[Cu(OH) ]2-。不考虑空间结构,[Cu(OH) ]2-
4 4 4
的结构可用示意图表示为________________。1 mol该离子中含有σ键个数为____________。
(3)胆矾CuSO ·5H O可写作[Cu(H O) ]SO ·H O,其结构示意图如下:
4 2 2 4 4 2
下列有关胆矾的说法正确的是________(填字母)。
A.所有氧原子都采取sp3杂化
B.氧原子存在配位键和氢键两种化学键
C.Cu2+的价层电子排布式为3d84s1
D.胆矾中的水在不同温度下会分步失去Ⅱ.经研究表明,Fe(SCN) 是配合物,Fe3+与SCN-不仅能以1∶3的个数比配合,还能以其
3
他个数比配合。按要求填空:
(4)若Fe3+与SCN-的配合物中,主要是Fe3+与SCN-以个数比1∶1配合所得离子显红色。
该离子的离子符号是____________。
(5)若Fe3+与SCN-以个数比1∶5配合,则FeCl 与KSCN在水溶液中发生反应的化学方程式
3
可以表示为____________________________________________________________________。
答案 (1)N、F、H三种元素的电负性:F>N>H,在NF 中,共用电子对偏向F原子、偏
3
离N原子,使得氮原子的原子核对孤电子对吸引力增强,难与Cu2+形成配位键
(2) 或 8N
A
(3)D
(4)[Fe(SCN)]2+
(5)FeCl +5KSCN===K[Fe(SCN) ]+3KCl
3 2 5
解析 (1)N、F、H三种元素的电负性:F>N>H,所以NH 中共用电子对偏向N原子,而
3
在NF 中,共用电子对偏向F原子,偏离N原子。(2)Cu2+中存在空轨道,而OH-中O原子
3
有孤电子对,故O与Cu之间以配位键结合。(3)A项,与S相连的氧原子没有杂化;B项,
氢键不是化学键;C项,Cu2+的价层电子排布式为3d9;D项,由图可知,胆矾中有1个
HO与基他微粒靠氢键结合,易失去,有4个HO与Cu2+以配位键结合,较难失去。
2 2
(1)单核配体的确认要注意是否带有电荷,如 F-、Cl-等,如配合物[CoCl(NH )]Cl ,中心离
3 5 2
子为Co3+,配体是Cl-和NH ,而不是氯原子。
3
(2)高考中常考有关配合物的结构示意图,不考虑空间结构,但要注意配体中的配位原子一
定要与中心原子或中心离子直接相连。如[Cu(NH )]2+中NH 中N原子为配位原子,所以N
3 4 3
原子必须要与铜离子直接相连。
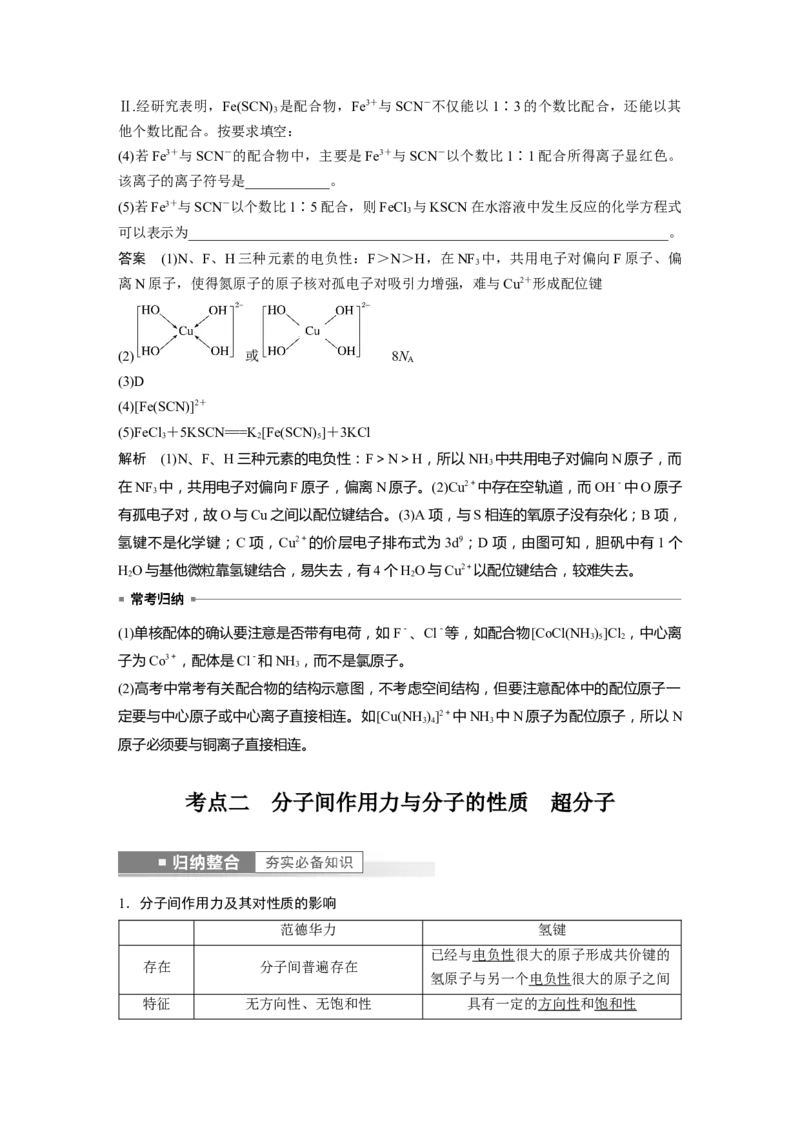
考点二 分子间作用力与分子的性质 超分子
1.分子间作用力及其对性质的影响
范德华力 氢键
已经与电负性很大的原子形成共价键的
存在 分子间普遍存在
氢原子与另一个电负性很大的原子之间
特征 无方向性、无饱和性 具有一定的方向性和饱和性强度 共价键>氢键>范德华力
①组成和结构相似的物质,相对分
影响其强 对于A—H…B,A、B的电负性越大,
子质量越大,范德华力越大;
度的因素 B原子的半径越小,氢键键能越大
②分子的极性越大,范德华力越大
范德华力主要影响物质的物理性 分子间氢键的存在,使物质的熔、沸点
对物质性
质,如熔、沸点等。范德华力越 升高,分子内氢键常使物质的熔、沸点
质的影响
大,物质的熔、沸点越高 降低,对电离、溶解度等产生影响
2.分子的性质
(1)分子的极性
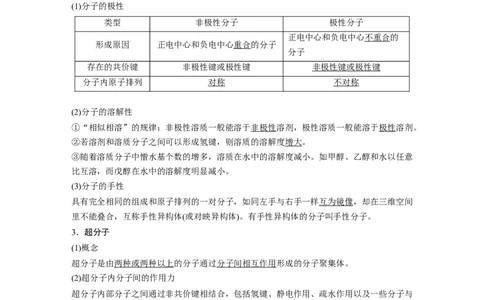
类型 非极性分子 极性分子
正电中心和负电中心不重合的
形成原因 正电中心和负电中心重合的分子
分子
存在的共价键 非极性键或极性键 非极性键或极性键
分子内原子排列 对称 不对称
(2)分子的溶解性
①“相似相溶”的规律:非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂。
②若溶剂和溶质分子之间可以形成氢键,则溶质的溶解度增大。
③随着溶质分子中憎水基个数的增多,溶质在水中的溶解度减小。如甲醇、乙醇和水以任意
比互溶,而戊醇在水中的溶解度明显减小。
(3)分子的手性
具有完全相同的组成和原子排列的一对分子,如同左手与右手一样互为镜像,却在三维空间
里不能叠合,互称手性异构体(或对映异构体)。有手性异构体的分子叫手性分子。
3.超分子
(1)概念
超分子是由两种或两种以上的分子通过分子间相互作用形成的分子聚集体。
(2)超分子内分子间的作用力
超分子内部分子之间通过非共价键相结合,包括氢键、静电作用、疏水作用以及一些分子与
金属离子形成的弱配位键等。
(3)超分子的应用
在分子水平上进行分子设计,有序组装甚至复制出一些新型的分子材料。
1.以极性键结合起来的分子一定是极性分子( )
2.碘化氢的沸点高于氯化氢的沸点是因为碘化氢分子间存在氢键( )3. 为手性分子( )
4.非极性分子中,一定含有非极性共价键( )
5.卤素单质、卤素氢化物、卤素碳化物(即CX)的熔、沸点均随着相对分子质量的增大而
4
增大( )
6.BCl 与NCl 均为三角锥形,为极性分子( )
3 3
7.HO比HS稳定是因为水分子间存在氢键( )
2 2
8.可燃冰(CH·8H O)中甲烷分子与水分子之间形成了氢键( )
4 2
答案 1.× 2.× 3.× 4.× 5.× 6.× 7.× 8.×
一、键的极性与分子的极性判断
1.下列各组分子中,都属于含极性键的非极性分子的是( )
A.CO、HS B.C H、CH
2 2 2 4 4
C.Cl、C H D.NH 、HCl
2 2 2 3
答案 B
解析 HS和NH 、HCl都是含极性键的极性分子;Cl 是含有非极性键的非极性分子;
2 3 2
CO 、CH 是只含有极性键的非极性分子;C H 和C H 是含有极性键和非极性键的非极性分
2 4 2 4 2 2
子。
2.下列叙述正确的是( )
A.以非极性键结合起来的双原子分子一定是非极性分子
B.以极性键结合起来的分子一定是极性分子
C.非极性分子只能是双原子单质分子
D.非极性分子中,一定含有非极性共价键
答案 A
分子极性的判断方法
(1)只含非极性键的分子一定是非极性分子,如H、P 等。
2 4
(2)含极性键的双原子分子一定是极性分子,如HCl、CO等。
(3)AB (n≥2)型分子:
n
①根据分子结构判断
若分子是对称的(直线形、正三角形、正四面体形等),极性键的极性向量和等于零时,为非
极性分子,否则是极性分子。如CH 、CO 等含有极性键,是非极性分子;HO、NH 等含
4 2 2 3
有极性键,是极性分子。②利用孤电子对判断
若中心原子A中无孤电子对,则为非极性分子;若有孤电子对,则为极性分子。
③利用化合价判断
若中心原子A的化合价的绝对值等于该元素所在的主族序数,则为非极性分子;若不等,
则为极性分子。如BCl 、CO 是非极性分子;SO 、NF 是极性分子。
3 2 2 3
二、分子间作用力对物质性质的影响
3.(1)H O在乙醇中的溶解度大于HS,其原因是___________________________________。
2 2
(2)已知苯酚( )具有弱酸性,其K=1.1×10-10;水杨酸第一步电离形成的离子
能形成分子内氢键,据此判断,相同温度下电离平衡常数K (水杨
2
酸)_______K(苯酚)(填“>”或“<”),其原因是_____________________________________。
(3)H O分子内的O—H、分子间的范德华力和氢键从强到弱依次为________________。
2
的沸点比 高,原因是___________________________。
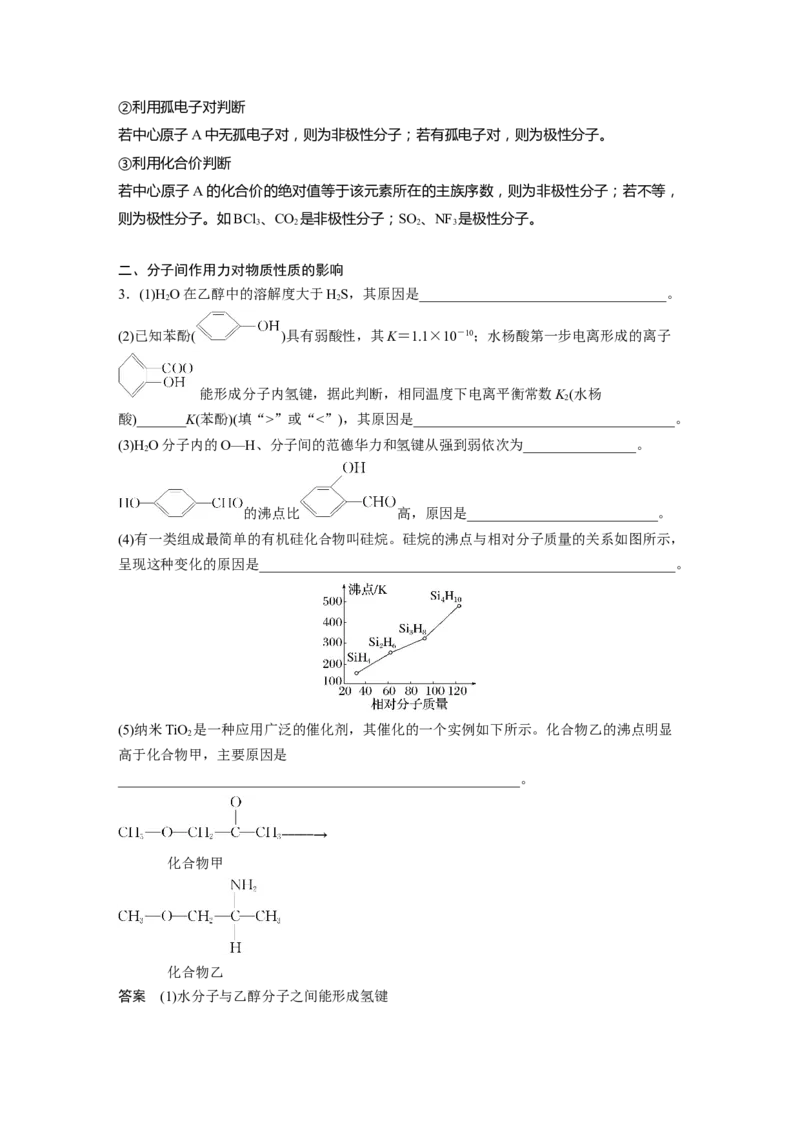
(4)有一类组成最简单的有机硅化合物叫硅烷。硅烷的沸点与相对分子质量的关系如图所示,
呈现这种变化的原因是___________________________________________________________。
(5)纳米TiO 是一种应用广泛的催化剂,其催化的一个实例如下所示。化合物乙的沸点明显
2
高于化合物甲,主要原因是
_________________________________________________________。
―――――→
化合物甲
化合物乙
答案 (1)水分子与乙醇分子之间能形成氢键(2)< 能形成分子内氢键,使其更难电离出H+ (3)O—H>氢键>范德华力
形成分子内氢键,而 形成分子间氢键,分子间氢键使
分子间作用力增大,沸点升高 (4)硅烷为分子晶体,随相对分子质量的增大,分子间作用
力增强,沸点升高 (5)化合物乙分子间存在氢键
答题规范(4) 分子结构与性质简答
类型一 和共价键有关的问题
1.Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或
三键。从原子结构角度分析,原因是_____________________________________________。
答案 Ge原子半径大,原子间形成的σ键较长,p-p轨道肩并肩重叠程度很小或几乎不能重
叠,难以形成π键,不易形成双键或三键
2.碳及其化合物广泛存在于自然界中,碳在形成化合物时,其键型以共价键为主,原因是
_____________________________________________________________________________。
答案 C原子有4个价电子且半径较小,难以通过得失电子达到稳定结构
3.硅是重要的半导体材料,构成了现代电子工业的基础。碳和硅的有关化学键键能如表所
示,简要分析和解释下列有关事实:
化学键 C—C C—H C—O Si—Si Si—H Si—O
键能/ (kJ·mol-1) 365 413 336 226 318 452
(1)硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是
_____________________________________________________________________________。
(2)SiH 的稳定性小于CH,更易生成氧化物,原因是________________________________。
4 4
答案 (1)C—C和C—H的键能较大,所形成的烷烃稳定。而硅烷中Si—Si和Si—H的键能
较小,易断裂,导致长链硅烷难以生成
(2)C—H的键能大于C—O,C—H比C—O稳定。而Si—H的键能小于Si—O,所以Si—H
不稳定而倾向于形成稳定性更强的Si—O
4.下表是CO和N 两者的键能数据(单位:kJ·mol-1)
2
A—B A==B A≡B
CO 351 745 1 071.9
N 139 418 946
2结合数据说明CO比N 活泼的原因:________________________________________。
2
答案 CO中第一个π键的键能是326.9 kJ·mol-1,N 中第一个π键的键能是528 kJ·mol-1,
2
则CO的第一个π键比N 的第一个π键更容易断裂
2
5.CH 的键角大于NH 的原因为_________________________________________________。
4 3
答案 CH、NH 的中心原子均为sp3杂化,NH 分子中有未成键的孤电子对,对成键电子对
4 3 3
斥力较大,键角较小
6.高温陶瓷材料Si N 晶体中键角N—Si—N______Si—N—Si(填“>”“<”或“=”),原
3 4
因是___________________________________________________________________________。
答案 > N原子上有孤电子对,由于孤电子对与成键电子对的排斥力更大,使得 Si—N—
Si键角较小
7.两种三角锥形气态氢化物膦(PH )和氨(NH )的键角分别为93.6°和107°,试分析PH 的键
3 3 3
角小于NH 的原因:_____________________________________________________________。
3
答案 N原子的电负性强于P原子,对成键电子对吸引能力更强,成键电子对离中心原子更
近,成键电子对之间距离更小,排斥力更大致使键角更大,因而PH 的键角小于NH
3 3
8 . NF 的 键 角 ______NH 的 键 角 ( 填 “ >”“<” 或 “ = ” ) , 理 由 是
3 3
________________________________________________________________________。
答案 < F的电负性比H大,NF 中N周围电子云密度减小,成键电子对之间的排斥力较
3
小
9.比较NH 和[Cu(NH )]2+中H—N—H键角的大小:NH ______[Cu(NH )]2+(填“>”或
3 3 4 3 3 4
“<”),并说明理由:_________________________________________________________。
答案 < NH 提供孤电子对与Cu2+形成配位键后,N—H成键电子对受到的排斥力减小
3
类型二 和氢键有关的问题
10.乙二胺分子(H N—CH —CH—NH )中氮原子杂化类型为sp3,乙二胺和三甲胺[N(CH )]
2 2 2 2 3 3
均属于胺,但乙二胺比三甲胺的沸点高得多,原因是
________________________________________________________________________。
答案 乙二胺分子间可以形成氢键,三甲胺分子间不能形成氢键
11.丙酸钠(CHCHCOONa)和氨基乙酸钠均能水解,水解产物有丙酸(CHCHCOOH)和氨
3 2 3 2
基乙酸(H NCH COOH),常温下丙酸为液体,而氨基乙酸为固体,主要原因是
2 2
________________________________________________________________________。
答案 羧基的存在使丙酸形成分子间氢键,而氨基乙酸分子中,羧基和氨基均能形成分子间
氢键
12.硝酸和尿素( )的相对分子质量接近,但常温下硝酸为挥发性液体,尿素
为固体,请解释原因:_________________________________________________________。
答案 尿素分子间存在氢键,使其熔、沸点升高,而硝酸分子内存在氢键,使其熔、沸点降
低
13.氨(NH )的熔、沸点比联氨(H N—NH)低的主要原因:__________________________。
3 2 2答案 联氨分子间形成的氢键数目多于氨分子间形成的氢键数目
14.苯胺( )与甲苯( )的相对分子质量相近,但苯胺的熔点
(-5.9 ℃)、沸点(184.4 ℃)分别高于甲苯的熔点(-95.0 ℃)、沸点(110.6 ℃),原因是
____________________________。
答案 苯胺分子之间存在氢键
1.(2021·山东,9)关于CHOH、NH 和(CH)NNH 的结构与性质,下列说法错误的是(
3 2 4 3 2 2
)
A.CHOH为极性分子
3
B.NH 空间结构为平面形
2 4
C.NH 的沸点高于(CH)NNH
2 4 3 2 2
D.CHOH和(CH)NNH 中C、O、N杂化方式均相同
3 3 2 2
答案 B
解析 甲醇可看成是甲烷中的一个氢原子被羟基取代得到的,为四面体结构,是由极性键组
成的极性分子,A正确;NH 中N原子的杂化方式为sp3,NH 的空间结构不是平面形,B
2 4 2 4
错误;NH 分子中连接 N 原子的 H 原子数多,存在氢键的数目多,而偏二甲肼
2 4
[(CH )NNH]只有一端可以形成氢键,另一端的两个甲基基团比较大,影响了分子的排列,
3 2 2
沸点比NH 的低,C正确;CHOH和(CH)NNH 中C、O、N杂化方式均为sp3,D正确。
2 4 3 3 2 2
2.(2020·山东,7)B NH(无机苯)的结构与苯类似,也有大π键。下列关于B NH 的说法错
3 3 6 3 3 6
误的是( )
A.其熔点主要取决于所含化学键的键能
B.形成大π键的电子全部由N提供
C.分子中B和N的杂化方式相同
D.分子中所有原子共平面
答案 A
解析 无机苯属于分子晶体,其熔点与分子间作用力有关,与键能无关,A项错误;B的最
外层电子排布式为2s22p1,N的最外层电子排布式为2s22p3,经过sp2轨道杂化后,N原子剩
下1个孤电子对,B原子剩下1个空的p轨道,所以形成大π键的电子全部由N提供,B项
正确;B和N都是sp2杂化,键角为120°,分子中所有原子共平面,C、D项正确。
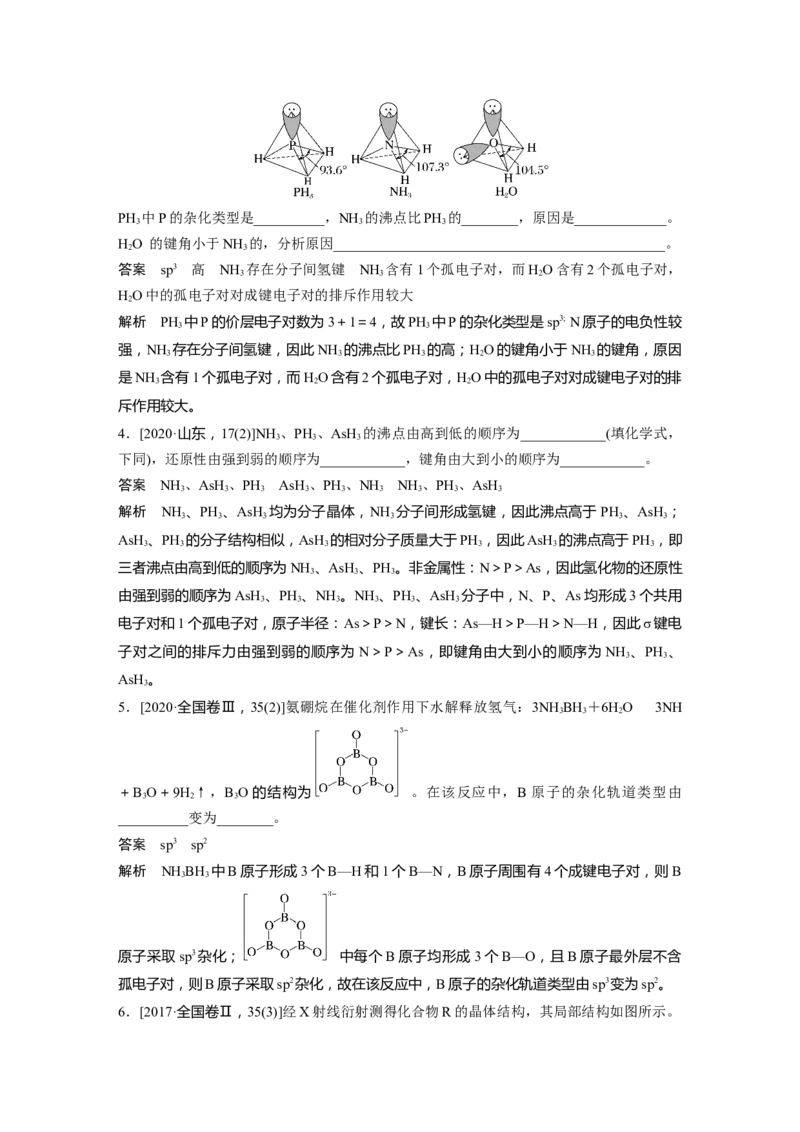
3.[2021·全国乙卷,35(3)][Cr(NH )(H O) Cl]2+中配体分子NH 、HO以及分子PH 的空间
3 3 2 2 3 2 3
结构和相应的键角如下图所示。PH 中P的杂化类型是__________,NH 的沸点比PH 的________,原因是_____________。
3 3 3
HO 的键角小于NH 的,分析原因_______________________________________________。
2 3
答案 sp3 高 NH 存在分子间氢键 NH 含有1个孤电子对,而HO含有2个孤电子对,
3 3 2
HO中的孤电子对对成键电子对的排斥作用较大
2
解析 PH 中P的价层电子对数为3+1=4,故PH 中P的杂化类型是sp3; N原子的电负性较
3 3
强,NH 存在分子间氢键,因此NH 的沸点比PH 的高;HO的键角小于NH 的键角,原因
3 3 3 2 3
是NH 含有1个孤电子对,而HO含有2个孤电子对,HO中的孤电子对对成键电子对的排
3 2 2
斥作用较大。
4.[2020·山东,17(2)]NH 、PH 、AsH 的沸点由高到低的顺序为____________(填化学式,
3 3 3
下同),还原性由强到弱的顺序为____________,键角由大到小的顺序为____________。
答案 NH 、AsH 、PH AsH 、PH 、NH NH 、PH 、AsH
3 3 3 3 3 3 3 3 3
解析 NH 、PH 、AsH 均为分子晶体,NH 分子间形成氢键,因此沸点高于PH 、AsH ;
3 3 3 3 3 3
AsH 、PH 的分子结构相似,AsH 的相对分子质量大于PH ,因此AsH 的沸点高于PH ,即
3 3 3 3 3 3
三者沸点由高到低的顺序为NH 、AsH 、PH 。非金属性:N>P>As,因此氢化物的还原性
3 3 3
由强到弱的顺序为AsH 、PH 、NH 。NH 、PH 、AsH 分子中,N、P、As均形成3个共用
3 3 3 3 3 3
电子对和1个孤电子对,原子半径:As>P>N,键长:As—H>P—H>N—H,因此σ键电
子对之间的排斥力由强到弱的顺序为N>P>As,即键角由大到小的顺序为NH 、PH 、
3 3
AsH 。
3
5.[2020·全国卷Ⅲ,35(2)]氨硼烷在催化剂作用下水解释放氢气:3NH BH +6HO3NH
3 3 2
+B O+9H↑,B O的结构为 。在该反应中,B原子的杂化轨道类型由
3 2 3
__________变为________。
答案 sp3 sp2
解析 NH BH 中B原子形成3个B—H和1个B—N,B原子周围有4个成键电子对,则B
3 3
原子采取sp3杂化; 中每个B原子均形成3个B—O,且B原子最外层不含
孤电子对,则B原子采取sp2杂化,故在该反应中,B原子的杂化轨道类型由sp3变为sp2。
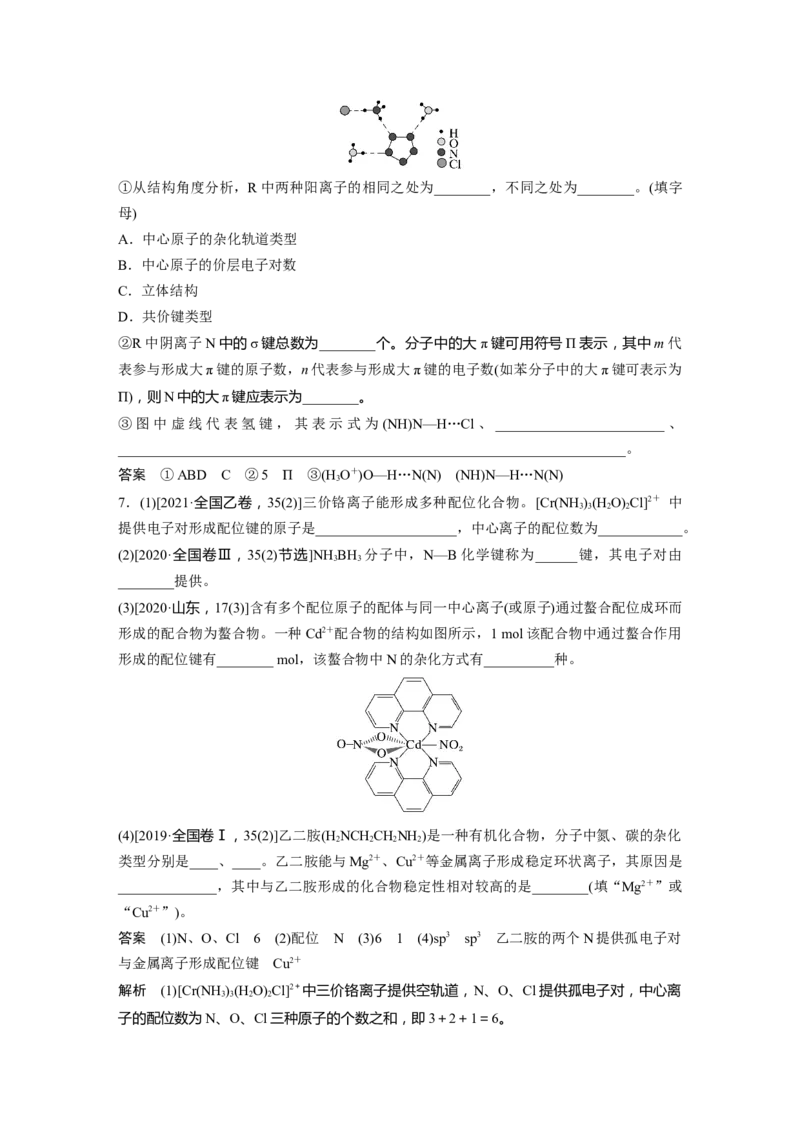
6.[2017·全国卷Ⅱ,35(3)]经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。①从结构角度分析,R中两种阳离子的相同之处为________,不同之处为________。(填字
母)
A.中心原子的杂化轨道类型
B.中心原子的价层电子对数
C.立体结构
D.共价键类型
②R中阴离子N中的σ键总数为________个。分子中的大π键可用符号Π表示,其中m代
表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
Π),则N中的大π键应表示为________。
③图中虚线代表氢键,其表示式为 (NH)N—H…Cl、________________________、
________________________________________________________________________。
答案 ①ABD C ②5 Π ③(H O+)O—H…N(N) (NH)N—H…N(N)
3
7.(1)[2021·全国乙卷,35(2)]三价铬离子能形成多种配位化合物。[Cr(NH )(H O) Cl]2+ 中
3 3 2 2
提供电子对形成配位键的原子是____________________,中心离子的配位数为____________。
(2)[2020·全国卷Ⅲ,35(2)节选]NH BH 分子中,N—B化学键称为______键,其电子对由
3 3
________提供。
(3)[2020·山东,17(3)]含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而
形成的配合物为螯合物。一种Cd2+配合物的结构如图所示,1 mol该配合物中通过螯合作用
形成的配位键有________ mol,该螯合物中N的杂化方式有__________种。
(4)[2019·全国卷Ⅰ,35(2)]乙二胺(H NCH CHNH )是一种有机化合物,分子中氮、碳的杂化
2 2 2 2
类型分别是____、____。乙二胺能与Mg2+、Cu2+等金属离子形成稳定环状离子,其原因是
______________,其中与乙二胺形成的化合物稳定性相对较高的是________(填“Mg2+”或
“Cu2+”)。
答案 (1)N、O、Cl 6 (2)配位 N (3)6 1 (4)sp3 sp3 乙二胺的两个N提供孤电子对
与金属离子形成配位键 Cu2+
解析 (1)[Cr(NH )(H O) Cl]2+中三价铬离子提供空轨道,N、O、Cl提供孤电子对,中心离
3 3 2 2
子的配位数为N、O、Cl三种原子的个数之和,即3+2+1=6。(3)由题给图示可知,1个Cd2+与4个N原子分别形成4个配位键,与2个O原子分别形成
2个配位键,因此1 mol该配合物中通过螯合作用形成的配位键有6 mol。
(4)乙二胺分子中,1个N原子形成3个单键,还有一个孤电子对,价层电子对数为4,采取
sp3杂化;1个C原子形成4个单键,没有孤电子对,价层电子对数为 4,采取sp3杂化。乙
二胺中2个氮原子提供孤电子对与金属镁离子或铜离子形成稳定的配位键,故能形成稳定环
状离子。由于铜离子半径大于镁离子,形成配位键时头碰头重叠程度较大,其与乙二胺形成
的化合物较稳定。
课时精练
1.下列物质:①HO+、②[B(OH) ]-、③CHCOO-、④NH 、⑤CH 中,存在配位键的是
3 4 3 3 4
( )
A.①② B.①③ C.④⑤ D.②④
答案 A
解析 HO+、[B(OH) ]-中,O原子能提供孤电子对,H+、B原子能提供空轨道,可形成配
3 4
位键;其余粒子不满足配位键的形成条件。
2.向下列配合物的水溶液中加入AgNO 溶液不能生成AgCl沉淀的是( )
3
A.[Co(NH )Cl]Cl B.[Co(NH )Cl]
3 4 2 3 3 3
C.[Co(NH )]Cl D.[Co(NH )Cl]Cl
3 6 3 3 5 2
答案 B
解析 配合物的内界与外界由离子键结合,只要外界存在 Cl-,加入AgNO 溶液即有AgCl
3
沉淀产生。B项的配合物[Co(NH )Cl]分子中,Co3+、NH 、Cl-全部处于内界,很难电离,
3 3 3 3
不存在Cl-,所以加入AgNO 溶液不能生成AgCl沉淀。
3
3.配合物在许多方面有着广泛的应用。下列叙述不正确的是( )
A.以Mg2+为中心的大环配合物叶绿素能催化光合作用
B.Fe2+的卟啉配合物是输送O 的血红素
2
C.[Ag(NH)]+是化学镀银试剂的有效成分
3 2
D.向溶液中逐滴加入氨水,可除去硫酸锌溶液中的Cu2+
答案 D
解析 Zn2+和Cu2+都能与NH 形成配合物,Zn(OH) 和Cu(OH) 都能溶解在过量的氨水中。
3 2 2
4.下列对分子的性质的解释,不正确的是( )
A.碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释
B.水在结冰时体积膨胀,是由于水分子之间存在氢键
C.SiCl 分子中硅氯键的极性比CCl 中碳氯键的弱
4 4
D.青蒿素分子式为C H O,结构如图,该分子中包含7个手性碳原子
15 22 5答案 C
解析 碘是非极性分子,易溶于非极性溶剂四氯化碳,甲烷属于非极性分子,难溶于极性溶
剂水,所以都可用相似相溶原理解释,故A正确;碳元素的电负性大于硅元素,因此Si、
Cl间的电负性差别较大,Si—Cl的极性强,故C错误;手性碳原子是指与碳原子相连的4
个原子或原子团都不相同。根据青蒿素的结构图知,该分子中包含 7 个手性碳原子,故D
正确。
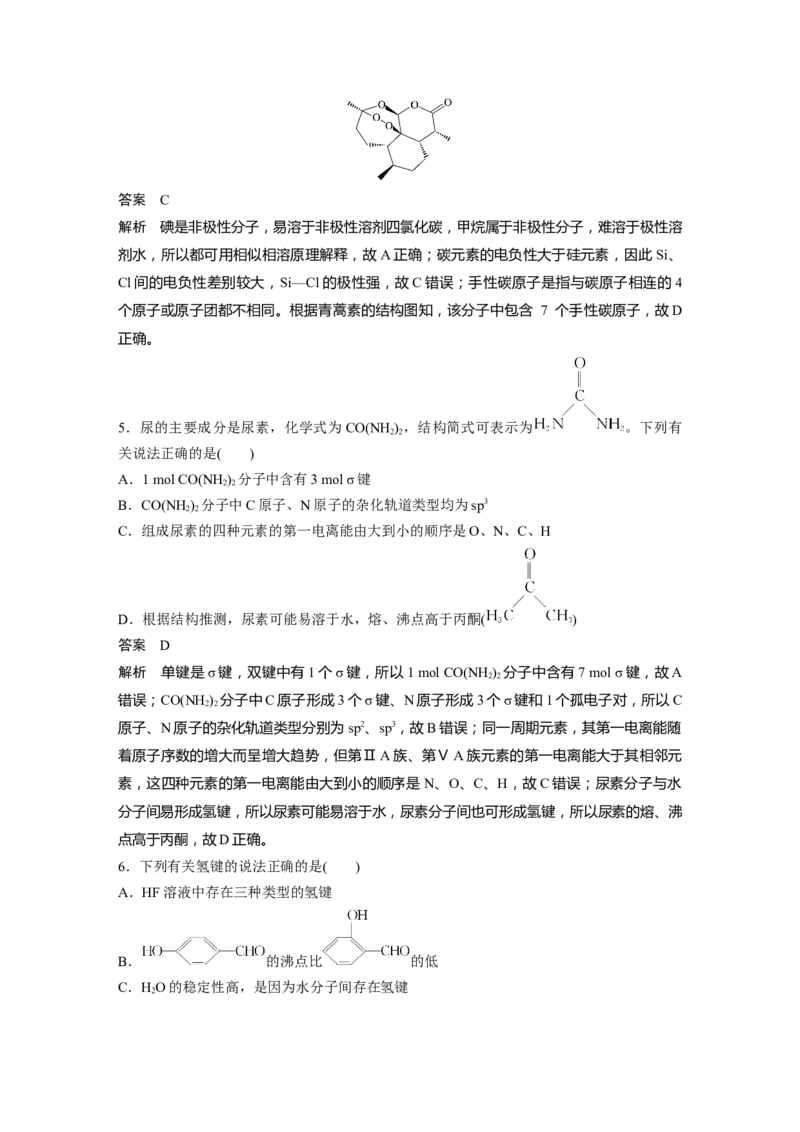
5.尿的主要成分是尿素,化学式为CO(NH) ,结构简式可表示为 。下列有
2 2
关说法正确的是( )
A.1 mol CO(NH ) 分子中含有3 mol σ键
2 2
B.CO(NH) 分子中C原子、N原子的杂化轨道类型均为sp3
2 2
C.组成尿素的四种元素的第一电离能由大到小的顺序是O、N、C、H
D.根据结构推测,尿素可能易溶于水,熔、沸点高于丙酮( )
答案 D
解析 单键是σ键,双键中有1个σ键,所以1 mol CO(NH ) 分子中含有7 mol σ键,故A
2 2
错误;CO(NH) 分子中C原子形成3个σ键、N原子形成3个σ键和1个孤电子对,所以C
2 2
原子、N原子的杂化轨道类型分别为sp2、sp3,故B错误;同一周期元素,其第一电离能随
着原子序数的增大而呈增大趋势,但第ⅡA族、第ⅤA族元素的第一电离能大于其相邻元
素,这四种元素的第一电离能由大到小的顺序是 N、O、C、H,故C错误;尿素分子与水
分子间易形成氢键,所以尿素可能易溶于水,尿素分子间也可形成氢键,所以尿素的熔、沸
点高于丙酮,故D正确。
6.下列有关氢键的说法正确的是( )
A.HF溶液中存在三种类型的氢键
B. 的沸点比 的低
C.HO的稳定性高,是因为水分子间存在氢键
2D. 形成分子内氢键,故 比 难电离
答案 D
解析 HF溶液中HF与HF、HO与HO、HF与HO之间均存在氢键,氢键类型有如下4种:
2 2 2
F—H…F、F—H…O、O—H…F、O—H…O,A项错误; 形成分子间氢
键,而 形成分子内氢键,分子间氢键使分子间作用力增大,故
的沸点比 的高,B项错误;HO的稳定性高,是因为水
2
分子中 H—O 的键能大,而氢键影响物理性质,C 项错误; 相对于
,苯环上多了一个—COO-,羟基上与氧结合的氢原子能与羧基上氧原子形成
氢键,使其更难电离出H+,D项正确。
7.下列有关说法不正确的是( )
A.C H 中碳原子都采取的是sp3杂化
3 8
B.O、CO、N 都是非极性分子
2 2 2
C.酸性:HCO<HPO <HSO <HClO
2 3 3 4 2 4
D.SnCl 的空间结构为正四面体形
4
答案 C
解析 C H 分子中每个C原子含有4个σ键,所以每个C原子价层电子对数是4,采取sp3
3 8
杂化,故A正确;O 、N 都是以非极性键结合的双原子分子,一定为非极性分子,CO 中
2 2 2
含有极性键,为直线形分子,结构对称,为非极性分子,故 B正确;非金属性:C<P<S<
Cl,元素的非金属性越强,其最高价氧化物对应水化物的酸性越强,HClO不是氯元素的最
高价氧化物对应的水化物,则酸性:HClO <HCO,故C错误。
2 3
8.通常情况下,NCl 是一种油状液体,其分子空间结构与NH 相似,下列对NCl 和NH 的
3 3 3 3
有关叙述错误的是( )
A.分子中N—Cl的键长与CCl 分子中C—Cl的键长不相等
4
B.NCl 分子是极性分子
3
C.NBr 比NCl 易挥发
3 3
D.在氨水中,大部分 NH 与 HO 以氢键(用“…”表示)结合形成 NH ·H O 分子,则
3 2 3 2NH ·H O的结构式为
3 2
答案 C
解析 C原子的原子半径大于N原子的原子半径,所以CCl 中C—Cl的键长比NCl 中N—
4 3
Cl的键长长,故A正确;NCl 分子的空间结构与氨分子相似,都是三角锥形,氨分子是极
3
性分子,所以NCl 分子也是极性分子,故B正确;分子晶体中物质的熔、沸点与相对分子
3
质量有关,相对分子质量越大其熔、沸点越高,所以NBr 比NCl 的熔、沸点高,NCl 比
3 3 3
NBr 易挥发,故C错误。
3
9.关于化学式为[TiCl(H O) ]Cl ·H O的配合物,下列说法正确的是( )
2 5 2 2
A.配位体是Cl-和HO,配位数是8
2
B.中心离子是Ti4+,配离子是[TiCl(H O) ]2+
2 5
C.内界和外界中Cl-的数目比是1∶2
D.在1 mol该配合物中加入足量AgNO 溶液,可以得到3 mol AgCl沉淀
3
答案 C
解析 配合物[TiCl(H O) ]Cl ·H O中配位体是Cl-和HO,配位数是6,故A错误;中心离
2 5 2 2 2
子是Ti3+,故B错误;配合物内界和外界中 Cl-的数目比是1∶2,故C正确;加入足量
AgNO 溶液,外界Cl-与Ag+反应,内界Cl-不与Ag+反应,1 mol该配合物只能生成2 mol
3
AgCl沉淀,故D错误。
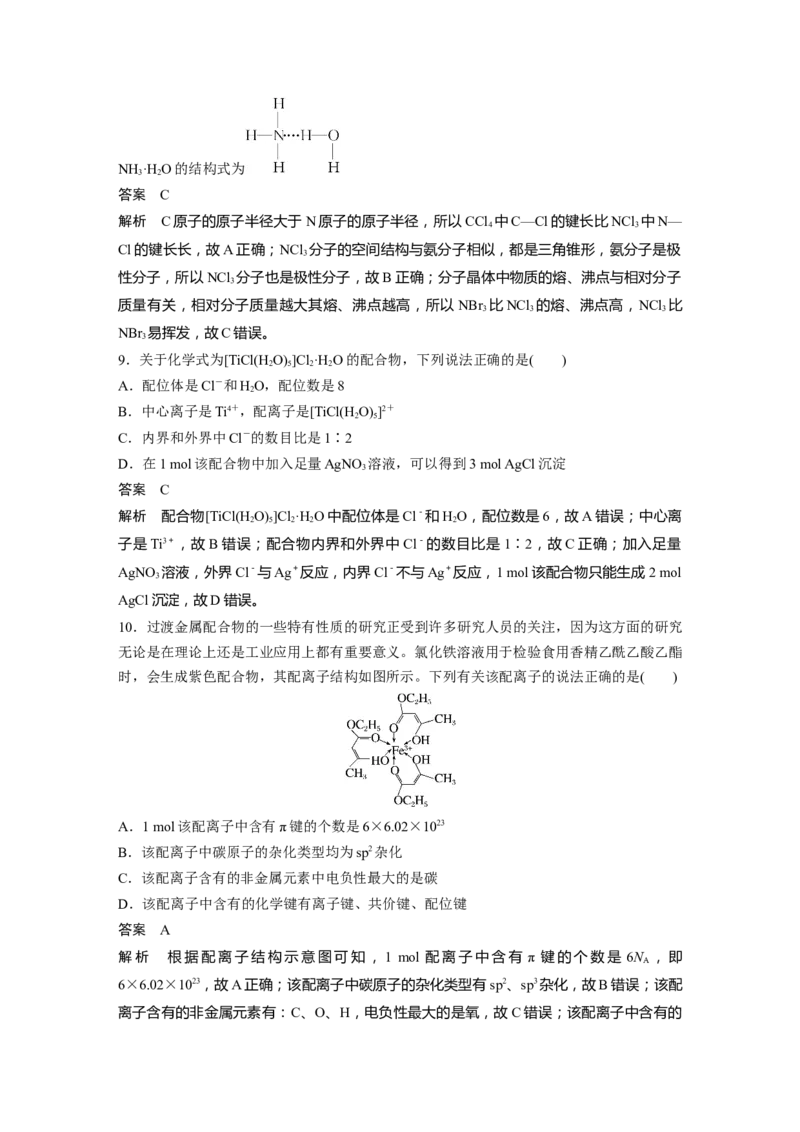
10.过渡金属配合物的一些特有性质的研究正受到许多研究人员的关注,因为这方面的研究
无论是在理论上还是工业应用上都有重要意义。氯化铁溶液用于检验食用香精乙酰乙酸乙酯
时,会生成紫色配合物,其配离子结构如图所示。下列有关该配离子的说法正确的是( )
A.1 mol该配离子中含有π键的个数是6×6.02×1023
B.该配离子中碳原子的杂化类型均为sp2杂化
C.该配离子含有的非金属元素中电负性最大的是碳
D.该配离子中含有的化学键有离子键、共价键、配位键
答案 A
解析 根据配离子结构示意图可知,1 mol 配离子中含有 π 键的个数是 6N ,即
A
6×6.02×1023,故A正确;该配离子中碳原子的杂化类型有sp2、sp3杂化,故B错误;该配
离子含有的非金属元素有:C、O、H,电负性最大的是氧,故C错误;该配离子中含有的化学键有共价键、配位键,故D错误。
11.下列现象与氢键有关的是( )
①NH 的熔、沸点比第ⅤA族其他元素氢化物的高
3
②小分子的醇、羧酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④水分子高温下很稳定
A.①②④ B.①②③ C.①② D.①③
答案 B
解析 水分子高温下很稳定是因为分子中O—H的键能大。
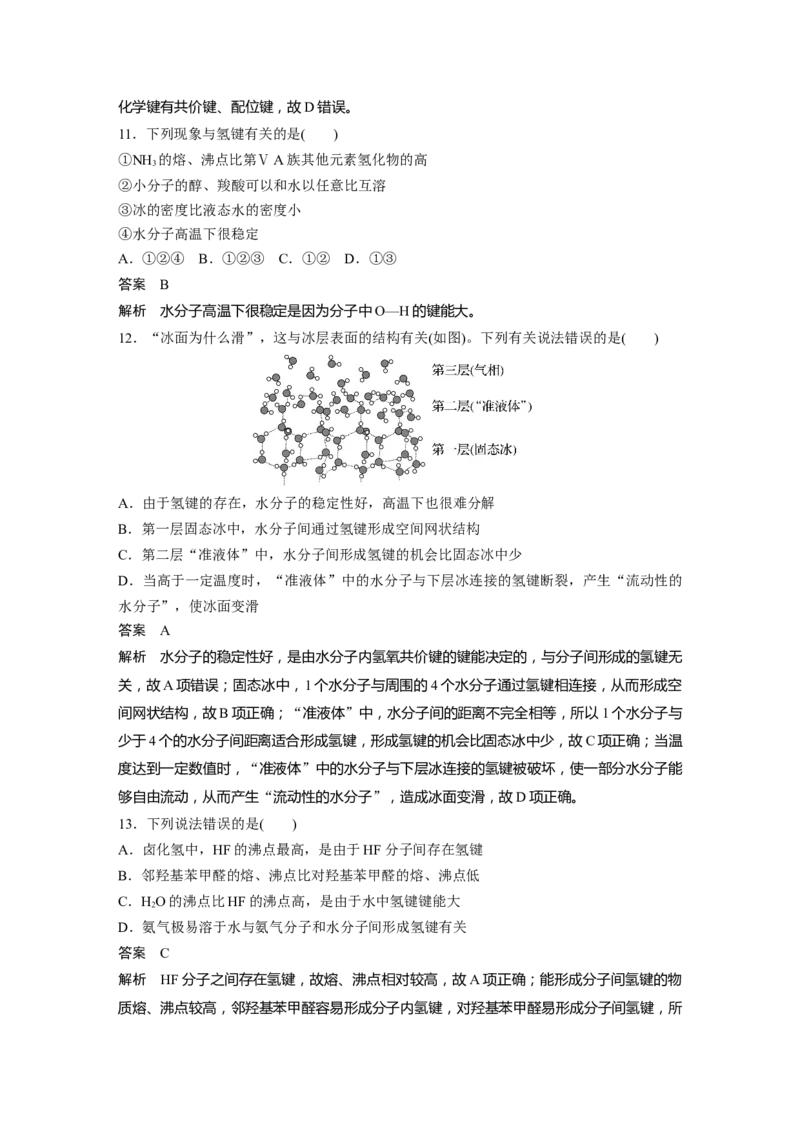
12.“冰面为什么滑”,这与冰层表面的结构有关(如图)。下列有关说法错误的是( )
A.由于氢键的存在,水分子的稳定性好,高温下也很难分解
B.第一层固态冰中,水分子间通过氢键形成空间网状结构
C.第二层“准液体”中,水分子间形成氢键的机会比固态冰中少
D.当高于一定温度时,“准液体”中的水分子与下层冰连接的氢键断裂,产生“流动性的
水分子”,使冰面变滑
答案 A
解析 水分子的稳定性好,是由水分子内氢氧共价键的键能决定的,与分子间形成的氢键无
关,故A项错误;固态冰中,1个水分子与周围的4个水分子通过氢键相连接,从而形成空
间网状结构,故B项正确;“准液体”中,水分子间的距离不完全相等,所以1个水分子与
少于4个的水分子间距离适合形成氢键,形成氢键的机会比固态冰中少,故C项正确;当温
度达到一定数值时,“准液体”中的水分子与下层冰连接的氢键被破坏,使一部分水分子能
够自由流动,从而产生“流动性的水分子”,造成冰面变滑,故D项正确。
13.下列说法错误的是( )
A.卤化氢中,HF的沸点最高,是由于HF分子间存在氢键
B.邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点低
C.HO的沸点比HF的沸点高,是由于水中氢键键能大
2
D.氨气极易溶于水与氨气分子和水分子间形成氢键有关
答案 C
解析 HF分子之间存在氢键,故熔、沸点相对较高,故A项正确;能形成分子间氢键的物
质熔、沸点较高,邻羟基苯甲醛容易形成分子内氢键,对羟基苯甲醛易形成分子间氢键,所以邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点低,故B项正确;HO分子最多与周
2
围HO分子形成4个氢键,而HF分子最多与周围HF分子形成2个氢键,氢键越多,熔、
2
沸点越高,所以HO的熔、沸点高,故C项错误;氨气分子和水分子间形成氢键,导致氨
2
气极易溶于水,故D项正确。
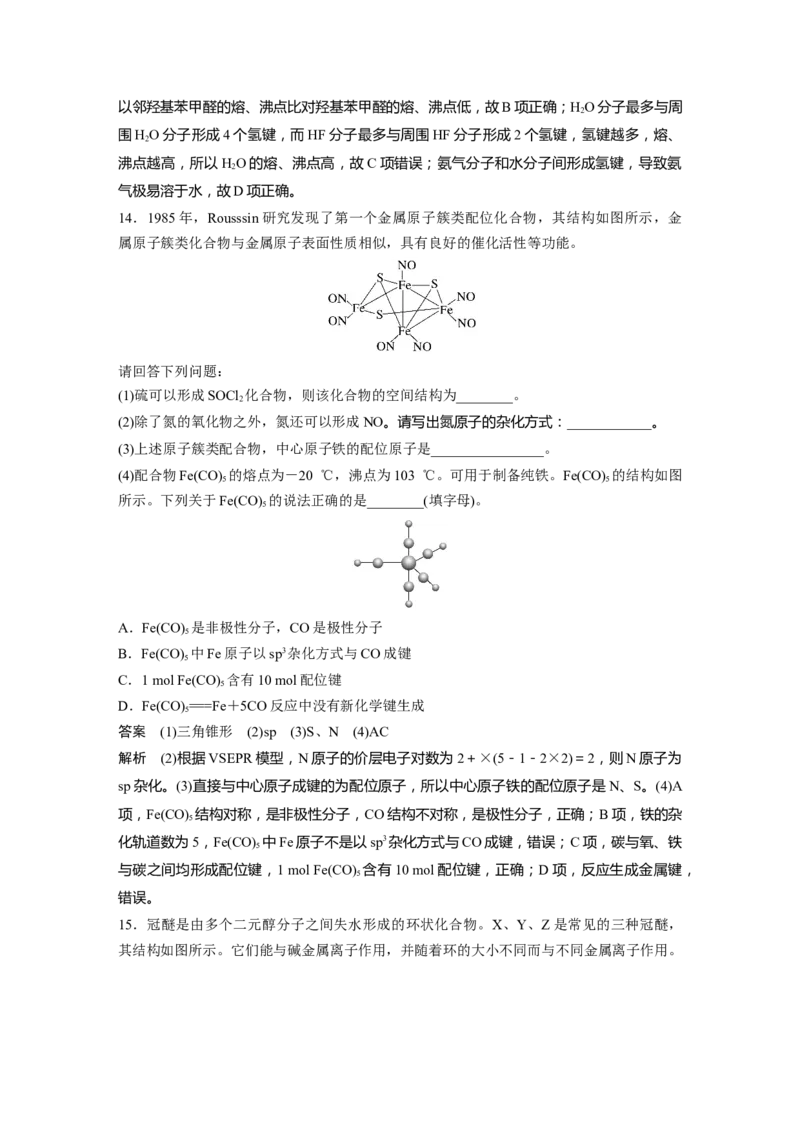
14.1985年,Rousssin研究发现了第一个金属原子簇类配位化合物,其结构如图所示,金
属原子簇类化合物与金属原子表面性质相似,具有良好的催化活性等功能。
请回答下列问题:
(1)硫可以形成SOCl 化合物,则该化合物的空间结构为________。
2
(2)除了氮的氧化物之外,氮还可以形成NO。请写出氮原子的杂化方式:____________。
(3)上述原子簇类配合物,中心原子铁的配位原子是________________。
(4)配合物Fe(CO) 的熔点为-20 ℃,沸点为103 ℃。可用于制备纯铁。Fe(CO) 的结构如图
5 5
所示。下列关于Fe(CO) 的说法正确的是________(填字母)。
5
A.Fe(CO) 是非极性分子,CO是极性分子
5
B.Fe(CO) 中Fe原子以sp3杂化方式与CO成键
5
C.1 mol Fe(CO) 含有10 mol配位键
5
D.Fe(CO) ===Fe+5CO反应中没有新化学键生成
5
答案 (1)三角锥形 (2)sp (3)S、N (4)AC
解析 (2)根据VSEPR模型,N原子的价层电子对数为2+×(5-1-2×2)=2,则N原子为
sp杂化。(3)直接与中心原子成键的为配位原子,所以中心原子铁的配位原子是N、S。(4)A
项,Fe(CO) 结构对称,是非极性分子,CO结构不对称,是极性分子,正确;B项,铁的杂
5
化轨道数为5,Fe(CO) 中Fe原子不是以sp3杂化方式与CO成键,错误;C项,碳与氧、铁
5
与碳之间均形成配位键,1 mol Fe(CO) 含有10 mol配位键,正确;D项,反应生成金属键,
5
错误。
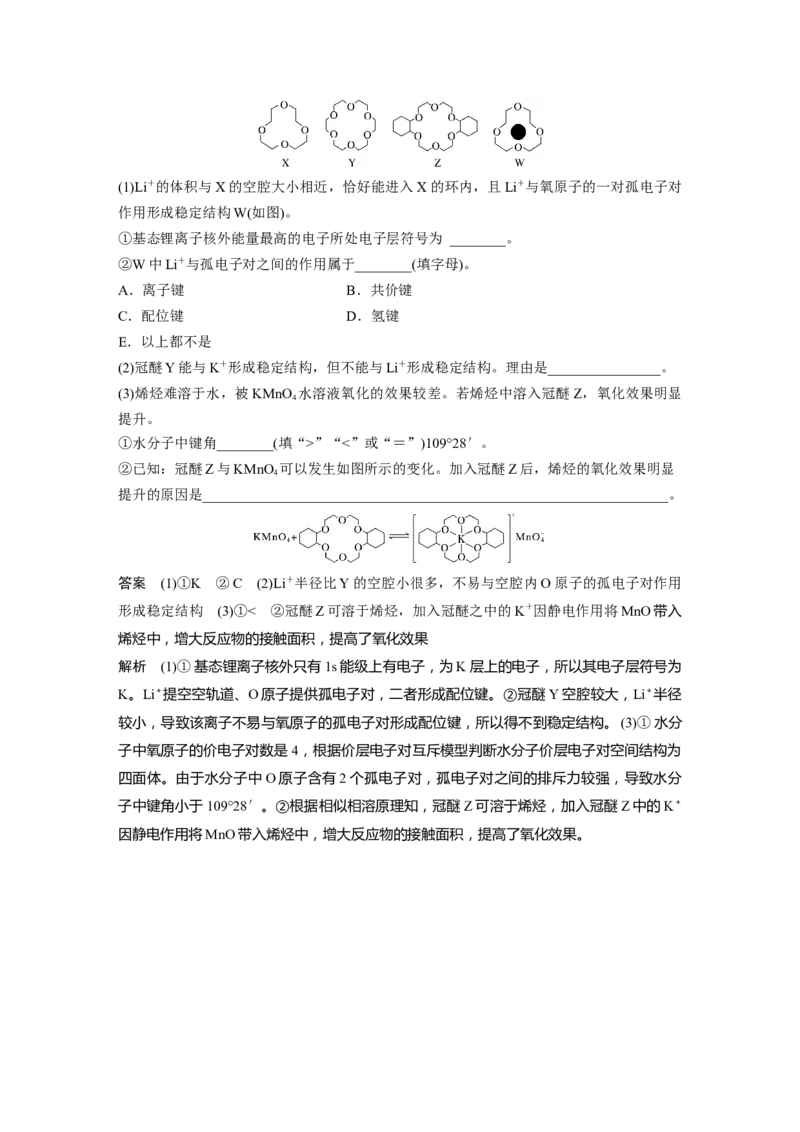
15.冠醚是由多个二元醇分子之间失水形成的环状化合物。X、Y、Z是常见的三种冠醚,
其结构如图所示。它们能与碱金属离子作用,并随着环的大小不同而与不同金属离子作用。(1)Li+的体积与X的空腔大小相近,恰好能进入X的环内,且Li+与氧原子的一对孤电子对
作用形成稳定结构W(如图)。
①基态锂离子核外能量最高的电子所处电子层符号为 ________。
②W中Li+与孤电子对之间的作用属于________(填字母)。
A.离子键 B.共价键
C.配位键 D.氢键
E.以上都不是
(2)冠醚Y能与K+形成稳定结构,但不能与Li+形成稳定结构。理由是________________。
(3)烯烃难溶于水,被KMnO 水溶液氧化的效果较差。若烯烃中溶入冠醚Z,氧化效果明显
4
提升。
①水分子中键角________(填“>”“<”或“=”)109°28′。
②已知:冠醚Z与KMnO 可以发生如图所示的变化。加入冠醚Z后,烯烃的氧化效果明显
4
提升的原因是__________________________________________________________________。
答案 (1)①K ②C (2)Li+半径比Y的空腔小很多,不易与空腔内O原子的孤电子对作用
形成稳定结构 (3)①< ②冠醚Z可溶于烯烃,加入冠醚之中的K+因静电作用将MnO带入
烯烃中,增大反应物的接触面积,提高了氧化效果
解析 (1)①基态锂离子核外只有1s能级上有电子,为K层上的电子,所以其电子层符号为
K。Li+提空空轨道、O原子提供孤电子对,二者形成配位键。②冠醚Y空腔较大,Li+半径
较小,导致该离子不易与氧原子的孤电子对形成配位键,所以得不到稳定结构。(3)①水分
子中氧原子的价电子对数是4,根据价层电子对互斥模型判断水分子价层电子对空间结构为
四面体。由于水分子中O原子含有2个孤电子对,孤电子对之间的排斥力较强,导致水分
子中键角小于109°28′。②根据相似相溶原理知,冠醚Z可溶于烯烃,加入冠醚Z中的K+
因静电作用将MnO带入烯烃中,增大反应物的接触面积,提高了氧化效果。