文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(福建专用)
黄金卷08
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Ga-70
第Ⅰ卷
一、单项选择题:共10题,每题4分,共40分。每题只有一个选项最符合题意。
1.《天工开物》中对“海水盐”有如下描述:“凡煎盐锅古谓之牢盆……其下列灶燃薪,多者十二三眼,
少者七八眼,共煎……火燃釜底,滚沸延及成盐”。下列分析错误的是
A.海水盐中不会含有溴元素 B.海水盐中含有多种杂质
C.“滚沸延及成盐”是物理变化 D.“火燃釜底”的目的是蒸发结晶
【答案】A
【详解】A.海水盐中含有溴元素,如NaBr,故A错误;
B.用海水制得的粗盐中含有多种可溶性杂质(MgCl 、CaCl 、NaSO 等)和不溶性杂质(泥沙等),故B正确;
2 2 2 4
C.“滚沸延及成盐”是盐的析出,是物理变化,故C正确;
D.“火燃釜底,滚沸延及成盐”,则“火燃釜底”的目的是蒸发结晶,故D正确;
故选A。
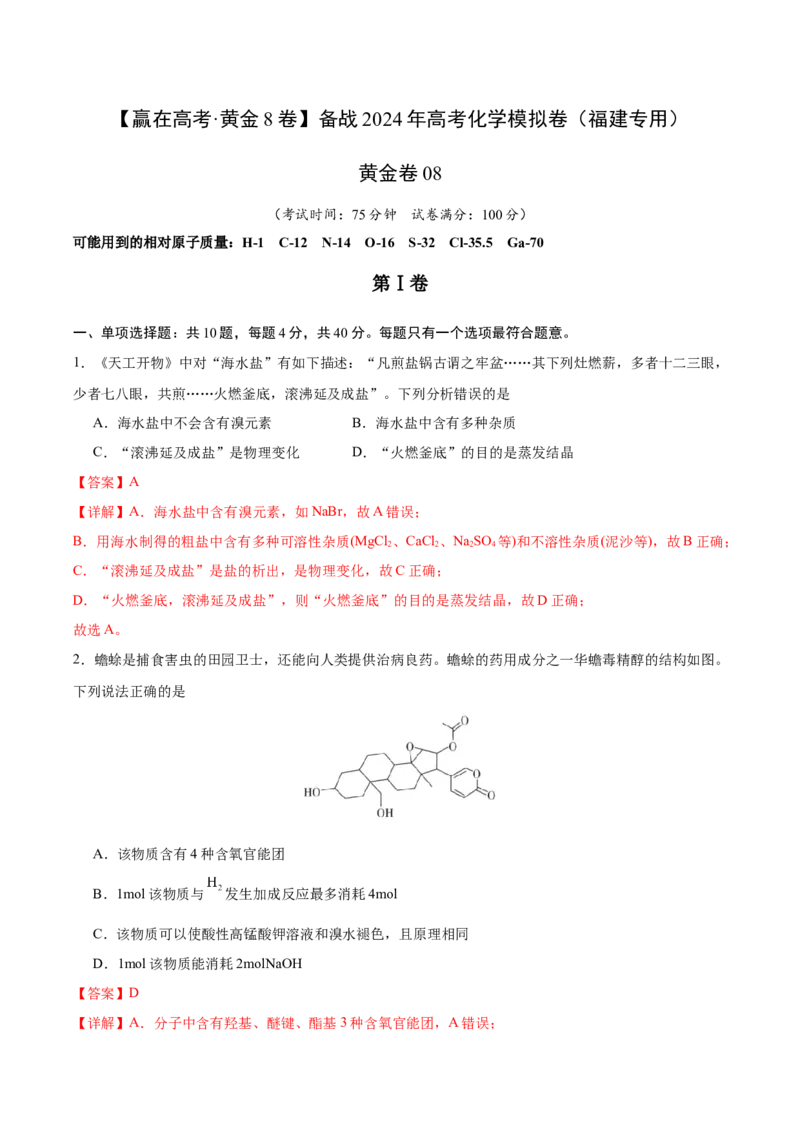
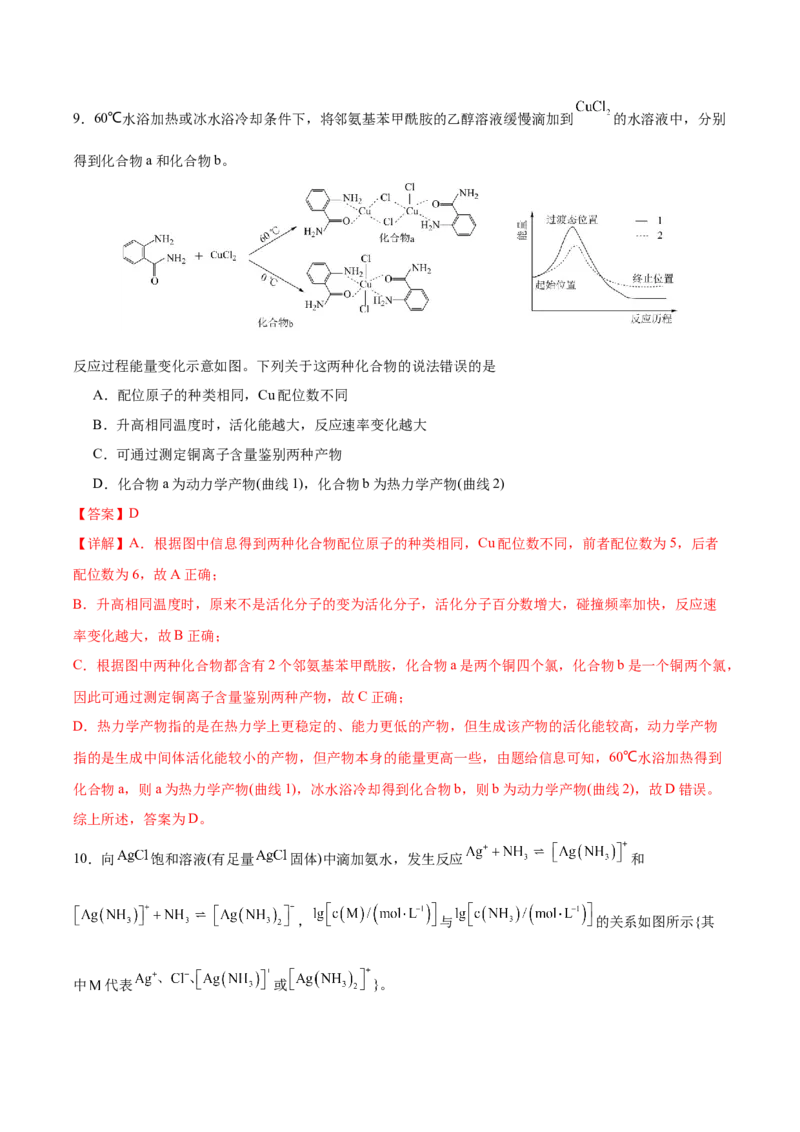
2.蟾蜍是捕食害虫的田园卫士,还能向人类提供治病良药。蟾蜍的药用成分之一华蟾毒精醇的结构如图。
下列说法正确的是
A.该物质含有4种含氧官能团
B.1mol该物质与 发生加成反应最多消耗4mol
C.该物质可以使酸性高锰酸钾溶液和溴水褪色,且原理相同
D.1mol该物质能消耗2molNaOH
【答案】D
【详解】A.分子中含有羟基、醚键、酯基3种含氧官能团,A错误;B.碳碳双键能与氢气加成,酯基不能与氢气发生加成反应,1mol该物质含2mol碳碳双键,最多消耗
2molH ,B错误;
2
C.该物质含碳碳双键,可以使酸性高锰酸钾溶液和溴水褪色,使酸性高锰酸钾溶液褪色,发生了氧化反
应,而使溴水褪色,发生了加成反应,原理不同,C错误;
D.该物质中只有酯基能与NaOH溶液反应,所以1mol该物质最多能消耗2molNaOH,D正确;
故选D。
3.用N 表示阿伏加德罗常数的值。下列说法正确的是
A
A.1 mol H O 中含有极性共价键的数目为3N
2 2 A
B.25℃1 L pH=1的HPO 溶液中H+数目为0.1N
3 4 A
C.20 g H18O含有的中子数为12N
2 A
D.足量铁粉与1 L14 mol/L浓硝酸加热充分反应转移电子数目为7N
A
【答案】B
【详解】A.1个HO 中含有2个极性键H-O键,则1 mol H O 中含有极性共价键的数目为2N ,A错误;
2 2 2 2 A
B.25℃1 L pH=1的HPO 溶液中H+的物质的量为n(H+)=1 L×0.1 mol/L=0.1 mol,故其中含有的H+数目为
3 4
0.1N ,B正确;
A
C.H18O的相对分子质量是20,1个分子中含有10个中子,20 g H18O的物质的量是1 mol,则在1 mol
2 2
H18O含有的中子数为10N ,C错误;
2 A
D.足量Fe与浓硝酸在加热时发生反应Fe+6HNO (浓)=Fe(NO )+3NO↑+3H O,随着反应的进行,溶液浓
3 3 3 2 2
度变稀,发生反应:3Fe+8HNO (稀)=3Fe(NO )+2NO↑+4HO,还原产物由NO 变为NO,因此无法计算反
3 3 3 2 2
应过程中电子转移的数目,D错误;
故合理选项是B。
4.下列实验及其结论都正确的是( )
实验 结论
A
氯气的水溶液可以导电 氯气是电解质
.
B 室温下,用pH试纸测定浓度均为0.1 mol·L-1的NaClO溶液和 比较HClO和CHCOOH的
3
. CHCOONa溶液的pH 酸性强弱
3
C 等体积、pH=3的两种酸HA和HB分别与足量的Zn反应,酸HA放出的
酸性HA比HB弱
. 氢气多
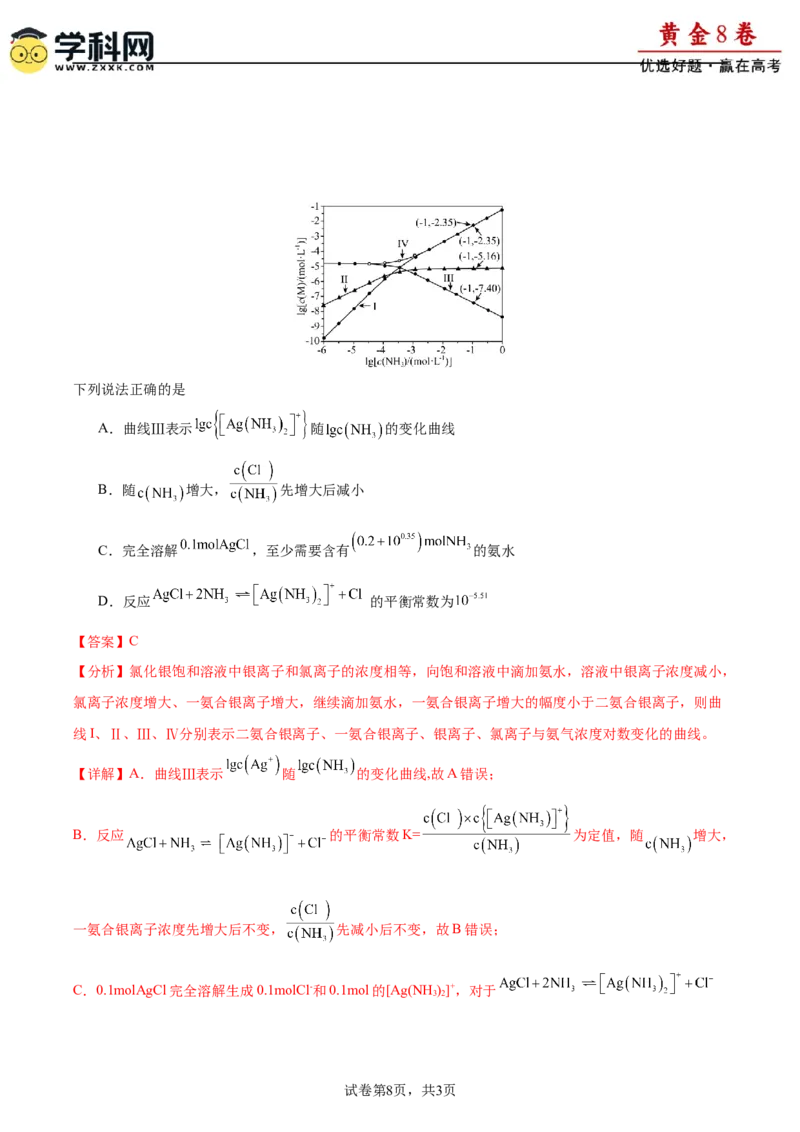
D 10mL 1mol·L-1的AgNO 3 溶液中先滴加1mol·L-1的NaCl溶液1mL,再 K sp (AgI)”、“=”或“<”)。
1
②进料组成中不含惰性气体Ar的图是 。
③图3中,当P=16MPa、x =0.25时,氮气的转化率a= 。该温度时,反应2NH (g)=N(g)
2 NH3 3 2
+3H (g)的平衡常数K= (MPa)2。
2 p
【答案】(1) (或 ) -92
(2) 7:2
(3) < 图4 50% 27
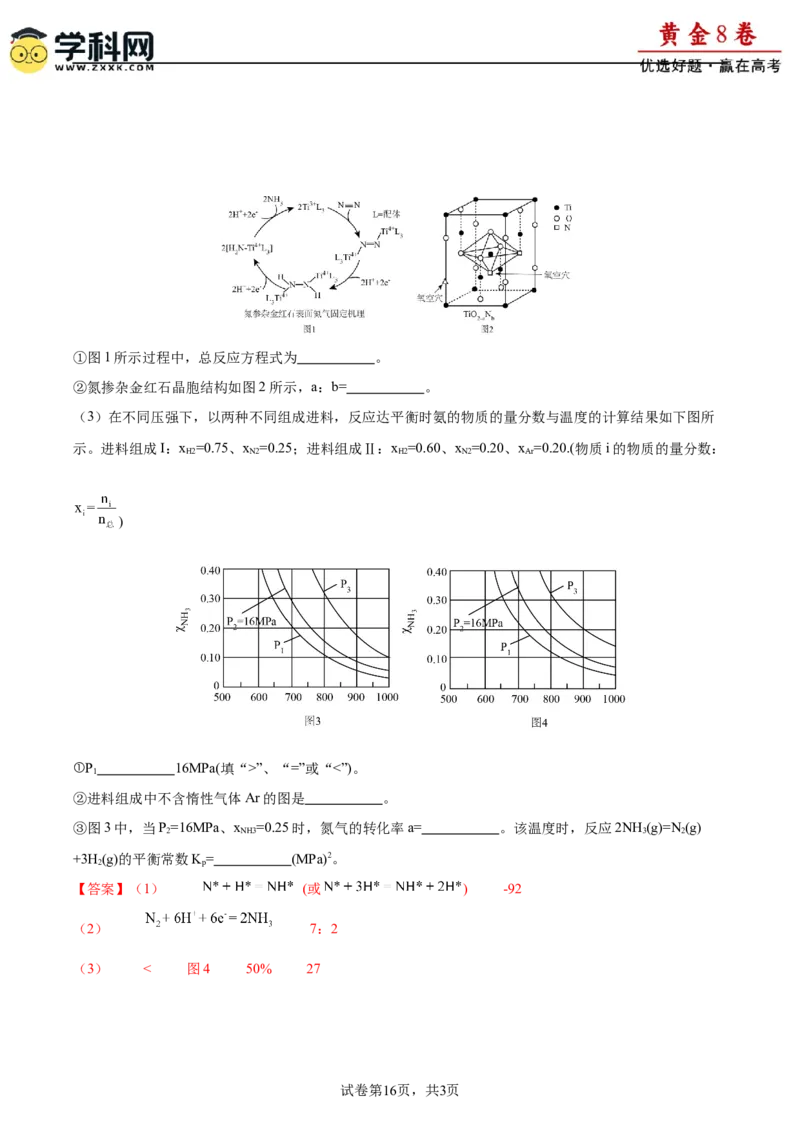
试卷第16页,共3页【详解】(1)在化学反应中,最大的能垒为速率控制步骤,根据题图可知,反应的化学方程式为
(或 );由题图可知,反应物总能量高于产物总能量,反应放热,且
的ΔH=-46kJ·mol-1,则合成氨反应 的
ΔH=-92kJ·mol-1,故答案为: (或 );-92;
(2)①依据氮掺杂金红石表面氮气固定机理可知,反应物为氮气和氢离子,生成物为氨气,金红石为催
化剂,总反应方程式为 ;
②由晶胞结构示意图可知, 晶胞中N原子数为 ,O原子数为 ,Ti原子
数为4,故 ; ,解得 , ;
(3)①合成氨的反应中,压强越大越利于氨的合成,则氨的物质的量分数越大,结合图像可知,在相同
温度下,氨的物质的量分数:p>p>p,所以压强:p>p>p,所以P<16MPa,故答案为:<;
3 2 1 3 2 1 1
②对比图3和图4可知,相同温度和相同压强下,图3中平衡时氨的物质的量分数较小,在恒压下充入惰
性气体Ar,导致反应混合物中各组分的浓度减小,各组分的分压也减小,化学平衡要向着气体分子数增大
的方向进行,即不利于合成氨,所以氨的物质的量分数小,因此进料组成中含惰性气体Ar的图是图3,不
含惰性气体Ar的图是图4,故答案为:图4;
③图3进料组成为 , , ,三者物质的量之比为3:1:1,假设进料中氢气、
氮气和氩气物质的量分别为3mol、1mol和1mol,平衡时氮气变化量为x,列三段式:
,当p=20MPa、 ,解得 ,
2
则氮气转化率 ;
平衡时氮气、氢气、氨气物质的量分别是 、1.5mol、 ,还有1molAr,物质的量分数分别是 、、 ,该温度下2NH (g)=N(g)+3H(g)的平衡常数 =
3 2 2
=27(MPa)2,故答案为:50%;27。
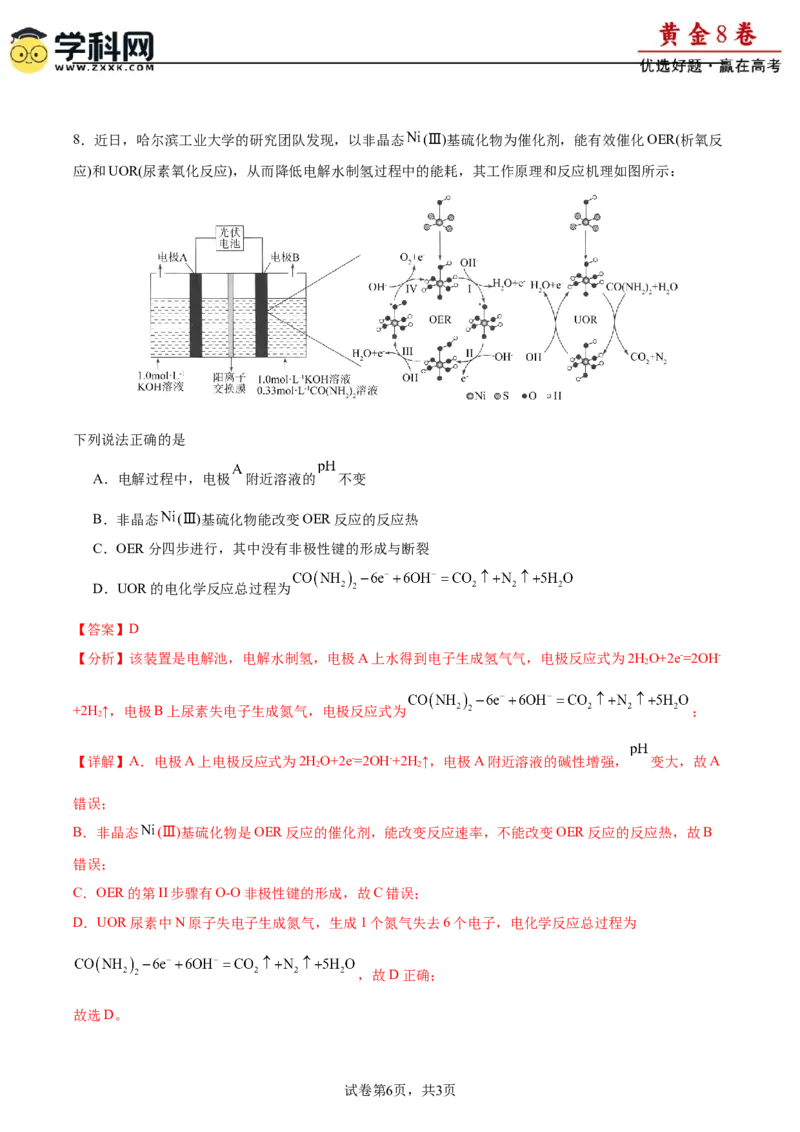
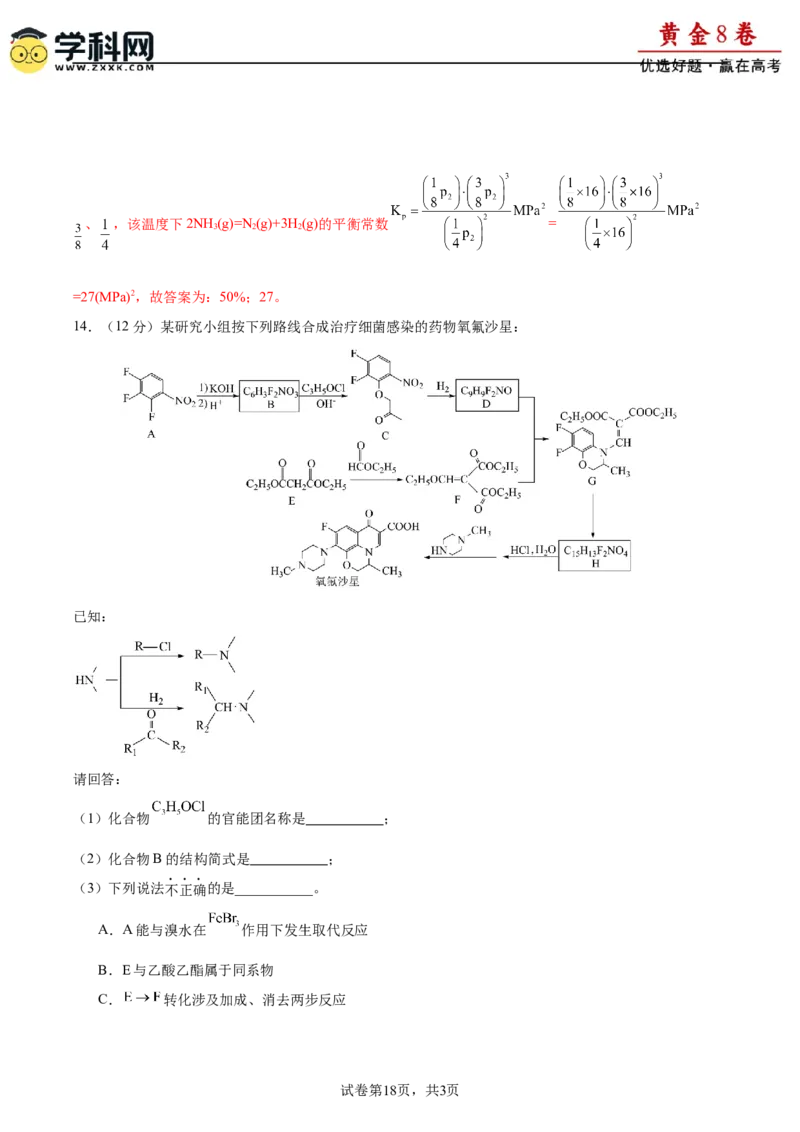
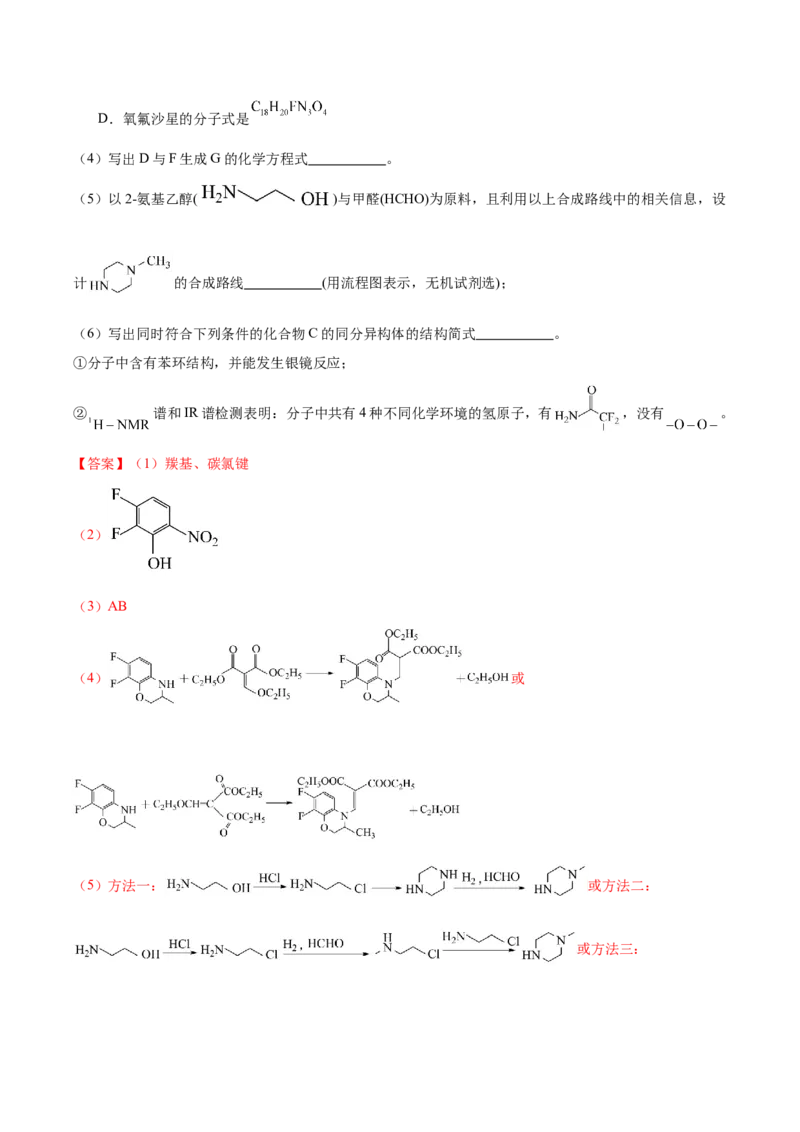
14.(12分)某研究小组按下列路线合成治疗细菌感染的药物氧氟沙星:
已知:
请回答:
(1)化合物 的官能团名称是 ;
(2)化合物B的结构简式是 ;
(3)下列说法不正确的是___________。
A.A能与溴水在 作用下发生取代反应
B.E与乙酸乙酯属于同系物
C. 转化涉及加成、消去两步反应
试卷第18页,共3页D.氧氟沙星的分子式是
(4)写出D与F生成G的化学方程式 。
(5)以2-氨基乙醇( )与甲醛(HCHO)为原料,且利用以上合成路线中的相关信息,设
计 的合成路线 (用流程图表示,无机试剂选);
(6)写出同时符合下列条件的化合物C的同分异构体的结构简式 。
①分子中含有苯环结构,并能发生银镜反应;
② 谱和IR谱检测表明:分子中共有4种不同化学环境的氢原子,有 ,没有 。
【答案】(1)羰基、碳氯键
(2)
(3)AB
(4) 或
(5)方法一: 或方法二:
或方法三:(6)
【分析】
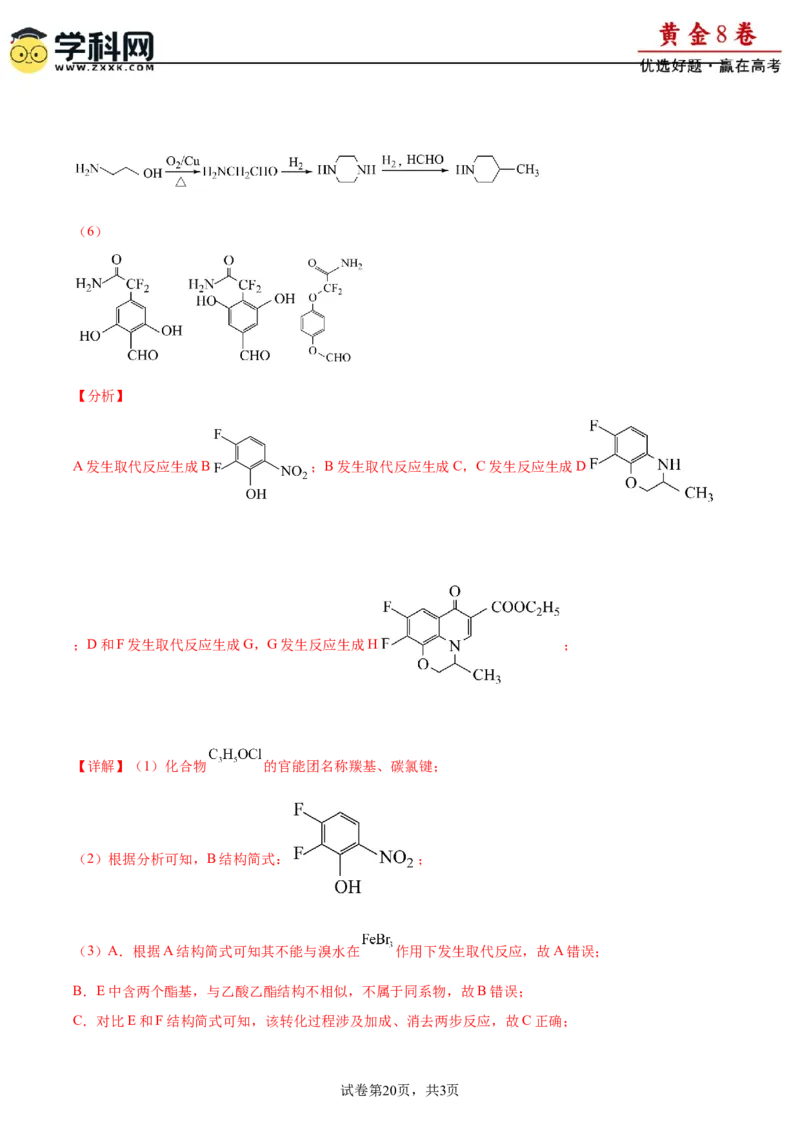
A发生取代反应生成B ;B发生取代反应生成C,C发生反应生成D
;D和F发生取代反应生成G,G发生反应生成H ;
【详解】(1)化合物 的官能团名称羰基、碳氯键;
(2)根据分析可知,B结构简式: ;
(3)A.根据A结构简式可知其不能与溴水在 作用下发生取代反应,故A错误;
B.E中含两个酯基,与乙酸乙酯结构不相似,不属于同系物,故B错误;
C.对比E和F结构简式可知,该转化过程涉及加成、消去两步反应,故C正确;
试卷第20页,共3页D.根据氧氟沙星结构简式可知,其分子式是 ,故D正确;
答案选AB;
(4)D与F生成G的化学方程式: 或
;
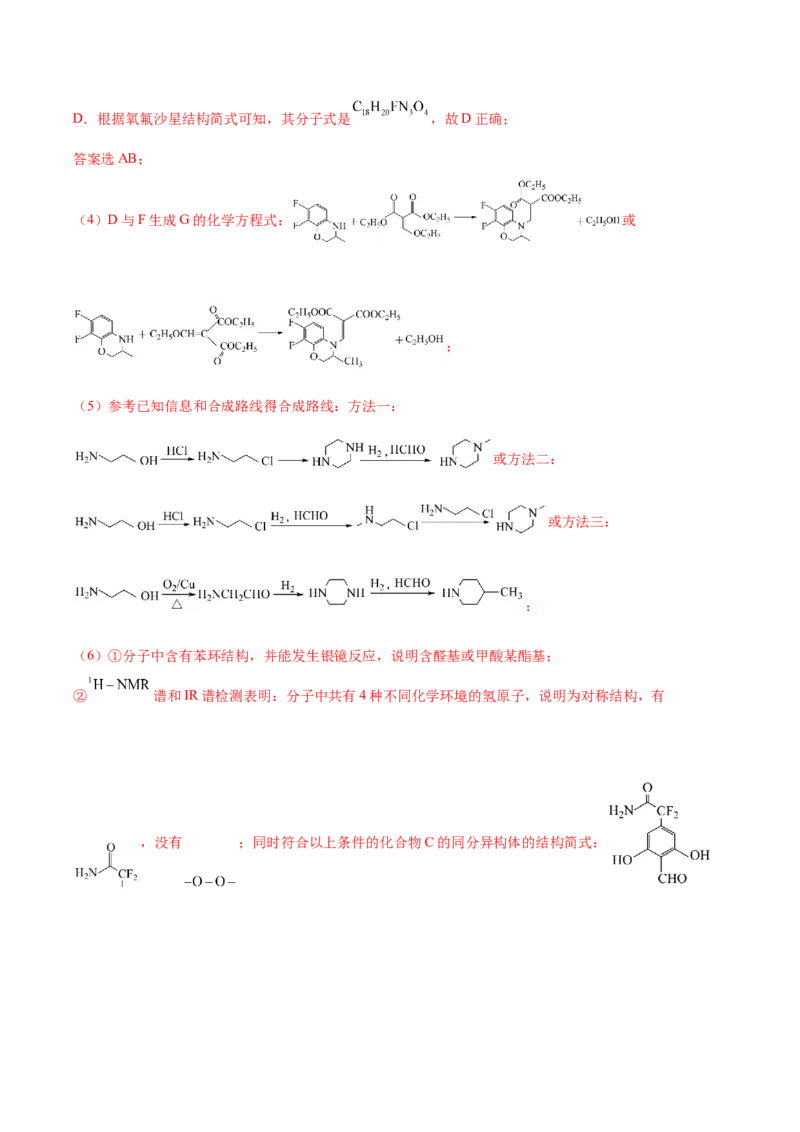
(5)参考已知信息和合成路线得合成路线:方法一:
或方法二:
或方法三:
;
(6)①分子中含有苯环结构,并能发生银镜反应,说明含醛基或甲酸某酯基;
② 谱和IR谱检测表明:分子中共有4种不同化学环境的氢原子,说明为对称结构,有
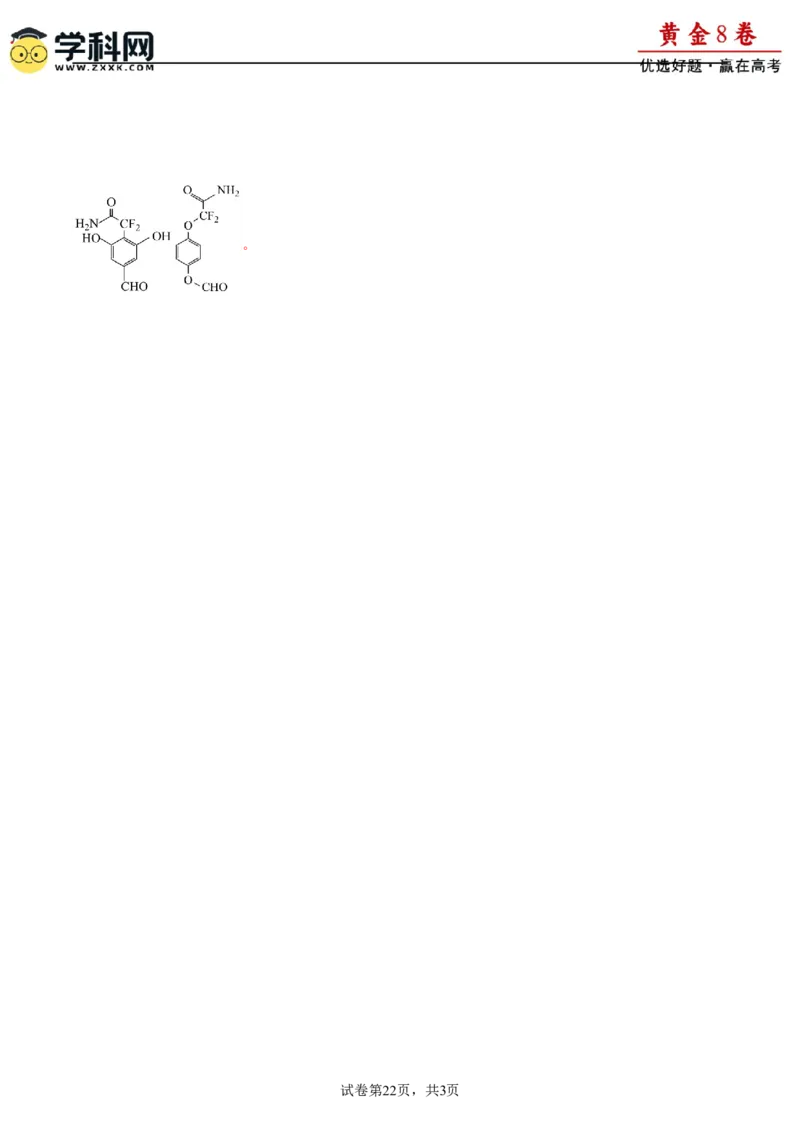
,没有 ;同时符合以上条件的化合物C的同分异构体的结构简式:。
试卷第22页,共3页