文档内容
重庆市 2025 年普通高等学校招生统一考试
化学试题
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试
卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.可能用到的相对原子质量:Se-79 Ag-108 Cl-35.5 I-127 O-16 Na-23
一、选择题:本大题共 14 小题,每小题 3 分,共 42 分,每题给出的四个选项中,只有一项
符合题目要求。
1. 抗日战争时期,根据地物资紧缺,军民自力更生,就地取材,采用下列方法生产化工产品,其中利用了
氧化还原反应原理的是
A. 用石磨代替打浆机碾碎硝化棉 B. 用陶缸作反应器以硫黄为原料生产硫酸
C. 通过蒸馏法以自酿的白酒为原料生产工业酒精 D. 通过水解法以植物油和熟石灰为原料生产甘油
【答案】B
【解析】
【详解】A.研磨硝化棉是物理粉碎过程,无化合价变化,不涉及氧化还原反应,A 错误;
B.硫磺(S)转化为硫酸(HSO )时,硫的化合价从 0 升至+6,发生氧化反应,涉及氧化还原反应,B 正
2 4
确;
C.蒸馏法分离酒精是物理过程,无新物质生成,不涉及氧化还原反应,C 错误;
D.植物油水解生成甘油和脂肪酸盐,属于水解反应,无化合价变化,不涉及氧化还原反应,D 错误;
故选 B。
2. 下列化学科普实验所涉及物质的性质或应用描述正确的是
选项 科普试验 性质或应用
A 焰色试验 Na 和 K 的焰色均为紫色
B 漂白实验 和 均可使品红溶液永久褪色
第 1页/共 21页C 蛋清变性 醋酸铅溶液和甲醛溶液均可使蛋白质变性
D 铜板刻蚀 氯化铁溶液和浓硫酸均可在常温下刻蚀铜板
A A B. B C. C D. D
【答案】C
【解析】
【详解】A.钠的焰色反应为黄色,钾需透过蓝色钴玻璃观察呈紫色,现象描述错误,A 错误;
B. 的漂白是暂时性, 需生成 HClO 才有漂白性且为永久性,但 本身不直接漂白,B 错误;
C.醋酸铅(重金属盐)和甲醛均能使蛋白质不可逆变性,性质与现象正确,C 正确;
D.铜在常温浓硫酸中表现出惰性,加热才能反应,故浓硫酸无法腐蚀铜电路板,而 溶液可以,D 错
误;
故选 C。
3. 下列有关离子反应错误的是
A Ca(OH) 溶液滴入 NaHSO 溶液中:
2 3
B. 加入水中:
C. 通入水中:
D. 通入 NaBr 溶液中:
【答案】A
【解析】
【详解】A.亚硫酸氢钠(NaHSO)与石灰水反应时,HSO 不能拆开,先与 OH-中和生成 SO ,再与
3
Ca2+结合生成 CaSO 沉淀,正确的方程式为: ,A 方程式错误;
3
B.Na
2
O
2
与水反应的离子方程式为 2Na
2
O
2
+2H
2
O=4Na++4OH-+O
2
↑,符合反应实际(生成 NaOH 和 O
2
),
B 离子方程式正确;
C.NO
2
与水反应的离子方程式为 3NO
2
+H
2
O=2H++2NO
3
-+NO,与化学方程式 3NO
2
+H
2
O=2HNO
3
+ NO 一
致,C 方程式正确;
D.Cl 与 NaBr 溶液反应的离子方程式 Cl+2Br-=Br +2Cl-,符合氧化还原反应规律(Cl 氧化 Br-为 Br ),D
2 2 2 2 2
第 2页/共 21页方程式正确;
故选 A。
4. 下列实验操作符合规范的是
A. 加热 B. 定容 C. 稀释 D. 滴定
【答案】A
【解析】
【详解】A.给试管中 物质加热时,液体体积不能超过试管容积的 ,且用酒精灯外焰加热,操作合理,
A 正确;
B.定容时,视线应与刻度线保持水平,操作错误,B 错误;
C.稀释浓硫酸应遵循“酸入水”的原则,操作错误,C 错误;
D.氢氧化钠溶液呈碱性,应放在碱式滴定管中进行滴定,装置使用错误,D 错误;
故选 A。
5. 根据元素周期律,同时满足条件(ⅰ)和条件(ⅱ)的元素是
(ⅰ)电负性大于同族其他元素;(ⅱ)第一电离能高于同周期相邻的元素
A. Al B. Si C. B D. Be
【答案】D
【解析】
【详解】A.Al 是第ⅢA 族元素,同主族中电负性最大的是 B,因此 Al 不满足条件(i),A 错误;
B.Si 是第ⅣA 族元素,同主族中电负性最大的是 C,因此 Si 不满足条件(i),B 错误;
C.B 是第ⅢA 族元素,电负性在同主族中最大,满足条件(i)。B 是ⅢA 族元素,同周期电离能从左往右
逐渐增加,但 Be 是第ⅡA 族元素,2p 为全空,比较稳定,电离能大于 B,所以 B 的第一电离能比相邻的
第 3页/共 21页Be 和 C 都小,不满足条件(ii),C 错误;
D.Be 是第ⅡA 族元素,电负性在同主族中最大,满足条件(i);Be 是第ⅡA 族元素,2p 为全空,比较稳
定,电离能大于 B 和 Li,所以 Be 的第一电离能大于同周期相邻主族元素,满足条件(ii),D 正确;
故选 D。
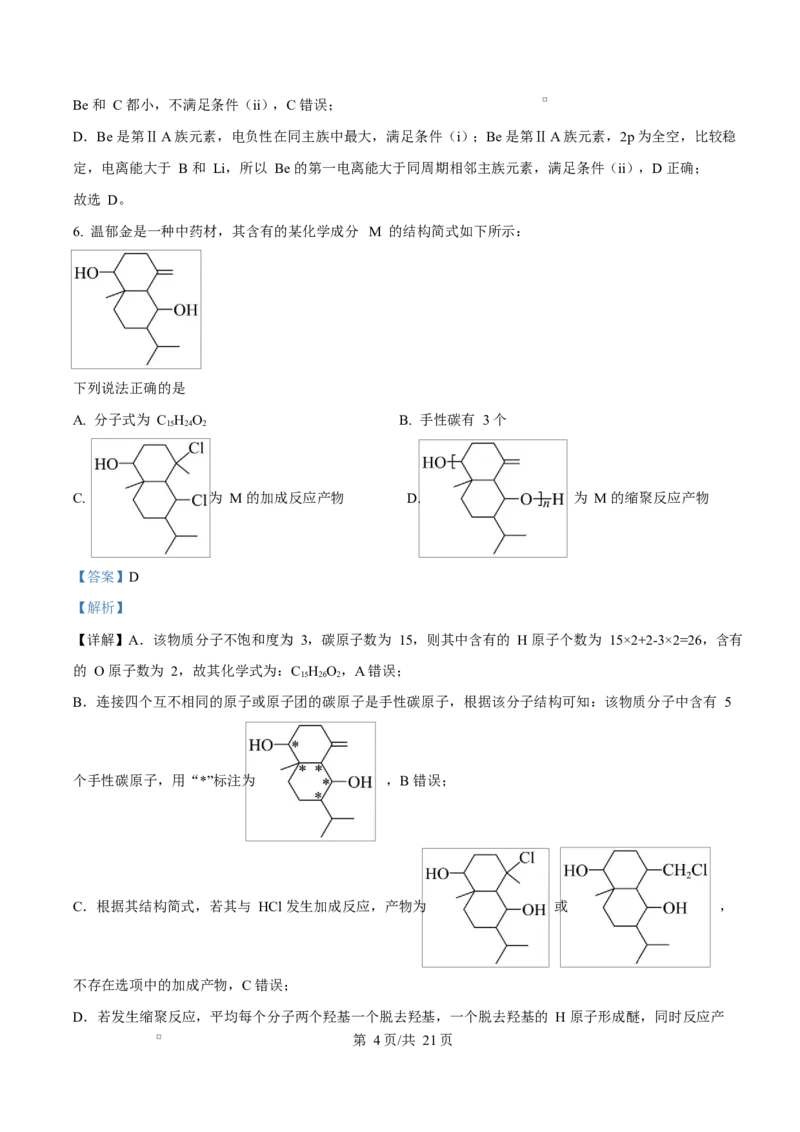
6. 温郁金是一种中药材,其含有的某化学成分 M 的结构简式如下所示:
下列说法正确的是
A. 分子式为 C H O B. 手性碳有 3 个
15 24 2
C. 为 M 的加成反应产物 D. 为 M 的缩聚反应产物
【答案】D
【解析】
【详解】A.该物质分子不饱和度为 3,碳原子数为 15,则其中含有的 H 原子个数为 15×2+2-3×2=26,含有
的 O 原子数为 2,故其化学式为:C H O,A 错误;
15 26 2
B.连接四个互不相同的原子或原子团的碳原子是手性碳原子,根据该分子结构可知:该物质分子中含有 5
个手性碳原子,用“*”标注为 ,B 错误;
C.根据其结构简式,若其与 HCl 发生加成反应,产物为 或 ,
不存在选项中的加成产物,C 错误;
D.若发生缩聚反应,平均每个分子两个羟基一个脱去羟基,一个脱去羟基的 H 原子形成醚,同时反应产
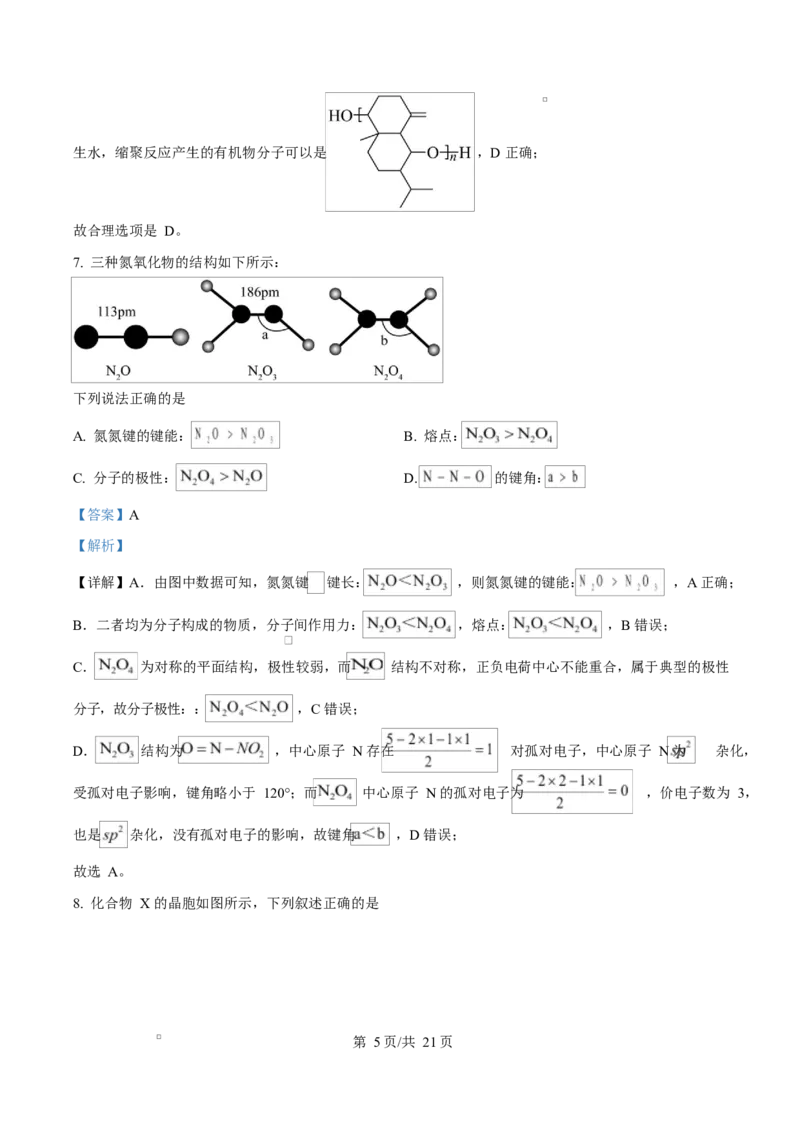
第 4页/共 21页生水,缩聚反应产生的有机物分子可以是 ,D 正确;
故合理选项是 D。
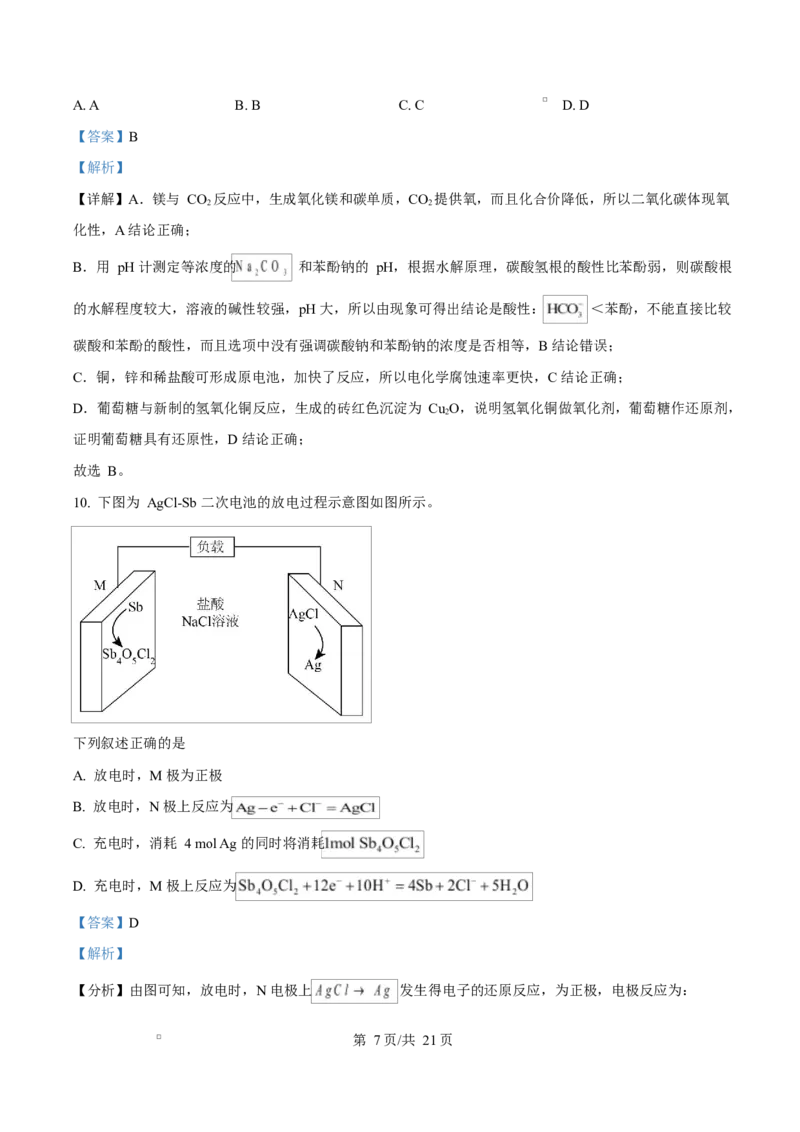
7. 三种氮氧化物的结构如下所示:
下列说法正确的是
A. 氮氮键的键能: B. 熔点:
C. 分子的极性: D. 的键角:
【答案】A
【解析】
【详解】A.由图中数据可知,氮氮键 键长: ,则氮氮键的键能: ,A 正确;
B.二者均为分子构成的物质,分子间作用力: ,熔点: ,B 错误;
C. 为对称的平面结构,极性较弱,而 结构不对称,正负电荷中心不能重合,属于典型的极性
分子,故分子极性:: ,C 错误;
D. 结构为 ,中心原子 N 存在 对孤对电子,中心原子 N 为 杂化,
受孤对电子影响,键角略小于 120°;而 中心原子 N 的孤对电子为 ,价电子数为 3,
也是 杂化,没有孤对电子的影响,故键角 ,D 错误;
故选 A。
8. 化合物 X 的晶胞如图所示,下列叙述正确的是
第 5页/共 21页A. X 中存在 键 B. X 属于混合型晶体 C. X 的化学式可表示为 D. X 中 C 原子上有
1 对孤电子对
【答案】C
【解析】
【分析】由图可知,晶胞中 C 原子的个数是 ,N 位于晶胞内部,个数为 4,则晶胞化学式为 ;
【详解】A.C、N 均以单键连接,晶胞中不含π键,A 错误;
B.晶胞内只存在共价键,不是混合型晶体,B 错误;
C.由分析可知,晶胞化学式为 ,C 正确;
D.位于面心的 C 原子,与周围 4 个氮原子(位于两个晶胞内)相连,其配位数为 4,不存在孤独电子,D 错
误;
故选 C。
9. 下列实验操作及其现象不能推出相应结论的是
选
操作及现象 结
论 项
A 将点燃的镁条迅速伸入集满 的集气瓶种,产生白烟和黑色固体 具有氧化性
B 用 pH 计测得碳酸钠溶液的 pH 小于苯酚钠溶液的 pH 酸性:碳酸>苯酚
在盛有稀盐酸的试管中加入锌片,产生气泡;再将铜丝插入试管且接触锌片, 反应速率:电化
学 C
产生气泡的速率增大 腐蚀>化学腐蚀
将一定浓度的葡萄糖溶液滴入新制 悬浊液中,加热,生成砖红色沉
D 葡萄属于还原糖
淀
第 6页/共 21页A. A B. B C. C D. D
【答案】B
【解析】
【详解】A.镁与 CO 反应中,生成氧化镁和碳单质,CO 提供氧,而且化合价降低,所以二氧化碳体现氧
2 2
化性,A 结论正确;
B.用 pH 计测定等浓度的 和苯酚钠的 pH,根据水解原理,碳酸氢根的酸性比苯酚弱,则碳酸根
的水解程度较大,溶液的碱性较强,pH 大,所以由现象可得出结论是酸性: <苯酚,不能直接比较
碳酸和苯酚的酸性,而且选项中没有强调碳酸钠和苯酚钠的浓度是否相等,B 结论错误;
C.铜,锌和稀盐酸可形成原电池,加快了反应,所以电化学腐蚀速率更快,C 结论正确;
D.葡萄糖与新制的氢氧化铜反应,生成的砖红色沉淀为 Cu O,说明氢氧化铜做氧化剂,葡萄糖作还原剂,
2
证明葡萄糖具有还原性,D 结论正确;
故选 B。
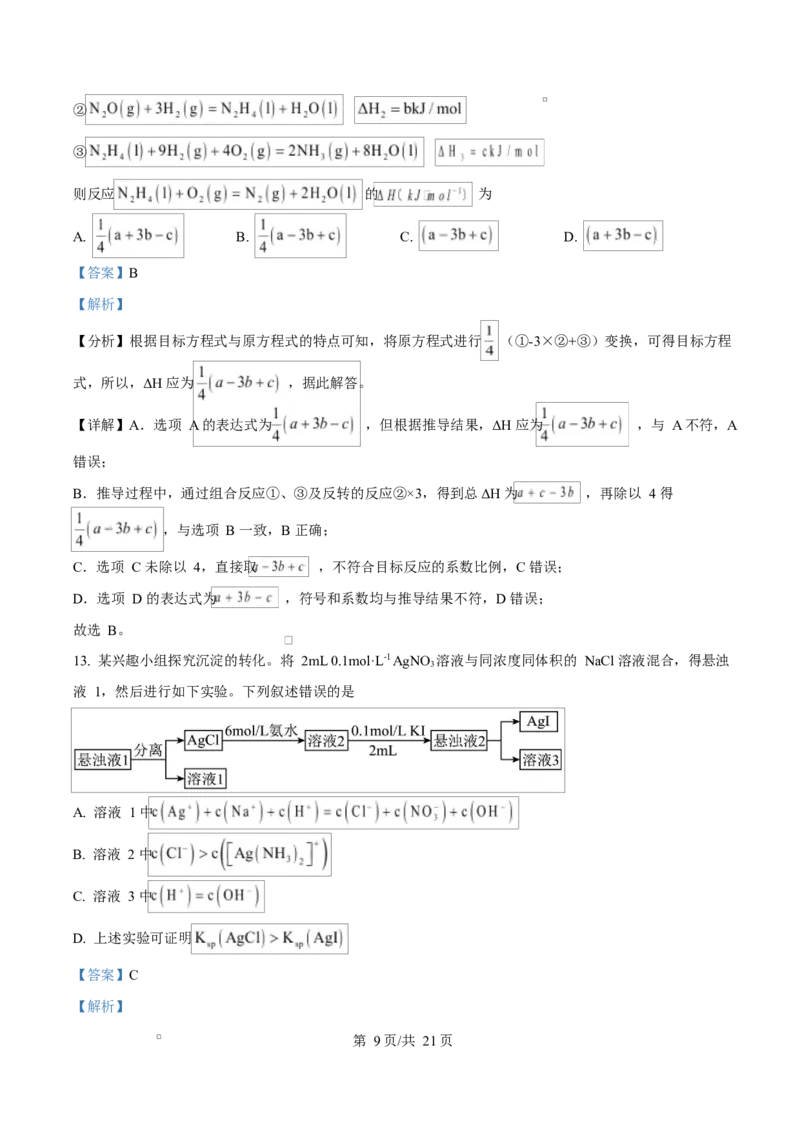
10. 下图为 AgCl-Sb 二次电池的放电过程示意图如图所示。
下列叙述正确的是
A. 放电时,M 极为正极
B. 放电时,N 极上反应为
C. 充电时,消耗 4 mol Ag 的同时将消耗
D. 充电时,M 极上反应为
【答案】D
【解析】
【分析】由图可知,放电时,N 电极上 发生得电子的还原反应,为正极,电极反应为:
第 7页/共 21页,M 电极为负极,电极反应为 ,充电时,
N 为阳极,M 为阴极,电极反应与原电池相反,据此解答。
【详解】A.由分析可知,放电时,M 电极为负极,A 错误;
B.由分析可知,放电时,N 电极反应为: ,B 错误;
C.由分析可知,建立电子转移关系式: ,由此可知,消耗 4molAg,同时消耗
,C 错误;
D.充电时,M 极为阴极,电极反应与原电池相反: ,D
正确;
故选 D。
11. 某化合物由原子序数依次增大的长周期主族元素 X、Y 和 Z 组成。X 的价层电子数为 4,Y 只有一个未
成对电子,Z+ 的电子占据的最高能级为全充满的 4p 能级。关于这三种元素说法正确的是
A. X、Y 和 Z 位于同一周期 B. 氧化物的水化物碱性最强的是 X
C. 单质熔点最高的是 Y D. 原子半径是最大的是 Z
【答案】D
【解析】
【分析】X、Y、Z 的原子序数依次增大且均为长周期主族元素。X 的价层电子数为 4(ⅣA 族),Y 有 1 个
未成对电子(可能为 IA 族或ⅦA 族), 的 4p 轨道填满,说明 Z 的原子序数为 37,即 Rb,根据原子序数
依次增大,可确定 X 为 Ge,Y 为 Br,据此解答。
【详解】A.分析可知,X 为 Ge,Y 为 Br,Z 为 Rb,不属于同一周期,A 错误;
B.X 为 Ge,Y 为 Br,Z 为 Rb,金属性最强的元素为 Rb,所以最高价氧化物对应水化物碱性最强的是 Z,
B 错误;
C.X 为 Ge,单质为金属晶体;Y 为 Br,单质为分子晶体;Z 为 Rb,单质为金属晶体;Ge 原子半径较小,
而且价电子数多,金属键较强,熔点较高,所以单质熔点最高的是 X,C 错误;
D.电子层数越多的,原子半径越大,X,Y 为第四周期,Z 为第五周期,所 Z 的原子半径最大,D 正确;
故选 D。
12. 肼( )与氧化剂剧烈反应,释放大量的热量,可作火箭燃料。已知下列反应:
①
第 8页/共 21页②
③
则反应 的 为
A. B. C. D.
【答案】B
【解析】
【分析】根据目标方程式与原方程式的特点可知,将原方程式进行 (①-3×②+③)变换,可得目标方程
式,所以,ΔH 应为 ,据此解答。
【详解】A.选项 A 的表达式为 ,但根据推导结果,ΔH 应为 ,与 A 不符,A
错误;
B.推导过程中,通过组合反应①、③及反转的反应②×3,得到总ΔH 为 ,再除以 4 得
,与选项 B 一致,B 正确;
C.选项 C 未除以 4,直接取 ,不符合目标反应的系数比例,C 错误;
D.选项 D 的表达式为 ,符号和系数均与推导结果不符,D 错误;
故选 B。
13. 某兴趣小组探究沉淀的转化。将 2mL 0.1mol·L-1 AgNO 溶液与同浓度同体积的 NaCl 溶液混合,得悬浊
3
液 1,然后进行如下实验。下列叙述错误的是
A. 溶液 1 中
B. 溶液 2 中
C. 溶液 3 中
D. 上述实验可证明
【答案】C
【解析】
第 9页/共 21页【分析】在 2mL0.2mol/L 的 溶液中加入等体积等浓度的 NaCl 溶液得悬浊液 1,经分离后,向
中滴加 6mol/L 的氨水,发生反应 ,加入 0.1mol/LKI 溶
液 2mL,发生反应: ,得到 沉淀,由物质的量关系可知,
不能完全反应,溶液 3 中可能还存在剩余的氨水以及 ;
【详解】A.溶液 1 中主要溶质是 ,同时由于存在溶解平衡: ,
还存在极少量的 ,选项中满足电荷守恒关系,A 正确;
B.根据元素守恒可知,若 不水解,则 ,但 会水解生成其他含银的微
粒,故 ,B 正确;
C.溶液 3 中可能存在氨水过量的情况,不能得出 的结论,C 错误;
D.由实验操作可知,存在转化 ,由此说明 AgI 更难溶,故可得出结
论 ,D 正确;
故选 C。
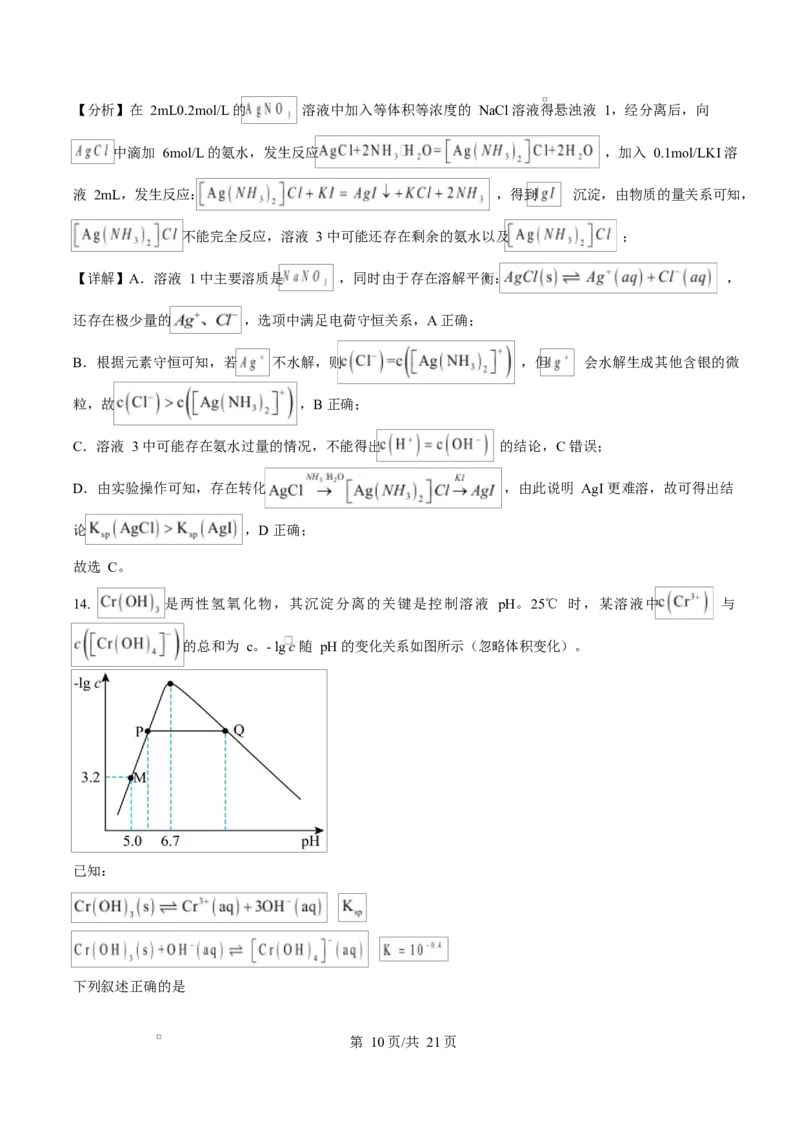
14. 是两性氢氧化物,其沉淀分离的关键是控制溶液 pH。25℃ 时,某溶液中 与
的总和为 c。- lg c 随 pH 的变化关系如图所示(忽略体积变化)。
已知:
下列叙述正确的是
第 10页/共 21页A. 由 M 点可以计算 B. 恰好沉淀完全时 pH 为 6.7
C. P 点沉淀质量小于 Q 点沉淀质量 D. 随 pH 增大 先减小后增大
【答案】A
【解析】
【分析】 与 的总和为 c,随着 pH 增大,发生反应:
,含铬微粒总浓度下降,随着 pH 继续增大,发生反应 :
含铬微粒总浓度上升,据此解答。
【 详 解 】 A. M 点 时 , , ,
, 几 乎 可 以 忽 略 不 计 , 含 Cr 微 粒 主 要 为 ,
,A 正确;
B. 恰好完全沉淀时, ,由 数据计算可知, ,
恰好完全沉淀 pH 最小值 5.6,B 错误;
C.P 和 Q 点溶液中含 Cr 微粒总和相等,生成的 质量相等,则 P 点沉淀质量等于 Q 点沉淀质
量,C 错误;
D.随着 pH 的增大, 减小,而 增大, 比值减小,D 错误;
故选 A。
二、非选择题:共 58 分。
15. 硒(Se)广泛应用于农业和生物医药等领域,一种利用 H2Se 热解制备高纯硒的流程如下:
第 11页/共 21页已知 HSe 的沸点为 231K,回答下列问题:
2
(1)真空焙烧时生成的主要产物为 ,其中 Se 的化合价为_______,Al 元素基态原子的电子排布式
为_______。
(2)氢化过程没有发生化合价的变化,Al 元素转化为 Al O·xHO,则反应的化学方程式为_______。
2 3 2
(3)热解反应: 。冷凝时,将混合气体温度迅速降至 500K 得到固
态硒。Se由气态直接转变为固态的过程称为_______。迅速降温的目的_______;冷凝后尾气的成分为_______
(填化学式)。
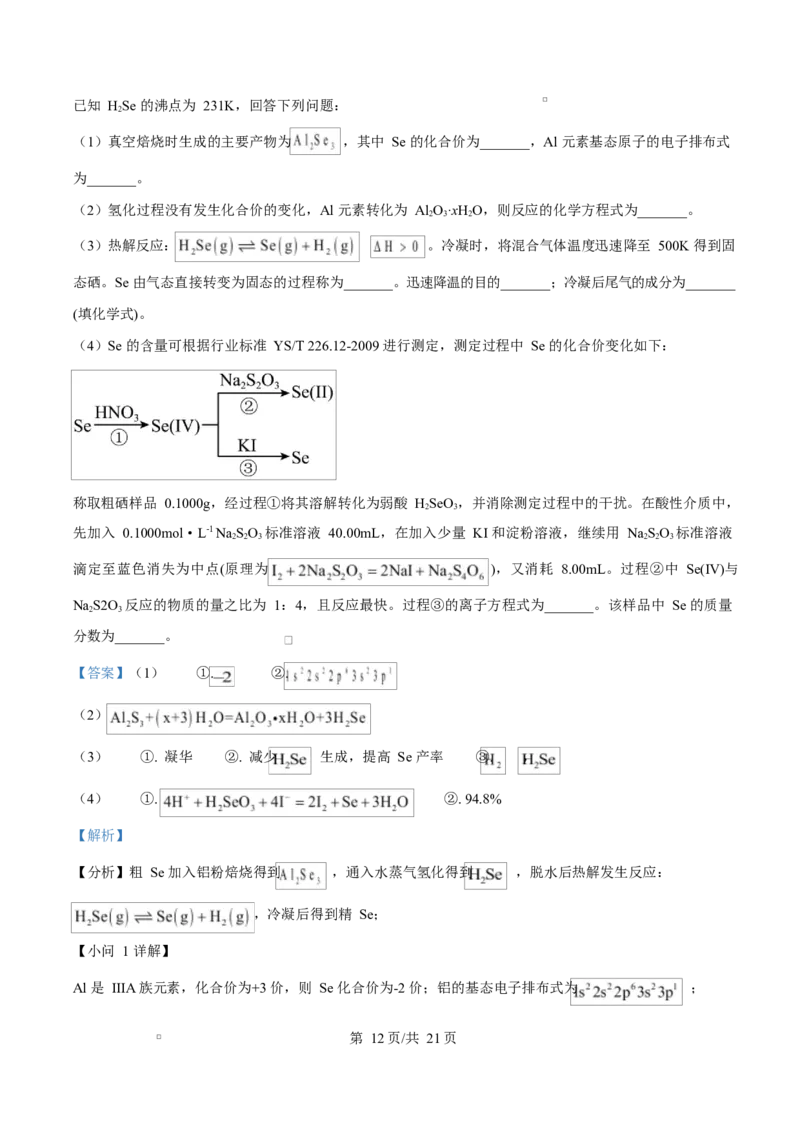
(4)Se 的含量可根据行业标准 YS/T 226.12-2009 进行测定,测定过程中 Se 的化合价变化如下:
称取粗硒样品 0.1000g,经过程①将其溶解转化为弱酸 HSeO,并消除测定过程中的干扰。在酸性介质中,
2 3
先加入 0.1000mol·L-1 NaSO 标准溶液 40.00mL,在加入少量 KI 和淀粉溶液,继续用 NaSO 标准溶液
2 2 3 2 2 3
滴定至蓝色消失为中点(原理为 ),又消耗 8.00mL。过程②中 Se(IV)与
NaS2O 反应的物质的量之比为 1:4,且反应最快。过程③的离子方程式为_______。该样品中 Se 的质量
2 3
分数为_______。
【答案】(1) ①. ②.
(2)
(3) ①. 凝华 ②. 减少 生成,提高 Se 产率 ③. ,
(4) ①. ②. 94.8%
【解析】
【分析】粗 Se 加入铝粉焙烧得到 ,通入水蒸气氢化得到 ,脱水后热解发生反应:
,冷凝后得到精 Se;
【小问 1 详解】
Al 是 IIIA 族元素,化合价为+3 价,则 Se 化合价为-2 价;铝的基态电子排布式为 ;
第 12页/共 21页【小问 2 详解】
“氢化”过程是 与水蒸气反应生成 ,化学方程式为
;
【小问 3 详解】
从气态变为固态的过程为凝华;已知热解正向是吸热反应,降温时,为避免平衡逆向移动,需要迅速冷凝
Se 蒸汽,故目的是减少 生成,提高 Se 产率;尾气种含有 以及少量的 ;
【小问 4 详解】
反应③是 被 KI 还原为 Se 的过程,离子方程式为: ;
第一次加入 40.00mL 的 溶液和 KI 溶液,二者同时做还原剂,将 还原为 Se,第二次再加
入同浓度的 滴定上一步生成的碘单质,整个过程相当于 48mL 0.1mol/L 的 溶液与
反应,根据已知条件 Se(IV)与 反应的物质的量之比为 ,则
,样品中 Se 的含量:
。
16. 糖精钠是一种甜味剂。某实验小组在实验室利用甲苯氯磺化法按一下五个步骤制备糖精钠(部分操作及
反应条件略)。
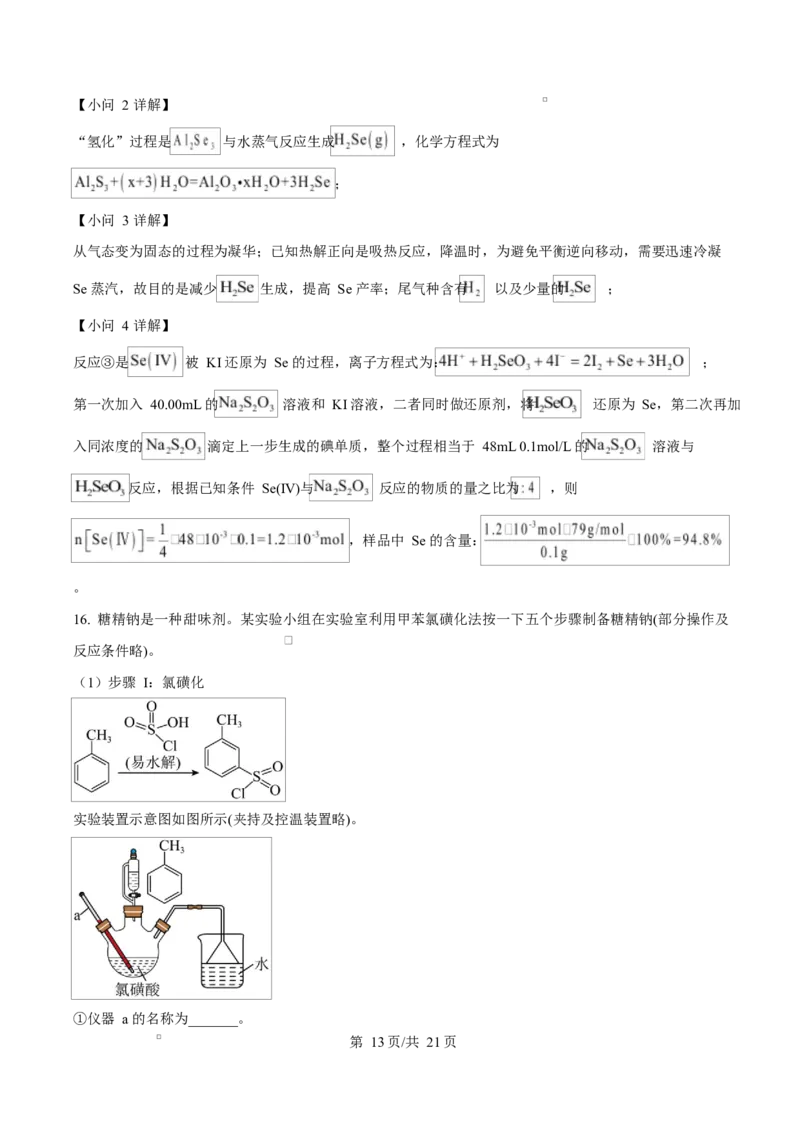
(1)步骤 I:氯磺化
实验装置示意图如图所示(夹持及控温装置略)。
①仪器 a 的名称为_______。
第 13页/共 21页②烧杯中吸收的尾气是_______(填化学式)。
(2)步骤 II:氨化
若取邻甲苯磺酰氯 0.3mol,理论上至少需加入 15mol·L-1 氨水_______mL。
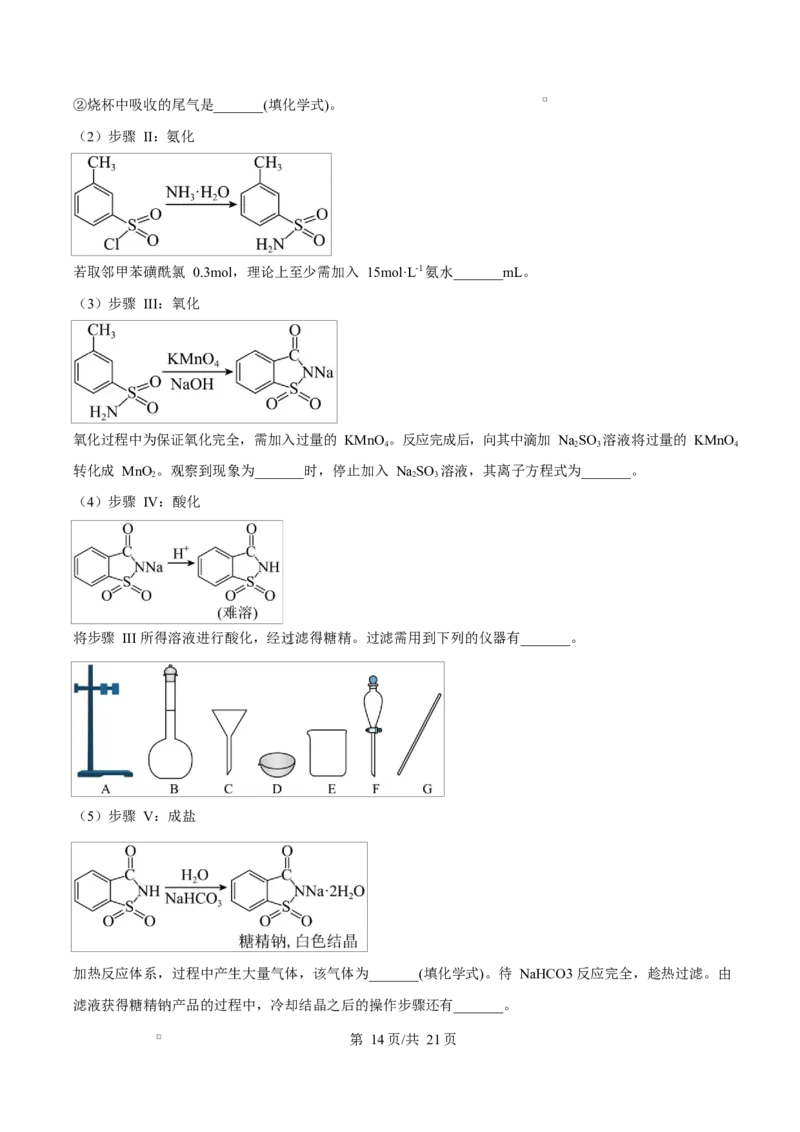
(3)步骤 III:氧化
氧化过程中为保证氧化完全,需加入过量的 KMnO 。反应完成后,向其中滴加 NaSO 溶液将过量的 KMnO
4 2 3 4
转化成 MnO 。观察到现象为_______时,停止加入 NaSO 溶液,其离子方程式为_______。
2 2 3
(4)步骤 IV:酸化
将步骤 III 所得溶液进行酸化,经过滤得糖精。过滤需用到下列的仪器有_______。
(5)步骤 V:成盐
加热反应体系,过程中产生大量气体,该气体为_______(填化学式)。待 NaHCO3 反应完全,趁热过滤。由
滤液获得糖精钠产品的过程中,冷却结晶之后的操作步骤还有_______。
第 14页/共 21页【答案】(1) ①. 温度计 ②. HCl
(2)40 (3) ①. 溶液紫色褪去 ②.
(4)ACEG (5) ①. ②. 过滤、洗涤、干燥
【解析】
【小问 1 详解】
由方程式可知,磺化过程中还生成了氯化氢,所以用水来吸收,由装置图可知,a 为温度计,故答案为:温
度计;HCl;
【小问 2 详解】
由方程式可知,邻甲基磺酸氯与氨水为 1:1 进行反应,0.3mol 邻甲基磺酸氯中消耗的氨水为 0.3mol,加入
15mol/L 的氨水,充分反应后,消耗 20 毫升的氨水,同时产生 0.3mol 的氯化氢,氯化氢与氨水中和反应,
消耗的氨水为 0.3mol,即 20 毫升,所以一共需要消耗 的体积为 40mL,故答案为:40;
【小问 3 详解】
氧化过程中为保证氧化完全,需要加入过量的 ,反应完全后,向其中滴加 以除去过量
溶液, 溶液被消耗,则反应完全的现象是溶液紫色褪去,该溶液为碱性,则 被
还原成二氧化锰,根据氧化还原规律,得出离子方程式为: ,
故答案为:溶液紫色褪去; ;
【小问 4 详解】
过滤需要烧杯,漏斗,玻璃棒,铁架台等,故需要的仪器为:ACEG;
【小问 5 详解】
能水解生成羧基,与 反应,产生大量的二氧化碳气体,当 完全反应,趁
热过滤,冷却结晶的后续操作是过滤,洗涤,干燥,故答案为:CO;过滤,洗涤,干燥。
2
17. 水是化学反应的良好介质,探索水溶液中的酸碱平衡具有重要意义。
(1)天然水中可以分离出重水(D
2
O)。D
2
O 溶液中存在电离平衡: ,c(D+)和 c(OD-)的
关系如图所示。
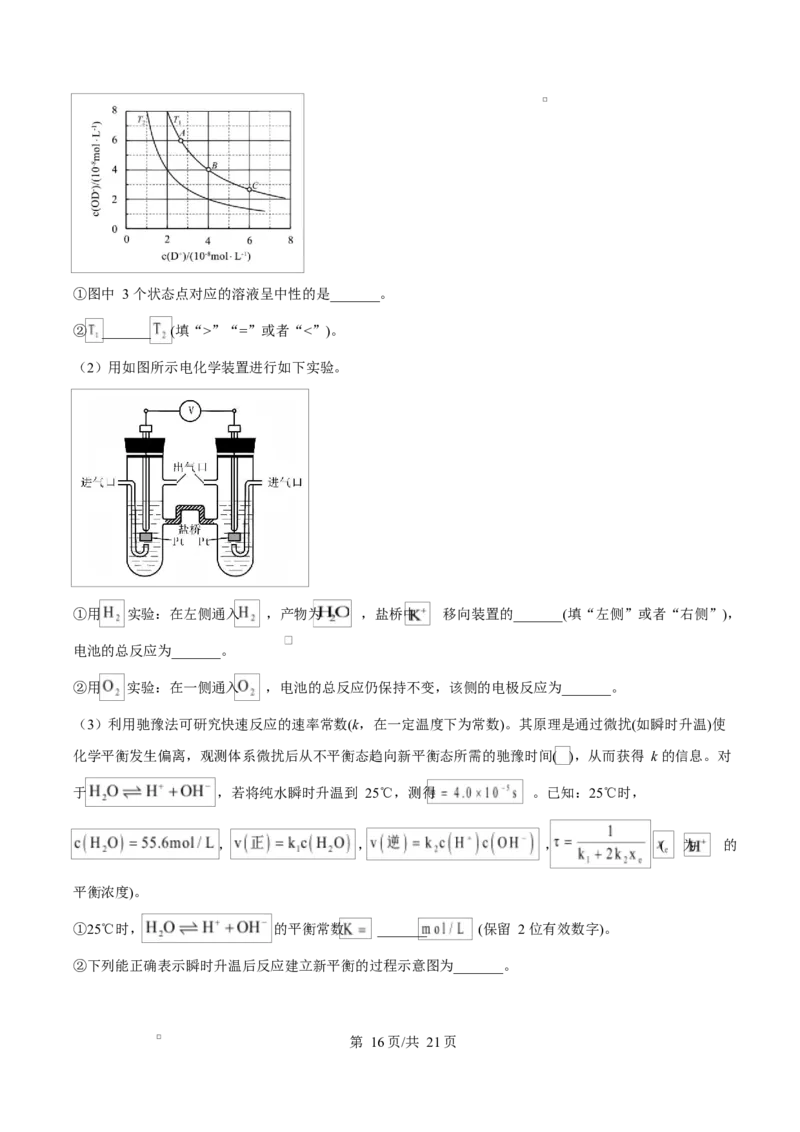
第 15页/共 21页①图中 3 个状态点对应的溶液呈中性的是_______。
② _______ (填“>”“=”或者“<”)。
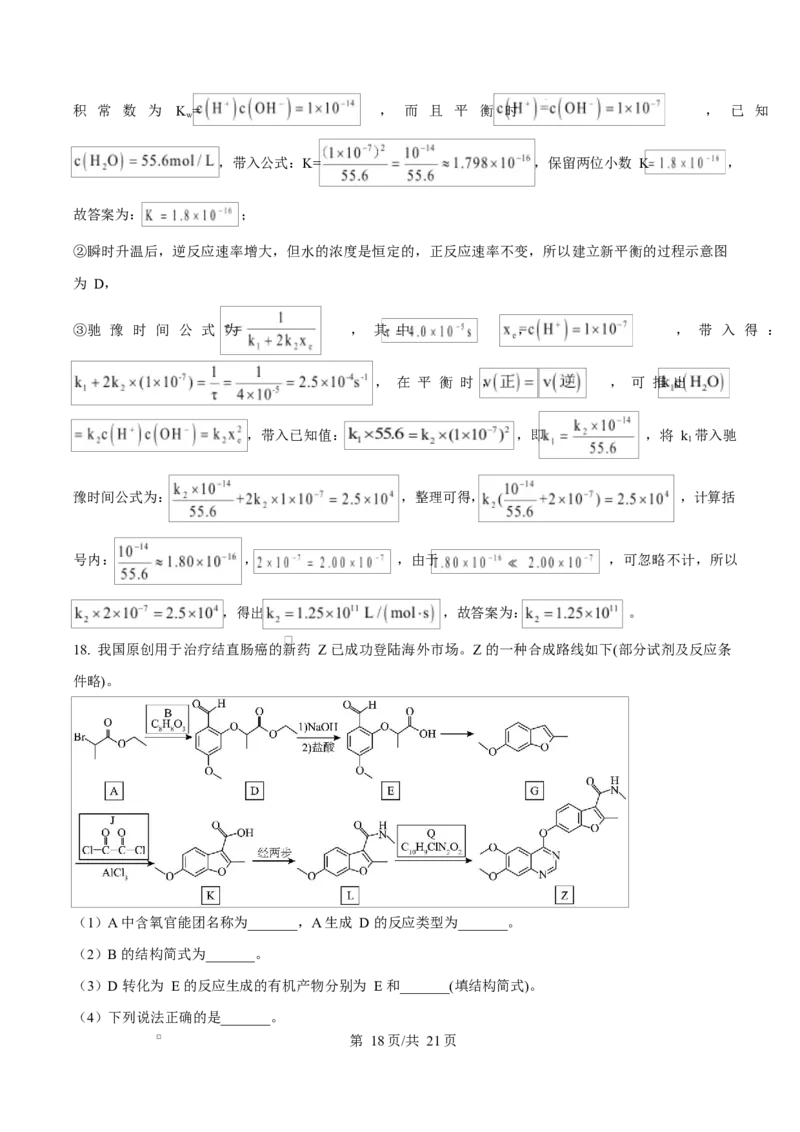
(2)用如图所示电化学装置进行如下实验。
①用 实验:在左侧通入 ,产物为 ,盐桥中 移向装置的_______(填“左侧”或者“右侧”),
电池的总反应为_______。
②用 实验:在一侧通入 ,电池的总反应仍保持不变,该侧的电极反应为_______。
(3)利用驰豫法可研究快速反应的速率常数(k,在一定温度下为常数)。其原理是通过微扰(如瞬时升温)使
化学平衡发生偏离,观测体系微扰后从不平衡态趋向新平衡态所需的驰豫时间( ),从而获得 k 的信息。对
于 ,若将纯水瞬时升温到 25℃,测得 。已知:25℃时,
, , , ( 为 的
平衡浓度)。
①25℃时, 的平衡常数 _______ (保留 2 位有效数字)。
②下列能正确表示瞬时升温后反应建立新平衡的过程示意图为_______。
第 16页/共 21页③25℃时,计算得 为_______ 。
【答案】(1) ①. B ②. >
(2) ①. 右侧 ②. ③.
(3) ①. ②. D ③.
【解析】
【小问 1 详解】
①重水中存在电离平衡 ,中性溶液中, ,只有 B 点符合,所以“A、
B、C”三点中呈中性的是 B 点,故答案为:B;
②水的电离平衡为吸热过程,温度升高,电离程度增大, , 均增大,Kw 也增大,由图可知,
T 时离子浓度更高,Kw 更大,所以 > ,故答案为:>;
1
【小问 2 详解】
①用 进行实验,左侧通入 ,产物为 ,电极方程式为: ,左侧为负极,右
侧为正极,电极方程式为 ,在原电池中,正电荷向正极移动,所以盐桥中 移
向正极,即右侧,该电池为燃料电池,原料为氢气和氧气,总反应方程式为 ,故答案为:
右侧; ;
②用 进行实验,一侧通入 ,电池总反应方程式不变,则该电池为氢气和氧气组成的燃料电池,该侧
的电极反应方程式为 ,故答案为: ;
【小问 3 详解】
①对于反应 ,平衡常数 K 的定义为:K= ,在 25℃的纯水中,水的离子
第 17页/共 21页积 常 数 为 K = , 而 且 平 衡 时 , 已 知
w
,带入公式:K= ,保留两位小数 K ,
故答案为: ;
②瞬时升温后,逆反应速率增大,但水的浓度是恒定的,正反应速率不变,所以建立新平衡的过程示意图
为 D,
③驰 豫 时 间 公 式 为 , 其 中 , , 带 入 得 :
, 在 平 衡 时 , , 可 推 出
,带入已知值: ,即 ,将 k 带入驰
1
豫时间公式为: ,整理可得, ,计算括
号内: , ,由于 ,可忽略不计,所以
,得出 ,故答案为: 。
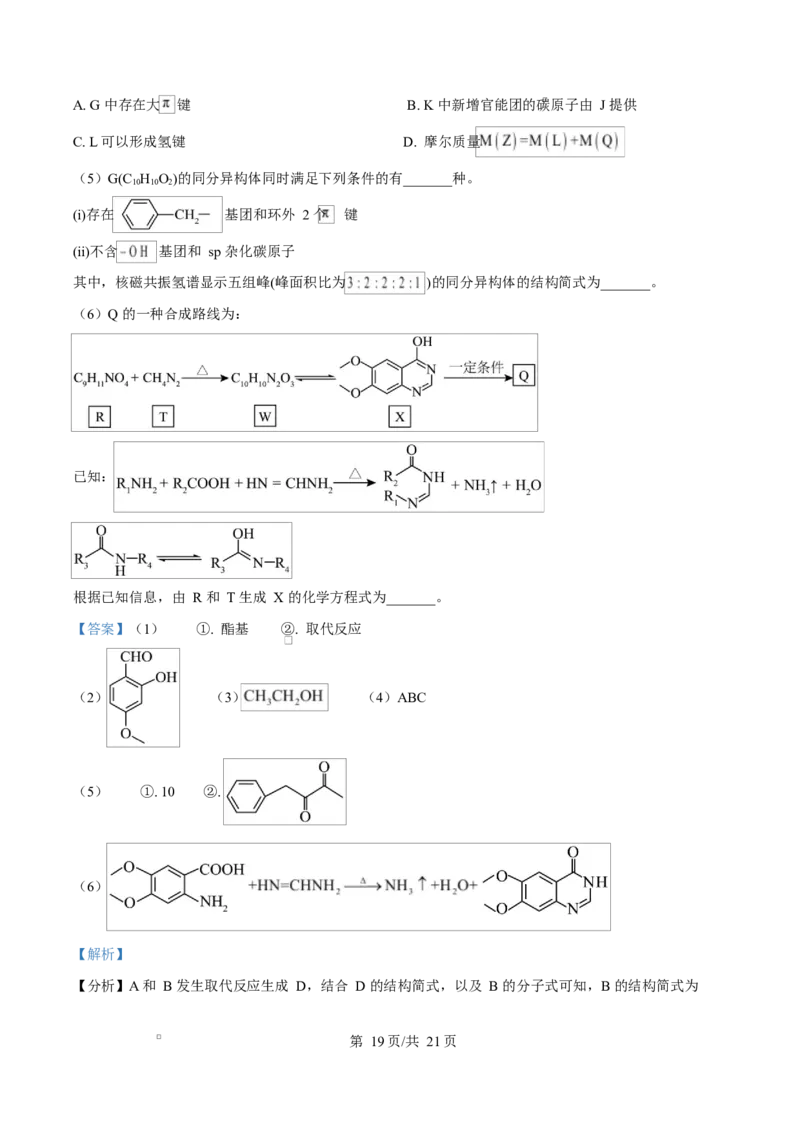
18. 我国原创用于治疗结直肠癌的新药 Z 已成功登陆海外市场。Z 的一种合成路线如下(部分试剂及反应条
件略)。
(1)A 中含氧官能团名称为_______,A 生成 D 的反应类型为_______。
(2)B 的结构简式为_______。
(3)D 转化为 E 的反应生成的有机产物分别为 E 和_______(填结构简式)。
(4)下列说法正确的是_______。
第 18页/共 21页A. G 中存在大 键 B. K 中新增官能团的碳原子由 J 提供
C. L 可以形成氢键 D. 摩尔质量
(5)G(C H O)的同分异构体同时满足下列条件的有_______种。
10 10 2
(i)存在 基团和环外 2 个 键
(ii)不含 基团和 sp 杂化碳原子
其中,核磁共振氢谱显示五组峰(峰面积比为 )的同分异构体的结构简式为_______。
(6)Q 的一种合成路线为:
已知:
根据已知信息,由 R 和 T 生成 X 的化学方程式为_______。
【答案】(1) ①. 酯基 ②. 取代反应
(2) (3) (4)ABC
(5) ①. 10 ②.
(6)
【解析】
【分析】A 和 B 发生取代反应生成 D,结合 D 的结构简式,以及 B 的分子式可知,B 的结构简式为
第 19页/共 21页,D 中的酯基先水解,再酸化生成 E,E 发生反应生成 G,G 和 J 发生取代反应生成 K,K 再发
生取代反应生成 L,L 和 Q 发生反应得到目标产物,结合目标产物的结构简式以及 Q 的分子式可知,Q 的
结构简式为 ,据此解答。
【小问 1 详解】
由 A 的结构简式可知,其含氧官能团名称为酯基,由结构简式可知,A 和 B 发生反应生成 D 的同时会生成
HBr,反应类型是取代反应;
【小问 2 详解】
由分析可知,B 的结构简式为 ;
【小问 3 详解】
D 到 E 先发生酯基的水解以及酸碱中和反应,再酸化生成羧基,另一种产物是乙醇,结构简式为
;
【小问 4 详解】
A.G 中含有苯环,存 大 键,A 正确;
B.由 G 和 K 的结构简式可知,K 中有 1 个碳原子来自于 J,B 正确;
C.L 中含有羟基和酰胺基,能形成氢键,C 正确;
D.L 与 Q 生成 Z 的反应中,发生的是取代反应,会生成小分子的 HCl,因此 ,D
错误
故选 ABC;
【小问 5 详解】
G 的分子式为 ,不饱和度为 6,存在 和 2 个环外 键,说明分子中除了苯环外
还存在 2 个双键结构,不含 与 sp 杂化的碳原子,说明不含有羟基、羧基、碳碳三键,则苯环的支链
可以为:
第 20页/共 21页属于醛或酮的有: 、 、 、
、 、 ;
属于酯的有: 、 、
、 总计 10 种同分异构体;
核磁共振氧谱峰面积比为( ),则分子总有 1 个甲基,满足条件的结构简式为
;
【小问 6 详解】
由已知信息的反应可知,T 的结构简式为 ,R 中即含有氨基,又含有羧基,由 X 的结构简式,
以及已知信息的反应,可推断出,R 中氨基和羧基处于邻位,R 的结构简式为 ,则由
R 和 T 生成 X 的化学方程式为
。
第 21页/共 21页