分子对接:分析图解/打分函数/对接软件/验证实验一文通!
点击蓝字,关注我们
分子对接是一种计算机模拟方法,通过预测分子间结合模式及亲和力,为功能研究与候选分子筛选提供理论依据。像锁与钥匙的匹配,在计算机里模拟 “钥匙(小分子)” 如何精准插入 “锁孔(蛋白活性口袋)”。
分子对接是在已有蛋白三维结构基础上,预测小分子在活性口袋中的可能结合构象、相互作用模式及相对结合倾向,从而为机制分析和候选分子筛选提供理论参考。
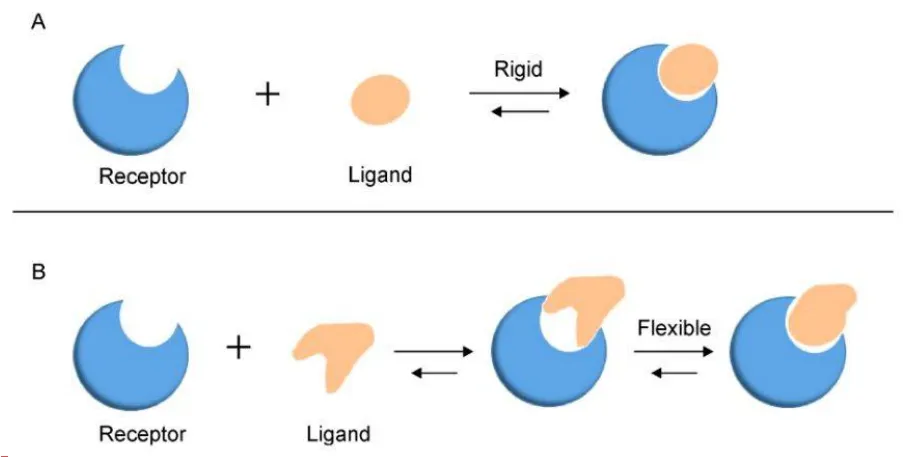
两种分子对接模型(A)钥匙锁模式(B)诱导拟合模型
DOI:10.1007/s40484-019-0172-y
分子对接可应用于以下领域:
✅ 药物研发:虚拟筛选、先导化合物优化、靶点研究及作用机制分析;✅ 材料科学:分子识别、分子自组装及超分子复合物设计;✅ 生物医学:蛋白-小分子、蛋白-蛋白及蛋白-核酸相互作用研究。
评价体系
1
核心结合作用力
小分子配体与蛋白受体在活性口袋稳定结合,依靠多种非共价弱相互作用,是打分函数计算的核心依据。
✅ 氢键:分子间的氢键是由氢原子与电负性较强的原子(如氮、氧、氟)之间的相互作用形成的通常由供体原子与受体原子之间形成,是影响分子识别特异性和结合稳定性的重要非共价相互作用之一,其强度受距离、方向性及局部环境共同影响。
✅ 范德华力:分子间的短距离相互作用力,通常在分子接近时起作用。
✅ 静电相互作用:带电分子或离子之间的吸引或排斥力。
✅ 疏水作用:非极性分子在水中聚集以减少与水的接触,从而影响分子对接的稳定性。
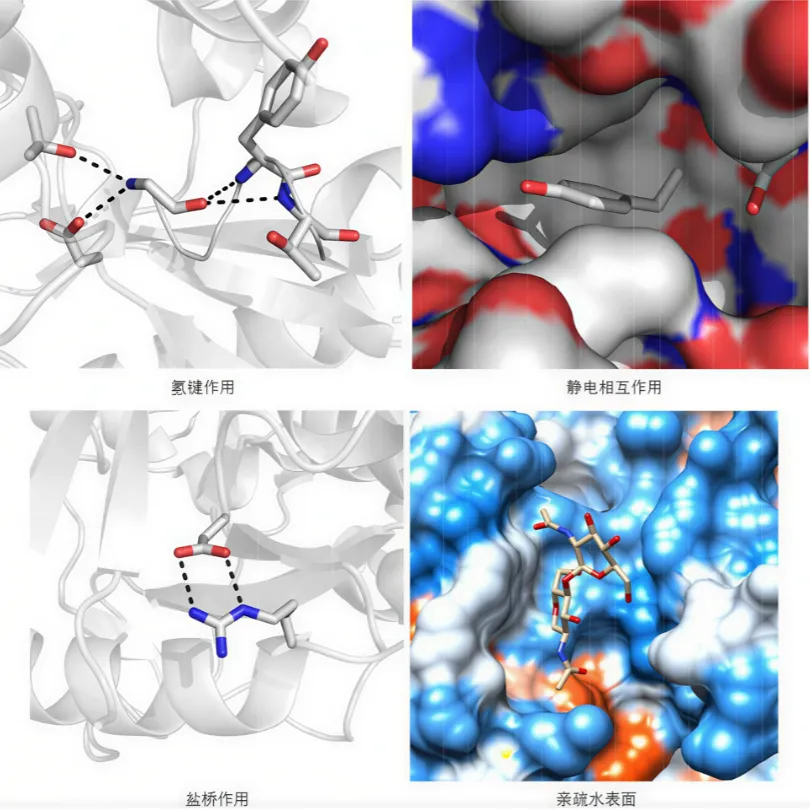
配体与受体结合相互作用示意图
DOI: 10.12677/CC.2019.31001
2
自由结合能
在热力学上,结合自由能与结合常数相关:结合越强,通常对应更低的 ΔG 和更小的 Kd。常写为 ΔG° = RT lnKd,或 ΔG° = -RT lnKa。
-
ΔG<0:一般而言,ΔG 越低,提示结合在热力学上越有利;
-
ΔG=0:ΔG 接近 0 时,提示结合驱动力较弱;
-
ΔG>0:通常提示该构象在当前模型下不利于稳定结合。
3
打分函数
1) 经验打分函数,也被称为能量函数,是分子对接中用来估计蛋白质受体和配体分子之间的结合亲和力或能量的数学模型。
2)基于知识的打分函数,是由已知的蛋白质-配体复合体的统计分析得出的。这些打分函数利用从现有复合物中获得的信息来指导结合亲和力的预测并对潜在的结合姿势进行排序。
3)基于力场的评分函数,是一种数学模型,它利用基于物理学的力场来估计蛋白质受体和配体分子之间的结合亲和力或能量,旨在预测蛋白质-配体结合的稳定性和质量。
4)基于机器学习的评分函数,利用在大型数据集上训练的计算模型来预测蛋白质受体和配体分子之间的结合亲和力。旨在捕捉蛋白质-配体相互作用的非线性性质,并解决传统的基于物理学的评分功能的局限性。
常见图例
1
蛋白三维结构图
-
α- 螺旋:长条螺旋状彩带 / 圆柱结构,维持蛋白刚性骨架;
-
β- 折叠:片状、箭头状平板结构,箭头指向 C 端;
-
无规卷曲 / 环区(Loop):杂乱柔性链条,多为活性口袋、结合区域,构象灵活。
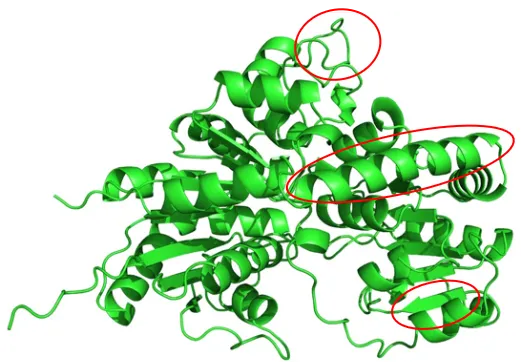
蛋白质的三维结构
2
相互作用图(二维 / 三维)
-
二维互作图图解
-
氢键(Hydrogen Bond):常以虚线表示,是影响分子识别特异性和结合稳定性的重要作用之一,但其贡献还与距离、方向性及局部环境有关
-
疏水作用(Hydrophobic):绿色 / 灰色区域,结合主要驱动力
-
π-π 堆积:芳香环间平行作用,增强稳定性
-
盐桥 / 静电作用:正负电荷吸引,强度高
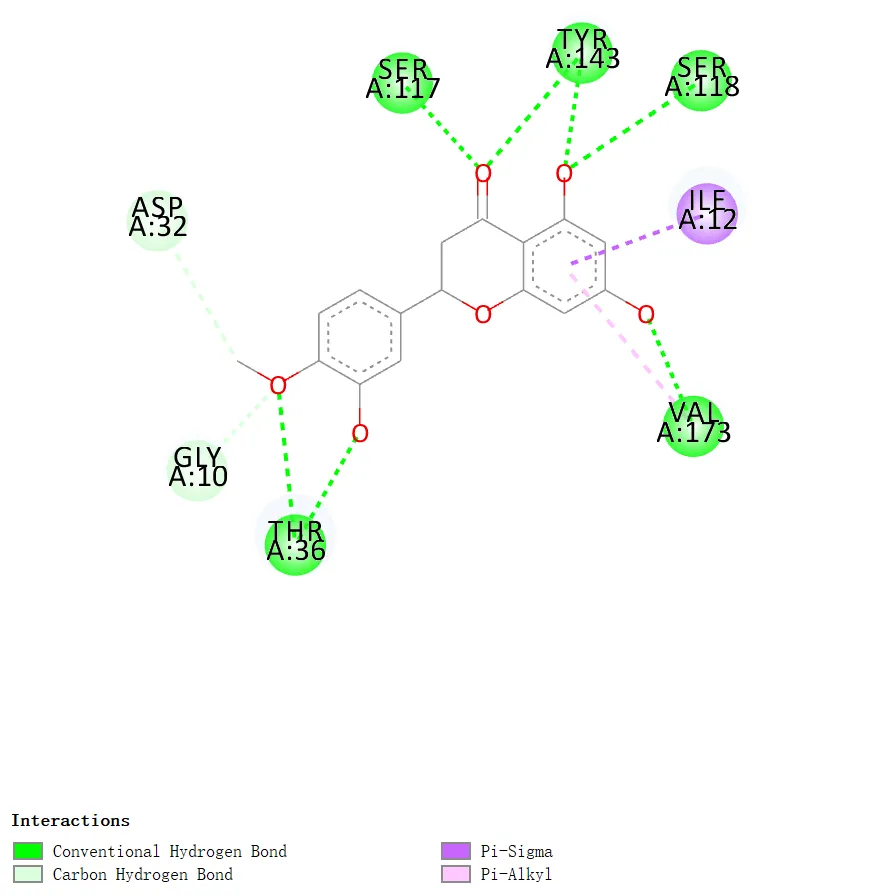
蛋白与化合物的二维互作图
-
三维互作图图解
-
结合口袋:绿色蛋白质包裹的蓝色小分子区域,这个凹陷区域就是”结合口袋”(Binding Pocket)
-
关键氨基酸残基:蛋白活性口袋里参与结合的氨基酸残基,如TYR代表酪氨酸
-
氨基酸后的数字(如 TYR-143、SER-117)
➡ 含义:该氨基酸在蛋白氨基酸序列中的位置编号(从蛋白 N 端开始计数)
➡ 作用:
①精准定位结合位点:明确是蛋白哪个位置的氨基酸参与了和小分子的结合
②实验验证的核心依据:后续可通过位点突变实验(把这个氨基酸换成其他氨基酸),验证它是否是结合的关键残基
③文献溯源:方便其他研究者复现、验证该结合模式
-
黄色虚线上的数字(如 2.9、3.3、3.0)
➡ 含义:原子间的距离,单位是 Å(埃,1 Å = 0.1 nm)
➡ 作用:
①验证氢键 / 弱相互作用的有效性:常规氢键的有效距离为 2.0–3.5 Å,图中所有数值都在这个范围内,证明这些虚线标注的是真实、稳定的氢键
②量化结合强度:距离越近(如 2.9 Å),氢键作用越强,结合越稳定
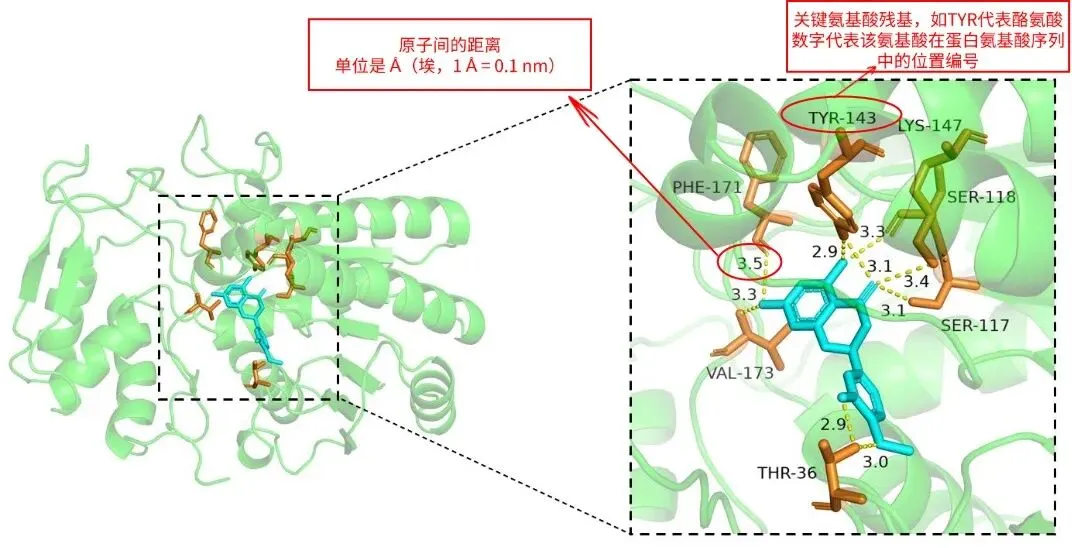
蛋白与化合物的三维互作图
常用工具
1
蛋白结构
-
PDB :https://www.rcsb.org/
-
UniProt:https://www.uniprot.org/
-
NCBI:https://www.ncbi.nlm.nih.gov/
-
BindingDB:https://www.bindingdb.org/
-
AlphaFold:https://alphafold.ebi.ac.uk/
2
配体相关资源
-
配体数据库:
➡ PubChem:https://pubchem.ncbi.nlm.nih.gov/
➡ TCMSP:https://www.tcmsp-e.com/tcmsp.php
➡ ZINC:https://zinc.docking.org/
➡ ChEMBL:https://www.ebi.ac.uk/chembl/
➡ DrugBank:https://go.drugbank.com/
-
化学结构绘制与处理工具:
➡ ChemDraw:https://www.chemdraw.com.cn/
➡ Open Babel:https://openbabel.org/
➡ RDKit:https://www.rdkit.org/
3
对接软件
-
AutoDock或AutoDock Vina:https://vina.scripps.edu/
-
Swiss Dock:https://www.swissdock.ch/
-
Paddlehelix:https://paddlehelix.baidu.com/app/drug/virtual-filter/forecast
4
口袋预测工具
-
Proteins Plus Server:https://proteins.plus/
-
CavityPlus Server:http://repharma.pku.edu.cn/cavityplus
-
CASTp:https://cfold.bme.uic.edu/castpfold/compute
-
P2Rank:https://prankweb.cz/
5
保守性与功能位点分析工具
-
ConSurf:https://consurf.tau.ac.il
-
HotSpot Wizard:https://loschmidt.chemi.muni.cz/hotspotwizard/
下游湿实验验证
1
体外互作验证(直接证明)
-
表面等离子体共振(SPR): 实时监测分子间结合过程,可获得亲和力(KD)及动力学参数(ka、kd),用于评估结合强度与结合特征
-
微量热泳动(MST):基于分子热泳动特性变化检测分子间相互作用,可快速测定结合亲和力(KD)
-
等温滴定量热(ITC):通过测量结合过程的热变化,获得ΔH、ΔS及结合亲和力(KD),用于系统解析热力学机制
-
生物膜干涉技术 (BLI):可测定亲和力(KD)及动力学参数(ka、kd),具备较高通量,适用于多样本筛选
-
细胞热迁移 (CETSA):基于蛋白热稳定性变化,在细胞或组织水平评估药物与靶点的结合情况
SPR/BLI/MST/ITC一篇拿捏,手把手教你体外分子互作结果解读及实验选择!
超全解析!细胞热迁移(CETSA),原理、流程、结果解读、文献案例、常见问题分享~
动物实验中的蛋白互作验证技术清单请查收!实验protocol、结果解读及文献案例
2
结合位点验证(定位证明)
-
突变实验:突变对接预测的关键氨基酸,观察结合是否消失
-
LiP-MS(有限蛋白水解质谱):定位小分子结合的蛋白区域
-
X 射线晶体衍射或冷冻电镜:解析复合物高分辨率结构,为验证预测结合模式提供关键结构依据
3
功能验证(效果证明)
细胞实验:小分子处理细胞,观察靶点活性 / 通路变化
细胞实验不用东拼西凑!一套覆盖:模型/转染/增殖/凋亡/周期/迁移/侵袭/定位/ROS/共聚焦
酶活实验:测小分子对酶活性的抑制 / 激活效果
AI分子智算平台及湿实验验证服务
南京瑞源医学专注医学服务线,提供从靶点挖掘到药物发现的全流程解决方案,包括AI分子互作智算、细胞互作、细胞分子常规、体外仪器互作和测序组学五大服务平台,以高效、精准、可靠的技术服务,赋能前沿科技探索。
https://www.bestofbest.top/cs/8.html
1
AI分子智算平台

2
体外仪器互作检测平台
3
分子互作验证平台


 夜雨聆风
夜雨聆风




