文档内容
东北育才学校高中高三年级第三次模考化学学科试卷
考试时长:75 分钟 命题人:郭玲 校对人:肖子歆
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Al-27 Si-28 Cl-35.5
V-51 Mn-55 Fe-56 Ge-73 I-127 Pb-207
一、选择题(本题共 15小题,每小题 3分,共 45分)
1. “十四五”期间,我国化学创新成果不断涌现。下列说法错误的是
A.“液态阳光”项目将CO₂转化为甲醇,有助于实现碳中和
B. 光导纤维作为量子通信技术中的传输介质,其主要成分为二氧化硅
C.“问天”实验舱采用了砷化镓太阳能电池,是因为砷化镓具有良好的导电性
D.“神舟二十一号”发动机的耐高温结构材料 Si₃N₄ 是一种新型无机非金属材料
2. 下列化学用语或图示表达正确的是
A.sp2杂化轨道示意图:
B. 基态 Zn原子的价层电子排布式:4s2
30
C.HCl中σ键的形成:
D. 电子式表示MgCl 形成过程:
2
3. 下列递变规律和原因均正确的是
选项 递变规律 原因分析
A 第一电离能:N<O<F 原子半径:N>O>F
B 与水反应置换出H 的能力:Na>Mg>Al 最外层电子数:Al>Mg>Na
2
C 离子半径:S2->Cl->Ca2+ 电子层结构相同,核电荷数:Ca>Cl>S
D 熔点:Cl <Br <I 键能:Cl-Cl>Br-Br>I-I
2 2 2
4. 用N 代表阿伏加德罗常数的值。下列说法正确的是
A
A.1mol甲基含有的电子数目为10N
A
化学试卷 第1页/共10页
学科网(北京)股份有限公司B.1molNa被完全氧化为Na O ,失去2N 个电子
2 2 A
C.26.7gAlCl 固体中,Al3+的数目为0.2N
3 A
D.13g聚乙炔中σ键数约为2N
A
5. 下列方程式与所给事实均正确的是
A. 用盐酸除去铁锈:Fe O xH O6H 2Fe3(3x)H O
2 3 2 2
B. 铝粉溶于少量氢氧化钠溶液,产生无色气体:2Al6H O2Al(OH) 3H
2 3 2
C. 草酸 H C O 使酸性KMnO 溶液褪色:
2 2 4 4
2MnO 5C O2 16H 2Mn2 10CO 8H O
4 2 4 2 2
D. 用足量氨水洗去银镜:Ag2NH H OAg NH OH
3 2 3 2
6. 下列事实不 . 能 . 用平衡移动原理解释的是
A. 用热的纯碱溶液更易去除油污
B. 工业合成氨N g+3H g 2NH g H0,采用400℃~500℃的高温条件
2 2 3
C. 用稀硫酸洗涤BaSO 沉淀比用等体积蒸馏水洗涤损失的BaSO 少
4 4
D. 电镀实验中,用 Cu NH SO 溶液作电镀液可以维持Cu2+浓度的稳定性
3 4 4
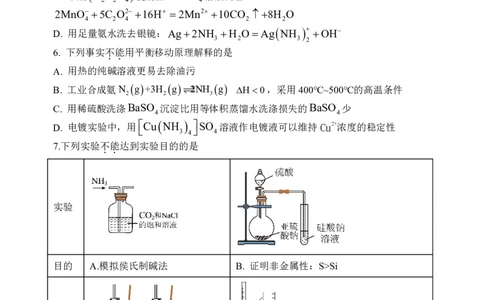
7.下列实验不
.
能
.
达到实验目的的是
实验
目的 A.模拟侯氏制碱法 B. 证明非金属性:S>Si
实验
目的 C.证明分子极性:H O>CCl D.准确量取14.80mL酸性KMnO 标准溶液
2 4 4
化学试卷 第2页/共10页
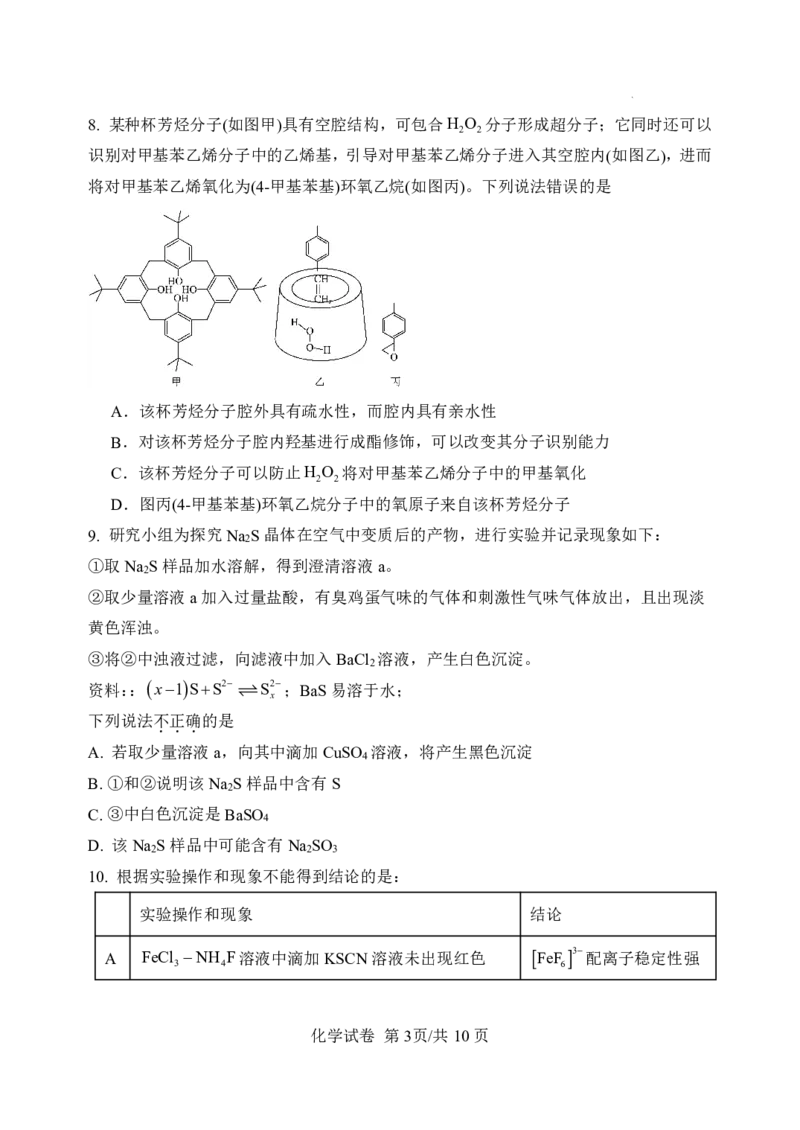
学科网(北京)股份有限公司8. 某种杯芳烃分子(如图甲)具有空腔结构,可包合H O 分子形成超分子;它同时还可以
2 2
识别对甲基苯乙烯分子中的乙烯基,引导对甲基苯乙烯分子进入其空腔内(如图乙),进而
将对甲基苯乙烯氧化为(4-甲基苯基)环氧乙烷(如图丙)。下列说法错误的是
A.该杯芳烃分子腔外具有疏水性,而腔内具有亲水性
B.对该杯芳烃分子腔内羟基进行成酯修饰,可以改变其分子识别能力
C.该杯芳烃分子可以防止H O 将对甲基苯乙烯分子中的甲基氧化
2 2
D.图丙(4-甲基苯基)环氧乙烷分子中的氧原子来自该杯芳烃分子
9. 研究小组为探究Na S晶体在空气中变质后的产物,进行实验并记录现象如下:
2
①取Na S样品加水溶解,得到澄清溶液a。
2
②取少量溶液a加入过量盐酸,有臭鸡蛋气味的气体和刺激性气味气体放出,且出现淡
黄色浑浊。
③将②中浊液过滤,向滤液中加入BaCl 溶液,产生白色沉淀。
2
资料::x1SS2 S2;BaS易溶于水;
x
下列说法不正确的是
...
A. 若取少量溶液a,向其中滴加CuSO 溶液,将产生黑色沉淀
4
B.①和②说明该Na S样品中含有S
2
C.③中白色沉淀是BaSO
4
D. 该Na S样品中可能含有Na SO
2 2 3
10. 根据实验操作和现象不能得到结论的是:
实验操作和现象 结论
A FeCl NH F溶液中滴加KSCN溶液未出现红色 FeF 3配离子稳定性强
3 4 6
化学试卷 第3页/共10页
学科网(北京)股份有限公司取两份新制氯水,分别滴加AgNO 溶液和淀粉KI溶 氯气与水的反应一定存
3
B
液,前者有白色沉淀,后者溶液变蓝色 在限度
将缺角的明矾晶体放入明矾饱和溶液中,得到有规则
C 晶体具有自范性
几何外形的完整晶体
相同条件下,向等体积pH2的HA溶液和H B溶
2
D 酸性:HAH B
2
液中,分别加入足量的Zn,HA溶液放出的氢气多
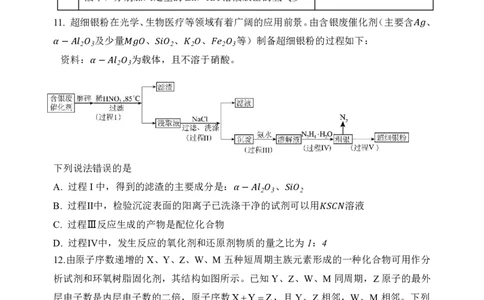
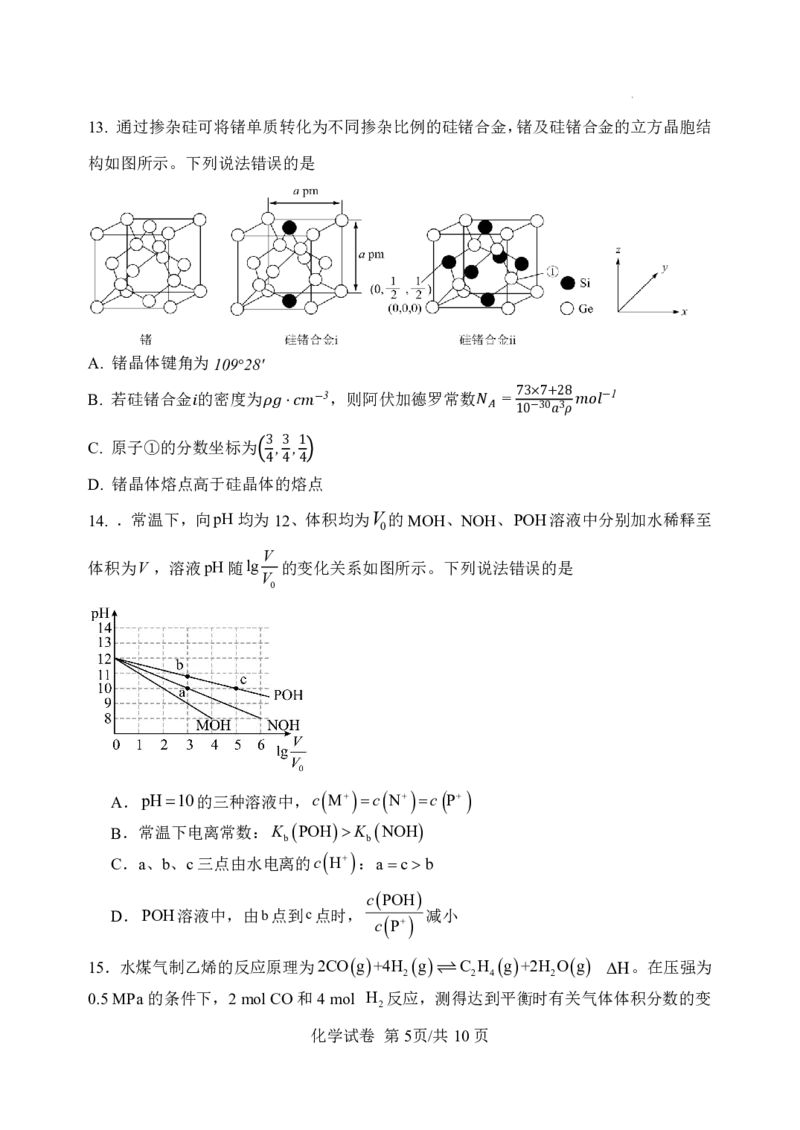
11. 超细银粉在光学、生物医疗等领域有着广阔的应用前景。由含银废催化剂(主要含 、
及少量 、 、 、 等)制备超细银粉的过程如下:
2 3 2 2 2 3
资料: 为载体,且不溶于硝酸。
− 2 3
−
下列说法错误的是
A. 过程I中,得到的滤渣的主要成分是: 、
2 3 2
B. 过程Ⅱ中,检验沉淀表面的阳离子已洗涤 干 − 净 的 试剂 可 以用 溶液
C. 过程Ⅲ反应生成的产物是配位化合物
D. 过程Ⅳ中,发生反应的氧化剂和还原剂物质的量之比为1:4
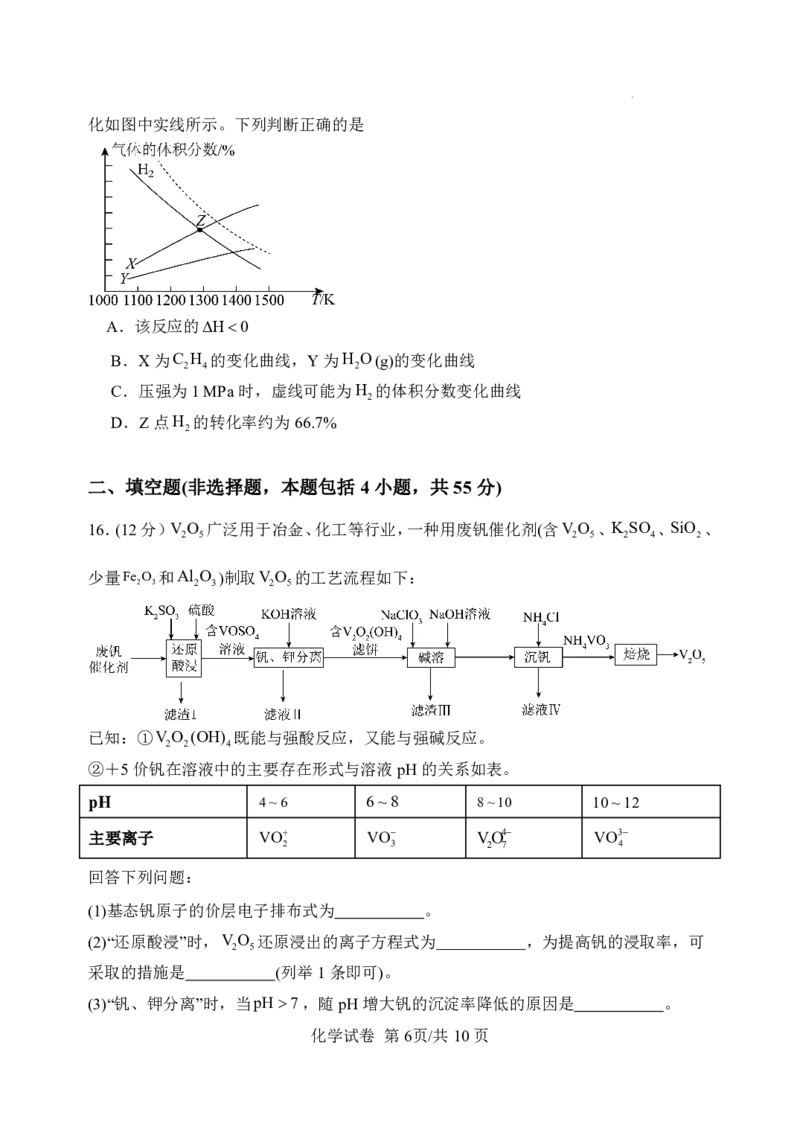
12.由原子序数递增的X、Y、Z、W、M五种短周期主族元素形成的一种化合物可用作分
析试剂和环氧树脂固化剂,其结构如图所示。已知Y、Z、W、M同周期,Z原子的最外
层电子数是内层电子数的二倍,原子序数XYZ,且Y、Z相邻,W、M相邻。下列
说法正确的是
A.不存在W与M形成的化合物 B.Z的氧化物对应的水化物为强酸
C.最简单氢化物的键角:ZW D.结构中Y、Z、W原子的杂化方式均不相同
化学试卷 第4页/共10页
学科网(北京)股份有限公司13. 通过掺杂硅可将锗单质转化为不同掺杂比例的硅锗合金,锗及硅锗合金的立方晶胞结
构如图所示。下列说法错误的是
A. 锗晶体键角为109 28′
B. 若硅锗合金 的密度°为 3,则阿伏加德罗常数 = 1
− 73×7+28 −
⋅ 10 −30 3
C. 原子①的分数坐标为 , ,
3 3 1
D. 锗晶体熔点高于硅晶体 4 的 4 熔 4 点
14. .常温下,向pH均为12、体积均为V 的MOH、NOH、POH溶液中分别加水稀释至
0
V
体积为V ,溶液pH随lg 的变化关系如图所示。下列说法错误的是
V
0
A.pH10的三种溶液中,c M c N c P
B.常温下电离常数:K POHK NOH
b b
C.a、b、c三点由水电离的c
H
:acb
cPOH
D.POH溶液中,由b点到c点时,
c
P
减小
15.水煤气制乙烯的反应原理为2COg+4H g C H g+2H Og H。在压强为
2 2 4 2
0.5MPa的条件下,2molCO和4mol H 反应,测得达到平衡时有关气体体积分数的变
2
化学试卷 第5页/共10页
学科网(北京)股份有限公司化如图中实线所示。下列判断正确的是
A.该反应的H0
B.X为C H 的变化曲线,Y为H O(g)的变化曲线
2 4 2
C.压强为1MPa时,虚线可能为H 的体积分数变化曲线
2
D.Z点H 的转化率约为66.7%
2
二、填空题(非选择题,本题包括 4小题,共 55分)
16.(12分)VO 广泛用于冶金、化工等行业,一种用废钒催化剂(含VO 、K SO 、SiO 、
2 5 2 5 2 4 2
少量Fe O 和Al O )制取VO 的工艺流程如下:
2 3 2 3 2 5
已知:①VO (OH) 既能与强酸反应,又能与强碱反应。
2 2 4
②+5价钒在溶液中的主要存在形式与溶液pH的关系如表。
pH 4~6 6~8 8~10 10~12
主要离子 VO VO VO4 VO3
2 3 2 7 4
回答下列问题:
(1)基态钒原子的价层电子排布式为 。
(2)“还原酸浸”时,VO 还原浸出的离子方程式为 ,为提高钒的浸取率,可
2 5
采取的措施是 (列举1条即可)。
(3)“钒、钾分离”时,当pH7,随pH增大钒的沉淀率降低的原因是 。
化学试卷 第6页/共10页
学科网(北京)股份有限公司(4)“沉钒”时,为了得到固体NH VO ,需控制溶液的pH7.5。当pH8时,NH VO 的
4 3 4 3
产量明显降低,原因是 。
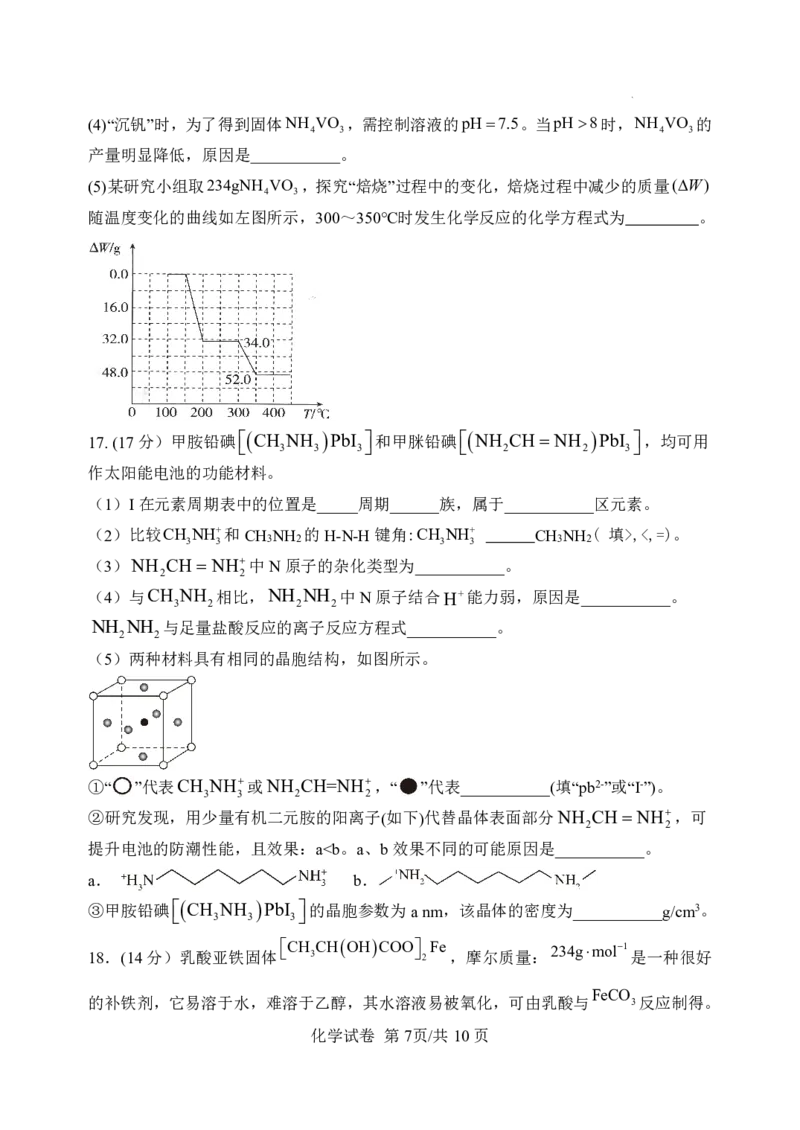
(5)某研究小组取234gNH VO ,探究“焙烧”过程中的变化,焙烧过程中减少的质量(W)
4 3
随温度变化的曲线如左图所示,300~350℃时发生化学反应的化学方程式为 。
17.(17分)甲胺铅碘
CH NH PbI
和甲脒铅碘
NH CH NH PbI
,均可用
3 3 3 2 2 3
作太阳能电池的功能材料。
(1)I在元素周期表中的位置是_____周期______族,属于___________区元素。
(2)比较CH NH和CH NH 的H-N-H键角:CH NH CH NH ( 填>,<,=)。
3 3 3 2 3 3 3 2
(3)NH CH NH中N原子的杂化类型为___________。
2 2
(4)与CH NH 相比,NH NH 中N原子结合H+能力弱,原因是___________。
3 2 2 2
NH NH 与足量盐酸反应的离子反应方程式___________。
2 2
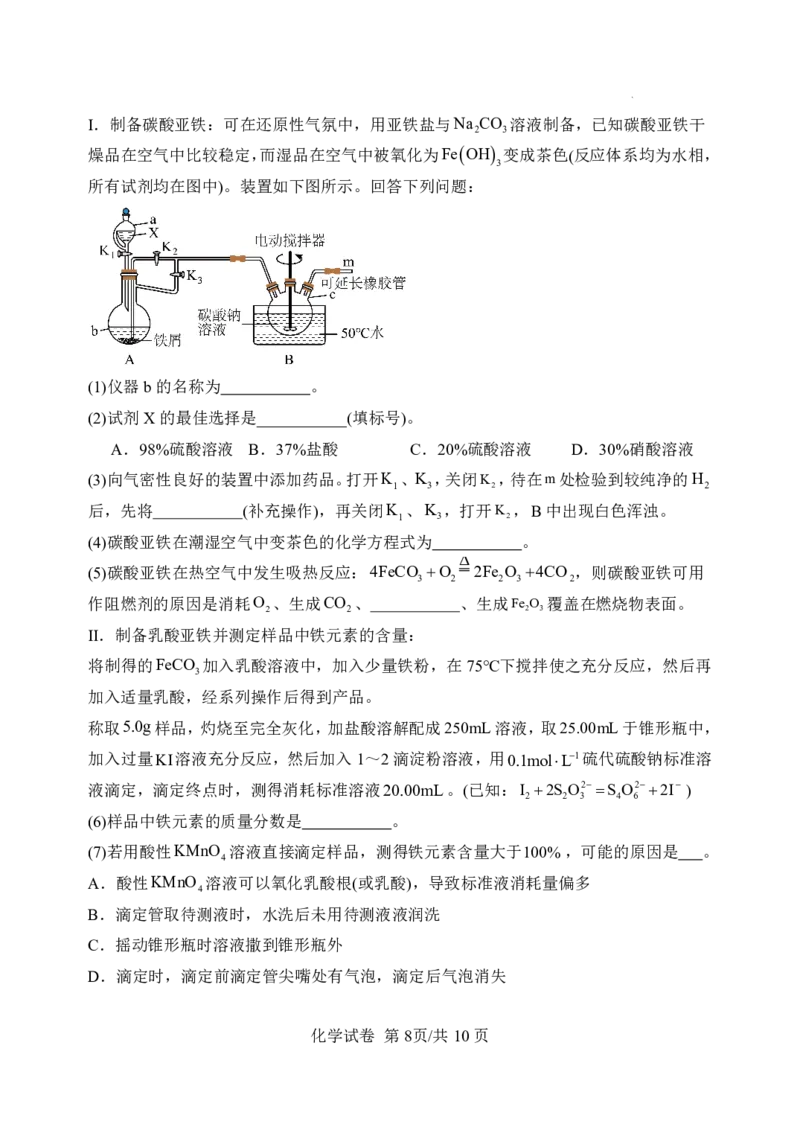
(5)两种材料具有相同的晶胞结构,如图所示。
①“ ”代表CH NH或NH CH=NH,“ ”代表___________(填“pb2-”或“I-”)。
3 3 2 2
②研究发现,用少量有机二元胺的阳离子(如下)代替晶体表面部分NH CH NH,可
2 2
提升电池的防潮性能,且效果:a”“<”或“=”)。
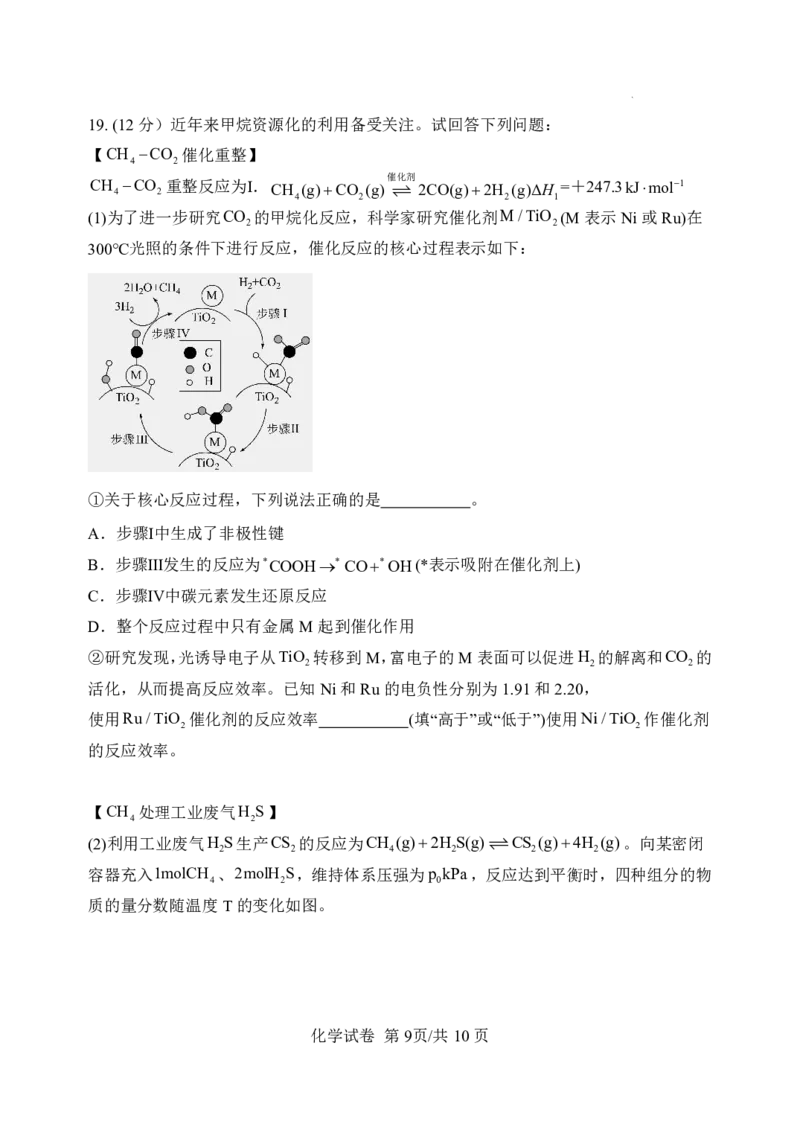
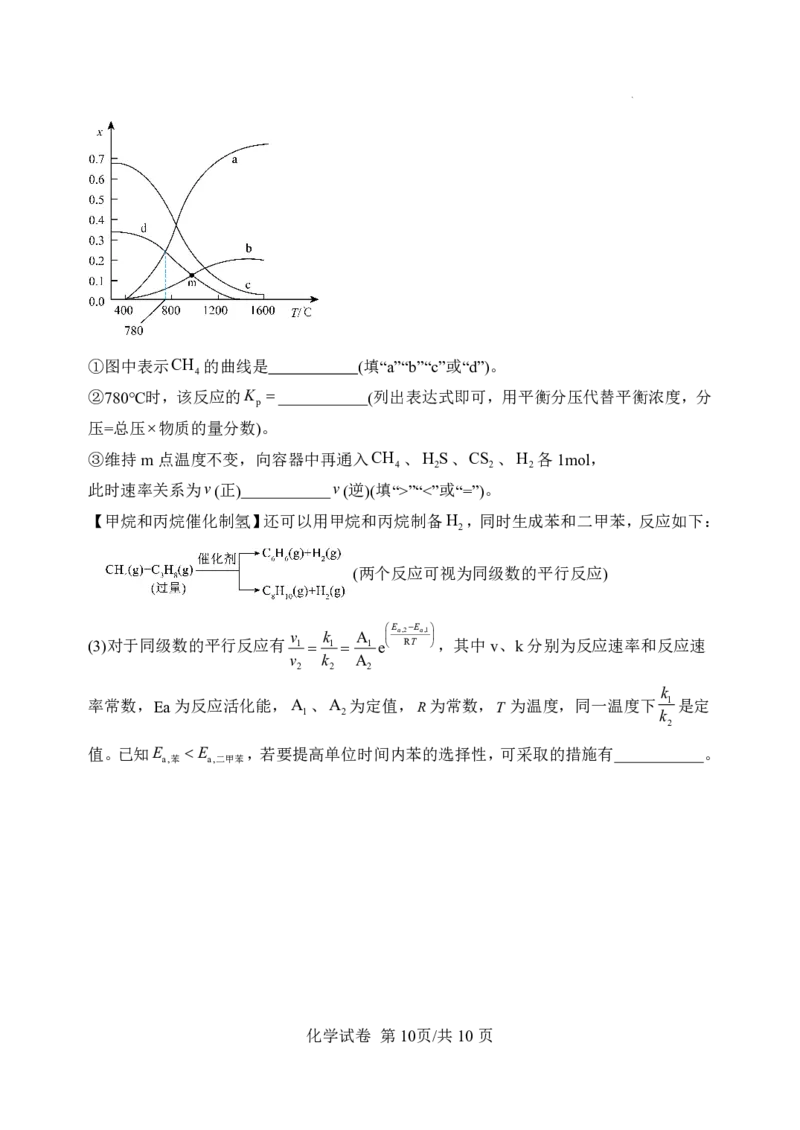
【甲烷和丙烷催化制氢】还可以用甲烷和丙烷制备H ,同时生成苯和二甲苯,反应如下:
2
(两个反应可视为同级数的平行反应)
v k A
Ea,2 Ea,1
(3)对于同级数的平行反应有 1 1 1 e RT ,其中v、k分别为反应速率和反应速
v k A
2 2 2
k
率常数,Ea为反应活化能,A 、A 为定值,R为常数,T 为温度,同一温度下 1 是定
1 2 k
2
值。已知E E ,若要提高单位时间内苯的选择性,可采取的措施有 。
a,苯 a,二甲苯
化学试卷 第10页/共10页
学科网(北京)股份有限公司