文档内容
第二单元 海水中的重要元素——钠和氯
第三节 物质的量(一)
一、基础巩固
1.已知N 是阿伏加德罗常数的值,下列说法正确的是( )
A
A.22.4L甲烷分子所含质子数为10N
A
B.标准状况下,22.4L二氯甲烷的分子数约为N 个
A
C.1mol苯分子中含有的碳碳单键数为6N
A
D.常温常压下,28.0g乙烯和丁烯的混合气体中含有的碳原子数目为2N
A
【答案】D
【解析】A.22.4L甲烷分子的温度压强不知,不能计算气体物质的量,故A错误;
B.标准状况下,22.4L二氯甲烷不是气体,气体物质的量不是1mol,分子数不是N 个,故B错误;
A
C.苯分子中碳碳原子间形成的是一种介于单双键之间的一种特殊的共价键,不存在碳碳单键,故 C错
误;
D.乙烯和丁烯的最简式都是CH ,28.0g乙烯和丁烯的混合气体中含有的碳原子数目为: =
2
2mol=2N ,故D正确;
A
故选:D。
2.N 表示阿伏加德罗常数的值。下列叙述正确的是( )
A
A.22.4L H 与2mol I 反应生成HI的分子数为2N
2 2 A
B.5.6g铁与足量稀硝酸反应转移的电子数为0.2N
A
C.32g氧气与32g硫所含的质子数相等
D.1L 0.1mol•L﹣1NH H PO 溶液中阴阳离子数相等
4 2 4
【答案】C
【解析】A.氢气所处的状态不明确,故22.4LH 的物质的量不一定是1mol,且反应是可逆反应,不能
2
进行彻底,故生成的HI的分子数无法计算,故A错误;
B.5.6g铁的物质的量为n= =0.1mol,而铁与足量稀硝酸反应生成铁离子,转移的电子数为0.3N ,故B错误;
A
C.32g氧气的物质的量为1mol,故含16mol质子,32g硫的物质的量也为1mol,也含16mol质子,所含
的质子数相等,故C正确;
D.1L0.1mol•L﹣1NH H PO 溶液中,铵根离子要水解,磷酸二氢根离子要电离和水解,阴阳离子数不相
4 2 4
等,故D错误;
故选:C。
3.N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.50mL 18.4mol•L﹣1浓硫酸与足量铜微热反应,生成SO 分子的数目为0.46N
2 A
B.含N 个Na+的Na O溶解于1L水中,所得溶液中Na+的物质的量浓度为1mol•L﹣1
A 2
C.在H O +Cl ═2HCl+O 反应中,每生成32g氧气,则转移2N 个电子
2 2 2 2 A
D.常温下,1L 0.50mol•L﹣1NH Cl溶液与2L 0.25mol•L﹣1NH Cl溶液所含NH +物质的量相同
4 4 4
【答案】C
【解析】A、铜只能与浓硫酸反应,和稀硫酸不反应,故50mL 18.4mol•L﹣1浓硫酸不能反应完全,则
生成的二氧化硫分子数小于0.46N 个,故A错误;
A
B、氧化钠溶于1L水后,溶液体积大于1L,故此溶液中钠离子的浓度小于1mol/L,故B错误;
C、H O +Cl ═2HCl+O 反应转移2mol电子,生成1mol氧气,故当生成32g氧气即1mol氧气时,转移
2 2 2 2
电子为2N 个,故C正确;
A
D、溶液越稀,铵根离子水解程度越大,故常温下,1L 0.50mol•L﹣1NH Cl溶液中铵根离子的水解程度
4
小于2L 0.25mol•L﹣1NH Cl溶液中的铵根离子的水解程度,故两溶液中所含NH +物质的量不相同,故
4 4
D错误。
故选:C。
4.设N 为阿伏加德罗常数的值,下列说法不正确的是( )
A
A.一定条件下,合成氨反应中有0.5mol N 发生反应,则反应中转移电子数为3N
2 A
B.10克环己烷与2﹣丙醇的混合液中,碳元素的质量分数为72%,则其中所含的氧原子数目为 N
A
C.过量铜与含0.4mol HNO 的浓硝酸反应,则反应中电子转移数为0.2N
3 A
D.常温常压下有28g单晶硅晶体,则其中所含的Si﹣Si键数目为2N
A
【答案】C
【解析】A.反应中N 转化为NH ,氮元素由0价变为﹣3价,即1molN 参与反应转移6mol电子,有
2 3 2
0.5molN 发生反应,反应中转移电子数为3mol电子,数目为3N ,故A正确;
2 A
B.环己烷的分子式为 C H ,2﹣丙醇的分子式为C H O,相当于C H •H O,碳元素的质量分数为
6 12 3 8 3 6 272%,根据 ,解得10g混合液中含CH 的质量为8.4g,含“H O”为1.6g,则其中含
2 2
有的氧原子数目为 N = N ,故B正确;
A A
C.过量铜与含 0.4molHNO 的浓硝酸反应,若只生成 NO ,发生反应为 Cu+4HNO (浓)=Cu
3 2 3
(NO ) +2H O+2NO ↑,氮元素由+5价变为+4价,0.4mol浓HNO 硝酸参与反应,其中0.2mol被还原,
3 2 2 2 3
电子转移数目为0.2N ,但随着反应发生,浓硝酸变稀,产物气体由NO 变为NO,氮元素由+5价变为
A 2
+2价,转移电子数目增多,则电子转移数目为大于0.2N ,故C错误;
A
D.单晶硅中一个Si原子平均含有两个Si﹣Si键,常温常压下有28g单晶硅晶体为1mol,则其中所含
的Si﹣Si键数目为2N ,故D正确;
A
故选:C。
5.设N 表示阿伏加德罗常数的值,下列说法正确的是( )
A
A.1L0.1mol•L﹣1氨水中含有0.1N NH 分子
A 3
B.46g NO 和N O 混合气体中含有的原子数为3N
2 2 4 A
C.1mol Na O 中含有的阴离子数为2N
2 2 A
D.常温常压下,12g14C所含中子数为6N
A
【答案】B
【解析】A.1L0.1mol•L﹣1氨水中含有溶质的物质的量为0.1mol,但氨水中主要以NH •H O的形式存
3 2
在,含有的NH 分子数小于0.1N ,故A错误;
3 A
B.46g NO 和N O 混合气体含有 46g最简式 NO ,含有最简式 NO 的物质的量为:n(NO )=
2 2 4 2 2 2
=1mol,则该混合气体中含有原子的总物质的量为3mol,含有的原子数为3N ,故B正确;
A
C.1mol Na O 中含有1mol过氧根离子,含有阴离子数为N ,故C错误;
2 2 A
D.12g14C的物质的量为: = mol,含有中子的物质的量为: mol×8= mol,所含中子
数为 N ,故D错误;
A
故选:B。
6.摩尔是( )
A.物质中所含的微粒数
B.表示物质质量的单位C.表示物质的量的单位
D.既是物质的数量单位又是物质质量的单位
【答案】C
【解析】摩尔是表示物质的量的单位,符号为mol,
故选:C。
7.(1)同温同压下,同体积的N 和SO 分子数之比为 ,物质的量之比为 ,原子总数之比
2 2
为 ,摩尔质量之比为 ,质量之比为 ,密度之比为 。
(2)现有质量比为11:14的CO 和CO的混合气体,则该混合气体中的CO 和CO物质的量之比为
2 2
,碳原子和氧原子的个数比为 ,该混合气体的摩尔质量为 。
(3)12.4gNa X中含Na+0.4mol,则Na X的摩尔质量是 ,X的相对原子质量是 。
2 2
(4)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,
11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是 ,氧气的质量是 。
(5)某元素的一个原子的质量为ag,一个12C原子的质量为bg,阿伏加德罗常数为N ,则该原子的
A
相对原子质量数值可表示为 或 。
【答案】(1)1:1;1:1;2:3;7:16;7:16;7:16;
(2)1:2;3:4;33.3g/mol;
(3)62g/mol;16;
(4)1:4;3.2g;
(5) ;a N 。
A
【解析】(1)因同温同压下,同体积的气体具有相同的分子数,则具有相同的物质的量,
则N 和SO 分子数之比为1:1,物质的量之比为1:1,
2 2
原子总数之比为1×2:1×3=2:3,
摩尔质量之比为28g/mol:64g/mol=7:16,
质量之比为1×7:1×16=7:16,
又由pM=ρRT可知,同温同压下气体的密度之比等于摩尔质量之比,
则密度之比为7:16。
(2)CO 和 CO 物质的量之比为: : =1:2,则碳原子和氧原子的个数比为
2
(1+2×1):(1×2+2×1)=3:4,平均摩尔质量为 =33.3g/mol。(3)n(Na X)= n(Na+)= ×0.4mol=0.2mol,故Na X的摩尔质量是:12.4g÷0.2mol=62g/mol,
2 2
X的相对原子质量为62﹣2×23=16。
(4)设氧气、氦气的物质的量分别为xmol、ymol:32x+4y=4.8;22.4x+22.4y=11.2;解得:x=0.1,
y=0.4,
故氧气和氦气的分子数之比是0.1mol:0.4mol=1:4,氧气的质量为0.1mol×32g/mol=3.2g。
(5)由定义式可知,该原子相对原子质量= = ;
1mol该原子含有N 原子,1mol该原子的质量为a N g,故其相对原子质量为a N 。
A A A
二、拓展提升
8.(1)在25℃、101 kPa的条件下,相同质量的CH 和A气体的体积之比是15:8,则A的摩尔质量为
4
。
(2)两个相同容积的密闭容器X、Y,在25℃下,X中充入a g A气体,Y中充入a g CH 气体,X与
4
Y内的压强之比是4:11,则A的摩尔质量为 。
【答案】(1)同30g/mol;
(2)44g/mol。
【解析】(1)同温同压下,气体的体积之比等于其物质的量之比,所以: : =15:
8,
故答案为:30g/mol;
(2)在相同温度,相同容积的容器内,气体的压强之比等于其物质的量之比,即 : =4:
11,解得M(A)=44(g/mol),
故答案为:44g/mol。
9.根据所学知识,回答下列问题:
(1)在配制 500mL 0.1mol•L﹣1硫酸亚铁溶液时,需要称量绿矾晶体(FeSO •7H O) 的质量为
4 2
。
(2)标准状况下,672mLSO 的物质的量是 mol,质量是 g;标准状况下,9.03×1023个H 分
2 2
子的物质的量是 mol,体积约为 L。
(3)胶体和溶液的本质区别是 。
A.能否发生电泳
B.分散质粒子直径大小不同C.能否发生丁达尔效应
【答案】(1)13.9g;
(2)0.03;1.92;1.5;33.6;
(3)B。
【解析】(1)m=cVM=0.5mL×0.1mol•L﹣1×278g/mol=13.9g;
(2)标准状况下,672mLSO 的物质的量是 =0.03mol,质量是0.03×64=1.92g;标准状况
2
下,9.03×1023个H 分子的物质的量是 =1.5mol,所以体积约为:1.5×22.4=33.6L;
2
(3)当分散剂是水或其它溶剂时,根据分散质粒子直径大小来分类,把分散系划分为:溶液(小于
1nm)、胶体(1nm~100nm)、浊液(大于100nm),所以溶液、胶体和浊液这三种分散系的本质的
区别在于分散质粒子直径大小,故选:B。
10.化学实验是科学探究过程中的一种重要方法,掌握化学实验的基本操作和物质的制备、转化及性质的
探究尤为重要,请结合所学化学实验知识回答以下问题。
Ⅰ.实验室配制220mL 1 mol•L﹣1的稀H SO 溶液:
2 4
(1)用量筒量取浓H SO (密度为1.84g•mL﹣1,质量分数为98%)的体积为 mL。
2 4
(2)误差分析:下列情况使配制结果偏大的是 。
①溶解后未冷却即转移、定容
②定容时仰视容量瓶刻度线
③用量筒量取一定体积的浓硫酸时俯视
④将量筒、烧杯、玻璃棒洗涤2~3次,转移至容量瓶
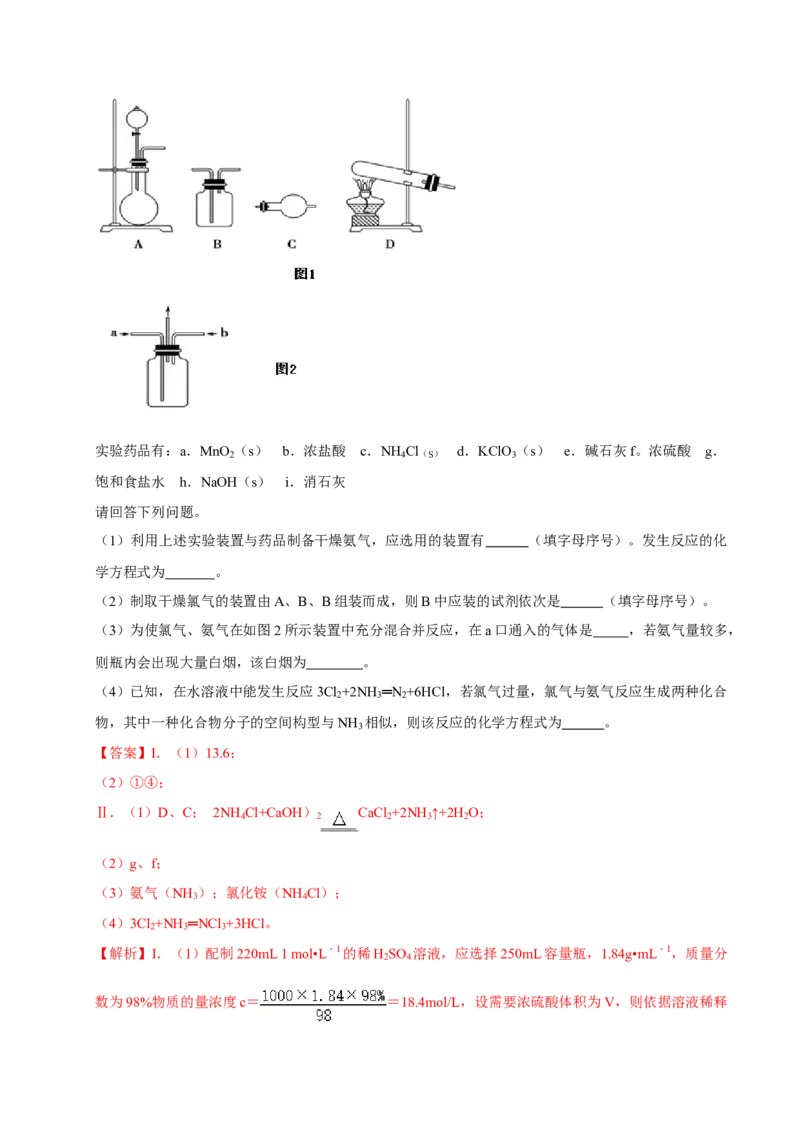
Ⅱ. 某研究性学习小组在查阅资料时发现:化工厂常用氨气来检验氯气是否泄漏。于是他们设计实验
探究氯气与氨气之间的反应。制备气体的实验装置有如图1(可重复选用):实验药品有:a.MnO
2
(s) b.浓盐酸 c.NH
4
Cl(S) d.KClO
3
(s) e.碱石灰f。浓硫酸 g.
饱和食盐水 h.NaOH(s) i.消石灰
请回答下列问题。
(1)利用上述实验装置与药品制备干燥氨气,应选用的装置有 (填字母序号)。发生反应的化
学方程式为 。
(2)制取干燥氯气的装置由A、B、B组装而成,则B中应装的试剂依次是 (填字母序号)。
(3)为使氯气、氨气在如图2所示装置中充分混合并反应,在a口通入的气体是 ,若氨气量较多,
则瓶内会出现大量白烟,该白烟为 。
(4)已知,在水溶液中能发生反应3Cl +2NH ═N +6HCl,若氯气过量,氯气与氨气反应生成两种化合
2 3 2
物,其中一种化合物分子的空间构型与NH 相似,则该反应的化学方程式为 。
3
【答案】I.(1)13.6;
(2)①④;
Ⅱ.(1)D、C; 2NH Cl+CaOH) CaCl +2NH ↑+2H O;
4 2 2 3 2
(2)g、f;
(3)氨气(NH );氯化铵(NH Cl);
3 4
(4)3Cl +NH ═NCl +3HCl。
2 3 3
【解析】I.(1)配制220mL 1 mol•L﹣1的稀H SO 溶液,应选择250mL容量瓶,1.84g•mL﹣1,质量分
2 4
数为98%物质的量浓度c= =18.4mol/L,设需要浓硫酸体积为V,则依据溶液稀释规律可知:18.4mol/L×V=250mL×1mol/L,解得V=13.6mL;
故答案为:13.6;
(2)①溶解后未冷却即转移、定容,冷却后溶液体积偏小,溶液浓度偏高,故选;
②定容时仰视容量瓶刻度线,导致溶液体积偏大,溶液浓度偏低,故不选;
③用量筒量取一定体积的浓硫酸时俯视,导致浓硫酸体积偏小,溶质物质的量偏小,溶液浓度偏低,
故不选;
④将量筒、烧杯、玻璃棒洗涤2~3次,转移至容量瓶,导致量取浓硫酸体积偏大,溶质物质的量偏大,
溶液浓度偏高,故选;
故选:①④;
Ⅱ.(1)氯化铵固体与氢氧化钙固体加热生成氯化钙、氨气和水,反应方程式:2NH Cl+CaOH)
4 2
CaCl +2NH ↑+2H O,固体与固体加热选择D发生装置,干燥氨气用碱石灰,选择装置C做干燥
2 3 2
装置,
故答案为:D、C; 2NH Cl+CaOH) CaCl +2NH ↑+2H O;
4 2 2 3 2
(2)制取氯气用到的浓盐酸易挥发,制取的氯气中含有氯化氢、水蒸气,先后通过盛有饱和食盐水的
洗气瓶,盛有浓硫酸的洗气瓶除去杂质气体;
故答案为:g、f;
(3)氨气密度小于空气密度,氯气密度大于空气密度,为使氯气、氨气在如图2所示装置中充分混合
并反应,a口通入氨气,b口通入氯气,二者反应生成氮气和氯化氢,氯化氢与过量氨气反应生成氯化
铵白色固体,产生大量白烟;
故答案为:氨气(NH );氯化铵(NH Cl);
3 4
(4)氯气过量,氯气与氨气反应生成两种化合物,其中一种化合物分子的空间构型与NH 相似,为
3
NCl ,依据原子个数守恒可知另一种物质为氯化氢,反应方程式:3Cl +NH ═NCl +3HCl;
3 2 3 3
故答案为:3Cl +NH ═NCl +3HCl。
2 3 3