文档内容
化 学
考生注意:
1.答题前,考生务必将自己的姓名、考生号填写在试卷和答题卡上,并将考生号条形码粘贴
在答题卡上的指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试
卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1 C12 N14 O16
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
1. 化学与生产、生活、技术密切相关。下列说法正确的是
A. 天然气燃烧过程中化学能全部转化成热能
B. 工业合成氨为提高氨的平衡产率,采取400~500℃的高温
C. 液态肼( )和液态过氧化氢作火箭推进剂,对环境影响较小
D. 化学家盖斯提出的盖斯定律,为化学动力学发展奠定了基础
2. 历史上曾用“地康法”制氯气,其反应原理为 。
若使HCl的平衡转化率和化学反应速率正均增大,可采取的措施是
A. 移走 B. 增大压强 C. 加入HCl D. 使用高效催化剂
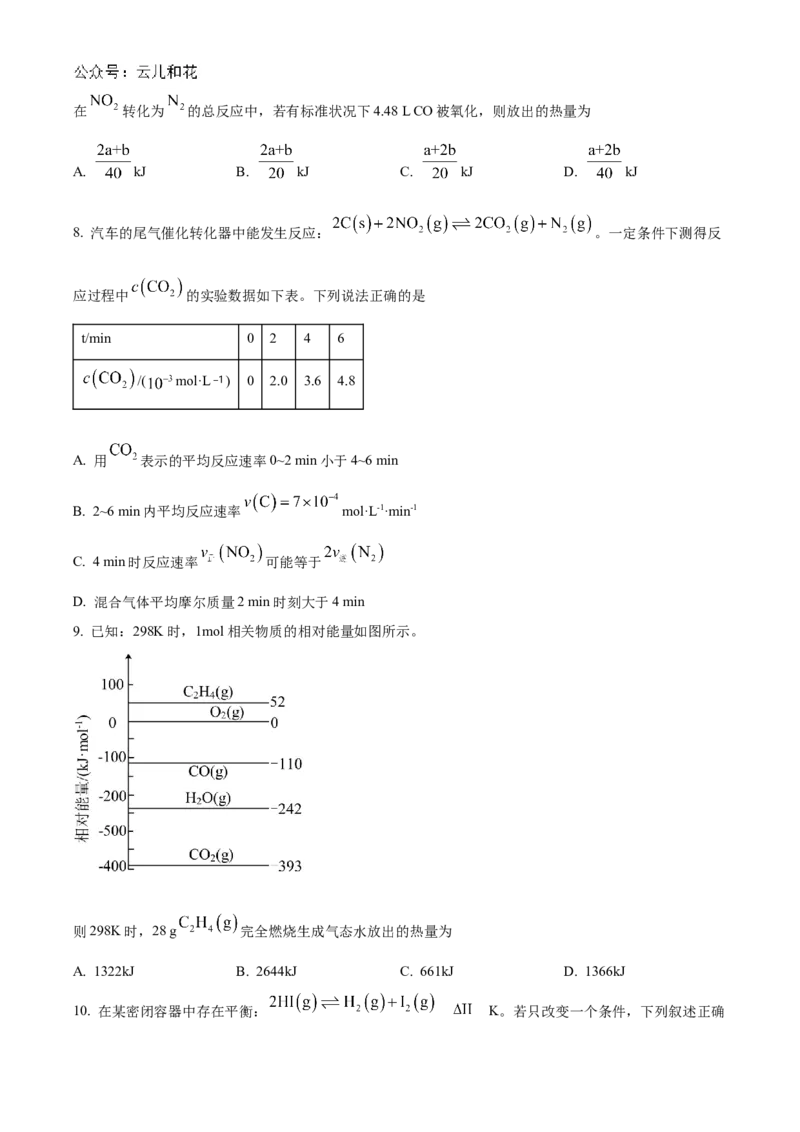
3. 天然气法合成 的相关反应为 kJ⋅mol
,关于该反应,下列图像描述可能正确的是
A. B.C. D.
4. 已知: kJ⋅mol-1,则下列热化学方程式书写正确的是
A. kJ⋅mol-1
B. kJ⋅mol-1
C. kJ⋅mol-1
D. kJ⋅mol-1
5. 已知: , ,下列判断正
确的是
A. , B.
C. D.
6. 下列事实或现象能用勒夏特列原理解释的是
A. 合成氨工业使用铁触媒能提高氨的产量
B. 溶液中加入铁粉后溶液红色变浅
C. 升高温度或使用催化剂,反应物活化分子百分数增大
D. 在硫酸工业中, 转化为 的反应,选用常压而不选用高压
7. 氮氧化物的治理对大气环境的净化有着重要的意义。已知:
① kJ⋅mol-1( )
② kJ⋅mol-1( )在 转化为 的总反应中,若有标准状况下4.48 L CO被氧化,则放出的热量为
A. kJ B. kJ C. kJ D. kJ
8. 汽车的尾气催化转化器中能发生反应: 。一定条件下测得反
应过程中 的实验数据如下表。下列说法正确的是
t/min 0 2 4 6
/( mol·L ) 0 2.0 3.6 4.8
A. 用 表示的平均反应速率0~2 min小于4~6 min
B. 2~6 min内平均反应速率 mol·L-1·min-1
C. 4 min时反应速率 可能等于
D. 混合气体平均摩尔质量2 min时刻大于4 min
9. 已知:298K时,1mol相关物质的相对能量如图所示。
则298K时,28 g 完全燃烧生成气态水放出的热量为
A. 1322kJ B. 2644kJ C. 661kJ D. 1366kJ
10. 在某密闭容器中存在平衡: K。若只改变一个条件,下列叙述正确的是
A. 若平衡正向移动,则 一定发生变化
B. 若体系颜色变深,则平衡一定正向移动
.
C 若平衡常数K增大,则平衡时HI转化率一定增大
D. 若HI分解速率加快,则体系颜色一定变深
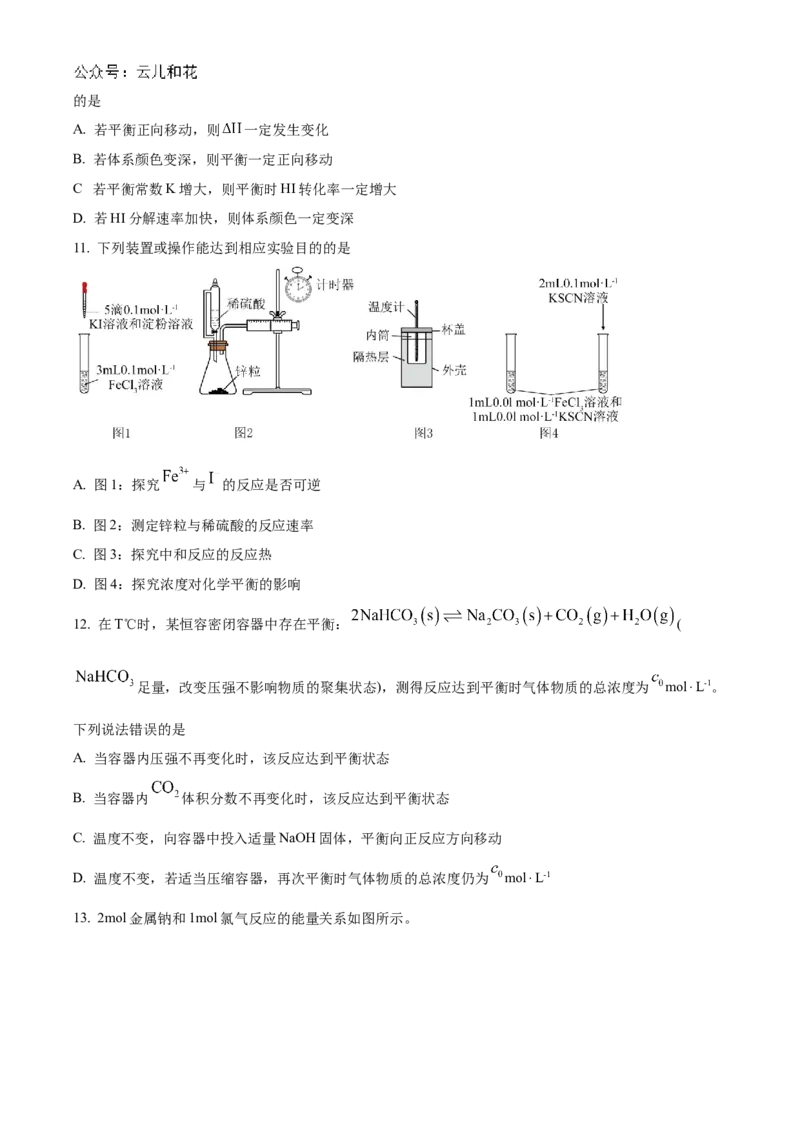
11. 下列装置或操作能达到相应实验目的的是
A. 图1:探究 与 的反应是否可逆
B. 图2:测定锌粒与稀硫酸的反应速率
C. 图3:探究中和反应的反应热
D. 图4:探究浓度对化学平衡的影响
12. 在T℃时,某恒容密闭容器中存在平衡: (
足量,改变压强不影响物质的聚集状态),测得反应达到平衡时气体物质的总浓度为 mol⋅L-1。
下列说法错误的是
A. 当容器内压强不再变化时,该反应达到平衡状态
B. 当容器内 体积分数不再变化时,该反应达到平衡状态
C. 温度不变,向容器中投入适量NaOH固体,平衡向正反应方向移动
D. 温度不变,若适当压缩容器,再次平衡时气体物质的总浓度仍为 mol⋅L-1
13. 2mol金属钠和1mol氯气反应的能量关系如图所示。已知: 、
下列说法错误的是
A.
B.
C.
D. 相同条件下, 的
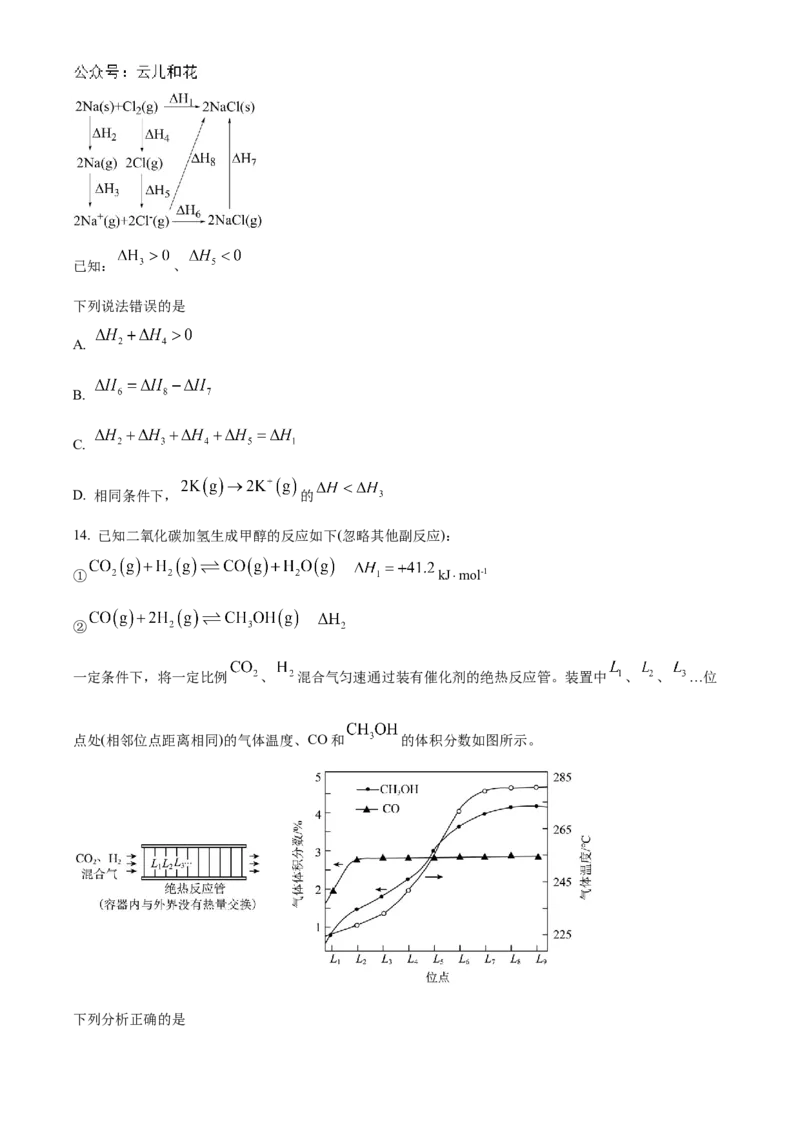
14. 已知二氧化碳加氢生成甲醇的反应如下(忽略其他副反应):
① kJ⋅mol-1
②
一定条件下,将一定比例 、 混合气匀速通过装有催化剂的绝热反应管。装置中 、 、 …位
点处(相邻位点距离相同)的气体温度、CO和 的体积分数如图所示。
下列分析正确的是A.
B. 物质具有的能量:1 mol 高于1 mol
C. 反应②的化学平衡常数K: 处温度下大于 处
D. 的体积分数: 处大于 处
二、非选择题:本题共4小题,共58分。
15. 从实验角度研究化学反应的能量变化和快慢,对工农业生产和人们生活有重要的意义。
(1)某化学兴趣小组用:50 mL 0.50 molL-1盐酸与50 mL 0.55 molL-1NaOH溶液进行中和反应的反应热测
定实验。某学生记录的实验数据如下表所⋅示。 ⋅
①请填写表格中的空白:
起始温度/℃
实验编 最高温度 温度差平均值
号 HCl溶 NaOH溶 平均值 /℃ /℃
液 液
/℃
1 26.3 26.1 26.2 29.4
.
2 27.0 27.4 27.2 325
_______
3 25.9 25.9 25.9 29.0
4 26.4 26.2 26.3 29.6
②若测得生成1 mol 时反应的 偏大,则原因可能是_______(填字母)。
a.实验时忘记盖杯盖
b.用量筒量取盐酸的体积时仰视读数
c.分多次把NaOH溶液倒入盛有盐酸的量热计内筒中
为
(2)查阅文献, 对 分解具有催化作用,反应机理如下(已知CuCl 白色沉淀):
第ⅰ步: (反应速率相对较慢)
第ⅱ步:_______(反应速率相对较快)
的
为探究“ 对 分解具有催化作用”,设计如下实验。向5支均盛有10 mL 5% 溶液 试管中滴加不同试剂,实验记录如下表(忽略溶液体积的微小变化):
实验 I Ⅱ Ⅲ Ⅳ Ⅴ
2滴1 mol·L-1 2滴1 mol·L-1 2滴1 mol·L-1
2滴1
滴加 mol·L-1NaCl溶 溶 溶液和2 溶液和2
_____
试剂 液和2滴蒸馏 液和2滴蒸馏 滴1 mol·L-1NaCl 滴2 mol·L-1NaCl
水
水 溶液 溶液
均产生气泡,且气泡产生速率从Ⅲ到Ⅴ依次增
现象 无气泡产生 无气泡产生 大,其中实验Ⅲ中无白色沉淀出现,实验Ⅳ中
能观察到有短暂的白色沉淀生成
①写出第ⅱ步反应的离子方程式:_______。
②结合表格和实验目的,实验Ⅲ中滴加的试剂应是_______。
③实验I和Ⅱ的目的是_______。
④实验Ⅴ比实验Ⅳ气泡产生速率快的原因可能为_______。
⑤由实验Ⅲ~Ⅴ能得出的结论是_______(填一条)。
16. 氨是一种重要的化工原料,主要用于化肥工业,也是一种优良的小分子储氢载体。请回答下列问题:
(1)已知: kJ⋅mol-1;
①氨气分解能在___________(填“相对低温”“任意温度”或“相对高温”)条件下自发进行。
②若该反应正反应的活化能为a kJ⋅mol-1,则逆反应的活化能为___________kJ⋅mol-1(用含a的代数式表示)。
(2)在催化剂作用下,相同条件、相同时间内 发生分解反应时, 的转化率与温度、催化剂
(Cat1、Cat2)的关系如图所示。
①a点 的转化率高于b点的原因为___________。
②b点 ___________ (填“>”“=”或“<”);在Cat1作用下,b→c变化的主要原因是___________。(3)在不同条件下,在某恒容密闭容器中以 , 体积比为1∶3起始投料合成氨,反应的平衡体系中
含量如下表所示。
序 压强/ 温 平衡体系中 体积分
号 MPa 度/℃
数
Ⅰ 1 500
Ⅱ 2 450 b
①实验发现 ,其原因为___________。
②Ⅰ条件下 的平衡常数 ___________(列出计算式即可, 为用平衡物
质的量分数代替平衡浓度计算的平衡常数)。
(4)选择合适的催化剂和温度,在不同压强下,从投料开始,反应开始后相同时间内混合气体中氨气的
体积分数如图所示。压强超过7MPa, 体积分数突然大幅度下降的原因可能是___________。
17. 化学反应提供的能量大大促进了社会的发展,研究化学反应中的能量变化具有重要意义。
(1)葡萄糖是一种重要的营养物质,它是人类生命活动所需能量的重要来源之一,已知葡萄糖
的燃烧热( )是-2800 kJ⋅mol-1,写出表示葡萄糖燃烧热的热化学方程式:___________。
(2)NO与CO一定条件下发生反应: ,在金属铑(Rh)催化作
用下,该反应过程经历以下两步基元反应,相对能量变化如图所示。①写出第一步基元反应的热化学方程式:___________。
②第___________(填“一”或“二”)步基元反应为总反应的决速步骤,其原因为___________。
(3)已知键能是指气态分子中1 mol化学键解离成气态原子所吸收的能量。几种共价键的键能如下表:
共价键
键能E/(kJ·mol-1) a 159 193 327
① kJ⋅mol-1,则
___________kJ⋅mol-1。
② 和 迅速反应可生成 ,已知 kJ⋅mol-1,
则a=___________[已知1 mol 含有8 mol 键] 。
(4)利用铁及其氧化物循环制氢,原理如图所示。
已知:流程中的 为生成或消耗1 mol 、生成或消耗 mol 时的能量变化。
①若用1 mol CO通过该方法制氢,理论上可获得___________mol 。②以生成1 mol 为基准,上述流程总反应的焓变 ___________。(用含 , , 的
代数式表示)。
18. 我国丙烷储量丰富,将丙烷转化为具有高附加值的丙烯是提高丙烷利用效率、实现碳基能源高效利用
的关键技术之一,工业上通过丙烷脱氢制备丙烯的主要反应如下:
PDH工艺(丙烷直接脱氢): kJ⋅mol-1,
ODHP工艺(丙烷氧化脱氢): 。
请回答下列问题:
(1)已知反应 kJ⋅mol-1,
① 的燃烧热( )___________-241.8 kJ⋅mol-1,(填“>”“<”或“=”)。
② ___________。
(2)已知PDH反应的 J·K-1·mol-1,则欲使PDH反应自发进行,需控制温度大于
___________K。
(3)PDH反应过程中利用膜反应新技术可以实现边反应边分离出生成的氢气。不同温度下。2.0 mol
在容积为2.0L的恒容密闭容器中发生PDH反应。氢气移出率
不同时, 的平衡转化率与反应温度的关系如图所示:
①相同温度时, , 、 由大到小的顺序为___________,判断方法为___________。②若A点时 ,则对应温度下,该反应的化学平衡常数为___________。
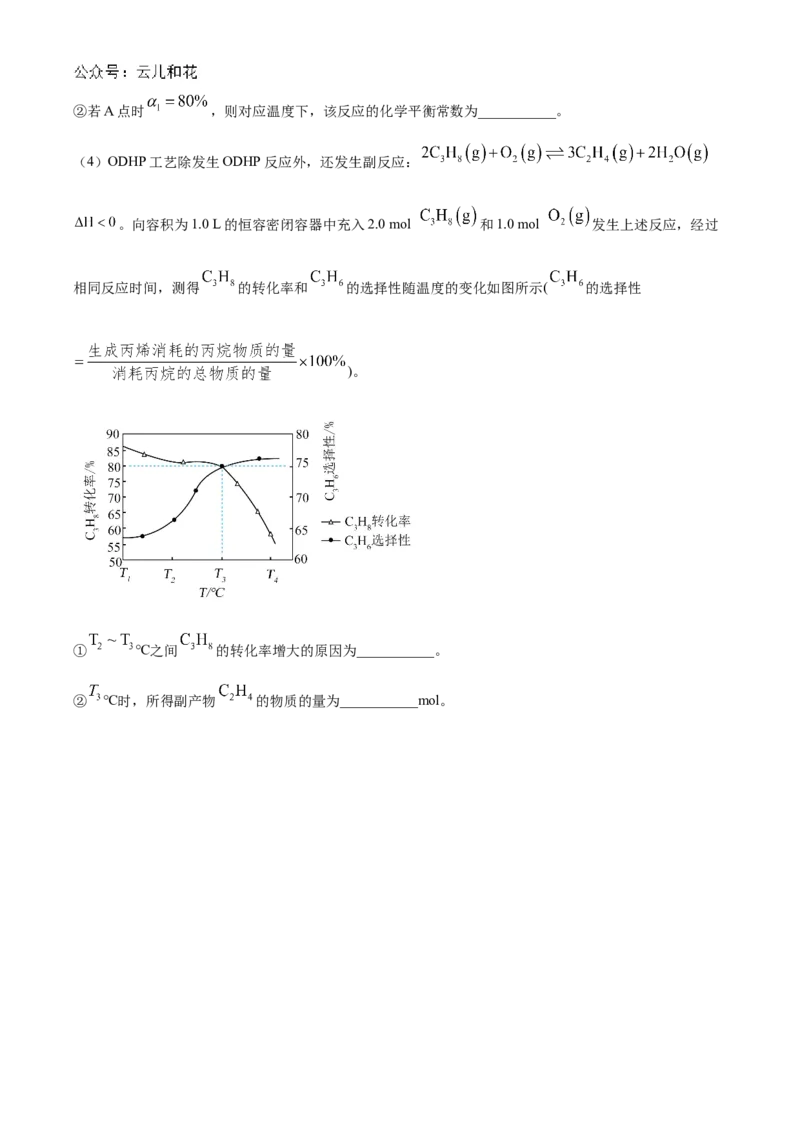
(4)ODHP工艺除发生ODHP反应外,还发生副反应:
。向容积为1.0 L的恒容密闭容器中充入2.0 mol 和1.0 mol 发生上述反应,经过
相同反应时间,测得 的转化率和 的选择性随温度的变化如图所示( 的选择性
)。
① ℃之间 的转化率增大的原因为___________。
② ℃时,所得副产物 的物质的量为___________mol。化学
考生注意:
1.答题前,考生务必将自己的姓名、考生号填写在试卷和答题卡上,并将考生号条形码粘贴
在答题卡上的指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试
卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1 C12 N14 O16
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
【1题答案】
【答案】C
【2题答案】
【答案】B
【3题答案】
【答案】D
【4题答案】
【答案】B
【5题答案】
【答案】D
【6题答案】
【答案】B
【7题答案】
【答案】B
【8题答案】
【答案】D
【9题答案】
【答案】A
【10题答案】
【答案】C
【11题答案】【答案】B
【12题答案】
【答案】B
【13题答案】
【答案】C
【14题答案】
【答案】D
二、非选择题:本题共4小题,共58分。
【15题答案】
【答案】(1) ①. 3.2 ②. ac
(2) ①. ②. 2滴1mol/LCuSO 液和2滴水 ③.
4
排除Cl-和 对HO 的分解没有催化作用 ④. CuCl 的浓度越大,催化效果越好 ⑤. CuCl 对
2 2 2 2
HO 的分解具有催化作用或Cl-和 对HO 的分解没有催化作用等
2 2 2 2
【16题答案】
【答案】(1) ①. 相对高温 ②. (a-92.4)
(2) ①. 相同温度下,Cat2的催化效率高于Cat1,反应速率更快, ②. > ③. 温度较高时,催
化剂活性减弱
(3) ①. 温度降低,平衡正向移动,反应物浓度减小,生成物浓度增大 ②.
(4)氨气易液化,当压强逐渐增大时,氨气可能会液化
【17题答案】
【答案】(1)
(2) ①. ②. 一
③. 反应的活化能越大,发生反应需消耗的能量越高,反应就越不容易进行,反应速率就越慢
(3) ①. -438 ②. 266(4) ①. ②.
【18题答案】
【答案】(1) ①. < ②. -225.6 kJ⋅mol-1
(2)860 (3) ①. > > ②. 相同温度下,氢气的移出率越大,生成物中氢气浓度越低,
越有利于平衡正向移动,对应的 的平衡转化率也越大 ③. 1.62
(4) ①. 反应未达平衡,温度升高,反应速率加快。 ②. 0.6