文档内容
萍乡实验学校2025届高三月考试卷(五)
化 学
命题人:李 姊 伍永丽 谭禹泽 审题人:李 姊 熊三莲 吕燕琴
注意事项:
1.答卷前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2 . 回答选择题,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号 。回答非选择题,将答案写在答题卡上。试卷上无效。
3. 考试结束后,将本试卷和答题卡一并交回。
第 卷选择题 (共 42分)
Ⅰ
一、选择题(本大题共 14小题,每小题 3分,共 42分。在每小题给出的四个选项中,只有一项是符合题目要求的)
1 ( 0.1molL1)
.下列两种试剂,相互滴加 试剂的浓度均为 ,反应现象没有明显差别的是
A Na CO B KMnO
. 2 3溶液和盐酸 .草酸溶液和 4溶液
C D NaHCO CaOH
.氨水和硝酸银溶液 . 3溶液和 2溶液
2
.下列离子方程式正确的是
A SO Ca(ClO) Ca2++ClO-+SO +H O=CaSO ↓+Cl-+2H+
.少量 2通入 2溶液: 2 2 4
B FeI Fe2++4H++NO=Fe3++NO↑+2H O
. 2溶于过量的硝酸溶液中: 3 2
C NaOH 3S+6OH-SO2+2S2-+3H O
.用热 溶液洗涤试管内壁的硫黄: 3 2
Δ
D Fe n(Fe) n(HNO )=1 3 3Fe+8H++2NO=3Fe2++2NO↑+4H O
. 与稀硝酸反应,当 ﹕ 3 ﹕ 时, 3 2
3 ( ) W X Y Z
.一种由短周期主族元素组成的化合物 如图所示 ,具有良好的储氢性能,其中元素 、 、 、 的原子序数依次增大
24
,且总和为 。下列有关叙述正确的是
A W X Y
.该化合物中, 、 、 之间存在离子键
B Y
. 的氧化物的水化物不一定为强酸
C Y>X
.原子半径:
D Z
. 的单质只能与水反应,不与乙醇反应
4 Fe Cu
.部分含 或 元素物质的分类与相应化合价关系如图所示。下列推断不合理的是
思思想政治
化学试题(萍实版)第1页共9页
{#{QQABCQQQogggQgBAARgCQwWgCAEQkgGAAQgOxBAMMAIAyAFABAA=}#}A a S f g e
. 和足量 混合加热,可能生成 或 ,不可能生成
B f NaOH i
.往 中加入浓 溶液,则最终会生成
C i d
.新制的和葡萄糖混合溶液加热,可能得到
D d j H SO f a
. 和溶于稀 2 4,如果有 生成,则有 生成
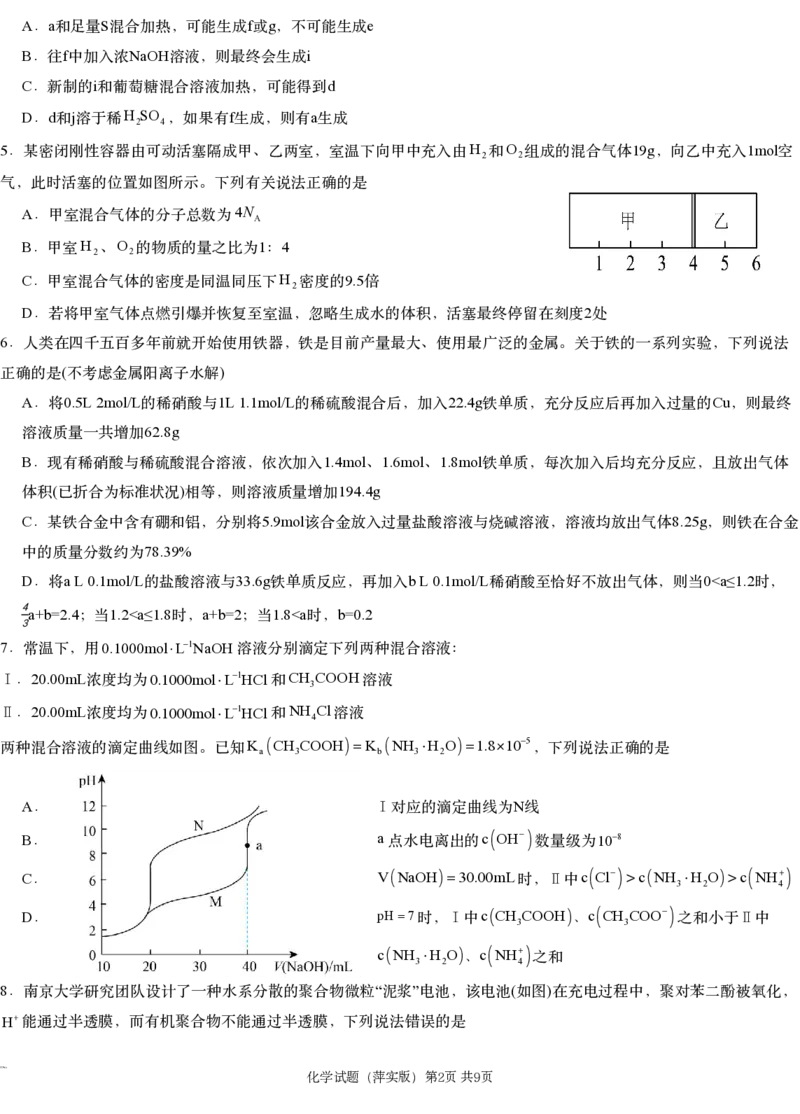
5 H O 19g 1mol
.某密闭刚性容器由可动活塞隔成甲、乙两室,室温下向甲中充入由 2和 2组成的混合气体 ,向乙中充入 空
气,此时活塞的位置如图所示。下列有关说法正确的是
A 4N
.甲室混合气体的分子总数为 A
B H O 1 4
.甲室 2、 2的物质的量之比为 :
C H 9.5
.甲室混合气体的密度是同温同压下 2密度的 倍
D 2
.若将甲室气体点燃引爆并恢复至室温,忽略生成水的体积,活塞最终停留在刻度 处
6
.人类在四千五百多年前就开始使用铁器,铁是目前产量最大、使用最广泛的金属。关于铁的一系列实验,下列说法
( )
正确的是 不考虑金属阳离子水解
A 0.5L2mol/L 1L1.1mol/L 22.4g Cu
.将 的稀硝酸与 的稀硫酸混合后,加入 铁单质,充分反应后再加入过量的 ,则最终
62.8g
溶液质量一共增加
B 1.4mol 1.6mol 1.8mol
.现有稀硝酸与稀硫酸混合溶液,依次加入 、 、 铁单质,每次加入后均充分反应,且放出气体
( ) 194.4g
体积 已折合为标准状况 相等,则溶液质量增加
C 5.9mol 8.25g
.某铁合金中含有硼和铝,分别将 该合金放入过量盐酸溶液与烧碱溶液,溶液均放出气体 ,则铁在合金
78.39%
中的质量分数约为
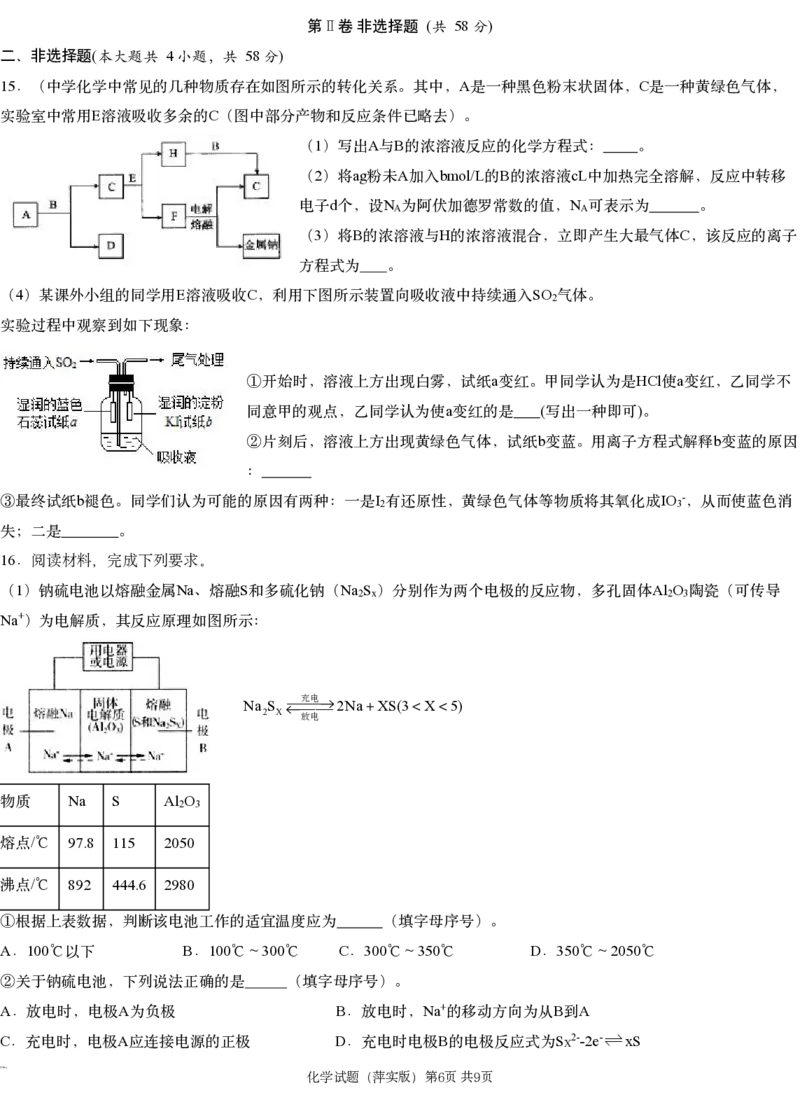
D aL0.1mol/L 33.6g bL0.1mol/L 0”“<” “=”)
反应①的活化能 a 逆 a 正 填 或 。
(2) CO H
一定温度下,在某一恒容密闭容器中充入一定量的 2和 2,发生反应①。下列能说明该反应已达到平衡状态的是
_______( )
填序号 。
A
.混合气体的平均摩尔质量不再随时间变化而改变
B
vCO :vCO 1:3
. 2 2
C CH OH
. 3 的物质的量不再随时间变化而改变
D 3mol HH 2mol OH
.单位时间内每形成 键,同时形成 键
(3) T 2.5mol CO 5.5mol H 2L
在 温度下,将 2和 2充入 的恒容密闭容器中发生反应①和
CH OHg CH OCH g 0.5mol
②,达到平衡状态时 3 和 3 3 的物质的量分别为 和
思思想政治
化学试题(萍实版)第7页共9页
{#{QQABCQQQogggQgBAARgCQwWgCAEQkgGAAQgOxBAMMAIAyAFABAA=}#}0.5mol T K
。则 温度时反应①的平衡常数 为 。
(4) CO H CO
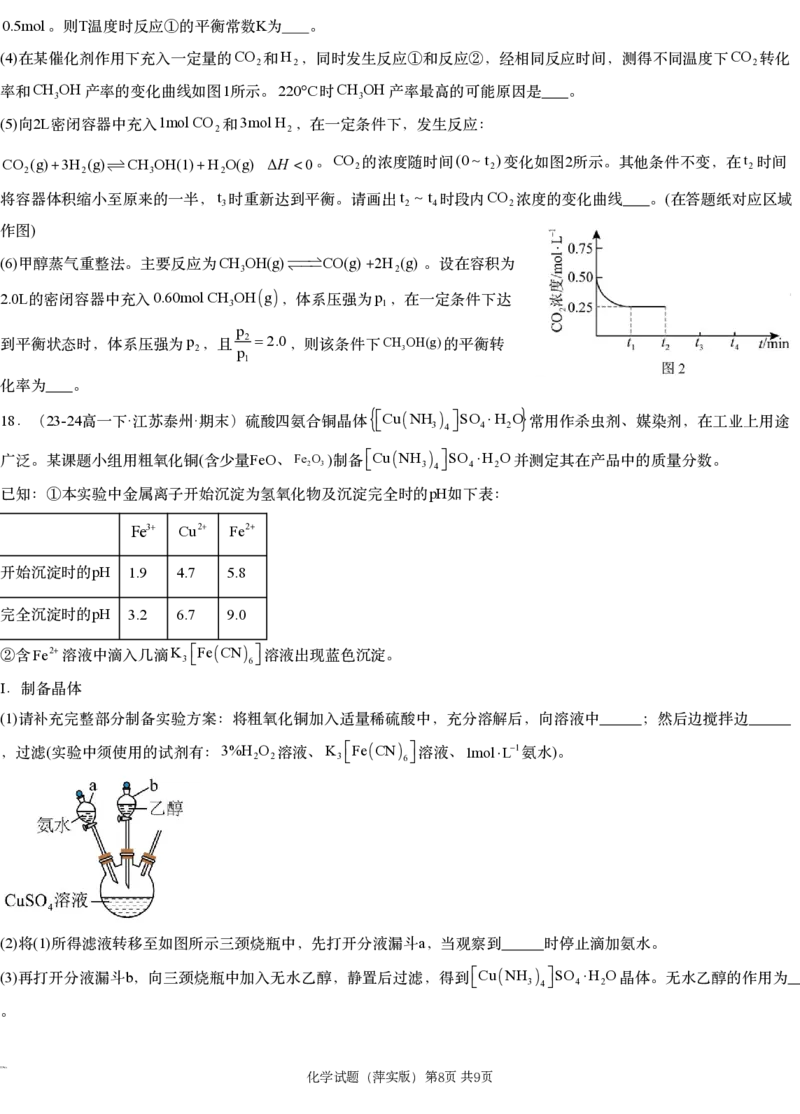
在某催化剂作用下充入一定量的 2和 2,同时发生反应①和反应②,经相同反应时间,测得不同温度下 2转化
CH OH 1 220C CH OH
率和 3 产率的变化曲线如图 所示。 时 3 产率最高的可能原因是 。
(5) 2L 1mol CO 3mol H
向 密闭容器中充入 2和 2,在一定条件下,发生反应:
CO 2 (g)3H 2 (g)CH 3 OH(1)H 2 O(g) ΔH 0 。 CO 2的浓度随时间 (0t 2 ) 变化如图 2 所示。其他条件不变,在 t 2时间
t t t CO (
将容器体积缩小至原来的一半, 3时重新达到平衡。请画出 2 4时段内 2浓度的变化曲线 。 在答题纸对应区域
)
作图
(6) CH OH(g)CO(g) 2H (g)
甲醇蒸气重整法。主要反应为 3 2 。设在容积为
2.0L 0.60mol CH OHg p
的密闭容器中充入 3 ,体系压强为 1,在一定条件下达
p
p 2 2.0 CH OH(g)
到平衡状态时,体系压强为 2,且 p ,则该条件下 3 的平衡转
1
化率为 。
18 .( 23-24 高一下 · 江苏泰州 · 期末)硫酸四氨合铜晶体 CuNH 3 4 SO 4 H 2 O 常用作杀虫剂、媒染剂,在工业上用途
广泛。某课题小组用粗氧化铜 ( 含少量 FeO 、 Fe 2 O 3 ) 制备 CuNH 3 4 SO 4 H 2 O 并测定其在产品中的质量分数。
pH
已知:①本实验中金属离子开始沉淀为氢氧化物及沉淀完全时的 如下表:
Fe3 Cu2 Fe2
pH 1.9 4.7 5.8
开始沉淀时的
pH 3.2 6.7 9.0
完全沉淀时的
②含
Fe2
溶液中滴入几滴
K
3
FeCN
6
溶液出现蓝色沉淀。
I
.制备晶体
(1)
请补充完整部分制备实验方案:将粗氧化铜加入适量稀硫酸中,充分溶解后,向溶液中 ;然后边搅拌边
,过滤 ( 实验中须使用的试剂有: 3%H 2 O 2溶液、 K 3 FeCN 6 溶液、 1molL1 氨水 ) 。
(2) (1) a
将 所得滤液转移至如图所示三颈烧瓶中,先打开分液漏斗 ,当观察到 时停止滴加氨水。
(3) 再打开分液漏斗 b ,向三颈烧瓶中加入无水乙醇,静置后过滤,得到 CuNH 3 4 SO 4 H 2 O 晶体。无水乙醇的作用为
。
思思想政治
化学试题(萍实版)第8页共9页
{#{QQABCQQQogggQgBAARgCQwWgCAEQkgGAAQgOxBAMMAIAyAFABAA=}#}II .测定产品中 CuNH 3 4 SO 4 H 2 OM246g/mol 的质量分数称取产品 0.492g ,加入稀 H 2 SO 4充分溶解后再加入足
10%KI 19.20mL0.1molL1Na S O
量 溶液,振荡充分反应。滴入几滴淀粉,溶液变蓝。再加入 2 2 3溶液,蓝色刚好褪去且半
( CuNH 2 4H Cu2 4NH 2Cu2 4I 2CuII I 2S O2 2IS O2)
分钟不变化。 已知: 3 4 4、 2、 2 2 3 4 6
(4) 由以上实验数据,计算可得产品中 CuNH 3 4 SO 4 H 2 O 的质量分数为 。 ( 直接写出结果 )
III . CuNH 3 4 SO 4 H 2 O 结构分析
(5)1molCuNH
2
mol
3 4 中含 键。
(6)CuNH 2 HNH NH HNH ( “ ” “ ”)
3 4 中 键角比 3分子中 键角 填 大、小 或 一样大 。
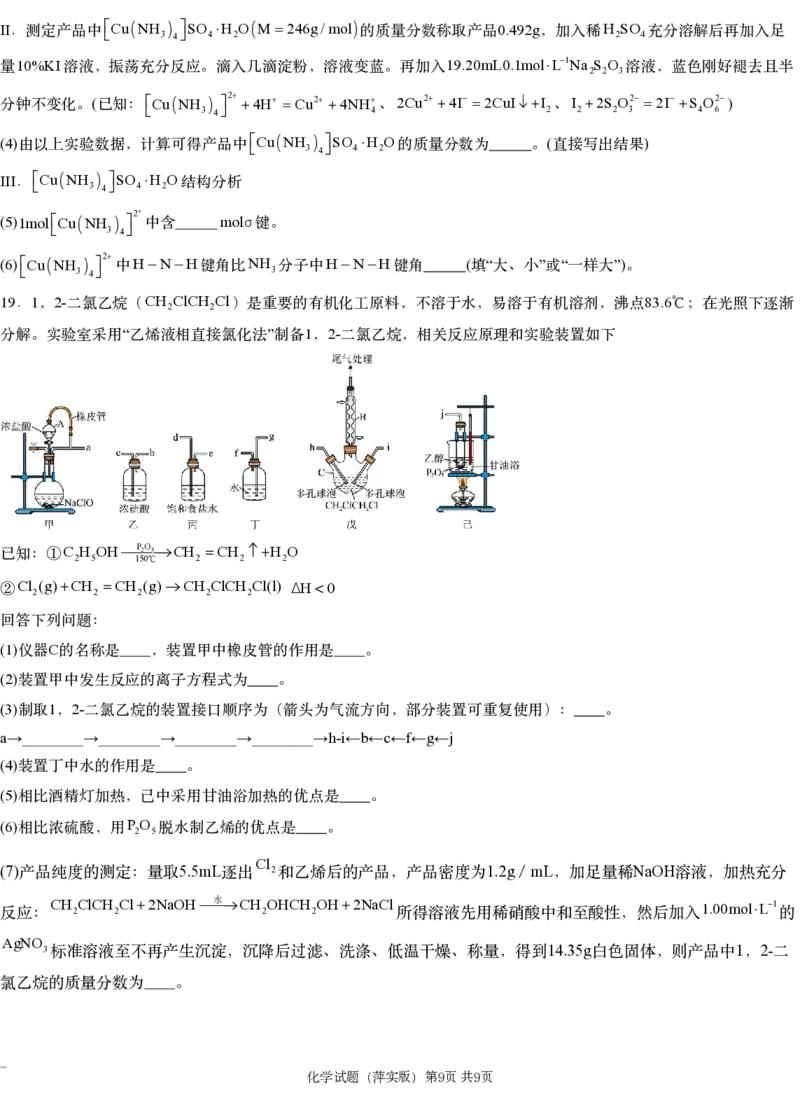
19 1 2- CH ClCH Cl 83.6
. , 二氯乙烷( 2 2 )是重要的有机化工原料,不溶于水,易溶于有机溶剂,沸点 ℃;在光照下逐渐
“ ” 1 2-
分解。实验室采用 乙烯液相直接氯化法 制备 , 二氯乙烷,相关反应原理和实验装置如下
C H OHP2O5CH CH H O
已知:① 2 5 150℃ 2 2 2
Cl (g)CH CH (g)CH ClCH Cl(l) H0
② 2 2 2 2 2
回答下列问题:
(1) C
仪器 的名称是 ,装置甲中橡皮管的作用是 。
(2)
装置甲中发生反应的离子方程式为 。
(3) 1 2-
制取 , 二氯乙烷的装置接口顺序为(箭头为气流方向,部分装置可重复使用): 。
a→________→________→________→________→h-i←b←c←f←g←j
(4)
装置丁中水的作用是 。
(5)
相比酒精灯加热,己中采用甘油浴加热的优点是 。
(6) PO
相比浓硫酸,用 2 5脱水制乙烯的优点是 。
Cl
(7) 5.5mL 2 1.2g mL NaOH
产品纯度的测定:量取 逐出 和乙烯后的产品,产品密度为 / ,加足量稀 溶液,加热充分
CH
2
ClCH
2
Cl2NaOH水CH
2
OHCH
2
OH2NaCl 1.00molL1
反应: 所得溶液先用稀硝酸中和至酸性,然后加入 的
AgNO
3 14.35g 1 2-
标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到 白色固体,则产品中 , 二
氯乙烷的质量分数为 。
思思想政治
化学试题(萍实版)第9页共9页
{#{QQABCQQQogggQgBAARgCQwWgCAEQkgGAAQgOxBAMMAIAyAFABAA=}#}