文档内容
东城区 2021—2022 学年度第一学期期末统一检测
初三化学
注意:
1.本试卷共8页,共两部分,39道小题,满分70分。考试时间70分钟。
2.在试卷和答题卡上准确填写学校、班级、姓名和教育ID号。
3.试题答案一律填涂或书写在答题卡上,在试卷上作答无效。
4.在答题卡上,选择题、画图题用2B铅笔作答,其他试题用黑色字迹签字笔作答。
5.考试结束,将本试卷和答题卡一并交回。
可能用到的相对原子质量:C12 O16 Na23 Mg24 S32 Hg201
第一部分选择题(共25分)
每小题只有1个选项符合题意。每小题1分,共25分。
1. 如图所示图标表示
A. 禁止烟火
B. 禁止燃放鞭炮
C. 禁止吸烟
D. 禁止放易燃物
2. 下列CO的性质中,属于化学性质的是
A. 无色、无味
B. 能燃烧
C. 难溶于水
D. 常温下为气体
3. 下列物质在氧气中燃烧,产生大量白烟的是
A. 红磷 B. 木炭 C. 铁丝 D. 氢气
4. 下列物质中,属于纯净物的是
A. 海水 B. 大理石 C. 天然气 D. 二氧化碳
5. 能表示两个氧原子的是A. B. C. 2O D.
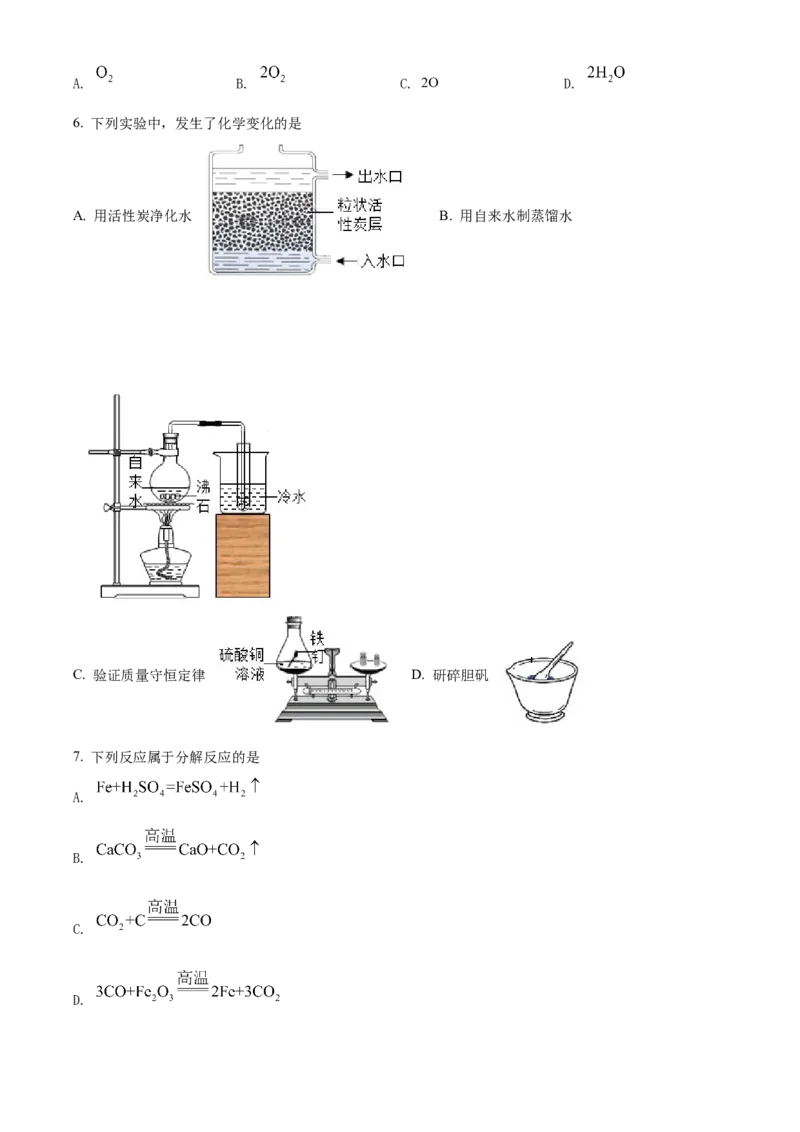
6. 下列实验中,发生了化学变化的是
A. 用活性炭净化水 B. 用自来水制蒸馏水
C. 验证质量守恒定律 D. 研碎胆矾
7. 下列反应属于分解反应的是
A.
B.
C.
D.8. 下列燃料不属于化石燃料的是( )
A. 煤 B. 石油 C. 天然气 D. 氢气
9. 下列属于金属元素的是
A. C B. H C. Na D. N
10. 实验室过滤操作中,不需要的仪器是
A. B. C. D.
的
11. 下列物质中,属于氧化物 是
A. HSO B. NaCO C. KCl D. HO
2 4 2 3 2
12. 地壳中含量最多的元素是( )
A. Si B. Al C. O D. Fe
13. 能闻到榴莲散发出的特殊气味,主要原因是
A. 分子之间有间隔 B. 分子的质量很小
C. 分子的体积很小 D. 分子在不断运动
14. 加热高锰酸钾制氧气的化学方程式正确的是
A.
B.
C.
D.
15. 下列化学式书写正确的是
A. 氧化铜
B. 二氧化硫
C. 氯化钠D. 氢氧化钾
16. 关于水的叙述不正确的是
A. 水由水分子构成
B. 水由氢分子和氧原子构成
C. 水由氢、氧元素组成
D. 1个水分子由2个氢原子和1个氧原子构成
17. 下列实验操作不正确的是
A. 点燃酒精灯 B. 检查装置气密性
C. 取用固体粉末 D. 加热液体
18. 下列方法能区分氧气和二氧化碳两瓶气体的是
A. 闻气味 B. 观察颜色
C. 向集气瓶中加入适量水 D. 将燃着的木条伸入集气瓶中
19. 下列气体极易与血液中的血红蛋白结合,导致人体中毒的是
A. CO B. C. D.
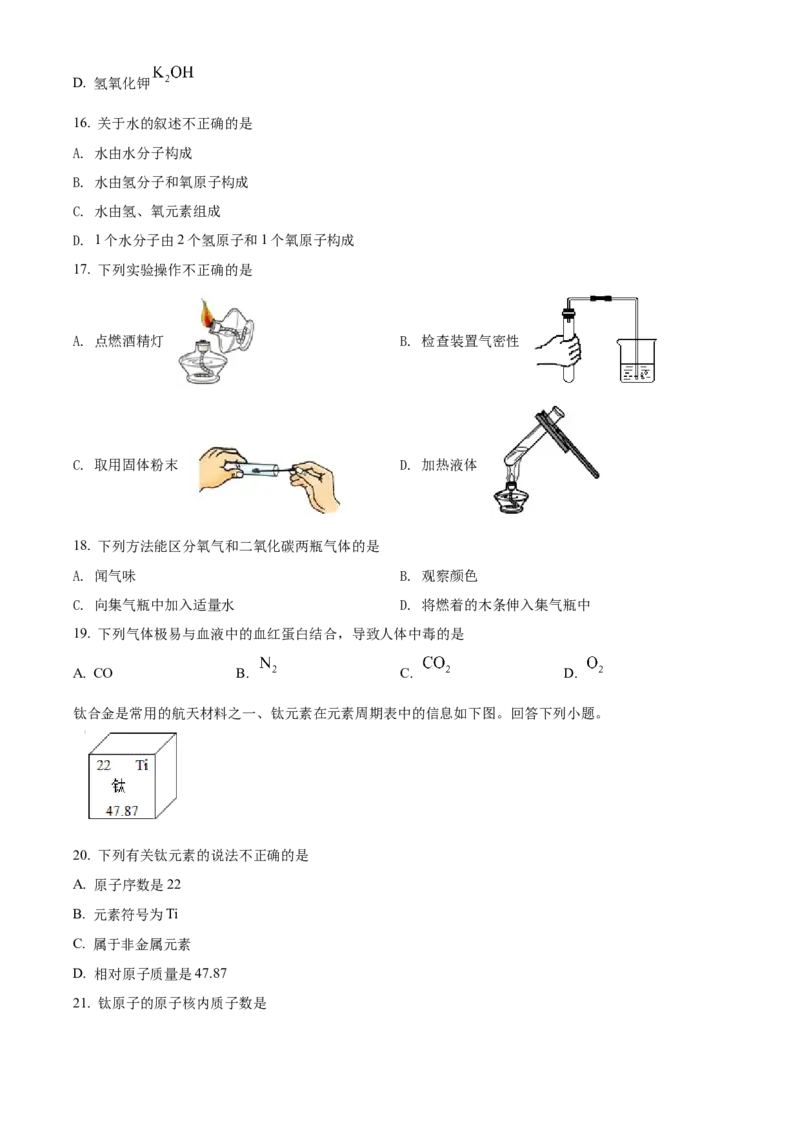
钛合金是常用的航天材料之一、钛元素在元素周期表中的信息如下图。回答下列小题。
20. 下列有关钛元素的说法不正确的是
A. 原子序数是22
B. 元素符号为Ti
C. 属于非金属元素
D. 相对原子质量是47.87
21. 钛原子的原子核内质子数是A. 70 B. 22 C. 26 D. 48
22. 下列由化学方程式 获取的信息中,错误的是
A. 反应条件是加热
B. 反应物是汞和氧气
C. 生成物是氧化汞
D. 参加反应的汞与氧气的质量比为
23. 下列关于物质用途的描述不正确的是
A. 石墨可用作电极
B. 氧气可用作燃料
C. 干冰可用于人工降雨
D. 氮气可用作保护气
24. 亚硫酸钠( )在造纸行业中广泛应用。下列关于亚硫酸钠的说法正确的是
A. 属于氧化物
B. 由两种元素组成
C. 硫元素的质量分数最小
D. 钠元素与氧元素的质量比为
25. 研究铁丝在氧气中燃烧出现火星四射现象的影响因素。取粗细相同的铁丝进行实验,记录如下。
编号 实验装置 铁丝种类 燃烧现象
① 含碳0.03%的铁丝 极少火星
② 含碳0.08%的铁丝 少量火星
③ 含碳0.15%的铁丝 明显火星四射
下列分析不正确的是
A. 所用铁丝均为混合物
B. 集气瓶中放少量水的作用是防止其炸裂
C. 铁丝中含碳量越低,火星四射现象越明显
D. 火星四射可能与铁丝中的碳和氧气反应有关第二部分非选择题(共45分)
【生活现象解释】
26. 2022年2月4日,第二十四届冬奥会将在北京开幕。北京冬奥会将向全世界展示绿色奥运理念。
(1)冬奥火矩“飞扬”(如图)采用氢气作燃料。氢气燃烧的化学方程式为___________;关闭火炬的燃
气开关,使火炬熄灭,采用的灭火原理是___________。
(2)冬奥场馆大多采用绿色能源供电。下列属于绿色能源的是___________(填序号)。
A. 太阳能 B. 风能 C. 化石燃料
27. 2022年2月4日,第二十四届冬奥会将在北京开幕。仪式火种台(如图)采用丙烷作燃料。丙烷燃烧
生成 和 ,则丙烷中一定含有的元素是___________。
28. 冬奥速滑场馆“冰丝带”采用 跨临界直冷制冰。 中碳元素的化合价是___________。
29. 中国的“茶文化”渊远流长。
(1)紫砂壶烧制原料中的紫砂黄泥含铁量很高,这里的“铁”是指___________(填序号)。
A. 单质 B. 离子 C. 元素
(2)用杂质少的软水泡茶,能充分体现茶的色、香、味,区别硬水和软水常用的试剂是___________。
(3)泡茶时,用茶漏将茶叶与茶水分离,该分离操作的名称是___________。
【科普阅读理解】
30. 阅读下面科普短文。
潜水员背着的瓶子叫做“水肺”。“水肺”中常见的潜水呼吸气有:压缩空气、富氧压缩空气、高压氨氧
混合气、高压氛氧混合气等。
压缩空气是通过压缩机将空气压缩而成,压缩前后空气中各气体的体积分数几乎保持不变。潜水呼吸气采用压缩空气时,气作为与氧气共存的气体,会导致潜水员出现“氮麻醉”的情况,限制了潜水的时间。因
此,潜水时常使用富氧压缩空气。但是过高浓度的氧气在高压环境下会引起潜水员“氧中毒”,其它条件
相同时,潜水员使用氧气体积分数不同的氮氧混合气潜水时,最大下潜深度及在此深度下的平均持续工作
时间如下表所示。
氮氧混合气中氧气体积分数(%) 最大下潜深度(m) 平均持续工作时间(min)
60 17 120
50 22 98
40 30 69
32 40 46
潜水呼吸气中用氦气、氖气替换氮气,可以避免出现类似于“氮麻醉”的情况,因为氦气、氖气在血液中
的溶解能力都明显小于氮气。
高压氦氧混合气作为潜水呼吸气时,由于氦气热传导系数高,潜水员会出现体温过低的症状。与此同时,
还因为氦气的密度过小,使潜水员在与岸上工作人员交流时声音传播受到影响。
高压氖氧混合气作为潜水呼吸气可以避免语音失真、体温过低等状况。但是氖气不容易大量获得,并且深
水潜水时,氖气的密度会增大进而造成潜水员呼吸受阻而限制了
其使用价值。
为了克服以上潜水呼吸气的缺陷和不足,氦氖氧混合气开始较为广泛应用。
依据文章内容回答下列问题。
(1)空气压缩前后,发生的变化是___________(填序号)。
A. 氧气体积分数增大 B. 分子间隔变小 C. 分子体积变小
(2)最大下潜深度与氮氧混合气中氧气体积分数的关系是___________。
(3)最大下潜深度为35m时,应选择氧气体积分数为___________(填序号)的氮氧混合气。
A. 50%~60% B. 40%~50% C. 32%~40%
(4)使用高压氦氧混合气时,声音传播会受到影响,因为氦气具有___________的性质。
(5)高压氖氧混合气作为潜水呼吸气的优点是___________(写出一点即可)。
(6)下列说法正确的是___________(填序号)。
A. 潜水呼吸气中氧气含量越高越好
B. 氦气和氖气在血液里的溶解能力均大于氮气
C. 使用高压氦氧混合气,潜水员往往出现体温过低的症状
【生产实际分析】
31. 一种利用畜禽粪便发酵制沼气的流程如下:(1)沼气可用作燃料,沼气燃烧是将化学能转化为___________能。
(2)沼气的主要成分是甲烷,甲烷燃烧的化学方程式为___________。
(3)上述流程 的优点是___________(写出一点即可)。
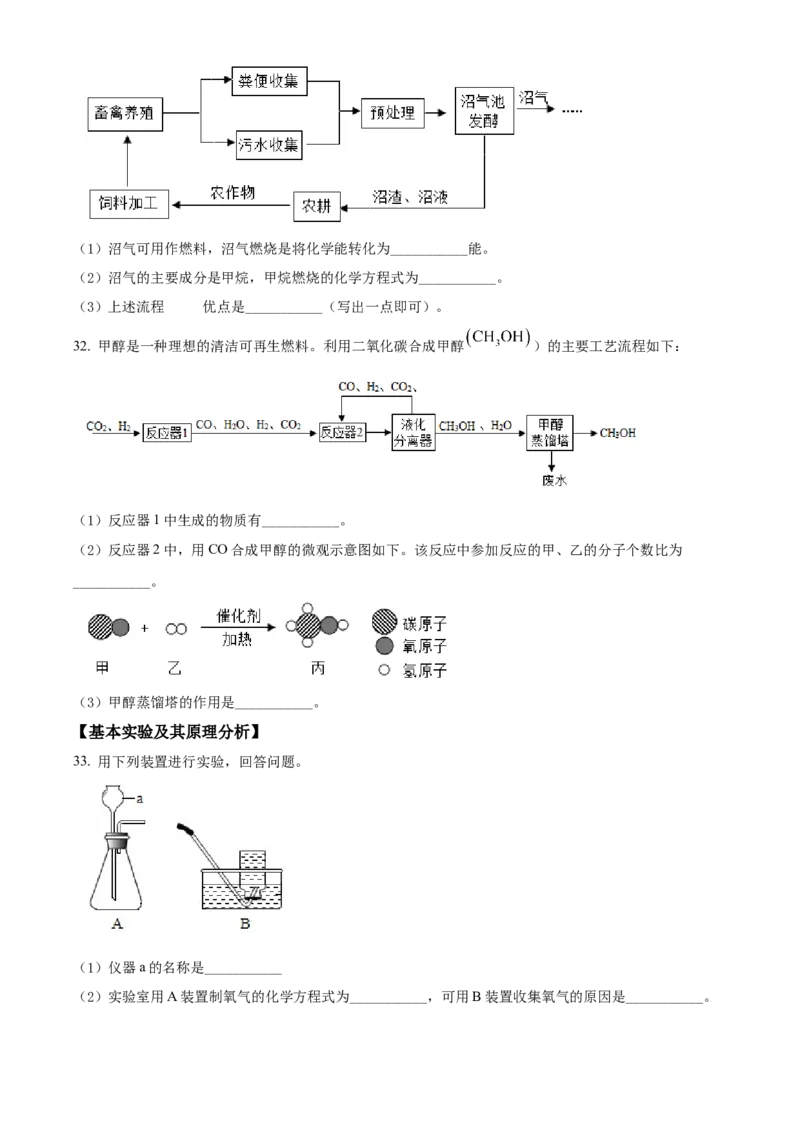
32. 甲醇是一种理想的清洁可再生燃料。利用二氧化碳合成甲醇 )的主要工艺流程如下:
(1)反应器1中生成的物质有___________。
(2)反应器2中,用CO合成甲醇的微观示意图如下。该反应中参加反应的甲、乙的分子个数比为
___________。
(3)甲醇蒸馏塔的作用是___________。
【基本实验及其原理分析】
33. 用下列装置进行实验,回答问题。
(1)仪器a的名称是___________
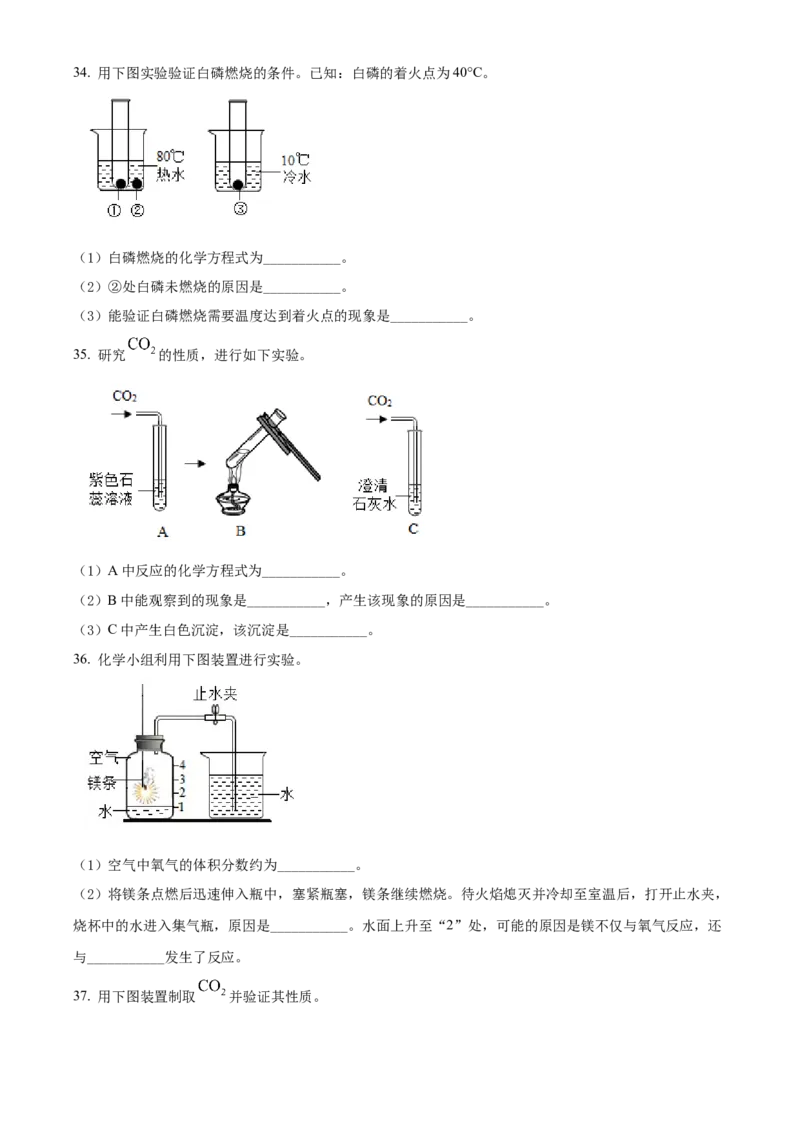
(2)实验室用A装置制氧气的化学方程式为___________,可用B装置收集氧气的原因是___________。34. 用下图实验验证白磷燃烧的条件。已知:白磷的着火点为40°C。
(1)白磷燃烧的化学方程式为___________。
(2)②处白磷未燃烧的原因是___________。
(3)能验证白磷燃烧需要温度达到着火点的现象是___________。
35. 研究 的性质,进行如下实验。
(1)A中反应的化学方程式为___________。
(2)B中能观察到的现象是___________,产生该现象的原因是___________。
(3)C中产生白色沉淀,该沉淀是___________。
36. 化学小组利用下图装置进行实验。
(1)空气中氧气的体积分数约为___________。
(2)将镁条点燃后迅速伸入瓶中,塞紧瓶塞,镁条继续燃烧。待火焰熄灭并冷却至室温后,打开止水夹,
烧杯中的水进入集气瓶,原因是___________。水面上升至“2”处,可能的原因是镁不仅与氧气反应,还
与___________发生了反应。
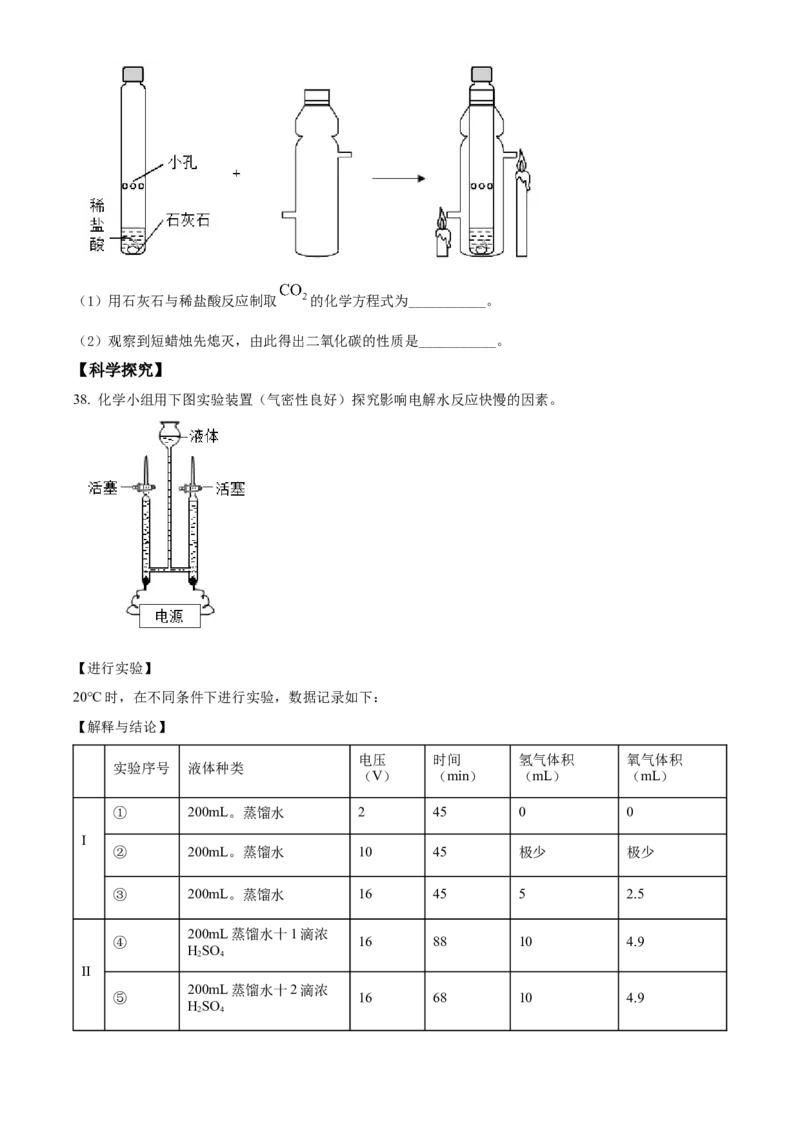
37. 用下图装置制取 并验证其性质。(1)用石灰石与稀盐酸反应制取 的化学方程式为___________。
(2)观察到短蜡烛先熄灭,由此得出二氧化碳的性质是___________。
【科学探究】
38. 化学小组用下图实验装置(气密性良好)探究影响电解水反应快慢的因素。
【进行实验】
20°C时,在不同条件下进行实验,数据记录如下:
【解释与结论】
电压 时间 氢气体积 氧气体积
实验序号 液体种类
(V) (min) (mL) (mL)
① 200mL。蒸馏水 2 45 0 0
I
② 200mL。蒸馏水 10 45 极少 极少
③ 200mL。蒸馏水 16 45 5 2.5
200mL蒸馏水十1滴浓
④ 16 88 10 4.9
HSO
2 4
Ⅱ
200mL蒸馏水十2滴浓
⑤ 16 68 10 4.9
HSO
2 4200mL蒸馏水+3滴浓
⑥ 16 52 10 4.9
HSO
2 4
200mL蒸馏水十
⑦ 10 3.0 10 4.9
0.8gNaOH
.
Ⅲ 200mL蒸馏水+1
⑧ x 2.6 10 4.9
6gNaOH
.
200mL蒸馏水+
⑨ 1ū 2.0 10 5 0
3.2gNaOH
【解释与结论】
(1)电解水的化学方程式为___________。
(2)与电源正极相连的玻璃管内产生的气体是___________。
的
(3)Ⅲ组实验⑧中 x=___________。
(4)对比实验②⑦,可得出的结论是___________。
(5)Ⅱ组实验的目的是___________。
(6)通过本实验得出,影响电解水反应快慢的因素有___________。
【反思与评价】
(7)表中部分数据氢气与氧气的体积比略大于 ,从物质性质角度分析可能的原因是___________。
【实际应用定量分析】
39. 封存 是实现碳中和的途径之一、矿物质碳化封存反应之一是氧化镁与二氧化碳反应生成碳酸镁,
该反应的化学方程式为 。若用此方法封存22 ,计算需要氧化镁的质量(写出
计算过程及结果)。