文档内容
热点强化 12 化学反应历程、机理的分析应用
1.大多数的化学反应不能一步完成,在微观上是分几步完成的,每一步反应都叫一个基元
反应。
如反应:HO+2Br-+2H+===Br +2HO,通过大量实验提出它们微观过程如下:
2 2 2 2
(1)H++HOHO;
2 2 3
(2)H O+Br-===HO+HOBr;
3 2
(3)HOBr+H++Br-===HO+Br 。
2 2
2.基元反应过渡状态理论
基元反应过渡状态理论认为,基元反应在从反应物到生成物的变化过程中要经历一个中间状
态,这个状态称为过渡态。
AB+C―→[A…B…C]―→A+BC
反应物 过渡态 生成物
过渡态是处在反应过程中具有最高能量的一种分子构型,过渡态能量与反应物的平均能量的
差值相当于活化能[活化能(能垒)越高,此步基元反应速率越慢]。例如,一溴甲烷与NaOH
溶液反应的过程可以表示为CHBr+OH-―→[Br…CH…OH]―→Br-+CHOH
3 3 3
3.活化能与反应机理
使用催化剂,可以改变活化能,改变反应机理,在反应机理中每一步反应的活化能不同,且
均比总反应的活化能低,故一般使用催化剂可以降低反应活化能,加快反应速率,如图所示:
E 为总反应的活化能,E、E 为使用催化剂反应机理中各步的活化能。
1 2 3
1.已知反应2NO(g)+2H(g)N(g)+2HO(g)
2 2 2
ΔH=-752 kJ·mol-1的反应机理如下:
①2NO(g)NO(g) (快)
2 2②NO(g)+H(g)NO(g)+HO(g) (慢)
2 2 2 2 2
③NO(g)+H(g)N(g)+HO(g) (快)
2 2 2 2
下列有关说法错误的是( )
A.①的逆反应速率大于②的正反应速率
B.②中NO 与H 的碰撞仅部分有效
2 2 2
C.NO 和NO是该反应的催化剂
2 2 2
D.总反应中逆反应的活化能比正反应的活化能大
答案 C
解析 ①为快反应,说明正反应的活化能和逆反应的活化能都较小,反应更容易发生;②为
慢反应,说明正反应的活化能和逆反应的活化能都较大,②中正反应的活化能大于①中逆反
应的活化能,因此①的逆反应速率大于②的正反应速率,A项正确;②为慢反应,反应慢说
明反应的活化能大,物质微粒发生碰撞时,许多碰撞都不能发生化学反应,因此碰撞仅部分
有效,B项正确;反应过程中NO 和NO是中间产物,不是催化剂,C项错误;总反应为
2 2 2
放热反应,则总反应中逆反应的活化能比正反应的活化能大,D项正确。
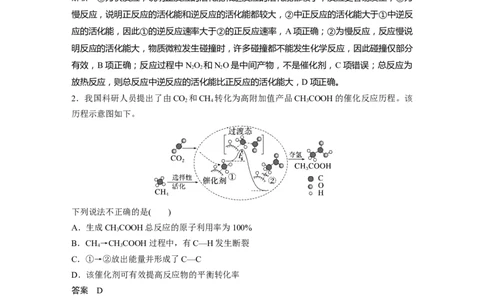
2.我国科研人员提出了由CO 和CH 转化为高附加值产品CHCOOH的催化反应历程。该
2 4 3
历程示意图如下。
下列说法不正确的是( )
A.生成CHCOOH总反应的原子利用率为100%
3
B.CH→CHCOOH过程中,有C—H发生断裂
4 3
C.①→②放出能量并形成了C—C
D.该催化剂可有效提高反应物的平衡转化率
答案 D
解析 根据图示 CH 与 CO 在催化剂存在时生成 CHCOOH,总反应为 CH +
4 2 3 4
CO――――→CHCOOH,只有CHCOOH一种生成物,原子利用率为 100%,A项正确;CH
2 3 3 4
选择性活化变为①过程中,有1个C—H断裂,B项正确;根据图示,①的总能量高于②的
总能量,①→②放出能量,对比①和②,①→②形成了C—C,C项正确;催化剂只影响化
学反应速率,不影响化学平衡,不能提高反应物的平衡转化率,D项错误。
3.(2022·哈尔滨质检)已知:2HO(l)===2H(g)+O(g) ΔH=+571.0 kJ·mol-1。以太阳能为
2 2 2
热源分解Fe O,经热化学铁氧化合物循环分解水制H 的过程如下:
3 4 2过程Ⅰ:2Fe O(s)===6FeO(s)+O(g) ΔH=+313.2 kJ·mol-1
3 4 2
过程Ⅱ:……
下列说法不正确的是( )
A.过程Ⅰ中每消耗232 g Fe O 转移2 mol电子
3 4
B.过程Ⅱ的热化学方程式为3FeO(s)+HO(l)===H(g)+Fe O(s) ΔH=+128.9 kJ·mol-1
2 2 3 4
C.过程Ⅰ、Ⅱ中能量转化的形式依次是太阳能→化学能→热能
D.铁氧化合物循环制H 具有成本低、产物易分离等优点
2
答案 C
解析 过程Ⅰ中每消耗232 g Fe O 反应生成0.5 mol O ,转移电子0.5×4 mol=2 mol,故A
3 4 2
正确;由盖斯定律可知,总反应×-过程Ⅰ反应×得过程Ⅱ反应及焓变,故B正确;过程
Ⅰ和过程Ⅱ都是吸热反应,过程Ⅰ是将光能转化为热能,热能转化为化学能,过程Ⅱ中能量
转化的形式还是热能转化为化学能,故C错误;铁氧化合物循环制H 以太阳能为热源分解
2
Fe O,以水和Fe O 为原料,具有成本低的优点,氢气和氧气分步生成,具有产物易分离的
3 4 3 4
优点,故D正确。
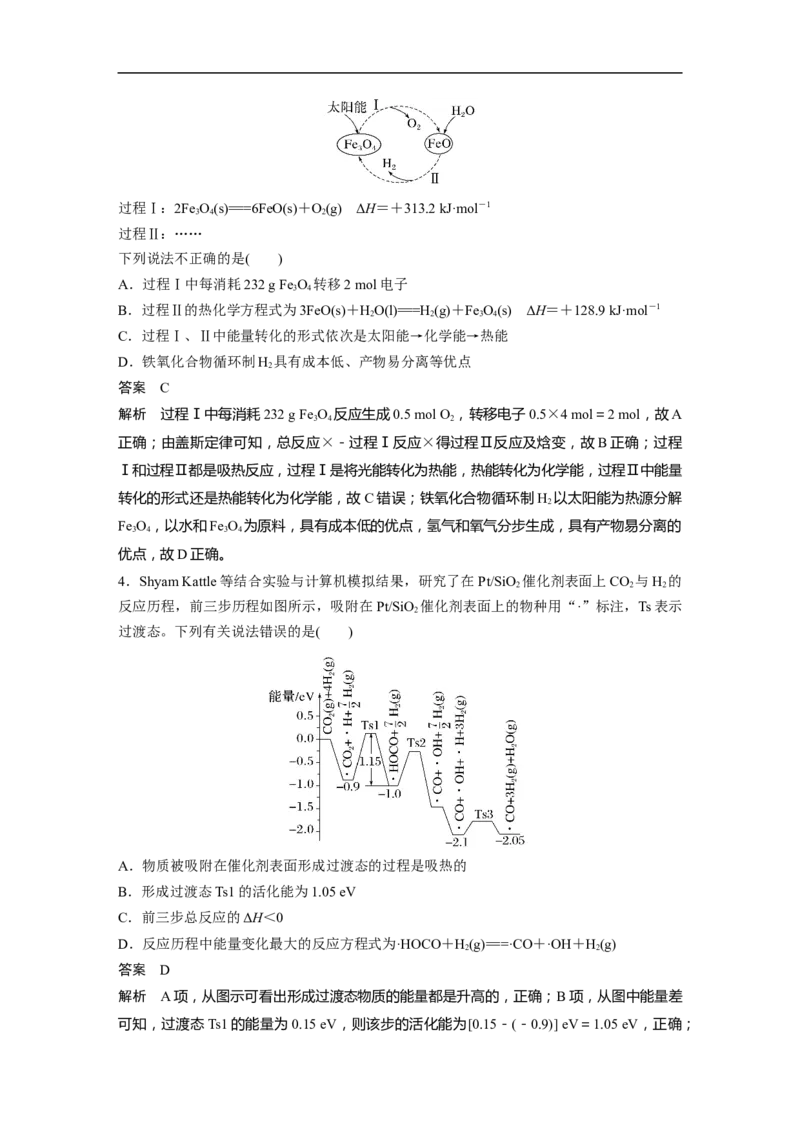
4.Shyam Kattle等结合实验与计算机模拟结果,研究了在Pt/SiO 催化剂表面上CO 与H 的
2 2 2
反应历程,前三步历程如图所示,吸附在Pt/SiO 催化剂表面上的物种用“·”标注,Ts表示
2
过渡态。下列有关说法错误的是( )
A.物质被吸附在催化剂表面形成过渡态的过程是吸热的
B.形成过渡态Ts1的活化能为1.05 eV
C.前三步总反应的ΔH<0
D.反应历程中能量变化最大的反应方程式为·HOCO+H(g)===·CO+·OH+H(g)
2 2
答案 D
解析 A项,从图示可看出形成过渡态物质的能量都是升高的,正确;B项,从图中能量差
可知,过渡态Ts1的能量为0.15 eV,则该步的活化能为[0.15-(-0.9)] eV=1.05 eV,正确;D项,前三步中能量变化最大的是第二步,该步骤分两步形成稳定的微粒,反应方程式为
·HOCO+H(g)===·CO+·OH+·H+3H(g),错误。
2 2
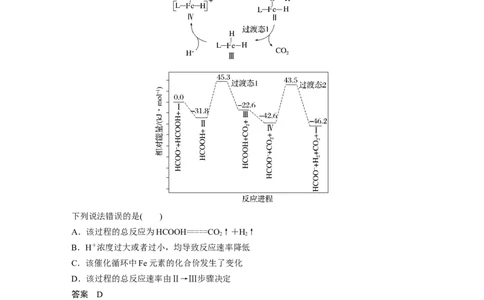
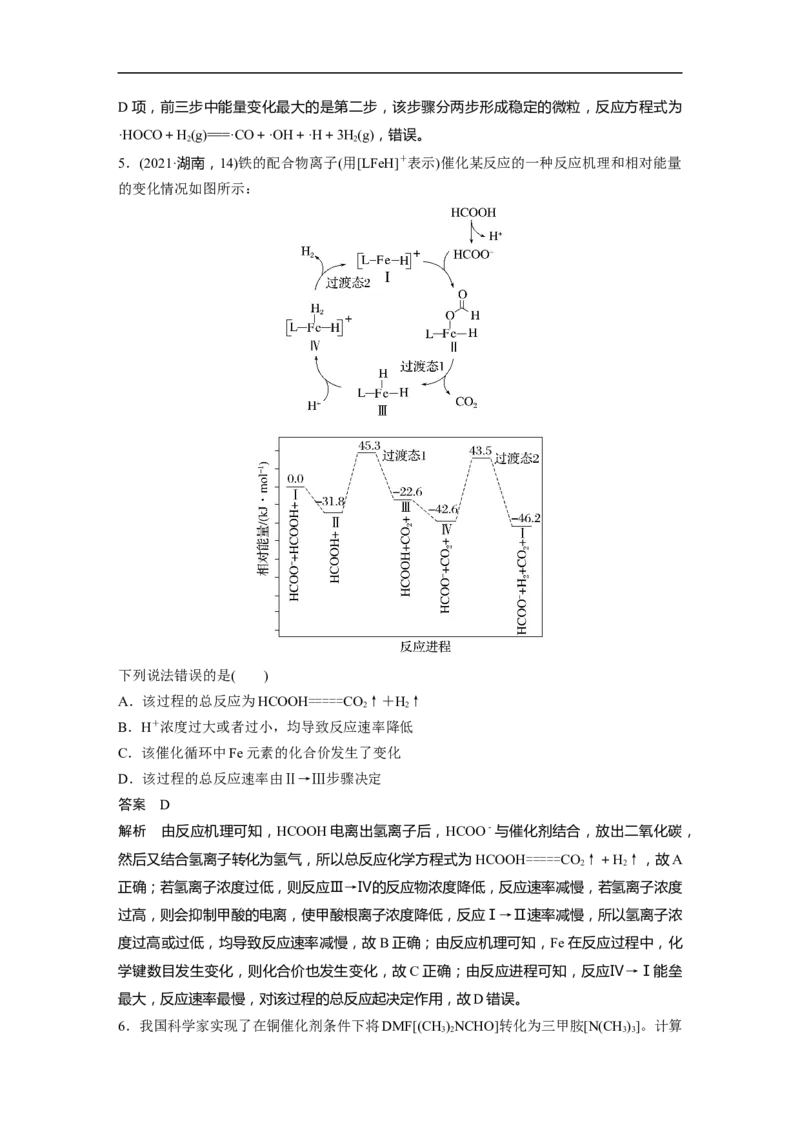
5.(2021·湖南,14)铁的配合物离子(用[LFeH]+表示)催化某反应的一种反应机理和相对能量
的变化情况如图所示:
下列说法错误的是( )
A.该过程的总反应为HCOOH=====CO↑+H↑
2 2
B.H+浓度过大或者过小,均导致反应速率降低
C.该催化循环中Fe元素的化合价发生了变化
D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定
答案 D
解析 由反应机理可知,HCOOH电离出氢离子后,HCOO-与催化剂结合,放出二氧化碳,
然后又结合氢离子转化为氢气,所以总反应化学方程式为HCOOH=====CO↑+H↑,故A
2 2
正确;若氢离子浓度过低,则反应Ⅲ→Ⅳ的反应物浓度降低,反应速率减慢,若氢离子浓度
过高,则会抑制甲酸的电离,使甲酸根离子浓度降低,反应Ⅰ→Ⅱ速率减慢,所以氢离子浓
度过高或过低,均导致反应速率减慢,故B正确;由反应机理可知,Fe在反应过程中,化
学键数目发生变化,则化合价也发生变化,故C正确;由反应进程可知,反应Ⅳ→Ⅰ能垒
最大,反应速率最慢,对该过程的总反应起决定作用,故D错误。
6.我国科学家实现了在铜催化剂条件下将DMF[(CH )NCHO]转化为三甲胺[N(CH )]。计算
3 2 3 3机模拟单个DMF分子在铜催化剂表面的反应历程如图所示,下列说法正确的是( )
A.该历程中最小能垒的化学方程式为 (CH)NCH OH*===(CH)NCH +OH*
3 2 2 3 2 2
B.该历程中最大能垒(活化能)为2.16 eV
C.该反应的热化学方程式为(CH)NCHO(g)+2H(g)===N(CH )(g)+HO(g) ΔH=
3 2 2 3 3 2
-1.02 eV·mol-1
D.增大压强或升高温度均能加快反应速率,并增大DMF的平衡转化率
答案 A
解析 从图中可以看出,在正向进行的三个吸热反应中,其能垒分别为[-1.23-(-2.16)]eV
=0.93 eV、[-1.55-(-1.77)]eV=0.22 eV、[-1.02-(-2.21)]eV=1.19 eV。从以上分析知,
该历程中最小能垒为0.22 eV,是由(CH)NCH OH*转化为(CH)NCH 的反应,化学方程式
3 2 2 3 2 2
为 (CH)NCH OH*===(CH)NCH +OH*,A正确;该历程中最大能垒(活化能)为1.19 eV,
3 2 2 3 2 2
B 不正确;该反应的总反应是由(CH)NCHO(g)转化为 N(CH )(g),但 1.02 eV 为单个
3 2 3 3
(CH)NCHO(g)反应时放出的热量,所以热化学方程式为(CH)NCHO(g)+2H(g)===
3 2 3 2 2
N(CH )(g)+HO(g) ΔH=-1.02N eV·mol-1,C不正确;增大压强或升高温度均能加快反
3 3 2 A
应速率,但升高温度平衡逆向移动,不能增大DMF的平衡转化率,D不正确。
7.[2019·全国卷Ⅰ,28(3)]我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上
水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。
可知水煤气变换的ΔH________0(填“大于”“等于”或“小于”)。该历程中最大能垒(活
化 能 )E = ________eV , 写 出 该 步 骤 的 化 学 方 程 式 :
正
____________________________________。
答案 小于 2.02 COOH*+H*+HO*===COOH*+2H*+OH*(或HO*===H*+OH*)
2 2
解析 观察始态物质的相对能量与终态物质的相对能量知,终态物质相对能量低于始态物质
相对能量,说明该反应是放热反应,ΔH小于0。过渡态物质相对能量与始态物质相对能量相差越大,活化能越大,由题图知,最大活化能E =1.86 eV-(-0.16 eV)=2.02 eV,该步
正
起始物质为COOH*+H*+HO*,产物为COOH*+2H*+OH*。
2