文档内容
课时检测(六十六) 羧酸及其衍生物
1.深海鱼油是从深海鱼类动物体内提炼出的含不饱和脂肪酸的油脂,具有降血脂等作用。下列关
于深海鱼油和植物油的说法错误的是( )
A.深海鱼油不稳定,容易被氧化
B.深海鱼油兼有酯和烯烃的一些化学性质
C.植物油可以用于生产氢化植物油
D.植物油不能使酸性高锰酸钾溶液褪色
2.等物质的量浓度的下列稀溶液:
①乙醇 ②苯酚 ③碳酸 ④乙酸,它们的pH由大到小排列正确的是( )
A.①②③④ B.③①②④ C.④②③① D.①③②④
3.实验室提供的玻璃仪器有圆底烧瓶、试管、导管、烧杯、酒精灯、量筒、胶头滴管,选用上述仪器
(非玻璃仪器任选)不能完成的实验是( )
A.由乙醇制取乙酸乙酯
B.由乙醇制取乙烯
C.由溴乙烷制取乙醇
D.由苯酚制取2,4,6三溴苯酚
4.(2023·全国新课标卷)光学性能优良的高分子材料聚碳酸异山梨醇酯可由如下反应制备。
下列说法错误的是( )
A.该高分子材料可降解
B.异山梨醇分子中有3个手性碳
C.反应式中化合物X为甲醇
D.该聚合反应为缩聚反应
5.卡莫氟具有抑制病毒复制的效果,其结构简式如图所示。下列关于卡莫氟的说法错误的是( )
A.分子式为C H ONF
11 16 3 3
B.分子中含有的官能团有碳碳双键、酰胺键和氟原子
C.该物质既能发生加成反应又能发生取代反应
D.1 mol该物质与足量NaOH溶液反应时消耗3 mol NaOH
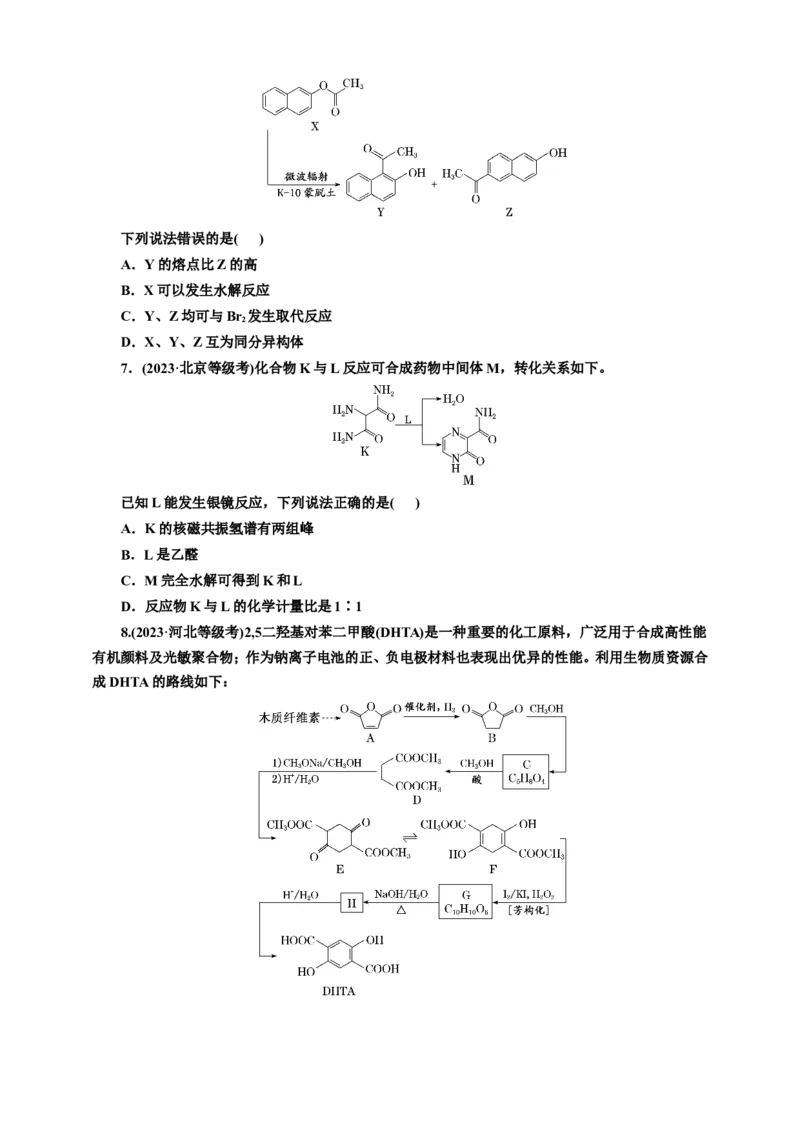
6.(2023·河北等级考)在K10蒙脱土催化下,微波辐射可促进化合物X的重排反应,如下图所示:下列说法错误的是( )
A.Y的熔点比Z的高
B.X可以发生水解反应
C.Y、Z均可与Br 发生取代反应
2
D.X、Y、Z互为同分异构体
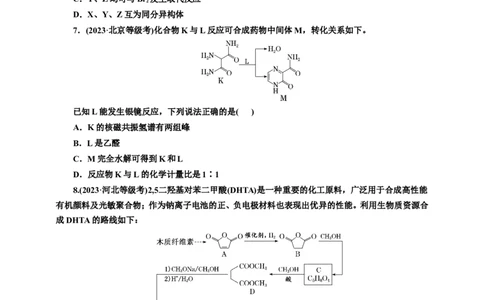
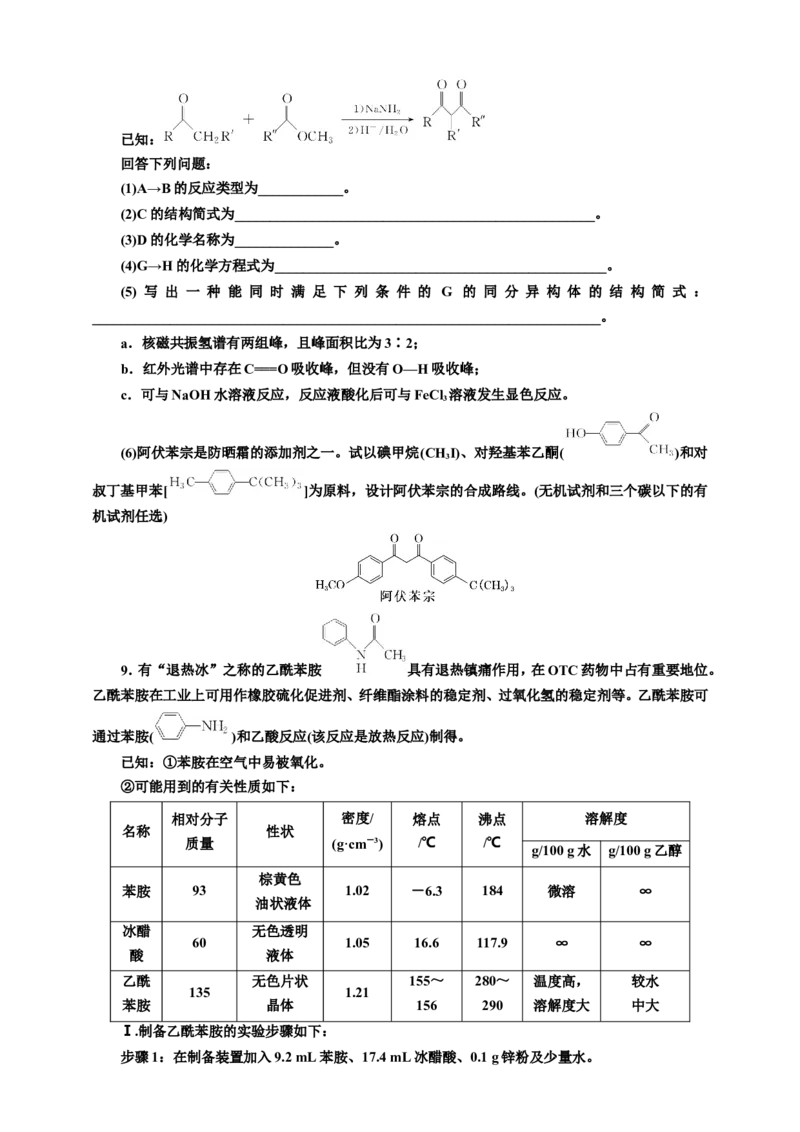
7.(2023·北京等级考)化合物K与L反应可合成药物中间体M,转化关系如下。
已知L能发生银镜反应,下列说法正确的是( )
A.K的核磁共振氢谱有两组峰
B.L是乙醛
C.M完全水解可得到K和L
D.反应物K与L的化学计量比是1∶1
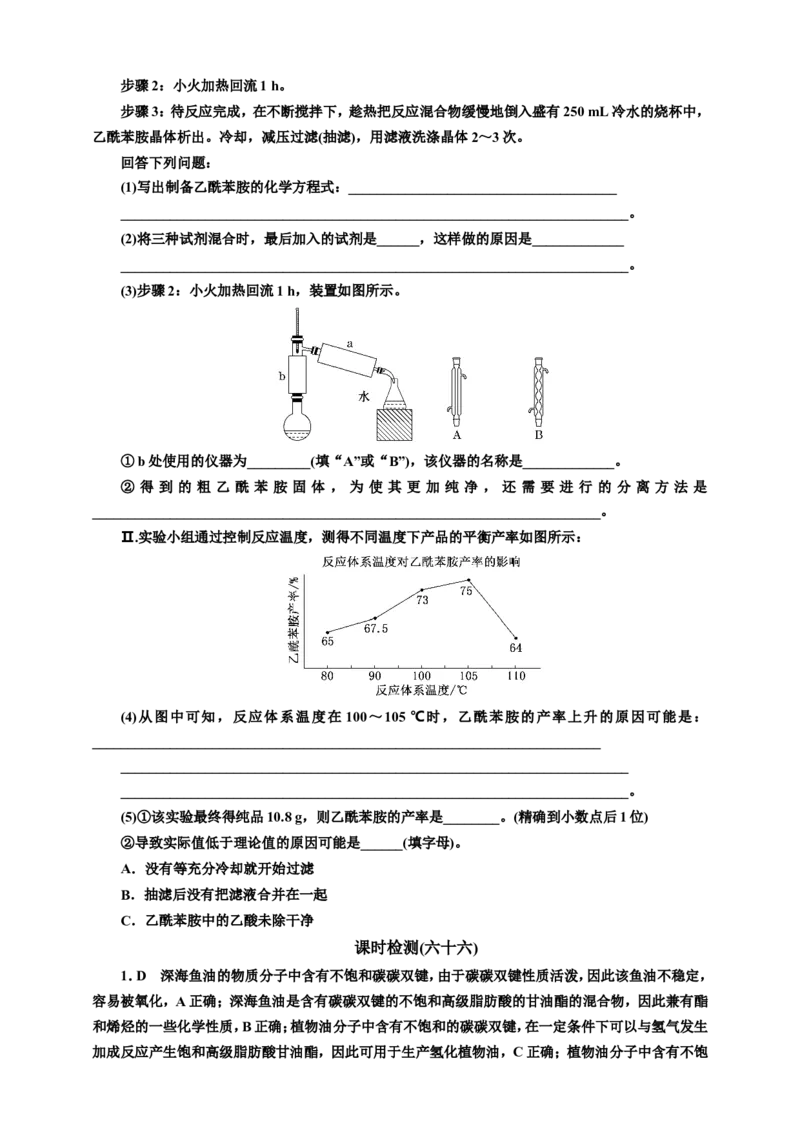
8.(2023·河北等级考)2,5二羟基对苯二甲酸(DHTA)是一种重要的化工原料,广泛用于合成高性能
有机颜料及光敏聚合物;作为钠离子电池的正、负电极材料也表现出优异的性能。利用生物质资源合
成DHTA的路线如下:已知:
回答下列问题:
(1)A→B的反应类型为____________。
(2)C的结构简式为___________________________________________________。
(3)D的化学名称为______________。
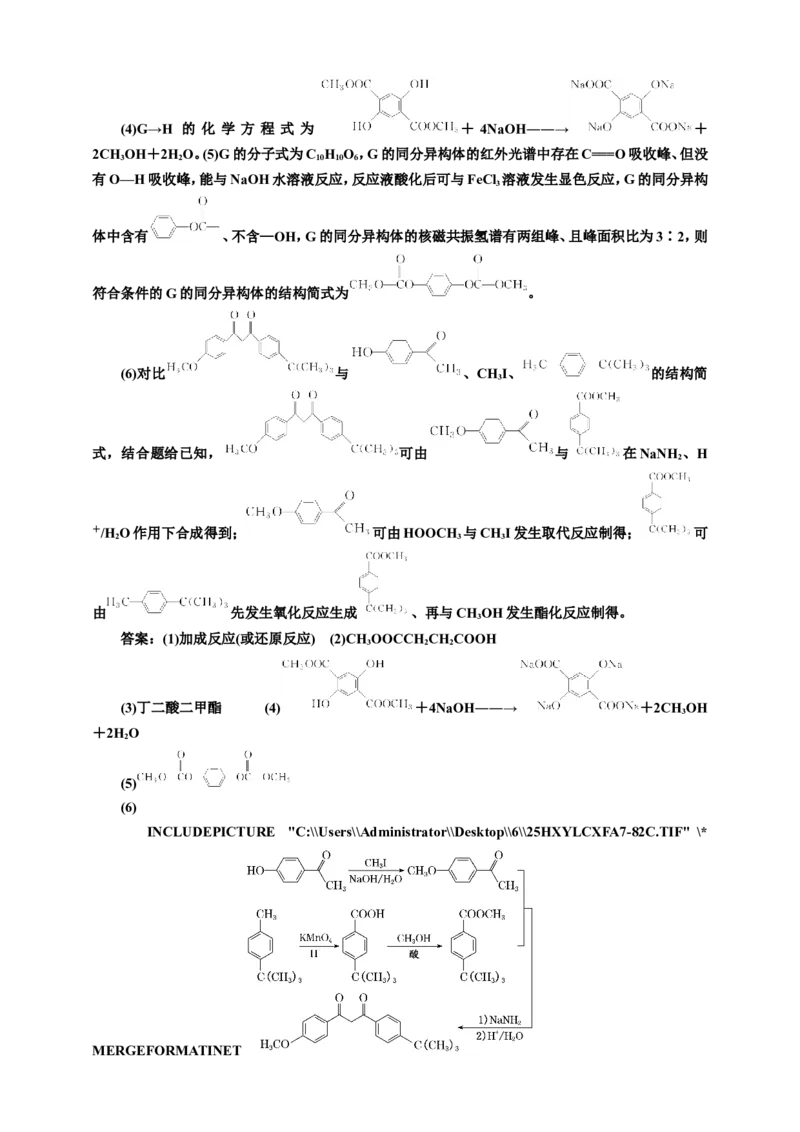
(4)G→H的化学方程式为_______________________________________________。
(5) 写 出 一 种 能 同 时 满 足 下 列 条 件 的 G 的 同 分 异 构 体 的 结 构 简 式 :
________________________________________________________________________。
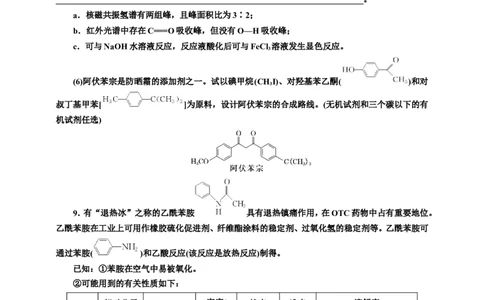
a.核磁共振氢谱有两组峰,且峰面积比为3∶2;
b.红外光谱中存在C===O吸收峰,但没有O—H吸收峰;
c.可与NaOH水溶液反应,反应液酸化后可与FeCl 溶液发生显色反应。
3
(6)阿伏苯宗是防晒霜的添加剂之一。试以碘甲烷(CHI)、对羟基苯乙酮( )和对
3
叔丁基甲苯[ ]为原料,设计阿伏苯宗的合成路线。(无机试剂和三个碳以下的有
机试剂任选)
9.有“退热冰”之称的乙酰苯胺 具有退热镇痛作用,在OTC药物中占有重要地位。
乙酰苯胺在工业上可用作橡胶硫化促进剂、纤维酯涂料的稳定剂、过氧化氢的稳定剂等。乙酰苯胺可
通过苯胺( )和乙酸反应(该反应是放热反应)制得。
已知:①苯胺在空气中易被氧化。
②可能用到的有关性质如下:
相对分子 密度/ 熔点 沸点 溶解度
名称 性状
质量 (g·cm-3) /℃ /℃
g/100 g水 g/100 g乙醇
棕黄色
苯胺 93 1.02 -6.3 184 微溶 ∞
油状液体
冰醋 无色透明
60 1.05 16.6 117.9 ∞ ∞
酸 液体
乙酰 无色片状 155~ 280~ 温度高, 较水
135 1.21
苯胺 晶体 156 290 溶解度大 中大
Ⅰ.制备乙酰苯胺的实验步骤如下:
步骤1:在制备装置加入9.2 mL苯胺、17.4 mL冰醋酸、0.1 g锌粉及少量水。步骤2:小火加热回流1 h。
步骤3:待反应完成,在不断搅拌下,趁热把反应混合物缓慢地倒入盛有250 mL冷水的烧杯中,
乙酰苯胺晶体析出。冷却,减压过滤(抽滤),用滤液洗涤晶体2~3次。
回答下列问题:
(1)写出制备乙酰苯胺的化学方程式:______________________________________
________________________________________________________________________。
(2)将三种试剂混合时,最后加入的试剂是______,这样做的原因是_____________
________________________________________________________________________。
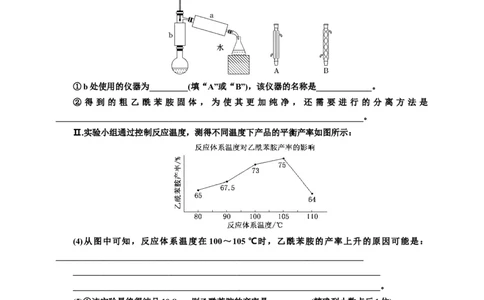
(3)步骤2:小火加热回流1 h,装置如图所示。
①b处使用的仪器为_________(填“A”或“B”),该仪器的名称是_____________。
② 得 到 的 粗 乙 酰 苯 胺 固 体 , 为 使 其 更 加 纯 净 , 还 需 要 进 行 的 分 离 方 法 是
________________________________________________________________________。
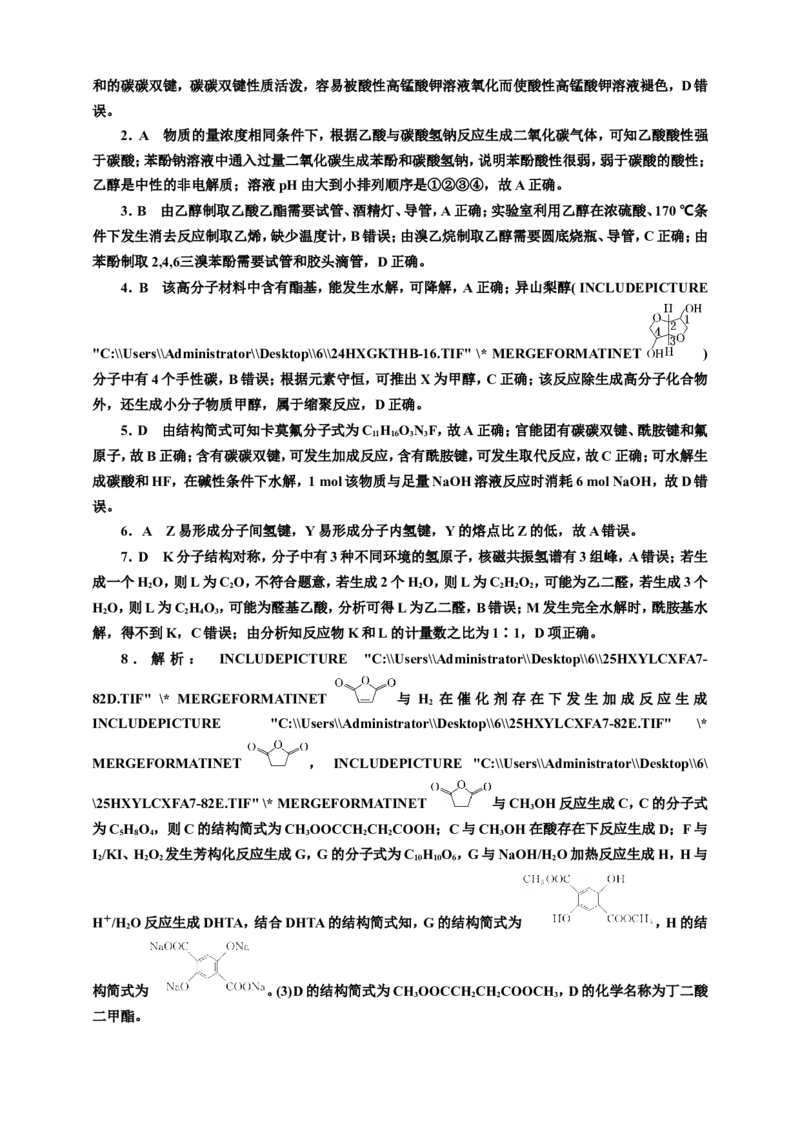
Ⅱ.实验小组通过控制反应温度,测得不同温度下产品的平衡产率如图所示:
(4)从图中可知,反应体系温度在 100~105 ℃时,乙酰苯胺的产率上升的原因可能是:
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(5)①该实验最终得纯品10.8 g,则乙酰苯胺的产率是________。(精确到小数点后1位)
②导致实际值低于理论值的原因可能是______(填字母)。
A.没有等充分冷却就开始过滤
B.抽滤后没有把滤液合并在一起
C.乙酰苯胺中的乙酸未除干净
课时检测(六十六)
1.D 深海鱼油的物质分子中含有不饱和碳碳双键,由于碳碳双键性质活泼,因此该鱼油不稳定,
容易被氧化,A正确;深海鱼油是含有碳碳双键的不饱和高级脂肪酸的甘油酯的混合物,因此兼有酯
和烯烃的一些化学性质,B正确;植物油分子中含有不饱和的碳碳双键,在一定条件下可以与氢气发生
加成反应产生饱和高级脂肪酸甘油酯,因此可用于生产氢化植物油,C正确;植物油分子中含有不饱和的碳碳双键,碳碳双键性质活泼,容易被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,D错
误。
2.A 物质的量浓度相同条件下,根据乙酸与碳酸氢钠反应生成二氧化碳气体,可知乙酸酸性强
于碳酸;苯酚钠溶液中通入过量二氧化碳生成苯酚和碳酸氢钠,说明苯酚酸性很弱,弱于碳酸的酸性;
乙醇是中性的非电解质;溶液pH由大到小排列顺序是①②③④,故A正确。
3.B 由乙醇制取乙酸乙酯需要试管、酒精灯、导管,A正确;实验室利用乙醇在浓硫酸、170 ℃条
件下发生消去反应制取乙烯,缺少温度计,B错误;由溴乙烷制取乙醇需要圆底烧瓶、导管,C正确;由
苯酚制取2,4,6三溴苯酚需要试管和胶头滴管,D正确。
4.B 该高分子材料中含有酯基,能发生水解,可降解,A正确;异山梨醇( INCLUDEPICTURE
"C:\\Users\\Administrator\\Desktop\\6\\24HXGKTHB-16.TIF" \* MERGEFORMATINET )
分子中有4个手性碳,B错误;根据元素守恒,可推出X为甲醇,C正确;该反应除生成高分子化合物
外,还生成小分子物质甲醇,属于缩聚反应,D正确。
5.D 由结构简式可知卡莫氟分子式为C H ONF,故A正确;官能团有碳碳双键、酰胺键和氟
11 16 3 3
原子,故B正确;含有碳碳双键,可发生加成反应,含有酰胺键,可发生取代反应,故C正确;可水解生
成碳酸和HF,在碱性条件下水解,1 mol该物质与足量NaOH溶液反应时消耗6 mol NaOH,故D错
误。
6.A Z易形成分子间氢键,Y易形成分子内氢键,Y的熔点比Z的低,故A错误。
7.D K分子结构对称,分子中有3种不同环境的氢原子,核磁共振氢谱有3组峰,A错误;若生
成一个HO,则L为CO,不符合题意,若生成2个HO,则L为CHO,可能为乙二醛,若生成3个
2 2 2 2 2 2
HO,则L为CHO,可能为醛基乙酸,分析可得L为乙二醛,B错误;M发生完全水解时,酰胺基水
2 2 4 3
解,得不到K,C错误;由分析知反应物K和L的计量数之比为1∶1,D项正确。
8 . 解 析 : INCLUDEPICTURE "C:\\Users\\Administrator\\Desktop\\6\\25HXYLCXFA7-
82D.TIF" \* MERGEFORMATINET 与 H 在 催 化 剂 存 在 下 发 生 加 成 反 应 生 成
2
INCLUDEPICTURE "C:\\Users\\Administrator\\Desktop\\6\\25HXYLCXFA7-82E.TIF" \*
MERGEFORMATINET , INCLUDEPICTURE "C:\\Users\\Administrator\\Desktop\\6\
\25HXYLCXFA7-82E.TIF" \* MERGEFORMATINET 与CH OH反应生成C,C的分子式
3
为CHO,则C的结构简式为CH OOCCH CH COOH;C与CH OH在酸存在下反应生成D;F与
5 8 4 3 2 2 3
I/KI、HO 发生芳构化反应生成G,G的分子式为C H O,G与NaOH/H O加热反应生成H,H与
2 2 2 10 10 6 2
H+/HO反应生成DHTA,结合DHTA的结构简式知,G的结构简式为 ,H的结
2
构简式为 。(3)D的结构简式为CH OOCCH CH COOCH ,D的化学名称为丁二酸
3 2 2 3
二甲酯。(4)G→H 的 化 学 方 程 式 为 + 4NaOH――→ +
2CH OH+2HO。(5)G的分子式为C H O,G的同分异构体的红外光谱中存在C===O吸收峰、但没
3 2 10 10 6
有O—H吸收峰,能与NaOH水溶液反应,反应液酸化后可与FeCl 溶液发生显色反应,G的同分异构
3
体中含有 、不含—OH,G的同分异构体的核磁共振氢谱有两组峰、且峰面积比为3∶2,则
符合条件的G的同分异构体的结构简式为 。
(6)对比 与 、CH I、 的结构简
3
式,结合题给已知, 可由 与 在NaNH 、H
2
+/HO作用下合成得到; 可由HOOCH 与CH I发生取代反应制得; 可
2 3 3
由 先发生氧化反应生成 、再与CH OH发生酯化反应制得。
3
答案:(1)加成反应(或还原反应) (2)CHOOCCH CH COOH
3 2 2
(3)丁二酸二甲酯 (4) +4NaOH――→ +2CH OH
3
+2HO
2
(5)
(6)
INCLUDEPICTURE "C:\\Users\\Administrator\\Desktop\\6\\25HXYLCXFA7-82C.TIF" \*
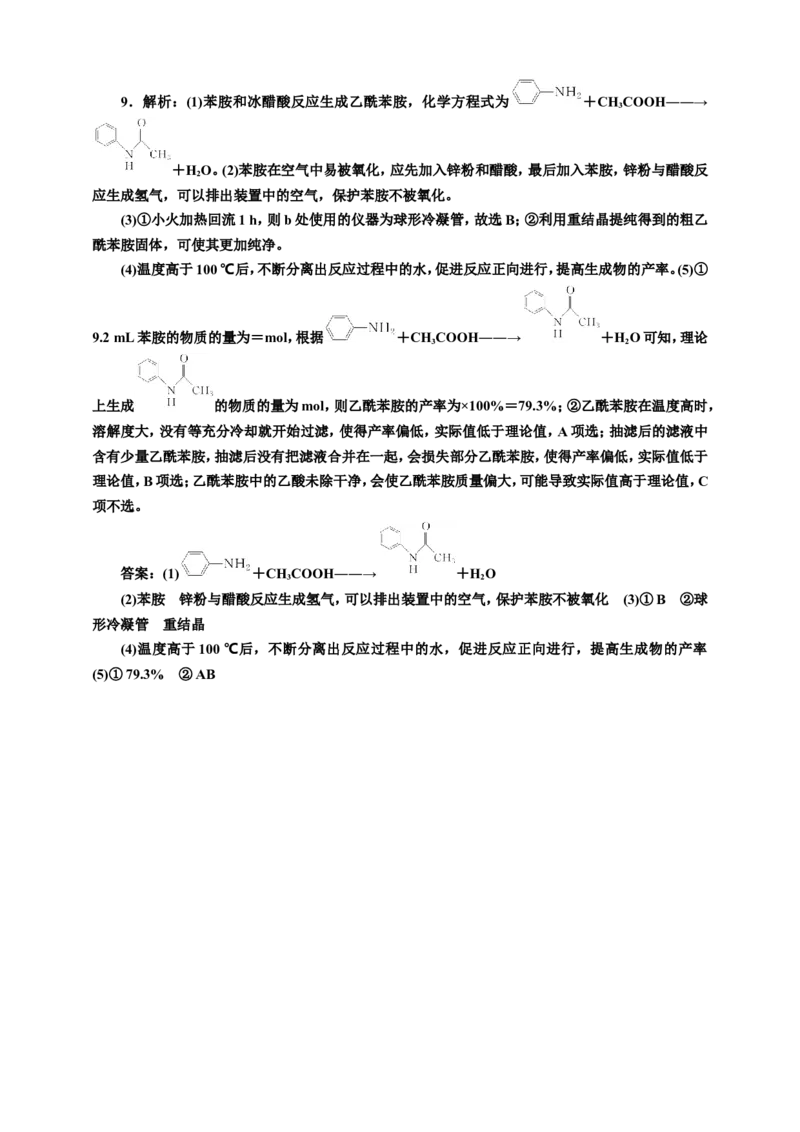
MERGEFORMATINET9.解析:(1)苯胺和冰醋酸反应生成乙酰苯胺,化学方程式为 +CH COOH――→
3
+HO。(2)苯胺在空气中易被氧化,应先加入锌粉和醋酸,最后加入苯胺,锌粉与醋酸反
2
应生成氢气,可以排出装置中的空气,保护苯胺不被氧化。
(3)①小火加热回流1 h,则b处使用的仪器为球形冷凝管,故选B;②利用重结晶提纯得到的粗乙
酰苯胺固体,可使其更加纯净。
(4)温度高于100 ℃后,不断分离出反应过程中的水,促进反应正向进行,提高生成物的产率。(5)①
9.2 mL 苯胺的物质的量为=mol,根据 +CH COOH――→ +HO可知,理论
3 2
上生成 的物质的量为mol,则乙酰苯胺的产率为×100%=79.3%;②乙酰苯胺在温度高时,
溶解度大,没有等充分冷却就开始过滤,使得产率偏低,实际值低于理论值,A项选;抽滤后的滤液中
含有少量乙酰苯胺,抽滤后没有把滤液合并在一起,会损失部分乙酰苯胺,使得产率偏低,实际值低于
理论值,B项选;乙酰苯胺中的乙酸未除干净,会使乙酰苯胺质量偏大,可能导致实际值高于理论值,C
项不选。
答案:(1) +CH COOH――→ +HO
3 2
(2)苯胺 锌粉与醋酸反应生成氢气,可以排出装置中的空气,保护苯胺不被氧化 (3)①B ②球
形冷凝管 重结晶
(4)温度高于100 ℃后,不断分离出反应过程中的水,促进反应正向进行,提高生成物的产率
(5)①79.3% ②AB