文档内容
一、选择题
1.(2019·大连第二十四中学高三质检)下列说法正确的一组是( )
①不溶于水的盐都是弱电解质
②可溶于水的盐都是强电解质
③0.5 mol·L-1一元酸溶液H+浓度为0.5 mol·L-1
④强酸溶液中的H+浓度一定大于弱酸溶液中的H+浓度
⑤电解质溶液导电的原因是溶液中有自由移动的阴、阳离子
⑥熔融的电解质都能导电
A.①③⑤⑥ B.②④⑤⑥
C.只有⑤ D.只有⑥
解析:选C。①电解质的强弱与溶解性无关,不溶于水的盐可能是强电解质,如硫酸钡,
故①错误;②电解质的强弱与溶解性无关,可溶于水的盐可能是弱电解质,如醋酸铅,故②错
误;③0.5 mol·L-1一元酸溶液H+浓度不一定为0.5 mol·L-1,如醋酸,故③错误;④强酸溶液
中的H+浓度不一定大于弱酸溶液中的H+浓度,H+浓度与酸的浓度、分子中氢离子的个数以
及电离程度有关,与电解质的强弱无关,故④错误;⑤电解质溶液导电的原因是溶液中有自
由移动的阴、阳离子,故⑤正确;⑥酸在熔融状态时均不导电,只有溶于水时才导电,故⑥错
误。
2.下列说法中正确的是( )
A.三氧化硫的水溶液能导电,所以三氧化硫是电解质
B.自由移动离子数目多的电解质溶液导电能力一定强
C.NaHSO 在水溶液及熔融状态下均可电离出Na+、H+、SO
4
D.NH 属于非电解质,但其水溶液能够导电
3
解析:选D。三氧化硫本身不能电离出离子,SO 是非电解质,A错误;离子数目多的溶液
3
中,离子浓度不一定大,离子所带电荷数不一定多,其导电能力不一定强,B错误;NaHSO 在
4
熔融状态下只能电离出Na+、HSO,C错误;NH 是非电解质,但其溶于水后可形成电解质
3
NH ·HO,溶液能导电,D正确。
3 2
3.(2019·高考江苏卷)下列指定反应的离子方程式正确的是( )
A.室温下用稀NaOH溶液吸收Cl:Cl+2OH-===ClO-+Cl-+HO
2 2 2
B.用铝粉和NaOH溶液反应制取少量H:Al+2OH-===AlO+H↑
2 2
C.室温下用稀HNO 溶解铜:Cu+2NO+2H+===Cu2++2NO ↑+HO
3 2 2
D.向NaSiO 溶液中滴加稀盐酸:NaSiO+2H+===H SiO↓+2Na+
2 3 2 3 2 3
解析:选A。A项,Cl 与NaOH反应生成NaCl、NaClO和HO,正确;B项,题给离子方程
2 2
式不符合电荷守恒与得失电子守恒,错误;C项,稀HNO 与Cu发生反应生成NO,错误;D
3
项,NaSiO 为可溶性的钠盐,应拆开,错误。
2 3
4.(2019·安徽皖江名校联考)摩尔盐[(NH )SO ·FeSO ·6HO]是分析化学中常用的还原剂,
4 2 4 4 2
常温下将其溶于水,下列有关该溶液的说法正确的是( )
A.通入少量Cl 后溶液中一定存在Fe2+、NH、Cl-、ClO-、SO
2
B.加入足量过氧化氢溶液发生反应为Fe2++2HO+4H+===Fe3++4HO
2 2 2
C.加入过量稀硝酸溶液发生反应为3Fe2++NO+4H+===3Fe3++NO↑+2HO
2
D.加入过量NaOH溶液,溶液中大量存在Na+、NH、SO、OH-
解析:选C。A.ClO-具有强氧化性,能将Fe2+氧化为Fe3+,故二者不能共存,错误;B.反应不符合电荷守恒和得失电子守恒,应该为2Fe2++HO+2H+===2Fe3++2HO,错误;C.加
2 2 2
入过量稀硝酸,稀硝酸具有氧化性,可将亚铁离子氧化为铁离子,根据电子和电荷守恒可得
3Fe2++NO+4H+===3Fe3++NO↑+2HO,正确;D.加入过量NaOH溶液,铵根离子与碱结
2
合生成弱电解质,不能共存,错误。
5.(2019·呼和浩特质量普查调研)下列解释事实的离子方程式正确的是( )
A.石灰水表面漂着的“白膜”可用醋酸溶解:CaCO +2H+===Ca2++CO↑+HO
3 2 2
B.NH HSO 溶液呈酸性的主要原因是NH+HONH ·H O+H+
4 4 2 3 2
C.盐碱地(含较多NaCl 、NaCO)中加入石膏,降低土壤的碱性:Ca2++CO===CaCO
2 3 3
↓
D.漂白粉溶液在空气中失效:Ca2++2ClO-+CO+HO===2HClO+CaCO ↓
2 2 3
解析:选D。石灰水表面漂着的“白膜”为碳酸钙,用醋酸溶解的离子方程式为CaCO
3
+2CHCOOH===2CH COO-+Ca2++HO+CO↑,A项错误;NH HSO 溶液呈酸性的主要
3 3 2 2 4 4
原因是NH HSO ===NH+H++SO, B项错误;盐碱地(含较多NaCl、NaCO)中加入石膏,
4 4 2 3
降低土壤的碱性,石膏微溶于水,反应的离子方程式为CaSO+CO===CaCO +SO,C项错误;
4 3
漂白粉溶液在空气中失效,是与空气中的二氧化碳反应,反应的离子方程式为Ca2++2ClO-
+CO+HO===2HClO+CaCO ↓,D项正确。
2 2 3
6.(2016·高考海南卷)下列反应可用离子方程式“H++OH-===H O”表示的是( )
2
A.NaHSO 溶液与Ba(OH) 溶液混合
4 2
B.NH Cl溶液与Ca(OH) 溶液混合
4 2
C.HNO 溶液与KOH溶液混合
3
D.NaHPO 溶液与NaOH溶液混合
2 4
解析:选C。A.NaHSO 溶液与Ba(OH) 溶液混合时,除了H+与OH-反应外,还有SO与
4 2
Ba2+反应生成BaSO 沉淀;B.NHCl溶液与Ca(OH) 溶液混合产生NH ·HO;C.HNO 溶液
4 4 2 3 2 3
与KOH溶液混合,为可溶性强酸与强碱反应只生成水的类型,符合该离子方程式;D.HPO不
能拆写成H+。
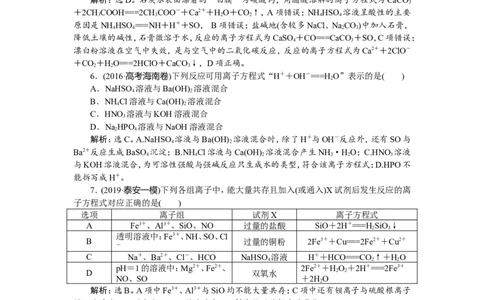
7.(2019·泰安一模)下列各组离子中,能大量共存且加入(或通入)X试剂后发生反应的离
子方程式对应正确的是( )
选项 离子组 试剂X 离子方程式
A Fe3+、Al3+、SiO、NO 过量的盐酸 SiO+2H+===H SiO↓
2 3
透明溶液中:Fe3+、NH、SO、Cl
B 过量的铜粉 2Fe3++Cu===2Fe2++Cu2+
-
C Na+、Ba2+、Cl-、HCO NaHSO 溶液 H++HCO===CO ↑+HO
4 2 2
pH=1的溶液中:Mg2+、Fe2+、 2Fe2++HO+2H+===2Fe3+
D 双氧水 2 2
NO、SO +2HO
2
解析:选B。A项中Fe3+、Al3+与SiO均不能大量共存;C项中还有钡离子与硫酸根离子
的沉淀反应;D项中在pH=1的溶液中,Fe2+会被硝酸根离子氧化。
8.(2019·晋豫省际大联考)下列解释事实的化学用语错误的是( )
A.盛放氢氧化钠溶液的试剂瓶不能用磨口玻璃塞:SiO+2OH-===SiO+HO
2 2
B.酸雨的pH小于5.6:CO+HOH COH++HCO
2 2 2 3
C.澄清石灰水中加入过量小苏打溶液出现浑浊:Ca2++2HCO+2OH-===CaCO ↓+
3
CO+2HO
2
D.在AlCl 溶液中加入过量氨水仍有浑浊:Al3++3NH ·H O===Al(OH) ↓+3NH
3 3 2 3
解析:选B。盛放氢氧化钠溶液的试剂瓶不能用磨口玻璃塞,是因为氢氧化钠会和玻璃
中的二氧化硅反应生成硅酸钠,A项正确;酸雨的pH小于5.6,是由大气中的SO 、NO 溶于
2 x
雨水造成的,B项错误;澄清石灰水中加入过量小苏打溶液,小苏打过量,以Ca(OH) 为标准
2书写离子方程式为Ca2++2HCO+2OH-===CaCO ↓+CO+2HO,C项正确;氨水与氯化铝
3 2
反应生成氢氧化铝,过量的氨水不会和氢氧化铝反应,所以在AlCl 溶液中加入过量氨水仍
3
有浑浊,D项正确。
9.(2019·湖南五市十校教研教改共同体联考)下列离子方程式正确的是( )
A.用惰性电极电解硫酸铜溶液:2Cu2++2HO=====2Cu+O↑+4H+
2 2
B.在强碱溶液中NaClO与Fe(OH) 反应生成NaFeO:3ClO-+2Fe(OH) ===2FeO+3Cl
3 2 4 3
-+HO+4H+
2
C.向NaAlO 溶液中通入过量CO 制取Al(OH) :2AlO+CO +3HO===2Al(OH) ↓+
2 2 3 2 2 3
CO
D.用浓盐酸酸化的KMnO 溶液氧化HC O :6H++5HC O +2MnO===10CO ↑+
4 2 2 4 2 2 4 2
2Mn2++8HO
2
解析:选A。用惰性电极电解硫酸铜溶液,反应的离子方程式为2Cu2++2HO=====2Cu
2
+O↑+4H+,A项正确;在强碱溶液中NaClO与Fe(OH) 反应生成NaFeO,反应的离子方
2 3 2 4
程式为3ClO-+2Fe(OH) +4OH-===2FeO+3Cl-+5HO,B项错误;向NaAlO 溶液中通入
3 2 2
过量CO 制取Al(OH) ,反应的离子方程式为AlO+CO+2HO===Al(OH) ↓+HCO,C项错
2 3 2 2 3
误;KMnO 具有强氧化性,会氧化浓盐酸,故不能用浓盐酸酸化KMnO 溶液,D项错误。
4 4
10.下列实验的反应原理用离子方程式表示正确的是( )
A.向明矾溶液中滴入氢氧化钡溶液使 SO恰好完全沉淀:2Ba2++3OH-+Al3++
2SO===2BaSO ↓+Al(OH) ↓
4 3
B.用高锰酸钾标准溶液滴定草酸:2MnO+16H++5C O===2Mn2++10CO↑+8HO
2 2 2
C.用白醋浸泡过的淀粉KI试纸检验加碘盐中的KIO :5I-+IO+6CHCOOH===3I +
3 3 2
3HO+6CHCOO-
2 3
D.在硬水中加入过量澄清石灰水除去 Mg(HCO ) :Mg2++2HCO+Ca2++2OH-
3 2
===MgCO↓+CaCO ↓+2HO
3 3 2
解析:选C。A项,SO恰好完全沉淀,则KAl(SO ) 与Ba(OH) 的物质的量之比为1∶2,
4 2 2
故反应应生成AlO,而不是Al(OH) ,错误;B项,草酸为弱酸,在离子方程式中应写化学式,
3
错误;C项,I-与IO在酸性条件下发生归中反应,正确;D项,氢氧化镁比碳酸镁更难溶,向
硬水中加入过量的氢氧化钙溶液,应生成氢氧化镁,离子方程式为Mg2++2HCO+2Ca2++
4OH-===Mg(OH) ↓+2CaCO ↓+2HO,错误。
2 3 2
二、非选择题
11.离子反应是中学化学中重要的反应类型。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在的有________(填序号)。
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)离子方程式是重要的化学用语。下列是有关离子方程式的一些错误观点,请在下列表
格中用相应的“离子方程式”否定这些观点。
①所有的离子方程式均可以表示一类反应
②酸碱中和反应均可表示为H++OH-
===H O
2
③离子方程式中凡是难溶性酸、碱、盐均要标
“↓”符号
(3)试列举出三种不同类别的物质(酸、碱、盐)之间的反应,它们对应的离子方程式都可
用“Ba2++SO===BaSO ↓”来表示,请写出有关反应的化学方程式(3个):
4
① ________________________________________________________________________
;
② ________________________________________________________________________;
③ ________________________________________________________________________
。
解析:(1)离子反应中一定有离子参与反应或有离子生成,因此一定有电解质(化合物)参
与反应或生成。
(2)①离子方程式不一定表示的是一类反应,如2CHCOOH+CaCO ===2CH COO-+
3 3 3
Ca2++HO+CO↑,该反应只表示醋酸和碳酸钙的反应;②有弱酸或弱碱参加或产生HO
2 2 2
以外不可拆分的产物的反应,不能用 H++OH-===H O 表示,如 CHCOOH+OH-
2 3
===CH COO-+HO;③离子方程式中,反应物若是难溶物,不需要标出沉淀符号,如CaCO
3 2 3
+2H+===Ca2++HO+CO↑。
2 2
(3)不同类别的物质(酸、碱、盐)之间的反应,它们对应的离子方程式都可用“Ba2++
SO===BaSO ↓”来表示,说明酸、碱和盐都是可溶性的,且反应后只有硫酸钡沉淀生成,没
4
有气体或弱电解质,如①氯化钡与硫酸的反应,反应的化学方程式:BaCl +
2
HSO ===BaSO ↓+2HCl,可用“Ba2++SO===BaSO ↓”来表示;②氢氧化钡与硫酸钠的
2 4 4 4
反应,反应的化学方程式:Ba(OH) +NaSO ===BaSO ↓+2NaOH,可用“Ba2++
2 2 4 4
SO===BaSO ↓”来表示;③硫酸氢钠与氯化钡反应,反应的化学方程式:NaHSO +
4 4
BaCl ===BaSO ↓+HCl+NaCl,可用“Ba2++SO===BaSO ↓”来表示。
2 4 4
答案:(1)③⑤
(2)①2CHCOOH+CaCO ===2CH COO-+Ca2++HO+CO↑ ②CHCOOH+OH-
3 3 3 2 2 3
===CH COO-+HO ③CaCO +2H+===Ca2++HO+CO↑(答案合理即可)
3 2 3 2 2
(3)①BaCl +HSO ===BaSO ↓+2HCl
2 2 4 4
②Ba(OH) +NaSO ===BaSO ↓+2NaOH
2 2 4 4
③NaHSO+BaCl ===BaSO ↓+HCl+NaCl(答案合理即可)
4 2 4
12.(2019·天津静海第一中学高三学业能力调研)请按要求书写下列离子方程式:
(1)复分解离子反应中,量变引起的变化。
①将NaHSO 溶液滴加到Ba(OH) 溶液中,当溶液恰好呈中性时,反应的离子方程式为
4 2
________________________________________________________________________
________________________________________________________________________。
②向Ba(HCO ) 溶液中滴入NaHSO 溶液,至沉淀完全,写出反应的离子方程式:
3 2 4
________________________________________________________________________
________________________________________________________________________。
在上述溶液中继续滴入NaHSO 溶液,此时离子方程式为_________________。
4
③ 0.2 mol·L-1的 NH Al(SO ) 溶液与 0.3 mol·L-1的 Ba(OH) 溶液等体积混合:
4 4 2 2
________________________________________________________________________
________________________________________________________________________。
(2)氧化还原反应中,反应物及量的变化。
向含有a mol FeBr 的溶液中,通入x mol Cl,若x=a,
2 2
________________________________________________________________________;
若x=4a,_________________________________________________________
________________________________________________________________________。
(3)特殊条件下离子反应方程式的书写。
①在碱性条件下,Cl 可将废水中的CN-氧化为无毒的CO、N,该过程的离子反应方程
2 2 2
式为________________________________________________________________________
________________________________________________________________________。②在酸性条件下,向含铬废水中加入FeSO ,可将Cr O还原为Cr3+,该过程的离子反应
4 2
方程式为_____________________________________________________________
________________________________________________________________________。
③在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,离子方
程式为___________________________________________________________________
________________________________________________________________________。
答案:(1)①2H++SO+Ba2++2OH-===BaSO ↓+2HO
4 2
②Ba2++SO+H++HCO===BaSO ↓+HO+CO↑ HCO+H+===CO ↑+HO
4 2 2 2 2
③2Al3++3SO+3Ba2++6OH-===2Al(OH) ↓+3BaSO↓
3 4
(2)2Fe2++2Br-+2Cl===Br +2Fe3++4Cl- 2Fe2++4Br-+3Cl===2Br +2Fe3++6Cl-
2 2 2 2
(3)①5Cl+2CN-+8OH-===2CO ↑+N↑+10Cl-+4HO
2 2 2 2
②Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
③ClO-+2I-+HO===I +Cl-+2OH-
2 2
13.Ⅰ.为探究NH HCO 和NaOH的反应,设计实验方案如下:向含0.1 mol NH HCO 的
4 3 4 3
溶液中加入0.1 mol NaOH,反应完全后,滴加氯化钙稀溶液。
(1)若有沉淀,则NH HCO 与NaOH的反应可能为
4 3
________________________________________________________________________(写
离子方程式)。
(2)若无沉淀,则NH HCO 与NaOH的反应可能为
4 3
________________________________________________________________________(写
离子方程式)。
Ⅱ.Ba(OH) 溶液与NaHSO 溶液的反应
2 4
(1)当反应后的溶液呈碱性时,反应的离子方程式:________________________
________________________________________________________________________。
(2)当n[Ba(OH) ]∶n(NaHSO)=1∶2时,反应的离子方程式:____________________
2 4
________________________________________________________________________。
Ⅲ.按要求完成下列离子方程式。
(1)生物硝化法:在富氧条件下,通过硝酸盐菌的作用,将氨氮(以NH表示,下同)氧化成
硝酸盐,其反应的离子方程式为________________________________________
________________________________________________________________________。
(2)将过碳酸钠(2Na CO·3H O)溶于水配成溶液,加入适量稀硫酸,再加入足量KI,充分
2 3 2 2
反应后加入少量淀粉试剂,溶液呈蓝色,其反应的离子方程式为__________________
________________________________________________________________________。
解析:Ⅰ.NHHCO 电离出的HCO、NH都能与OH-反应,滴加少量的氢氧化钠,反应完
4 3
全后,滴加氯化钙稀溶液,有沉淀生成,说明是HCO与OH-反应生成碳酸根离子,反应离子
方程式为HCO+OH-===CO+HO;没有沉淀生成,说明NH与OH-反应生成一水合氨,反
2
应离子方程式为NH+OH-===NH·HO。
3 2
Ⅱ.Ba(OH) 溶液与NaHSO 溶液的反应,反应后的溶液呈碱性,说明Ba(OH) 溶液过量,
2 4 2
反应离子方程式为Ba2++OH-+SO+H+===BaSO ↓+HO;当n[Ba(OH) ]∶n(NaHSO)=
4 2 2 4
1∶2时,生成硫酸钡、水的物质的量之比为1∶2,反应离子方程式为Ba2++2OH-+SO+2H
+===BaSO ↓+2HO。
4 2
Ⅲ.(1)在富氧条件下,通过硝酸盐菌的作用,NH被氧气氧化为NO,反应离子方程式为
NH+2O===NO+HO+2H+;(2)加入足量KI,充分反应后加入少量淀粉试剂,溶液呈蓝色,
2 2
说明I-被过氧化氢氧化为碘单质,反应离子方程式为HO+2I-+2H+===I +2HO。
2 2 2 2答案:Ⅰ.(1)HCO+OH-===CO+HO
2
(2)NH+OH-===NH·H O
3 2
Ⅱ.(1)Ba2++OH-+SO+H+===BaSO ↓+HO
4 2
(2)Ba2++2OH-+SO+2H+===BaSO ↓+2HO
4 2
Ⅲ.(1)NH+2O===NO+HO+2H+
2 2
(2)H O+2I-+2H+===I +2HO
2 2 2 2
14.化学用语是化学学科的特色语言,化学用语可以准确表述化学现象、变化以及本质。
完成下列有关方程式。
(1)Na SO 还原性较强,在溶液中易被Cl 氧化成SO,常用作脱氯剂,该反应的离子方程
2 2 3 2
式为___________________________________________________________________
________________________________________________________________________。
(2)物质氧化性和还原性的强弱是相对的。已知氧化性:KMnO (H+)>H O>Fe2+,分别写
4 2 2
出酸性环境下KMnO 与HO 混合、HO 与FeCl 混合的离子方程式:___________、
4 2 2 2 2 2
________________________________________________________________________。
(3)化学反应多姿多彩,把SO 通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,但立即又
2
变为棕黄色,此时向溶液中滴加氯化钡溶液,有白色沉淀产生。请写出上述变化中溶液由棕
黄色变为浅绿色,但立即又变为棕黄色所涉及的两个离子方程式:_________________、
________________________________________________________________________。
(4)向含有n mol溴化亚铁的溶液中通入等物质的量的氯气,请写出离子方程式:
________________________________________________________________________
________________________________________________________________________。
(5)向NH Al(SO ) 中加Ba(OH) ,二者以物质的量比为4∶9混合,请写出离子方程式:
4 4 2 2
________________________________________________________________________
________________________________________________________________________。
答案:(1)S O+4Cl+5HO===2SO+8Cl-+10H+
2 2 2
(2)5H O+2MnO+6H+===2Mn2++5O↑+8HO 2Fe2++2H++HO===2Fe3++2HO
2 2 2 2 2 2 2
(3)SO +2Fe3++2HO===SO+2Fe2++4H+
2 2
3Fe2++NO+4H+===3Fe3++NO↑+2HO
2
(4)2Fe2++2Br-+2Cl===2Fe3++4Cl-+Br
2 2
(5)2NH+2Al3++4SO+4Ba2++9OH-===Al(OH) ↓+2NH ·H O+AlO+2HO+
3 3 2 2
4BaSO↓
4