文档内容
一、选择题
1.(2019·吉林高三模拟)下列说法中不正确的是( )
A.一般σ键比π键重叠程度大,形成的共价键强
B.两个原子之间形成共价键时,最多有一个σ键
C.气体单质中,一定有σ键,可能有π键
D.N 分子中有一个σ键,两个π键
2
解析:选C。单键均为σ键,双键和三键中各存在一个σ键,其余均为π键。稀有气体单
质中,不存在化学键。
2.(2019·吉林高三模拟)在硼酸[B(OH) ]分子中,B原子与3个羟基相连,其晶体具有与
3
石墨相似的层状结构。则分子中B原子杂化轨道的类型及同层分子间的主要作用力分别是(
)
A.sp,范德华力 B.sp2,范德华力
C.sp2,氢键 D.sp3,氢键
解析:选C。由石墨的晶体结构知 C原子为sp2杂化,故B原子也为sp2杂化,由于
B(OH) 中B原子与3个羟基相连,羟基间能形成氢键,故同层分子间的主要作用力为氢键。
3
3.(2019·天津高三模拟)关于氢键,下列说法正确的是( )
A.所有含氢元素的化合物中都存在氢键,氢键比范德华力强
B.HO是一种非常稳定的化合物,就是由于水分子间形成氢键所致
2
C.氢原子和非金属性很强的元素原子(F、O、N)形成的共价键,称为氢键
D.分子间形成的氢键使相应物质的熔点和沸点升高,氢键也可存在于分子内
解析:选D。氢键存在于H和非金属性很强的原子F、O、N之间,不属于化学键,大多存
在于分子间,也有少数存在于分子内,氢键的存在影响物质的熔、沸点。
4.(2019·武汉高三模拟)用价层电子对互斥理论(VSEPR)预测HS和COCl 的立体构型,
2 2
两个结论都正确的是( )
A.直线形;三角锥形
B.V形;三角锥形
C.直线形;平面三角形
D.V形;平面三角形
解析:选D。HS分子中的中心原子S原子上的孤电子对数是×(6-1×2)=2,则HS分
2 2
子中的中心原子的价层电子对数是4,其中2对是孤电子对,因此分子立体构型是V形;而
COCl 分子中的中心原子C原子上的孤电子对数是×(4-2×1-1×2)=0,则COCl 分子中
2 2
的中心原子的价层电子对数是3,因此分子立体构型是平面三角形,故选D。
5.(2019·榆林高三模拟)下列分子中的中心原子杂化轨道的类型相同的是( )
A.BeCl 与BF B.CO 与SO
2 3 2 2
C.CCl 与NH D.C H 与C H
4 3 2 2 2 4解析:选C。BeCl 、BF 分子中的中心原子杂化类型分别为sp、sp2;CO、SO 分子中的中
2 3 2 2
心原子杂化类型分别为sp、sp2;C H、C H 分子中的中心原子杂化类型分别为sp、sp2。
2 2 2 4
6.关于化学式为[TiCl(H O)]Cl ·H O的配合物,下列说法中正确的是( )
2 5 2 2
A.配体是Cl-和HO,配位数是9
2
B.中心离子是Ti4+,配离子是[TiCl(H O)]2+
2 5
C.内界和外界中Cl-的数目比是1∶2
D.加入足量AgNO 溶液,所有Cl-均被完全沉淀
3
解析:选C。配合物[TiCl(H O)]Cl ·HO中,配离子是[TiCl(H O)]2+;配体是Cl-和
2 5 2 2 2 5
HO,配位数是6;中心离子是Ti3+;配合物中内界中的Cl-不与Ag+反应,外界中的Cl-与Ag
2
+反应,据此分析解答。
7.(2019·本溪质检)通常把原子总数和价电子总数相同的分子或离子称为等电子体。人
们发现等电子体的空间结构相同,则下列有关说法中正确的是( )
A.CH 和NH是等电子体,键角均为60°
4
B.NO和CO是等电子体,均为平面三角形结构
C.HO+和PCl 是等电子体,均为三角锥形结构
3 3
D.B NH 和苯是等电子体,B NH 分子中不存在“肩并肩”式重叠的轨道
3 3 6 3 3 6
解析:选B。CH 和NH是正四面体结构,键角是109°28′,A错;NO和CO是等电子体,
4
均为平面三角形结构,B对;HO+和PCl 的价电子总数不相等,不互为等电子体,C错;苯分
3 3
子中存在“肩并肩”式重叠的轨道,故其等电子体B NH 分子中也存在,D错。
3 3 6
8.(2019·株洲一模)研究表明:三硫化四磷分子中没有不饱和键,且各原子的最外层均已
达到了八电子的稳定结构。在一个三硫化四磷分子中含有的P—S共价键的个数是( )
A.6 B.7
C.8 D.9
解析:选A。三硫化四磷分子中没有不饱和键,且各原子的最外层均已达到了八电子的
稳定结构。P可形成 3 个共价键,S可形成 2 个共价键,因此一个三硫化四磷分子中含有的
共价键个数为=9,其中一个硫原子形成2个P—S共价键,则三个硫原子形成6个P—S共价
键。
二、非选择题
9.指出下列分子或离子的立体构型和中心原子的杂化类型。
(1)H S__________________,CO___________________________________,
2 2
PH ______________________,PCl _________________________________,
3 3
BF______________________,HCN______________________________,
3
HCHO______________________,SO ________________________________,
2
SiH______________________。
4
(2)NH______________________,NO_____________________________,
SO______________________,SO______________________________,ClO______________________,ClO_____________________________,
SiO______________________。
答案:(1)V形、sp3 直线形、sp 三角锥形、sp3 三角锥形、sp3 平面三角形、sp2 直线
形、sp 平面三角形、sp2
V形、sp2 正四面体形、sp3
(2)正四面体形、sp3 V形、sp2 正四面体形、sp3 三角锥形、sp3 三角锥形、sp3 正四
面体形、sp3 平面三角形、sp2
10.(2019·大连双基测试)Q、R、X、Y、Z五种元素的原子序数依次增大。已知:①Z的原
子序数为29,其余的均为短周期元素;②Y原子价电子排布式为msnmpn;③R原子核外L层
电子数为奇数;④Q、X原子p轨道上的电子数分别为2和4。请回答下列问题:
(1)Z的核外电子排布式是_________________________________。
(2)在[Z(NH )]2+中,Z2+的空轨道接受NH 分子提供的____________形成配位键。
3 4 3
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是________。
a.稳定性:甲>乙,沸点:甲>乙
b.稳定性:甲>乙,沸点:甲<乙
c.稳定性:甲<乙,沸点:甲<乙
d.稳定性:甲<乙,沸点:甲>乙
(4)Q、R、Y三种元素的第一电离能数值由小到大的顺序为____________(填元素符号)。
(5)Q的一种氢化物的相对分子质量为26,其分子中σ键与π键的数目之比为________,
其中心原子的杂化类型是________。
(6)若电子由3d能级跃迁至4p能级时,可通过光谱仪直接摄取________。
A.电子的运动轨迹图像
B.原子的吸收光谱
C.电子体积大小的图像
D.原子的发射光谱
(7)某元素原子的价电子排布式为 3d54s1,该元素属于________区元素,该元素是
________(填元素符号)。
答案:(1)1s22s22p63s23p63d104s1(或[Ar]3d104s1)
(2)孤电子对
(3)b
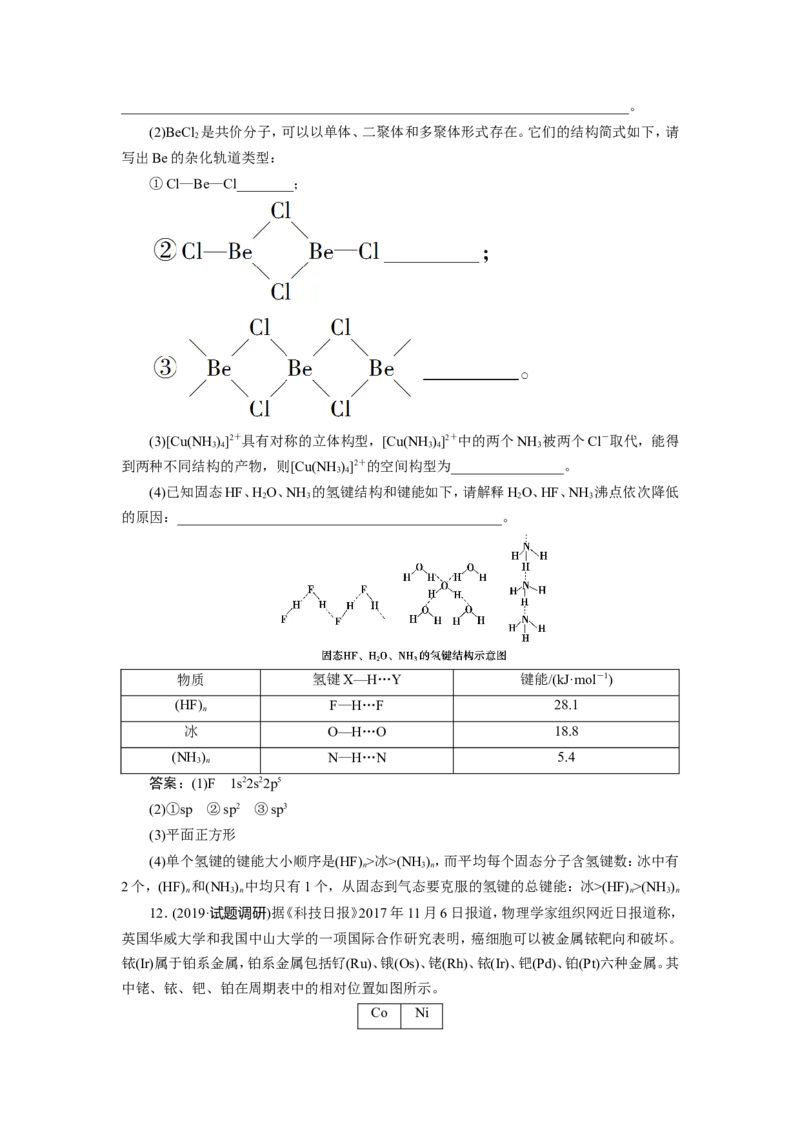
(4)Si冰>(NH),而平均每个固态分子含氢键数:冰中有
n 3 n
2个,(HF) 和(NH ) 中均只有1个,从固态到气态要克服的氢键的总键能:冰>(HF) >(NH )
n 3 n n 3 n
12.(2019·试题调研)据《科技日报》2017年11月6日报道,物理学家组织网近日报道称,
英国华威大学和我国中山大学的一项国际合作研究表明,癌细胞可以被金属铱靶向和破坏。
铱(Ir)属于铂系金属,铂系金属包括钌(Ru)、锇(Os)、铑(Rh)、铱(Ir)、钯(Pd)、铂(Pt)六种金属。其
中铑、铱、钯、铂在周期表中的相对位置如图所示。
Co NiRh Pd
Ir Pt
回答下列问题:
(1)基态铱原子的价层电子排布式为_______________________________。
(2)实验室常用氯化钯(PdCl )溶液检验CO,发生反应为PdCl +CO+HO===Pd↓+CO
2 2 2 2
+2HCl。
①在标准状况下,V L CO 含π键数目为________(N 表示阿伏加德罗常数的值)。
2 A
②HCl分子中σ键类型是________(填字母)。
A.ss B.sp
C.ssp2 D.ssp3
(3)实验证明,PtCl (NH ) 的结构有两种:A呈棕黄色,有极性,有抗癌活性,在水中的溶
2 3 2
解度为0.258 g,水解后能与草酸(HOOC—COOH)反应生成Pt(C O)(NH );B呈淡黄色,无极
2 4 3 2
性,无抗癌活性,在水中的溶解度为0.037 g,水解后不能与草酸反应。
①PtCl (NH ) 的空间构型是____________(填“四面体形”或“平面四边形”)。
2 3 2
②画出A的结构图示:____________________________________。
③C O中碳原子的杂化类型是________,提供孤电子对的原子是________(填元素符号)。
2
④ C、N、O 的第一电离能由大到小的顺序为 __________,判断依据是
__________________。
解析:(1)根据钴原子的价层电子排布式可推出铱原子的价层电子排布式:
3d74s2→5d76s2。(3)①如果PtCl (NH ) 是四面体形,类似甲烷的空间构型,只有一种结构,与
2 3 2
题意不符。②A具有极性,在水中的溶解度比B的大,说明A分子中2个NH 位于邻位,B分
3
子中2个NH 位于对位。③C O中碳原子没有孤电子对,2个氧原子提供2对孤电子对。
3 2
答案:(1)5d76s2 (2)① ②B
(3)①平面四边形 ② ③sp2 O
④N>O>C O的原子半径小于C,N的2p轨道处于半充满状态,较稳定
13.在人类文明的历程中,许多物质发挥过重要作用,如铁、硝酸钾、青霉素、聚乙烯、二
氧化硅、富勒烯、含铬物质等。
(1)Fe3+在基态时,价电子排布式为____________。
(2)KNO 中NO的立体构型为________,写出与NO互为等电子体的另一种阴离子的化
3
学式:__________________________________________。
(3)6氨基青霉烷酸的结构如图所示。结构中S原子的杂化方式是________。
(4)富勒烯(C )的分子结构如图所示,该物质能与氯气反应形成 C Cl 分子,1 mol
60 60 10C Cl 分子中含有碳碳单键的数目为________。
60 10
(5)已知配合物CrCl ·6H O的中心离子Cr3+的配位数为6,向含0.1 mol CrCl ·6H O的溶
3 2 3 2
液中滴加2 mol·L-1 AgNO 溶液,反应完全后共消耗AgNO 溶液50 mL,则该配离子的化学
3 3
式为_______________________________________。
答案:(1)3d5 (2)平面三角形 CO (3)sp3
(4)65N (5)[CrCl (H O)]+
A 2 2 4